高频电切术与氩离子凝固术对胃息肉患者疗效和各项因子的比较分析
蒋丽丽 于 霞
胃息肉是消化内科十分常见的一种良性隆起性病变,在我国的发病率较高,发病原因目前尚不完全清楚。早期没有明显的症状或不适,随着病情进展,可出现上腹痛、腹胀,恶心、呕吐等症状,部分患者可能会出现胃出血,从而引起隐血试验阳性或黑便,严重的患者可能会出现幽门狭窄,甚至引起癌变,严重影响患者的生命健康[1-2]。因此,息肉治疗的原则是早发现、早切除,以防止其进一步恶变加重。
高频电切术是目前临床应用较为广泛的技术,主要是通过高频的电压电流与组织接触时产生热量,从而起到分离、切割组织以及止血的作用[3-4]。该技术应用较成熟、操作方便且安全性较好。近年来研究表明,该技术存在较多不足,比如患者复发率高、术后并发症发生率较高,甚至还有发生恶变的报道[5]。随着内镜技术是不断进步,氩离子凝固术(argon plasma coagulation,APC)在消化道内镜中的作用和地位逐渐受到重视,是一种非接触性的电凝固技术。主要是利用高频单极电流技术,通过电离氩气产生高频能量,对患者的组织进行引导,同时产生凝固效应。该技术的特点是凝固深度限制较好,穿孔率大大降低[6-8]。本研究主要探讨高频电切术与氩离子凝固术对胃息肉患者疗效和各项因子的比较,现报道如下。
材料与方法
一、一般资料
将我院2016年5月至2017年5月收治的90例胃息肉患者随机分为两组,各45例。两组性别、年龄、病程、息肉数目、发生部位以及息肉直径等一般资料见表1,两组比较差异无统计学意义(P>0.05),具有可比性。
二、入选标准
1.纳入标准
①经胃镜检查,黏膜正常,病理活检诊断为胃息肉;②不同程度出现腹痛、腹胀、恶心、呕吐、黑便等症状;③肝肾功能、心电图等无明显异常;④本研究经我院医学伦理委员会批准,患者签署知情同意书。
2.排除标准
①患严重心血管、肝脏及肾等脏器疾病者;②患有血液系统疾病患者;③患有精神疾病者;④妊娠或哺乳期妇女。
三、治疗方法
所有入组患者均给予健康指导、常规护理和常规检查等,术前8~12 h禁食禁水,术前进行常规麻醉后,给患者口服盐酸利多卡因凝胶1支(生产厂家:北京紫竹药业有限公司,国药准字 H11022396,2%20 mL/支)。
对照组患者进行高频电切术,调节仪器到30 W功率,选择自动凝切,将圈套器插入患者体内,调整患者体位和导管,伸出钢丝圈套,套住息肉的蒂部,收紧蒂部使其变为暗红色,先凝后切,息肉脱落取出。
观察组患者给予氩离子凝固术。患者常规手术体位,调节仪器功率在40~60 W,氩气流量为1~2 L/min,标准电凝指数在A 40~60。将电子胃镜送至胃部,观察清楚息肉的情况后,插入氩离子凝固导管,在息肉上方大约3 mm处以1~3 s/次的频率凝固治疗,观察息肉变化,直至其表面泛白或黝黑。凝固完成之后,使用氩气刀和圈套器将息肉切除,若电凝效果不佳导致息肉蒂部出血,可再次使用氩气刀凝固止血。所有患者术后禁食24 h,同时均给予奥美拉唑肠溶片(商品名:耐信,生产厂家:阿斯利康制药有限公司,国药准字H20046380,40 mg/片),口服,40 mg/次,1 次/d,以及胃黏膜保护剂等。服用2周后,进行复诊并复查胃镜。

表1 两组一般资料比较
四、设备与仪器
电子胃镜(型号:CV-290,产家:日本 Olympus公司);圈套器(型号:SD-221U-25,产家:日本 Olympus公司);氩离子凝固器(型号:APC300,产家:德国 ERBE公司);高频电刀(型号:ICC300E,产家:德国 ERBE 公司)。
五、观察指标
术后观察两组患者的临床疗效,一次性切除成功情况,胃蛋白酶原Ⅰ(PGⅠ)、胃蛋白酶原Ⅱ(PGⅡ)、胃蛋白酶原比值(PGR)及血清胃泌素-17(G-17)等的检验结果,术后2周及半年后并发症发生情况。PGR=PGⅠ/PGⅡ。
六、疗效评价
根据患者临床症状和胃镜检查情况,将疗效分为:痊愈、显效、有效和无效。痊愈:患者腹痛、腹胀、恶心、呕吐等症状消失,且电子胃镜显示息肉完全消失;显效:患者上述临床症状明显改善,且电子胃镜显示息肉缩小程度>70%;有效:患者上述临床症状稍有改善,且电子胃镜显示息肉缩小程度为30%~70%;无效:上述症状无明显改善或电子胃镜提示息肉缩小程度<30%[9]。总有效率=痊愈率+显效率+有效率。
七、统计方法
采用SPSS 22.0软件对研究数据进行统计处理。计量资料均以x±s表示,采用t检验;计数资料以%表示,采用χ2检验。若P<0.05,则差异有统计学意义。
结 果
一、两组总有效率比较
观察组的总有效率为88.9%,明显高于对照组的68.9%,差异具有统计学意义(P<0.05),见表2。
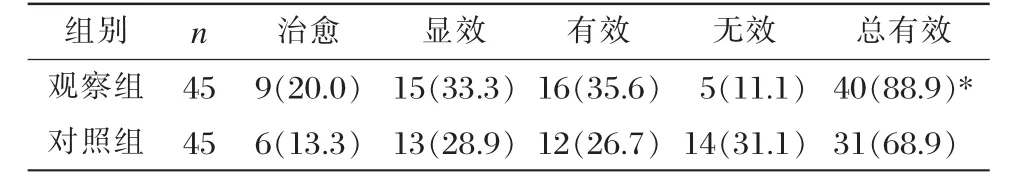
表2 两组总有效率比较 [n(%)]
二、两组息肉切除情况比较
观察组一次性切除成功率92.3%(121/131),明显高于对照组的 81.7%(103/126),差异具有统计学意义(χ2=6.473,P= 0.011)。
三、两组治疗前后各种因子的比较
治疗前,两组PGⅠ、PGⅡ、PGR及G-17水平比较差异无统计学意义(P>0.05)。治疗后,两组PGⅠ、PGR及G-17均较治疗前明显升高,且观察组显著高于对照组,差异均具有统计学意义(P<0.05);两组PGⅡ水平差异无统计学意义(P>0.05)。 见表 3。

表3 两组治疗前后各种因子水平比较 (x±s)
四、两组术后2周并发症发生率比较
观察组术后2周并发症总发生率为15.6%,明显低于对照组的40.0%,差异具有统计学意义(P<0.05),见表4。

表4 两组术后2周并发症发生率比较[n(%)]
五、两组半年后并发症发生率比较
两组患者密切随访,观察组失访2例,对照组失访1例,总随访率96.7%。随访半年后,观察组并发症总发生率为11.6%,明显低于对照组的31.8%,差异具有统计学意义(P<0.05),见表 5。
讨 论
胃息肉是消化内科十分常见的一种良性隆起性病变,在我国的发病率较高,发病原因目前尚不完全清楚。早期没有明显的症状,后期可出现上腹痛、腹胀,恶心、呕吐等症状,部分患者可能会出现胃出血,从而引起隐血试验阳性或黑便,严重的患者可能会出现幽门狭窄,甚至引起癌变,严重影响患者的生活质量和生命健康[10-12]。在临床上,息肉治疗的原则是早发现、早切除、早治疗,防止进一步恶变加重。

表5 两组半年后并发症发生率比较 [n(%)]
高频电切术是目前临床应用较为广泛的技术,主要是通过高频的电压电流与组织接触时产生热量,从而起到分离、切割组织以及止血的作用。该技术应用较成熟、操作方便且安全性较好[13]。近年来研究表明,该技术存在较多不足,比如患者复发率高、术后并发症发生率较高,甚至还有发生恶变的报道[14]。内镜下行APC手术近年在我国逐步开始应用,在消化道内镜中的作用和地位逐渐受到重视,APC是一种非接触性的电凝固技术。其原理主要是利用高频单极电流技术,通过电离氩气产生高频能量,对患者的病灶组织进行引导和产生凝固效应。目前该技术的特点是:凝固深度限制较好,减少术后出血及大大降低手术穿孔率[15-16]。本研究主要在于探讨高频电切术与氩离子凝固术对胃息肉患者疗效和各项因子的比较,取得了较为满意的效果。
PG主要由泌酸腺产生,在酸性环境中发挥作用,是胃蛋白酶的前体。主要分为PGⅠ和PGⅡ两型,PGⅠ主要由主细胞和黏液颈细胞产生;PGⅡ主要由黏液颈细胞和十二指肠上部细胞产生。PGⅠ的浓度代表了胃泌酸腺细胞的状态和功能,其浓度越高表示胃酸分泌功能越好,黏膜萎缩或功能减弱时,其产生的浓度降低;PGⅡ的升高与胃底腺管以及上皮化生等有关,PGR(PGⅠ/PGⅡ)可以反映胃黏膜的功能和萎缩情况。G-17是胃G细胞的主要标志之一,可以通过检测G-17水平来反映胃的功能[17-18]。本研究表明:术后2周,两组患者PGⅠ、PGR及G-17较治疗前明显升高,且APC组比高频电切术组升高更显著,差异具有统计学意义。提示:APC手术对胃息肉患者的疗效显著,可以明显改善胃黏膜泌酸腺细胞和G细胞的功能恢复,促进胃黏膜修复,缓解胃黏膜的萎缩以及肠上皮化生等病变。APC是一种非接触性的电凝固技术,主要是通过电离氩气产生高频能量,对患者的病灶组织进行引导和产生凝固效应,其最大的优点就是凝固的深度限制较好,不会很深的损伤到黏膜上皮,从而可以有效的减少术后出血并降低手术穿孔率。同时,由于胃深层的血管和胃黏膜组织未受到严重的损伤,因此,对胃黏膜的修复和泌酸腺细胞功能的恢复起到促进作用,防止胃黏膜萎缩、肠上皮化生及恶性病变的发生。
本研究表明,APC组患者总有效率(88.9%)明显高于高频电切术组(68.9%),且前者一次性切除成功率(92.3%)明显高于后者(81.7%);此外,APC组术后2周及随访半年后的并发症总发生率均明显低于高频电切术组。提示:APC组治疗胃息肉患者的疗效显著,可以明显提高手术成功率,同时显著降低术后并发症的发生。APC是一种非接触性的电凝固技术,主要是通过电离氩气产生高频能量,对患者的病灶组织进行引导和产生凝固效应,其最大的优点就是凝固的深度限制较好,因此胃深层的血管和胃黏膜组织未受到严重的损伤,有利于胃黏膜的修复和泌酸腺细胞功能的恢复,促进PGⅠ、PGR及G-17等指标的恢复,减少术后出血并降低手术穿孔率。本研究结果与国内外相关研究结果保持一致,效果显著[19-22]。
综上所述,胃镜下氩离子凝固术对胃息肉患者的疗效显著,可以明显提高手术成功率,改善胃蛋白酶原和胃泌素水平,且术后并发症较少,安全可靠,值得推广应用。

