利奈唑胺联合利福平治疗 C5 椎体次全切除钛网植骨融合内固定术后凝固酶阴性表皮葡萄球菌感染一例报告
陶利江 西尔买买提·艾哈提 丁舒晨 刘志荣 潘虹
颈椎前路手术包括颈椎椎体次全切除钛网植骨融合术 ( anterior cervical corpectomy and fusion,ACCF )、颈椎前路椎间盘切除植骨融合术 ( anterior cervical discectomy and fusion,ACDF ) 等,在临床广泛开展,其术后感染发生率极低[1]。回顾文献,既往报道多建议积极清创引流。笔者联合应用利奈唑胺及利福平治疗了 1 例颈椎前路 C5椎体次全切钛网植骨融合内固定术后发生凝固酶阴性表皮葡萄球菌感染的患者,经 1 年随访,疗效满意,报告如下。
临床资料
患者,男,63 岁,以“颈肩部酸痛 1 年,加重伴左上肢麻木 1 个月”于 2016 年 6 月 7 日入院。患者 1 年前无明显诱因下出现颈部酸痛不适症状,无双侧肩背部、双上肢疼痛,患者未引起足够重视。1 个月前患者感颈部酸痛逐渐加重,并出现左肩背部疼痛,左前臂及左手示指麻木,于劳累后加重,休息后缓解,无畏寒、发热,无行走不稳,无头晕等症状,无胸、腹部束带感,无四肢无力,无二便失禁等不适。患者在当地医院行颈椎 MRI 示:颈椎退行性改变,C4~5、C5~6椎间盘突出。查体:左手皮肤浅感觉较对侧减弱;左手握力 5- 级;左侧 Eaten 征 ( + )、Spurling 征 ( + );双侧 Hoffmann 征 ( - )。肺部 CT 示:右下肺肺大泡及肺气囊,两肺轻度气肿。输血三项确诊为隐性梅毒。OGTT 试验确诊为 2 型糖尿病,予以胰岛素控制血糖 ( 空腹血糖:术前 2 天 8.7 mmol / L,术前 1 天8 mmol / L,术晨 6 mmol / L )。术前诊断:( 1 ) 颈椎病( C4~6);( 2 ) 高血压 II 级高危;( 3 ) 2 型糖尿病;( 4 ) 脾切除术后。于 2016 年 6 月 13 日在全麻下颈椎前路 C5次全切髓核摘除植骨内固定术,手术顺利,历时约 1 h。鉴于患者头孢、青霉素过敏,术前半小时及术后各予以一剂林可霉素注射液 0.6 g 静滴预防感染。术后患者自诉左肩、左上臂酸痛较术前明显缓解,术后 5 天左右患者自诉左肩、左上臂又出现酸痛,术后 1 周患者伤口愈合良好,拆线后出院。
术后 10 天左右,患者发现切口红肿,吞咽、饮食后右胸部疼痛不适,故来院就诊。查体:颈前路右侧斜切口局部红肿,触之软,有浮动感,轻度压痛 ( 图 1 )。病理征未引出。四肢肌力与术前无明显改变。体温:36.8 ℃。实验室检查:白细胞计数 16.72×109/ L↑;中性粒细胞计数11.52×109/ L↑;中性粒细胞比例 68.9%;超敏 C 反应蛋白 ( 快速法 ) 51.32 mg / L↑;血沉 72 mm / h↑;取脓液行细菌培养及药敏试验示:凝固酶阴性表皮葡萄球菌生长,对利奈唑胺注射液 ( 斯沃 ) 及利福平敏感。复查颈椎正侧位 X 线片示内固定位置良好,无明显松动迹象 ( 图 2 )。颈椎 MRI 示:C6~7椎管内异常信号,脓肿可能 ( 图 3 )。食管钡剂造影示:食管中下段炎性改变首先考虑,无食管瘘迹象 ( 图 4 )。切口 B 超示:皮下低回声区。诊断:( 1 )颈椎病前路椎体次全切术后感染;( 2 ) 2 型糖尿病;( 3 )食管炎;( 4 ) 隐性梅毒;( 5 ) 肺气肿。治疗:( 1 ) 严格制动;( 2 ) 利奈唑胺注射液 ( 斯沃 ) 0.6 g 静滴每 12 h 1 次,
联合利福平胶囊 0.15 g 口服,3 次 / 日抗感染治疗;( 3 )胰岛素控制血糖、抑酸药物治疗食管炎;( 4 ) 人血白蛋白注射液 10 g 静滴每天 1 次、复方氨基酸注射液 250 ml 静滴每天 1 次等营养支持治疗;( 5 ) 怯风止痛胶囊 6 粒每天2 次,活血止痛及护肝治疗。术后 3 周,即抗感染治疗后8 天,患者自诉吞咽、饮食后右胸部疼痛不适感消失,双肩部、左上臂酸痛感较前缓解。四肢肌力与术前无明显改变。复查伤口分泌物培养示:未见细菌、真菌生长。复查颈椎 MRI 示:C6~7椎管脓肿明显缩小 ( 图 5 )。联合用药 1 个月后停用利奈唑胺,继续口服利福平胶囊 0.15 g,3 次 / 日继续治疗 5 周。2016 年 7 月 24 日再次复查颈椎MRI 示:C6~7椎管脓肿消失 ( 图 6 )。患者自述无特殊不适,伤口无红肿热痛表现。患者自第一次入院至第二次出院期间白细胞计数、中性粒细胞计数、C 反应蛋白、血沉、丙氨酸氨基转移酶及谷氨酰胺转移酶变化详见图 7。术后 1 年电话随访,患者无感染复发。
讨 论
近年来随着我国人口老龄化的进展,颈椎病的发病率逐年提高。由于颈椎病压迫多来自于前方,颈椎前路手术,包括 ACCF、ACDF 等在临床已广泛开展,且疗效满意[1]。由于颈椎前路手术多采用 Smith-Robinson 入路,对颈前软组织及椎旁肌肉损伤较小,临床中颈椎前路手术后切口感染的发生率很低。2017 年,AO 组织对在北美21 家大型外科中心接受 ACDF 治疗的 8887 例进行回顾性研究,其中发生术后感染者仅 6 例,发生率为 0.07%[2]。2007 年,Fountas 等[3]对 1015 例 ACDF 术后患者进行随访研究,仅 1 例发生术后切口感染,发生率为 0.15%。既往文献报道颈椎前路手术后感染的发生率介于 0.1%~1.6%之间[3]。

图1 颈前路右侧斜切口局部红肿,触之软,有浮动感,轻度压痛图 2 a~b:复查颈椎正侧位 X 线片示内固定位置良好,无明显松动迹象图3 a~b:颈椎 MRI 示 C6~7 椎管内异常信号,脓肿可能图4 食管钡剂造影示:食管中下段炎性改变首先考虑,无食管瘘
由于既往各研究的样本量均较少,无法进行统计分析,因此颈椎前路术后感染的危险因素目前尚无确切证据。AO 报道的 6 例感染者中 3 例为吸烟者,因此吸烟史可能为颈椎前路术后感染的危险因素之一[2]。其次,术中颈前路拉钩牵拉过紧、持续牵拉时间过长或术中操作不当造成食管损伤可能引起细菌播散。此外,笔者建议对颈椎前路手术患者尽量采用皮内缝合,理由是颈前路手术间隙疏松,且颈阔肌多不作紧密缝合,细菌易由丝线缝线处渗入,造成感染。另外,本例病例采用颈前路斜切口,可能也是感染的危险因素之一。斜切口虽然暴露广泛,但相较于横切口,局部损伤大:在颈前路手术中,横切口平行于皮纹方向,因皮下的血管网走行多与皮纹方向一致, 横切口不但避开了颈外静脉和颏下静脉,而且可以减少皮下血管损伤概率,减少术中皮下电凝止血的范围,改善局部组织条件,降低感染率。因此,建议经验丰富的医师尽量采用颈前路横切口。其余可能的危险因素还包括:糖尿病病史、内植物移位、zenker 憩室、手术时间过长等。
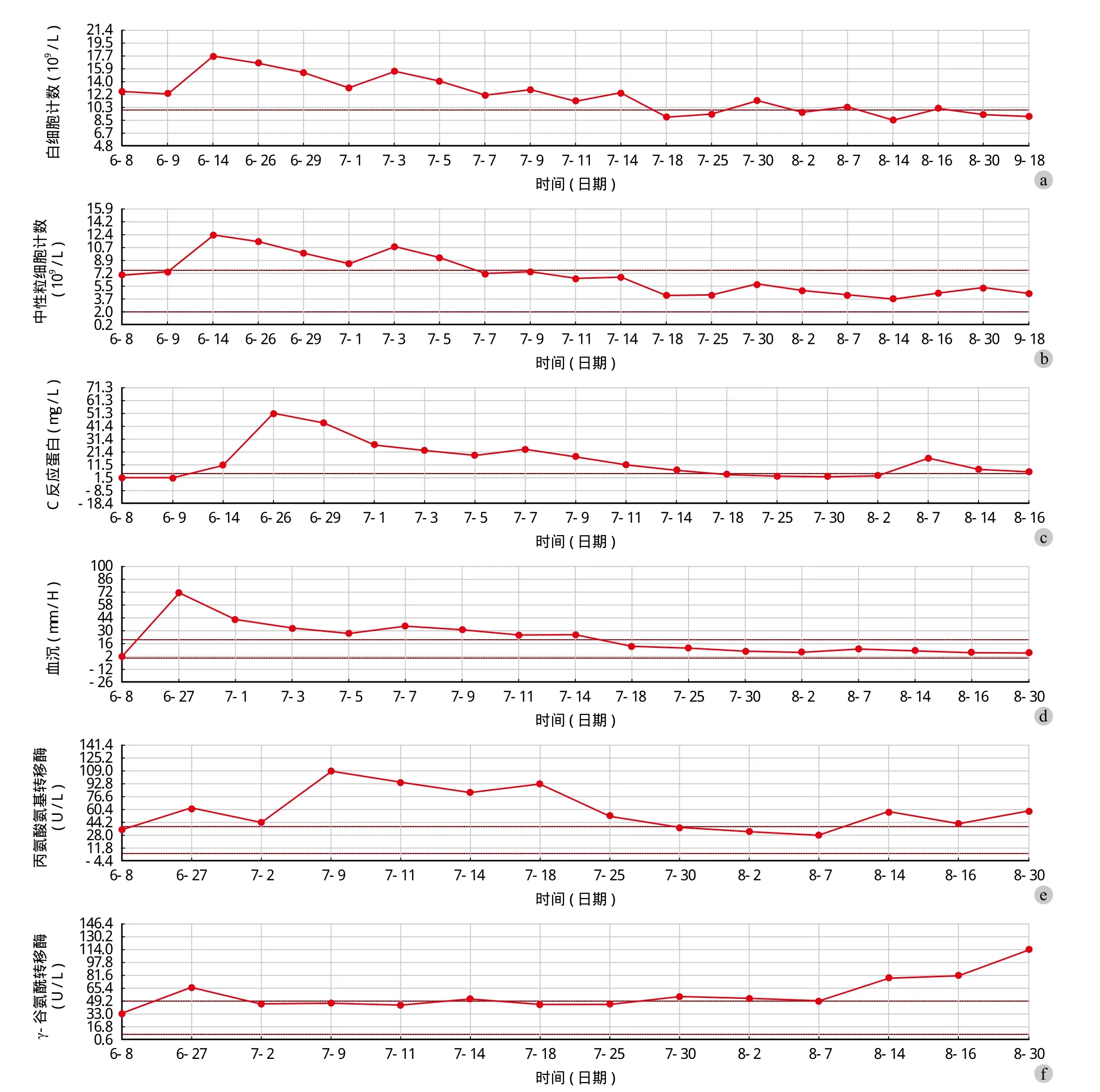
图7 生化指标变化趋势图 a:白细胞计数;b:中性粒细胞计数;c:超敏 C 反应蛋白 ( 快速法 );d:血沉;e:丙氨酰氨基转移酶;f:γ- 谷氨酰转移酶Fig.7 Trends in biochemical indicators a: White blood cell count; b: Neutrophil count; c: Hypersensitive C-reactive protein ( rapid method ); d:Erythrocyte sedimentation rate; e: Alanyl aminotransferase; f: γ- Glutamyl transferase
颈椎前路术后感染的诊断须结合患者症状、体征、影像学表现及实验室检查等综合分析。患者症状多表现为切口红肿,触之有波动感或出现渗液、流脓等,部分患者可有胸部或腋下钝痛[4]。若感染累及咽后壁,患者可出现吞咽痛,或进一步发展为纵隔炎[5]。若感染侵犯椎管内,患者可出现脊髓压迫或神经根性症状。体征方面多表现为超过 38.5 ℃ 的发热[6],若为低毒性细菌感染,如本例表皮葡萄球菌感染者,也可能无体温明显升高。若怀疑颈前路术后感染,应积极完善食管造影、颈椎 X 线片、颈椎 MRI等检查。通过食管造影 X 线片可明确是否存在食管瘘;颈椎 X 线片明确是否存在内固定松动或移位,是否存在颈前气体影,后者提示食管瘘可能。颈椎 MRI 可观察脓肿大小及位置,明确侵袭范围,但 MRI 中血肿和脓肿较难区分。实验室检查需监测血沉、C 反应蛋白等,并完善脓液或血液细菌培养及药敏试验。Bengzon 等[7]报道颈椎前路融合术后 C 反应蛋白于术后第 2 天达高峰,之后逐渐下降。而 Rosahl 等[8]的研究提示若 C 反应蛋白术后第 5 天降至峰值的 50% 以下,可排除感染,反之则须警惕术后感染可能。
由于颈椎前路术后感染的发生率较低,临床处理颈椎前路术后感染的经验也较少,目前尚缺乏规范性的处置指南[2]。治疗方案主要有:( 1 ) 手术治疗:行颈部清创+置管冲洗术,术后予以敏感抗生素抗感染治疗等;( 2 ) 保守治疗:严格制动,先予以敏感抗生素抗感染治疗,严密观察患者症状、体征变化,期间复查血常规、CRP 及颈椎 MRI,判断感染控制情况,若感染无法有效控制,甚至蔓延,则需手术治疗。回顾既往文献,多主张积极切开清创引流[2-6],若无明显内固定松动,清创术中可保留内固定,反之则需更换内固定[6]。
在骨科内置物术后感染中,耐甲氧西林金黄色葡萄球菌、凝固酶阴性表皮葡萄球菌是产生生物膜的主要病原体[9]。据文献报道,利福平对于处于静止期的细菌仍具有优良的杀菌能力,且可有有效渗入生物膜中,可作为内置物术后感染的首选药物[10]。但是,单独使用利福平可能迅速产生耐药性[11],联合使用另一种抗生素可有效避免这一现象[9]。此外,利福平与部分抗生素联用具有显著的协同效应,可有效增强杀菌能力并减少细菌耐药,包括:喹诺酮类、克林霉素、夫西地酸及利奈唑胺等。同时,利福平应避免与 β-内酰胺类或糖肽类抗生素联用,有文献报道与这两类抗生素联用会迅速产生细菌耐药性[12]。利奈唑胺与万古霉素是临床治疗耐药革兰阳性菌所致感染较为常用的抗生素,文献报道,利奈唑胺治疗革兰阳性菌所致复杂性皮肤软组织感染,疗效优于万古霉素,总体细菌清除率亦高于万古霉素[13]。因此,笔者联合使用利奈唑胺与利福平,使两者发挥协同杀菌效应,减少耐药并有效杀灭静止期细菌,破坏细菌生物膜,避免感染复发。
本例患者考虑为低毒感染,且与患者及其家属沟通,言明利弊后患方选择先行保守治疗。经 1 周的联合抗生素治疗,患者症状缓解明显,各项炎性指标持续下降,颈椎MRI 示感染病灶有缩小迹象,表明抗感染治疗有效,遂继续采用保守治疗。保守治疗期间需要注意长期抗生素时间带来的并发症,如肝肾功能损害、菌群失调、真菌感染、假膜性肠炎等,最好联合保肝药物治疗,并监测肝功能。此外,须注意抗生素可能无法完全杀灭内植入物表面特别是钛笼植骨区内细菌,而且表皮葡萄球菌为条件致病菌,一旦患者抵抗力减弱,感染有再次暴发可能。
通过术后 1 年回访,提示保守治疗颈椎前路 ACCF 术后低毒性细菌感染具有可行性。对于诊断明确,尝试保守治疗后各项炎性指标下降,影像学提示脓肿局限者,可参考笔者提供的治疗方案予以处理,但也须警惕保守治疗的并发症。

