持续营养干预对高危急性淋巴细胞白血病患儿维持治疗阶段营养状况及并发症的影响*
李智英 ,张婷婷 ,黄惠 ,钟婷 ,蔡敏
(1中山大学附属第一医院儿科,广东广州,510080;2中山大学肿瘤防治中心儿科,广东广州,510060;3中山大学孙逸仙纪念医院儿科,广东广州,510120)
近年来,随着治疗水平的提高,儿童高危急性淋巴细胞白血病(acute lymphoblastic leukaemia,ALL)的治愈率达 80%[1],但经过了诱导治疗及强化疗程,尚有长达1年左右的维持治疗阶段,此期是患儿复发与死亡的高风险阶段之一,直接影响患儿的治疗结局[2]。ALL在治疗过程中营养不良的发生率较高[3],严重的营养不良常导致并发症和死亡率上升、治疗副反应增加、生活质量下降等[4-5]。营养不良的程度对疾病预后的影响在肿瘤儿童中更明显[6]。研究显示[7],早期的营养状况与白血病的并发症及预后风险呈密切相关。然而,国内对维持治疗阶段ALL儿童营养状况与治疗结局的关系关注较少,鲜有相关研究报道[8]。 本研究通过应用由加拿大SECKER等专家修订的住院儿童营养风险筛查工具-主观全面营养风险评价(subjective global nutritional risk assessment,SGNA)[9]作为临床住院儿童的营养评价工具,并对研究目标在此期间进行持续性营养干预。旨在了解高危ALL患儿在维持治疗阶段的营养状况的同时为患儿提供有效的营养支持,从而改善其营养状况的目的,现报道如下。
1 对象与方法
1.1 对象
选取2015年7月至2017年6月在广州市3家三级甲等医院(1家专科医院、2家综合医院)就诊的高危ALL患儿172例。入选标准:符合2008年中华医学会儿科分会血液组制订的CCLG-2008方案分组标准[10],诊断为高危急性淋巴细胞白血病、目前处于维持治疗阶段患儿;患儿家属知情同意。排除标准(符合下列条件1条或以上者):合并其他系统恶性肿瘤;有先天性代谢障碍疾病者;精神障碍者。本研究已通过参与研究的医院医学伦理委员会审批。按照住院号码(ID)的单双号,将单号设为对照组86例,双号设为观察组86例。对照组因中途退出,资料缺失2例,最终入选84例,其中男 46 例,女 38 例,年龄 3~14 岁,平均(7.8±3.2)岁;观察组因中途退出,资料缺失2例,最终入选84例,其中男 42例,女 42例,年龄 2.5~14岁,平均(7.7±3.6)岁。两组患儿一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
1.2 方法
1.2.1 对照组 在进行维持治疗阶段开始,患儿按要求每3个月复诊并评估营养状况,由接诊医生根据患儿检验、检查结果,给予常规、间断性饮食指导。指导轻度营养不良的患儿饮食中增加优质蛋白,减少高脂肪饮食;中度营养不良的患儿指导家属少量多餐,选用优质蛋白;重度营养不良患儿则在饮食基础上增加肠内、肠外营养。
1.2.2 观察组
1.2.2.1 成立营养支持团队(nurtrition support team,NST) NST由医生、护士、营养师组成。小组成员的条件:需经过营养专业知识培训,并取得营养师资格者。职责:为入组患儿建立营养档案,根据患儿身高、体重、年龄、营养状况、病情及饮食情况拟定持续性营养计划,指导患儿或家属执行营养计划,并进行信息反馈,针对患儿情况随时调整计划;建立微信群,定期推送营养处方等资料。
1.2.2.2 营养风险评估 采用SGNA评估工具进行营养风险评估[9]。营养良好为4周内体重下降<5%,2周内饮食无变化、无消化道症状、无乏力、脂肪及肌肉消耗不明显,血清白蛋白浓度≥35g/L。轻度营养不良为4周内体重下降5%~10%,2周内饮食减少不明显、偶有消化道症状、轻度乏力、脂肪及肌肉消耗轻度改变,血清白蛋白浓度30~35g/L。中度营养不良为4周内体重下降10%~15%,2周内饮食明显减少、持续>2W出现消化道症状、明显乏力、脂肪及肌肉消耗明显,血清白蛋白浓度25~30g/L。重度营养不良为4周内体重下降>15%,2周内拒食、恶心呕吐频繁、活动不便、卧床、皮下脂肪消失、肌肉萎缩,血清白蛋白浓度<30g/L。
1.2.2.3 制订营养干预方案 根据患儿营养状况,合理调配营养结构,拟定个性化营养处方,既要保持日常身体需求量,亦要保证生长发育的需求量。确保营养素的摄入量与质量,尤其是蛋白质、脂肪、碳水化合物的合理搭配,每日总热量(kcal)=1000+年龄×(70~100)。 蛋白质不低于 1.5g·kg-1·d-1。轻度营养不良者,开始阶段蛋白质的供给量为每日推荐量的2/3,脂肪占全日量的20%,无营养不耐受后,逐渐增加至正常需要量;补充维生素A、E、C等,在膳食中加入适量的微量元素钙、锌;以优质蛋白为主,少量多餐,避免油腻、高糖及辛辣食物,减少不必要的肾脏、肝脏负担。中度营养不良者,当患者频繁呕吐,无法进食或发热时,配置纯短肽的肠内营养液口服或管饲,以保证营养素的摄入。重度营养不良者提供优质蛋白>50%,以不饱和脂肪酸为主,避免进食高糖淀粉类食物。鼓励患儿经口进食。如化疗副作用严重,因频繁呕吐或口腔黏膜损伤严重无法进食采用短期管饲的肠道内营养,必要时采用肠道外营养。
1.2.2.4 实施营养干预 患儿每个月复诊1次,研究小组成员在患儿复诊后的第1周根据患儿的蛋白质、淀粉酶等检验结果及营养状况,及时调整饮食结构,将营养处方或膳食种类及搭配方法通过微信群推送给患儿家长并每2周进行电话随访,对患儿及家属进行饮食宣教,及时纠正不正确的饮食习惯及营养搭配。每天患儿家属通过微信反馈患儿情况,研究小组人员针对患儿存在的问题提出改正的措施,提高患儿及家属依从性。干预时间1年。
1.2.2.5 质量控制 所有研究对象均采用统一治疗方案。对各参与研究人员进行集中培训,采用统一设计的调查方案及指标。所有数据均需两人核对,对数据的逻辑性及准确性进行核查,剔除不正确数据,并由团队负责人定期抽查、检查数据的准确性与真实性,确保措施与数据的同质性。
1.3 效果观察
1.3.1 营养状况 由专人负责,应用SGNA评价患儿维持治疗阶段营养状况,干预前及干预后每3个月评估1次,至1年后维持治疗阶段结束。
1.3.2 并发症 并发症观察包括重症感染、皮肤黏膜损伤、胰腺炎、血糖异常。重症感染是指病原体侵入人体而引发的具有损伤性的剧烈全身反应,并具有对组织、器官损伤性的病理、生理过程及一组临床症状,包括全身炎症性反应(systemic inflammatory response syndrome, SIRS), 脓毒血症(sepsis)以及发热超过 1 周的任何感染等[11]。 皮肤黏膜损伤是指由各种因素造成皮肤黏膜上皮细胞损伤、坏死,通常以口腔、会阴、肛门等部位常见[5]。急性胰腺炎诊断标准参照2014年中华医学会外科分会胰腺外科学组制订的急性胰腺炎诊治指南[12]。血糖异常为血糖值低于或高于正常值范围[5]。
1.4 统计学方法
数据采用SPSS17.0进行统计学分析。计数资料采用百分比和频数表示,组间比较采用χ2检验;计量资料采用均数±标准差表示,组间比较采用t检验;等级资料采用秩和检验。检验水准α=0.05。
2 结果
2.1 干预前后两组患儿营养状况比较
干预前后两组患儿营养状况比较见表1。从表1可见,干预后,观察组患儿营养状况优于对照组,两组比较,差异有统计学意义(P<0.01)。
2.2 两组患儿并发症发生情况的比较
两组患儿并发症发生情况的比较见表2。从表2可见,观察组患儿重症感染、皮肤黏膜损伤、急性胰腺炎、血糖异常的发生率低于对照组,两组比较,差异均有统计学意义(P<0.05)。
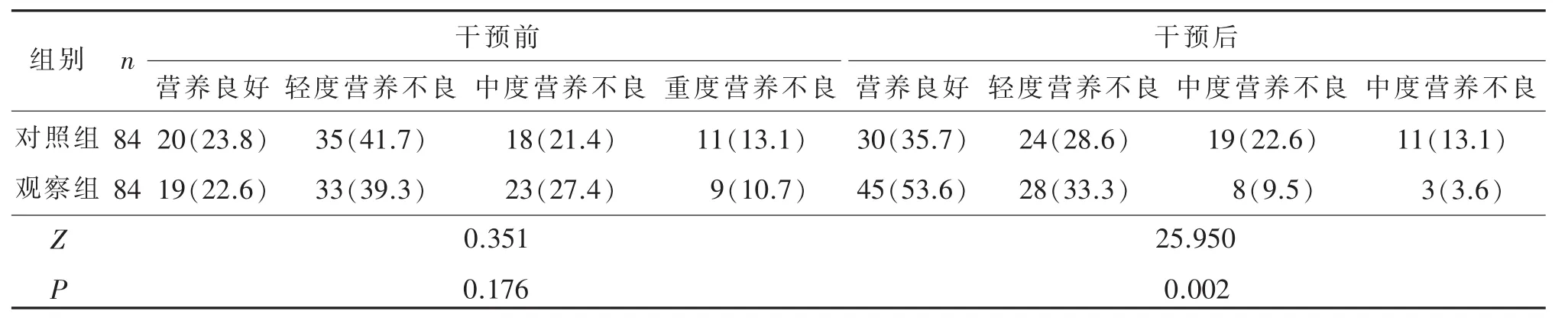
表1 干预前后两组患儿营养状况比较 n/%

表2 两组患儿并发症发生情况的比较 n/%
3 讨论
3.1 持续营养干预有助于改善ALL患儿维持治疗阶段的营养状况
研究表明[13-15],40%~80%的恶性肿瘤患者存在严重的营养不良,高危ALL患儿在维持治疗阶段发生营养不良的风险为20%~80%。本结果显示,干预前两组患儿发生营养不良(包含轻度、中度、重度)的发生率分别为76.2%、77.4%,中重度营养不良的患儿分别为34.5%、38.1%。原因可能与以下因素有关:血液肿瘤患儿的能量、碳水化合物、脂肪及蛋白质代谢均有很大程度改变[16-17],尤其是高危ALL患儿由于体内分解代谢增加,蛋白质、脂肪与糖原合成减少,加上特殊治疗使患儿出现呕吐、食欲下降等不良反应,导致各种营养素摄入不足,蛋白质的代谢处于负氮平衡状态[18]。评估患儿营养状态是保证治疗效果的一项很重要的工作。本研究采用由加拿大SECKER等专家修订的SGNA[9]作为营养评价工具,该工具曾被视为筛查营养不良的金标准,其适用于31d~17.9岁儿童营养风险预测,具有较高的特异性,与传统的营养指标有较高的一致性,并能预测与营养相关的临床结局和营养支持效果,操作简单易掌握,使患儿的营养风险评估准确、有效,为营养干预提供依据[19-20]。相关学者认为[21],营养支持团队及有效的营养支持方案有助于尽早达到目标能量。本研究根据评估情况,对于不同程度营养不良的患儿,实施个体化及持续性的营养干预,给予患儿及时的营养调整指引,避免了患儿及家属因盲目增加营养素,导致机体负氮平衡失调,加大了代谢紊乱的风险,同时减少了因营养素构成不合理所造成的营养不足,有效地满足了患儿不同阶段、不同现状的营养需求,从而达到改善ALL儿童营养状况的目的。本结果显示,干预后,观察组患儿营养状况优于对照组,两组比较,差异有统计学意义(P<0.01)。
3.2 持续营养干预可降低ALL患儿维持治疗阶段并发症的发生
患儿的营养状况已成为各类并发症发生的重要相关因素之一[22],并直接影响了患儿的治疗结局。营养不良不仅可造成儿童生长发育的速度减慢甚至停止,还可引起患儿抵抗力下降。结果显示[23],营养不良患者存在T淋巴细胞亚群的变化,即存在细胞免疫功能缺陷,表明营养不良程度与免疫系统的受损程度相关,营养不良的患者较无营养不良的患者化疗后并发症发生率明显增加,其实质是由于营养不良的患者更易存在免疫系统的受损。ANDREAS[24]在对希腊 139例 ALL患儿的调查中发现,营养状况是患儿感染及死亡的重要影响因子。宁方颖[25]对恶性肿瘤患者营养状况的调查结果显示,营养状况越差,其重症感染发生率越高,预后越差。由于化疗药物的毒性作用导致上皮细胞的损伤,破坏了皮肤黏膜屏障,加上化疗引起的恶心、呕吐,导致营养素及微量元素摄入不足,加重了皮肤黏膜的再生及修复功能的损伤[26]。因此需要合理补充营养素及微量元素以促进上皮细胞的修复与再生功能。因患儿的胰岛被白血病细胞浸润,及化疗药(如左旋门冬酰胺)使胰岛功能受损,容易发生糖耐量异常和胰岛素抵抗,引起高血糖或低血糖。饮食质量的改变容易诱发急性胰腺炎的发生[5]。因此,进行血糖及消化酶的定时监测,适当调整葡萄糖及蛋白质的摄入,调整饮食结构,对防止血糖异常及保护胰腺功能非常重要。本结果显示,营养干预后的观察组患儿皮肤黏膜损伤、重症感染、胰腺炎、血糖异常的发生率低于对照组,两组比较,差异均有统计学意义(P<0.05)。
4 结论
维持治疗阶段是影响高危ALL患儿治疗成功与否的重要阶段之一,此期仍然是患儿营养不良发生的高峰期,患儿的营养状况与治疗结局密切相关。本结果表明,持续营养干预有助于改善ALL患儿维持治疗阶段营养状况及降低并发症的发生。因本研究是单一省内的多中心研究,具有一定的地域局限性,尚需要扩大研究区域,增加样本的代表性,才能进一步反映该方法的临床意义,下一步将继续研究。

