生活用水中氟含量的测定
赵俊英,赵俊明
(1.陇东学院 化学化工学院,甘肃 庆阳 745000;2.山东华宇工学院,山东 德州 253000)
1 引言
氟元素是人和畜禽正常生长所必需的微量元素之一,适量的氟对机体牙齿、骨骼的钙化、神经系统的传导和酶系统的代谢均有促经作用。而过量的氟会够破坏钙、磷的代谢。当人体内存在过量的氟或其化合物时,可引起各种急性或慢性的氟中毒[1],可形成骨刺、骨节硬化、骨质疏松等氟骨病病症。饮水型氟中毒在我国流行最广,危害最严重,主要是通过饮水使机体摄入过量氟所致。在水质检验,尤其是地下水、自来水检验中,氟化物是一项比较重要的参数[2]。
生活用水中氟含量的测定经过了比较慢长的过程,但在近几年发展比较迅速。一些专家对好多地区饮用水中的氟含量进行了测定,1996年卫平民等[3]对淮南地区饮用水中氟含量进行过测定和分析;1999年王珊珊等[4]测定分析过云南腾冲县温泉区的泉水与居民用水的氟含量;全国地氟病监测组报道了我国15个饮水型地方性氟中毒省区的17个县、32个村的检测结果[5]。这引起了一些化学专家的极度重视,他们开始致力于研究如何用一些简单的办法来测定水中的氟含量[6]。1996年李建军用氟-镧-茜素氟蓝法测定了水中氟的含量,该法利用反应生成的蓝色配合物氟-镧-茜素氟蓝对光的吸收测定水中氟含量,方法比较简单,选择性好,但是采用的萃取剂具有毒性,对环境造成污染;2004年黎晓敏等用氟离子选择电极法[7]对重庆市饮用水中氟的含量进行了测定分析,该法测量简便、灵敏度高、选择性好以及容易实现连续自动测量。但是该法经常出现示值不稳,重现性较差;2009年李东明等依据国标方法离子选择性电极法的原理[8]应用便携式快速水质检测仪测定了生活用水中的氟化物,该法是在对磺基苯偶氮变色酸钠(SPADNS)法的基础上利用便携式快速水质监测仪测定生活饮用水中的氟化物,具有方便快速的特点。此外还有氟试剂分光光度法[9]、离子选择性电极法[10-11]和离子色谱法[12]等,本文采用磺基水杨酸合铁分光光度法测定水中的氟含量。
2 实验部分
2.1 检测原理
本文以三价铁离子为中心原子,磺基水杨酸为显色剂建立分光光度法测定氟离子。氟离子与三价铁离子络合,生成无色络合物,三价铁离子与磺基水杨酸在酸性条件下反应生成紫红色络合物。水样中的氟离子与三价铁离子生成较稳定的络合物,且水样中的其他阴离子不干扰,致使Fe3+络合度降低,吸光度降低,氟离子的浓度与吸光度成反比,据此可以测定氟离子的含量。
2.2 仪器和试剂
仪器:电子天平、7230型分光光度计。
试剂:硫酸铁铵、磺基水杨酸、氟化钠、硫酸。
2.3 实验过程
2.3.1 溶液的配制
Fe3+离子溶液:准确称取一定量的硫酸铁铵,加入20mL浓硫酸和去离子水溶解,1L容量瓶中定容,摇匀,作为储备液备用。再移取上述溶液5mL于500mL容量瓶中,加水稀释定容至刻度,摇匀,配成Fe3+标准溶液。
氟离子标准溶液:准确称取一定量的氟化钠,加去离子水溶解后转移至500mL容量瓶中,稀释至刻度,摇匀,备用。再移取上述溶液2mL于100mL的容量瓶中,加水稀释定容至刻度,摇匀,配成F-标准溶液。
0.2%磺基水杨酸溶液:准确称取一定量的磺基水杨酸,加去离子水溶解后转移至50mL的容量瓶中稀释至刻度,摇匀,备用。
2.3.3 样品处理
取50mL的本地区生活用水待用。
2.3.3 样品检测
在六支已编号的50mL的容量瓶中,依次加人5.00 mL 的Fe3+标准溶液,1.00 mL 0.2%磺基水杨酸,分别精密量取0,2.00,4.00,6.00,8.00,10.00 mL氟标准溶液于6支容量瓶中,摇匀。分别取少量于六支1cm的比色皿中,分别测定其吸光度。
再移取5.00 mL 的Fe3+标准溶液,1.00 mL 0.2%磺基水杨酸于50mL的容量瓶中,加10mL的待测水样,按照上述方法测其吸光度,平行测定三次。
3 结果与讨论
3.1 测定条件的优化
3.1.1 吸收光谱
按照实验方法,在7230型分光光度计上于400~600nm范围内扫描吸收光谱,根据表1,以波长为横坐标,吸光度为纵坐标作图,见图1。由图1可知,随波长增大,吸光度先增大后减小,当波长为500nm,吸光度最大,故选择500nm作为最佳测定波长。

表1 波长与吸光度的关系
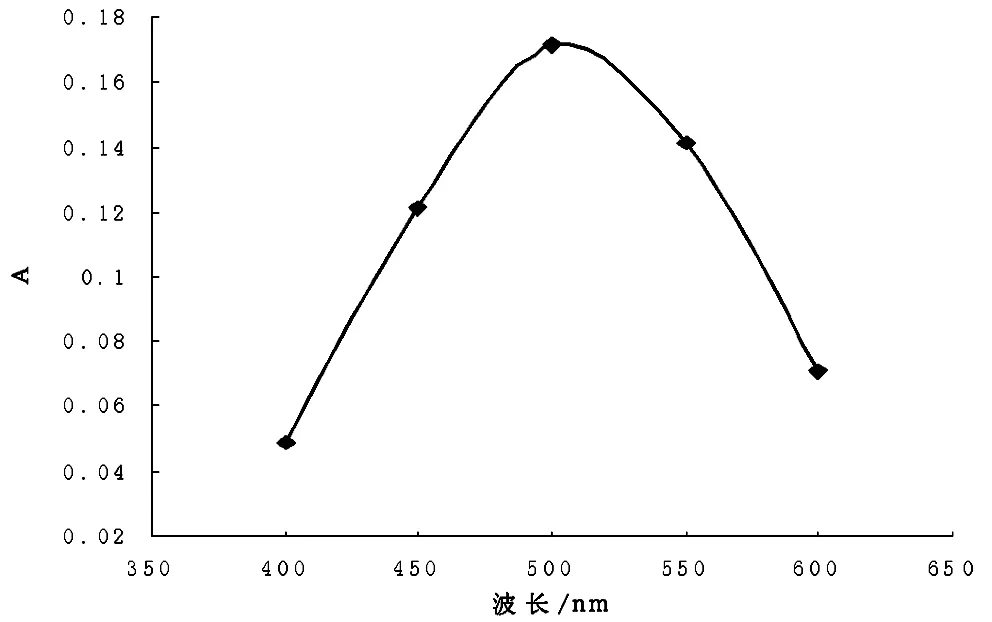
图1 Fe3-F--磺基水杨酸体系吸收光谱
3.1.2 反应时间的影响
将配制好的待测溶液按照实验方法分别放置0、 5、10、30、50、60min后测定其吸光度,测得其吸光度分别为0.170、0.171、0.170、0.172、0.171、0.170结果表明,在1h内体系吸光度基本不变化,说明Fe3+和F-的络合反应速度很快且此显色体系非常稳定。
3.1.3 显色剂用量的影响
固定Fe3+标准溶液用量,改变0.2%磺基水杨酸用量,不加F-标准溶液,按照实验方法,考察显色剂用量对体系的影响,数据见表2,以显色剂用量为横坐标,吸光度为纵坐标作图,见图2。由图可知,随着磺基水杨酸用量增加,体系的吸光度随之增大,当磺基水杨酸用量0.8~1.5mL时,体系吸光度趋于稳定,故本实验选用0.2%磺基水杨酸1.0mL。

表2 吸光度与显色剂的关系
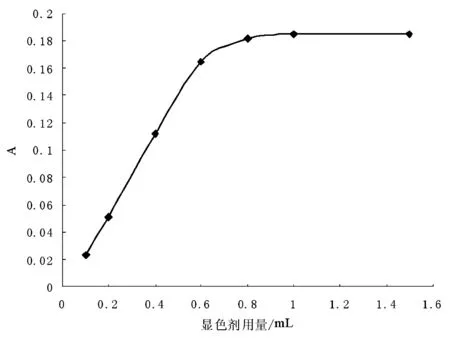
图2 显色剂用量对吸光度的影响
3.1.4 pH的影响
分别向体系中加入不同量的盐酸(0.1mol/L)和NaOH(0.1mol/L),测定其pH值和对应的吸光度,数据见表3,以pH值为横坐标,以吸光度为纵坐标作图,见图3。由图3中可见,pH值的变化对显色影响很大,随着pH值的增大,吸光度先增大后减小,当pH值控制在2.8~3.2时,显色较稳定且吸光度最高。

表3 吸光度与pH值的关系
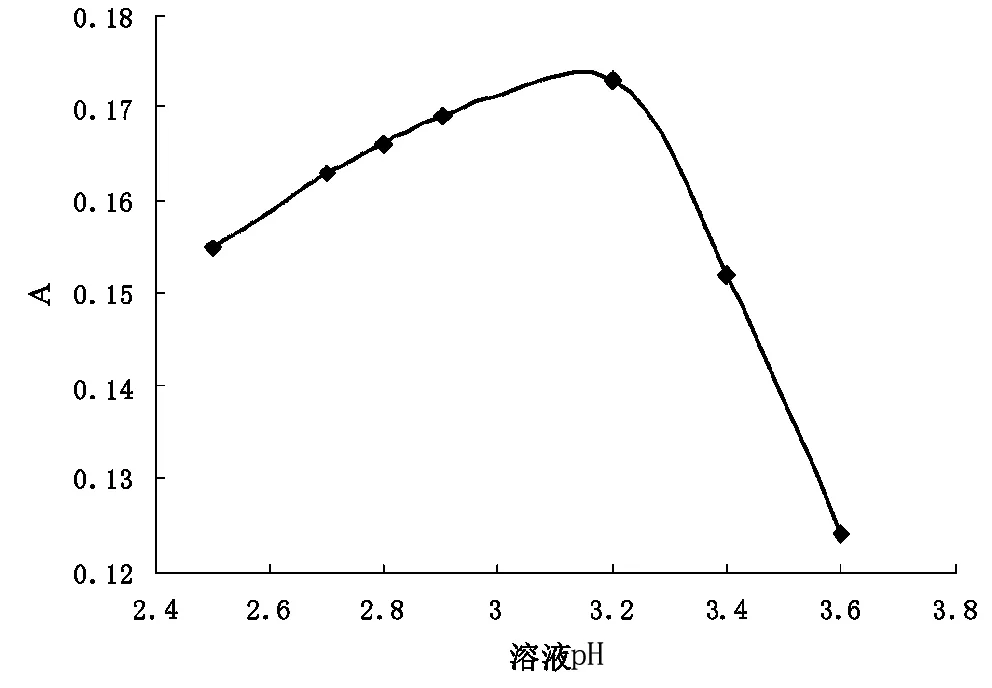
图3 体系pH值对吸光度的影响
3.1.5 干扰离子的影响
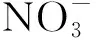
3.2 F-标准曲线回归方程
在最优条件测定体系吸光度,根据实验的方法绘制工作曲线(见下图)。结果表明氟离子质量浓度在0.4~4μg/mL范围内与A呈良好的线性关系,其线性回归方程为:A=-0.0543+0.0524c,R2=0.9844。
3.3 水样测定
移取5.00 mL 的Fe3+标准溶液,1.00 mL 0.2%磺基水杨酸于50mL的容量瓶中,加10mL的待测水样,按照上述方法测其吸光度,平行测定三次。测得其吸光度分别为0.053、0.052、0.053,参考标准曲线利用回归方程计算得本地区生活用水中的氟含量为0.68mg/L。
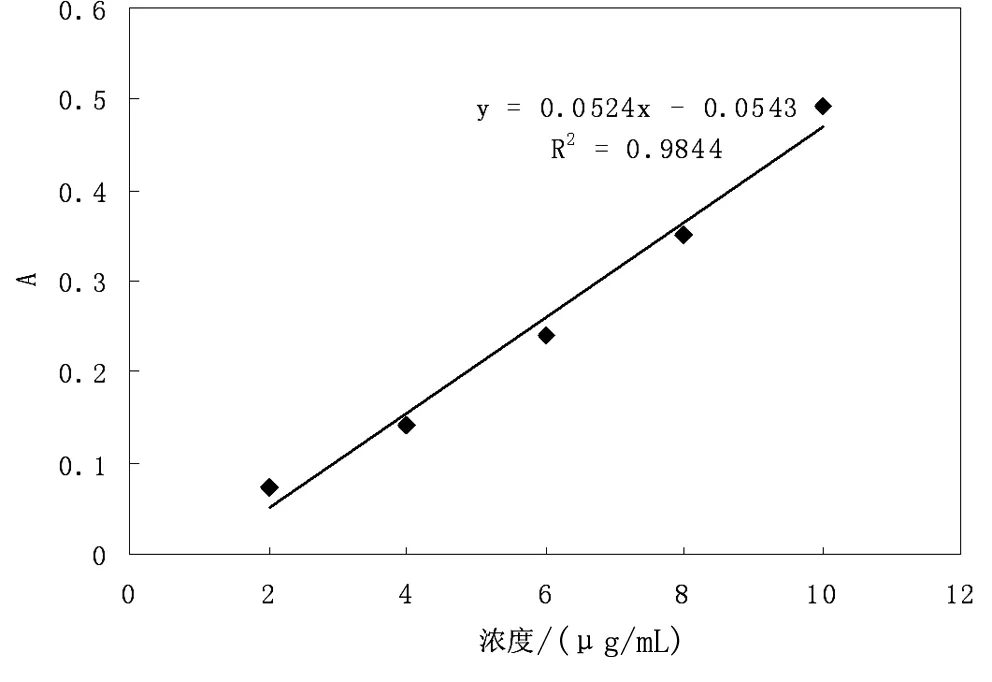
图4 标准曲线绘制
4 结论
(1)Fe3+-磺基水杨酸显色分光光度法测定水中氟离子操作简单、方便、平行性好,其方法的精密度、准确度均符合要求,可较好地应用于水中氟离子的测定。
(2)平行测定三次的水样吸光度值分别为0.053、0.052、0.053,参考标准曲线利用回归方程计算得本地区生活用水中的氟含量为0.68mg/L。(不超过国家规定的标准含量)。

