北芪五加颗粒长期毒性试验研究
赵留涛 ,吴洪银,吴冠连,陈五常,徐洪德,袁之润,吴春丽,4*
(1.郑州大学药学院,河南郑州 450001;2.商丘爱己爱牧生物科技股份有限公司,河南虞城 476300;3.郑州爱己爱牧生物技术有限公司,河南郑州 450001;4.郑州市新型兽药制剂创新重点实验室,河南郑州 450001)
北芪五加颗粒由黄芪和刺五加,经水煎煮提取,减压浓缩成浸膏,加辅料混合均匀,制成颗粒,具有益气健脾功能[1-2]。本研究在前期急性毒性试验的基础上,参照《中药、天然药物长期毒性研究技术指导原则》相关规定[3],对其长期用药的安全性进行评价。
1 材料与方法
1.1 材料
1.1.1 药品 北芪五加颗粒,批号20110203(北芪五加颗粒浸膏和北芪五加颗粒原料),规格1 g∶1 g生药,由商丘爱己爱牧生物科技股份有限公司提供。临用前用无菌水配成0.250、0.125、0.062 5 g/mL的液体。
1.1.2 实验动物 5周龄SD大鼠120只,SPF级,雌雄各半,购自河南省实验动物中心,许可证号为SCXK(豫)2010-0002。
1.1.3 主要仪器与试剂 ABX-PENTRA-80全自动血液细胞分析仪检测,法国Horiba ABX公司产品;BT-2000PLUS生化分析仪,意大利产Biotemcnica公司产品;XSP-24N型生物显微镜,南京江南光电集团股份有限公司生产;FA1004N电子天平,上海精密科学仪器公司天平仪器厂生产;YD-12P型全自动生物组织脱水机、 YD-6L型全自动生物组织冷冻包埋机、 YD-6D型全自动生物组织包埋机、 YD-B型智能型生物组织烤片机、 YD-A型智能型生物组织摊片机,浙江金华益迪医疗设备厂生产;LEICA RM2235型生物组织切片机,德国LEICA公司生产;XSP-24N型光学显微镜,南京江南光电集团股份有限公司生产;DM-BA300数码生物显微镜,厦门麦克奥迪公司生产。谷丙转氨酶(ALT)测试盒、谷草转氨酶(AST)测试盒、尿素氮(BUN)测试盒、血清(浆)尿肌酐(Cr)测试盒、总蛋白(TP)测试盒、白蛋白(ALB)测试盒、葡萄糖(GLU)测试盒和甘油三酯(TG)测试盒等,均购自南京建成生物工程研究所。
1.2 方法
1.2.1 分组及给药 选用临床健康大鼠80 只,随机分为4 个组,每组20只,雌雄各半,分笼饲养,每笼5只,用双染色法进行编号标记。由实验室前期对北芪五加颗粒原料急性毒性试验研究结果可知,以最大给药量(即67.5 g/kg 体重)给药后,小鼠未见任何异常与死亡。依据兽药研究技术指导原则汇编(2006年-2011年)中《兽药30 d和90 d喂养试验指导原则》[4]及不同种类动物间用药剂量换算公式[5-6]。猪,每kg饲料4.0 g,连用7 d,即等同于猪每天每kg体重颗粒用量0.32 g~0.4 g(相当于猪每天每kg体重用干浸膏0.04~0.05 g)。设计给药剂量,即北芪五加颗粒原料5、2.5、1.25 g/kg和空白对照组,给药各组分别以猪每日临床100、50、25倍剂量的北芪五加颗粒原料给大鼠灌胃,按20 mL/kg体重的用量,每天上午灌胃给药1次,空白对照组灌服同体积的无菌水。
1.2.2 观察指标[7-10]
1.2.2.1 一般观察 试验期间逐日观察并记录大鼠的精神状态、行为表现、采食情况、粪便。
1.2.2.2 体重影响 每周逐只称重1次,并根据体重变化调整灌胃量,连续给药28 d,观察至给药结束。
1.2.2.3 血液学及血液生化指标测定 给药第28天停药,各组末次给药 24 h后,称重、采血,用于生理和生化指标测定,血液学检查指标包括白细胞数(WBC)、红细胞数(RBC)、血红蛋白含量(HGB)、白细胞计数(WBC)及其分类[中性粒细胞(NEU)、淋巴细胞(LYM)、单核细胞(MON)、嗜酸性粒细胞(EOS)、嗜碱性粒细胞(BAS)];血液生化检查指标包括谷丙转氨酶(ALT)、谷草转氨酶(AST)、尿素氮(BUN)、肌酐(CRE)、血清白蛋白(ALB)、血葡萄糖(GLU)和甘油三酯(TG)。
1.2.2.4 剖检情况 给药第28天,将采血后的20只大鼠处死,进行系统剖检,肉眼观察其组织器官,同时取其心、肝、肾、肺、脾睾丸、卵巢、子宫等脏器进行称重,计算脏器系数。脏器系数(%)= 脏器(mg)/体重(g)×100%
1.2.3 数据分析处理 采用SPSS11.0进行统计分析,One-way ANOVA法检验,组间用LSD法两两比较,P<0.05表示差异显著,P<0.01 表示差异极显著。
2 结果
2.1 一般观察
整个试验过程中,4组大鼠精神状态、行为表现、采食情况均正常,粪便呈棕黑色颗粒状。
2.2 体重变化情况
大鼠连续灌胃给药28 d后,各给药组雌雄动物的体重及增值与对照组动物比较,除雌性小鼠2.5 g/kg给药组给药第21天体重与对照组相比体重增加且差异显著(P<0.05)外,其余各组均未见显著性差异(表1)。
2.3 血常规指标变化
大鼠灌胃给药28 d后对所有实验动物进行血液学检测。其中,雌性动物2.5 g/kg给药组RBC数较对照组极显著升高(P<0.01),雄性动物2.5 g/kg、5 g/kg给药组WBC较对照组极显著降低(P<0.01),雄性动物2.5 g/kg给药组MONO较对照组显著升高(P<0.05),其他指标均未出现统计学差异(表2)。
2.4 血液生化指标变化
大鼠灌胃给药28 d后对所有实验动物进行血液生化学检测。其中,雄性动物2.5 g/kg给药组、5 g/kg给药组TG较对照组极显著降低(P<0.01)。其他指标均未出现统计学差异(表3)。
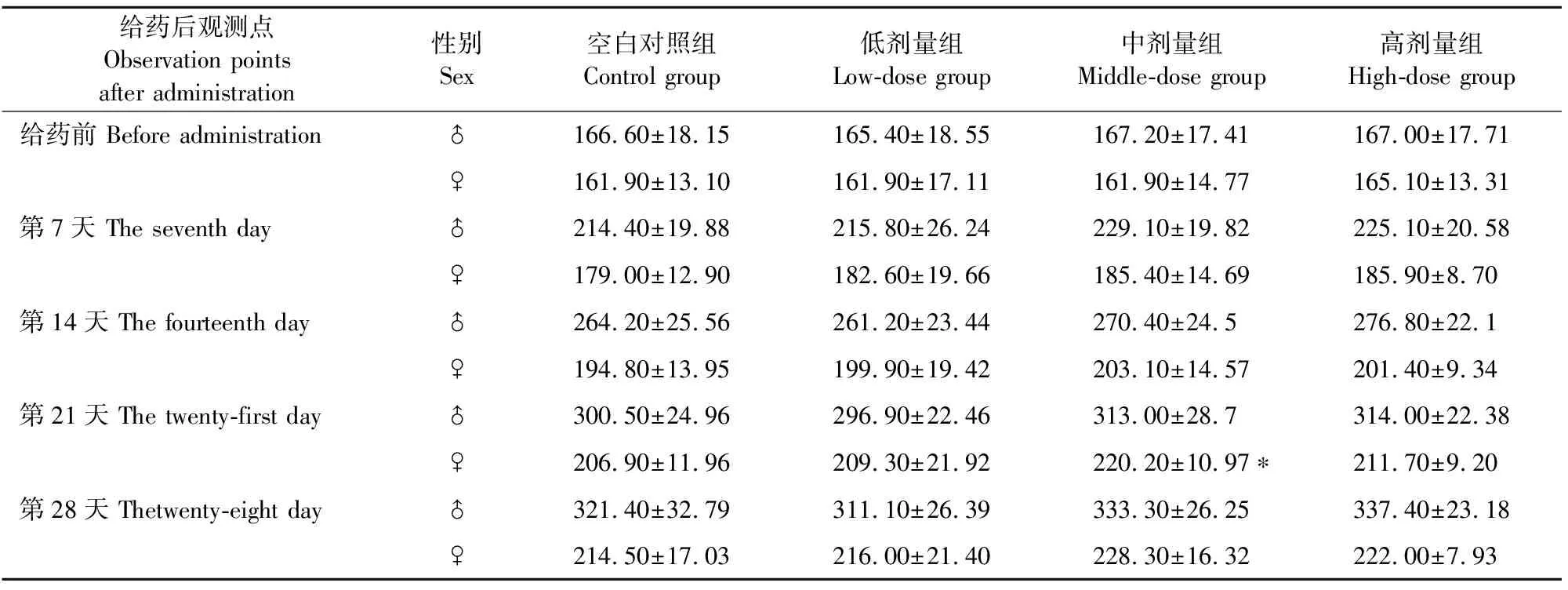
表1 北芪五加颗粒对大鼠体重的影响
注:与空白对照组相比,“*”P<0.05 差异显著。
Note:Compared with blank control group,“*”significant difference(P<0.05).

表2 北芪五加颗粒对大鼠血常规的影响
注:与空白对照组相比,“*”P<0.05 差异显著,“* *”P<0.01 差异极显著。
Note:Compared with blank control group,“*”significant difference(P<0.05); “* *”very significant difference(P<0.01).
2.5 主要脏器系数测定结果
大鼠连续给药28 d后雄性动物2.5 g/kg、5 g/kg给药组肝脏的脏器系数较对照组极显著减小(P<0.01),并呈浓度依赖性;而在雌性动物,只有5 g/kg给药组肝脏的脏器系数较对照组极显著减小(P<0.01)。其余各组均未见显著性差异(表4)。
2.6 组织病理学检查
HE染色后镜检观察,高剂量组大鼠的心、肝、脾、肺、肾与空白对照组相比,均未见与受试物毒性作用相关的组织病理学变化。
3 讨论

表3 北芪五加颗粒对大鼠血生化指标影响
注:与空白对照组相比,“* *”P<0.01 差异极显著。
Note:Compared with blank control group,“* *”very significant difference(P<0.01).

表4 北芪五加颗粒对大鼠主要脏器系数测定结果
注:与空白对照组相比,“* *”P<0.01 差异极显著。
Note:Compared with blank control group,“* *”very significant difference(P<0.01).
北芪五加颗粒原料以1.25、2.5、5 g/kg等3个剂量,连续给药28 d,试验观察期间,各组动物的精神状态、行为表现、采食、饮水、粪便均正常。其中,雌性大鼠2.5 g/kg给药组第21天体重与对照组相比有统计学差异,其余各组均无统计学差异。在血液学及血液生化学分析中显示雌性动物2.5 g/kg给药组RBC数较对照组有统计学差异,雄性动物2.5 g/kg、5 g/kg给药组WBC较对照组有统计学差异,雄性动物1.25 g/kg给药组MONO较对照组有统计学差异,雄性动物2.5 g/kg、5 g/kg给药组TG较对照组有统计学差异,这些指标改变均无剂量依赖趋势,也未超出本试验参考范围[11-13],提示该项改变与供试品毒性无关。在脏器指数检测中,肝的脏器系数高剂量组较对照组有统计学差异[14],但改变无剂量依赖关系,且病理学组织检查未见与药物毒性相关的病理改变,表明上述改变非药物毒性所致。卞愧等在五加芪粉长期毒性试验研究结果表明,五加芪粉以8.4 g/kg连续灌胃给药28 d未对大鼠产生毒副作用[15],与本研究结果一致。
综上所述,SD大鼠灌胃给予北芪五加颗粒原料以1.25、2.5、5 g/kg等3个剂量,分别是临床拟用量的25、50、100倍,连续给药28 d并未对大鼠产生毒副作用。因此,北芪五加颗粒按照推荐的给药剂量和疗程使用,无长期毒性,临床应用安全。

