RRLC-Q-TOF MS法分析鲜人参与 仙人掌果配伍发酵前后人参皂苷成分的变化
郑 飞,张 琰,韩铭鑫,乔梦丹,戴雨霖,越 皓,刘淑莹
(长春中医药大学,吉林省人参科学研究院,吉林 长春 130117)
人参是五加科植物人参(PanaxginsengC.A.Mey.)的干燥根,具有多种药理活性,广泛应用于药品、保健品和食品等领域。人参的主要有效成分是人参皂苷,根据皂苷元母核6位取代基的不同[1-5],可分为原人参二醇型和原人参三醇型人参皂苷。有研究表明,去糖基化的人参皂苷更易进入血液循环并发挥作用,药理活性和药用价值优于天然含量较高的人参皂苷Rb1、Rb2、Rc、Rd、Rg1、Re[6-7]。
仙人掌果为仙人掌科植物仙人掌的果实,果肉微酸甜,含有多糖类、黄酮类、三萜化合物等物质[8-10]。研究表明,仙人掌果具有行气活血、祛湿退热、提高免疫力、抗肿瘤、降低血糖血脂血压、清除自由基等作用[11]。
以人参和仙人掌果为原料,经发酵制得的保健酒仙参果酒,具有提高免疫力、抗疲劳、防治老年性痴呆等保健功能。在酸性和微生物发酵等条件下,人参皂苷可失去1~5个糖基,转化生成小分子质量的稀有人参皂苷,具有更好的生物利用度和药效活性。
本研究拟采用高分离度快速液相色谱-四极杆飞行时间质谱(RRLC-Q-TOF MS/MS)联用技术分析鲜人参与仙人掌果配伍发酵过程中的人参皂苷成分,鉴定其中的化合物,并进行定量分析,推测发酵过程中人参皂苷的转化规律,希望建立基于生物技术的人参配伍主要化学成分分析方法,为质量控制提供监测数据,并为药品和保健食品开发提供参考。
1 实验部分
1.1 主要仪器与试剂
Agilent Zorbax C18色谱柱(2.1 m×150 mm×3.5 μm);6520 Accurate-Mass Q-TOF LC/MS(配有电喷雾离子源ESI),Mass hunter Qualitative AnalysisB.03.01数据处理系统:美国Agilent公司产品。
仙人掌果:海南富汇达农业开发有限公司产品;人参:购于吉林省抚松县万良人参市场;人参皂苷Rh1、Rg2、F2、Rg3、Rh2、CK对照品:纯度均不低于98%,南京泽朗医药生物有限公司产品;甲醇、乙腈、甲酸:均为色谱纯,美国Tedia公司产品。
1.2 溶液的制备
1.2.1对照品溶液的制备 分别各取约10 mg人参皂苷对照品Rh1、Rg2、F2、Rg3、Rh2、CK于10 mL量瓶中,精密称定,用甲醇溶解并定容至刻度,配制成标准品储备液,备用。不同浓度的对照品溶液由储备液稀释制得。
1.2.2鲜人参和仙人掌果发酵液的制备 按照仙参果酒的制备工艺,将清洗后的鲜人参与仙人掌果分别打浆混合,经调整糖度与pH值,接种发酵,经2次发酵,过滤后灭菌灌封。
1.2.3样品溶液的制备 精密量取各10 mL 3批发酵液,平行测定,于60 ℃水浴挥干后,用10 mL水溶解,再用同体积的饱和正丁醇萃取4次,合并上清液,于60 ℃挥干,用甲醇溶解于10 mL量瓶中,稀释并定容,摇匀,待测。
1.3 实验条件
1.3.1色谱条件 色谱柱:Agilent Zorbax Eclipse Plus C18柱(2.1 m×150 mm×3.5 μm);流动相:A为0.1%甲酸水溶液,B为乙腈;梯度洗脱程序:0~5 min(15%~17%B),5~10 min(17%~19%B),10~20 min(19%~21%B),20~26 min(21%~28%B),26~37 min(28%~30%B),37~45 min(30%~36%B),45~50 min(36%~45%B),50~58 min(45%~65%B),58~60 min(65%~80%B);柱温35 ℃;流速0.3 mL/min;进样量5 μL。
1.3.2质谱条件 电喷雾负离子扫描模式(ESI-);干燥气(N2)流速9 L/min,温度300 ℃;雾化气压力2.41×105Pa;毛细管电压为3.5 kV;碎裂电压175 V;锥孔电压65 V;质量扫描范围m/z100~2 000。
2 结果与讨论
2.1 RRLC-Q-TOF MS化学成分分析
利用RRLC-Q-TOF MS/MS法对鲜人参与仙人掌果发酵前后溶液中人参皂苷成分进行比较分析,其总离子流图示于图1。RRLC可以较好地分离溶液中皂苷类化合物,高分辨质谱和串联质谱可获得化合物的分子质量和结构信息,在负离子模式一级质谱图中,人参皂苷准分子离子以[M-H]-和[M+HCOO-H]-形式存在。在相同条件下,通过对照品的保留时间、一级质谱中分子质量信息以及二级串联质谱图中碎片离子信息,可以确定皂苷的类型及结构[12]。
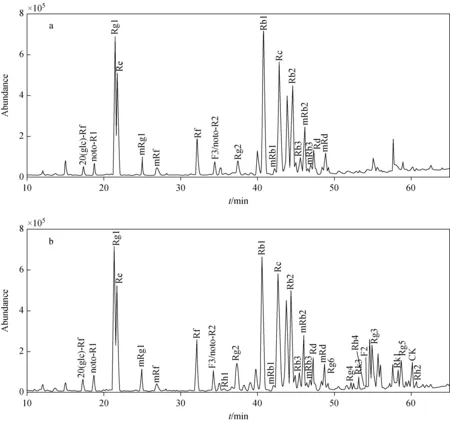
图1 鲜人参与仙人掌果发酵前(a)与发酵后(b)人参皂苷总离子流图Fig.1 Total ion chromatograms of ginsenosides before (a) and after (b) fermentation process
以人参皂苷Rb2为例,阐述人参皂苷的裂解规律。人参皂苷Rb2为原二醇型人参皂苷,其C-3位取代是2分子葡萄糖侧链,C-20位取代为1分子葡萄糖和1分子吡喃型阿拉伯糖侧链。在负离子模式下,人参皂苷Rb2主要以准分子离子[M-H]-(m/z1 077.585 1)的形式存在。在一定的碰撞能量下,[M-H]-进一步碎裂,产生相应的结构碎片信息。人参皂苷Rb2的二级串联质谱图示于图2。其中,m/z459离子是原人参二醇皂苷元的特征离子,主要碎片离子m/z945.54、783.48、621.43、459.38是m/z1 077通过丢失1分子阿拉伯糖残基(132 u)和3分子葡萄糖残基(162 u)产生的,这与文献[13-15]报道一致。由此推测,该物质为人参皂苷Rb2。使用同样的方法[16],可以推断其他人参皂苷的RRLC-MS/MS数据,结果列于表1。
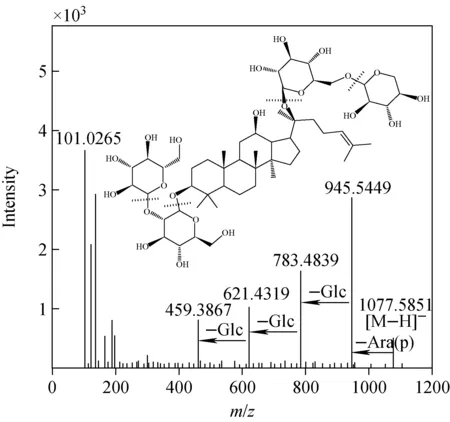
图2 人参皂苷Rb2的二级质谱图Fig.2 MS/MS spectrum of ginsenoside Rb2
由表1可知,溶液发酵前检测到19种人参皂苷,而发酵后检测到27种人参皂苷,与发酵前相比,人参皂苷Rg1、Re、Rb1、Rc的含量明显减少,人参皂苷Rb2、Rd的含量相对增加,同时生成了Rh1、Rg2、Rg4/Rg6、F2、Rk3/Rh4、Rg3、Rh2、CK、Rk1/Rg5等稀有人参皂苷。有研究报道[17-19],糖苷类化合物由于极性强、分子质量较大,口服吸收生物利用度相对较低,难以直接发挥药效作用。该类化合物在肠道中被肠道菌群代谢生成次级代谢产物或苷元,这些代谢产物可能是人参在体内发挥药效作用的活性物质。因此,本研究重点对发酵液中相对含量较高的稀有人参皂苷Rh1、Rg2、F2、Rg3、Rh2、CK进行定量分析。
2.2 方法学考察
2.2.1线性关系考察 按1.2.1节方法制备各对照品储备液,用甲醇稀释,配制成系列梯度质量浓度的对照品混合溶液。进样5 μL,记录峰面积。以峰面积(y)对分析物质浓度(x)做线性回归,绘制标准曲线,得到回归方程和相关系数,并以3倍信噪比(S/N=3)计算检测限,10倍信噪比(S/N=10)计算定量限[20],结果列于表2。
2.2.2回收率和精密度 精密吸取6份已知含量的供试品溶液,加入近似等量混标含量的对照品溶液进行含量测定。Rh1、Rg2、F2、Rg3、Rh2、CK的回收率分别为98.37%、99.57%、101.12%、100.77%、99.71%、98.80%,RSD分别为1.25%、1.35%、1.11%、1.67%、1.43%、1.25%。结果表明,该方法的回收率和精密度较好,可以满足分析要求。
2.3 样品测定
采用该方法检测自制的3批发酵液,采用外标法以峰面积进行定量分析。3批样品中人参皂苷Rh1、Rg2、F2、Rg3、Rh2、CK的平均含量分别为6.345 2、20.452 2、6.255 9、27.452 8、55.384 6、30.472 9 mg/L。
2.4 转化途径分析
2.4.1原人参二醇型人参皂苷转化途径 在发酵过程中,原二醇型人参皂苷主要有两种转化途径,示于图3。初步推断,Rb1脱掉C-20位的1分子葡萄糖、Rb2脱掉C-20位的1分子阿拉伯糖、Rb3脱掉C-20位的1分子木糖、Rc脱掉C-20位的1分子阿拉伯糖转化为Rd。第一种转化方式为:Rd脱掉C-20位的1分子葡萄糖转化为Rg3,Rg3进一步脱水转化为Rg5/Rk1;第二种转化方式为:Rd脱掉C-3位的1分子葡萄糖转化为F2,F2脱掉C-3位的1分子葡萄糖直接转化成CK,也可脱掉C-20位的1分子葡萄糖转化为Rh2。
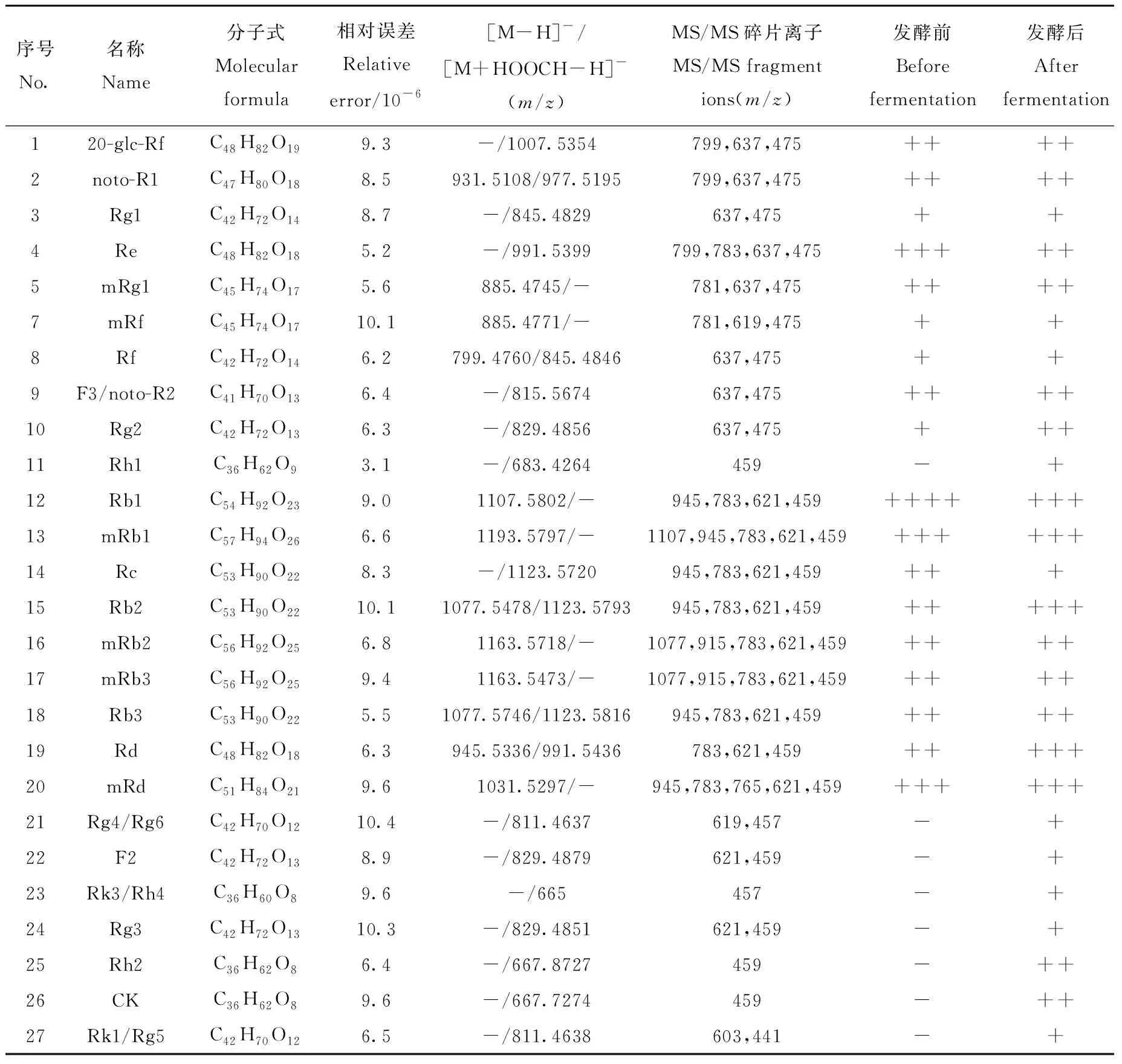
表1 鲜人参与仙人掌果发酵液中人参皂苷的MS/MS数据(n=3)Table 1 MS/MS data of ginsenosides in fermentation process of fresh ginseng and prickly pear (n=3)
注:“-”代表未检测到;“+”代表峰面积小于106;“++”代表峰面积为(1~5)×106;“+++”代表峰面积为(5~10)×106;“++++”代表峰面积为(1~5)×107
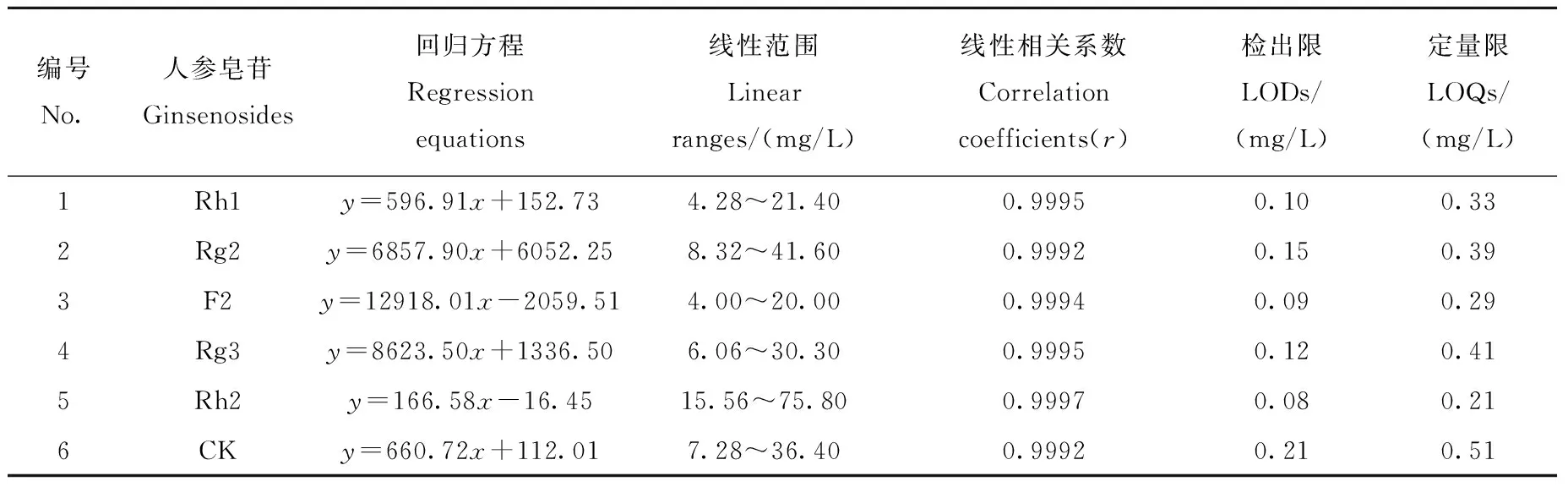
表2 人参皂苷对照品的回归方程、线性范围、线性相关系数、检出限和定量限(n=3)Table 2 Regression equations, linear ranges, correlation coefficients (r), limits of detection(LODs) and limits of quantification (LOQs) of ginsenosides (n=3)
2.4.2原人参三醇型人参皂苷转化途径 在发酵过程中,原三醇型人参皂苷主要有两种转化途径,示于图4。初步推断,人参皂苷Re脱掉C-20位的1分子葡萄糖转化为Rg2,Rg2进一步脱水转化为Rg4/Rg6;另一途径为人参皂苷Re脱掉C-6位的1分子鼠李糖转化为Rg1,Rg1继续脱掉C-20位的1分子葡萄糖转化为Rh1,Rh1进一步脱水可转化为Rk3/Rh4。
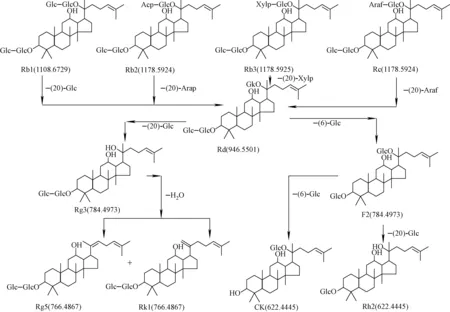
图3 发酵过程中原人参二醇型皂苷的可能转化途径Fig.3 Possible pathways of protopanaxadiol ginsenosides in fermentation process
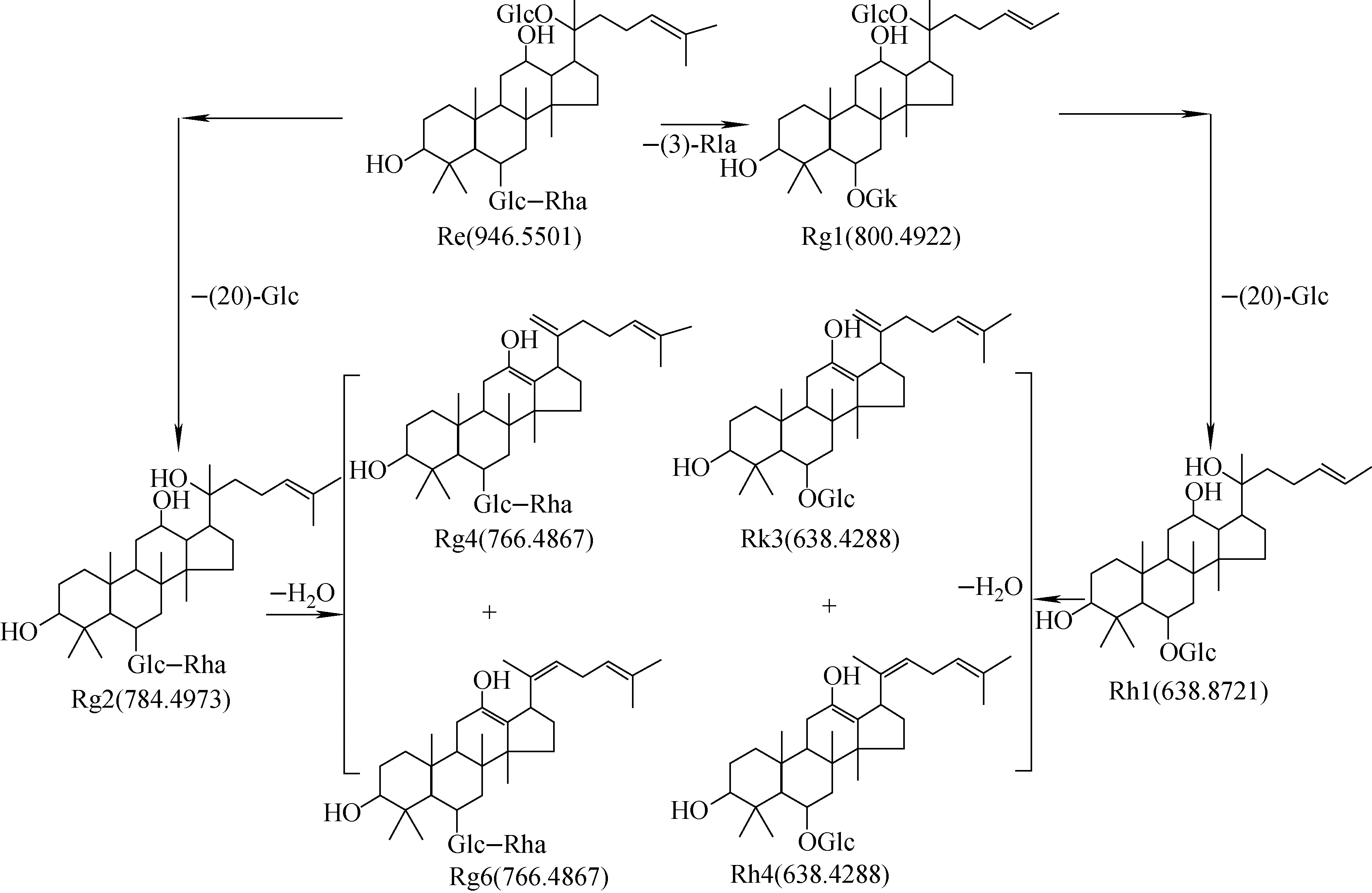
图4 发酵过程中原人参三醇型皂苷的可能转化途径Fig.4 Possible pathways of protopanaxatriol ginsenosides in fermentation process
3 结论
长白山道地药材人参和热带植物仙人掌果配伍,经发酵工艺制得保健酒仙参果酒,不仅降低了人参的燥性,同时转化生成稀有人参皂苷,提高了抗氧化、增强免疫力等活性。本研究对人参与仙人掌果配位发酵液中的人参皂苷Re、Rb1、Rg1进行测定,同时分析多种人参皂苷含量的变化及转化路径,经RRLC-Q-TOF MS/MS检测鉴定出27种人参皂苷,其中转化生成了相对含量较高的人参皂苷Rh1、Rg2、F2、Rg3、Rh2、CK,该过程中人参皂苷的转化主要是由仙人掌果为发酵体系提供了酸性条件和糖。本研究不仅为仙参果酒的功能性提供了物质基础研究,同时还可为相关产品质量标准的制订提供依据。

