由七水合硫酸亚铁制备草酸亚铁的工艺优化
姜 伟,尚煜栋,高美丽,游 越,章亚东
(郑州大学化工与能源学院,河南郑州450000)
磷酸铁锂作为锂电池正极材料,比其他尖晶石和层状正极材料更加安全,有着极为特殊的优势[1]。草酸亚铁作为合成磷酸铁锂的常用原料,目前市场上出售的草酸亚铁在纯度上并不能很好地满足磷酸铁锂合成的要求,Fe2+容易被氧化成Fe3+导致合成的磷酸铁锂的电容量下降。含杂质较多的更达不到电池级纯度的要求,而纯度达到要求的却达不到粒径的要求,粒径大的草酸亚铁固体颗粒在合成磷酸铁锂的过程中反应活性较差,也得不到优质磷酸铁锂[2-3]。所以高纯度、粒径细小均匀的草酸亚铁是合成磷酸铁锂的理想原料。本文采用FeSO4·7H2O和H2C2O4·2H2O为原料,采用沉淀法制备草酸亚铁粉体,并研究了硫酸亚铁质量分数、反应温度、陈化时间、添加剂种类及添加量对草酸亚铁粉体纯度和粒径的影响。
1 实验材料和方法
1.1 试剂
草酸(H2C2O4·2H2O)、硫酸亚铁(FeSO4·7H2O)、草酸钠、硫氰酸钾、氯化钡、聚乙二醇(200,400,600,800,1000)、N,N-二甲基甲酰胺、N,N-二甲基乙酰胺、丙三醇、1,2-丙二醇、无水乙醇、乙二醇、1-甲基-2-吡咯烷酮、高锰酸钾、浓硫酸、磷酸、盐酸,以上均为分析纯。实验用去离子水为自制。
1.2 实验流程
电池级草酸亚铁主要是以硫酸亚铁和草酸为原料,采用液相沉淀法制备,化学方程式如式(1)所示,制备流程如图 1 所示[4]。


图1 草酸亚铁的制备流程图
1.3 分析测试仪器
ASDWE型全谱型等离子体发射光谱仪、FEI Talos F200S型透射电子显微镜、Zeiss/Auriga FIB SEM型聚焦离子束扫描电子显微镜、STA 409 PC型同步热分析仪、WJL-628型激光粒度分析仪、FXB101-3型电热鼓风干燥箱、DZF-6050型真空干燥箱、TG16-WS型台式高速离心机、ZNCL-T型磁力搅拌器、DF-101S型集热式恒温加热磁力搅拌器、DFY-5/25型低温循环水浴、SHZ-D(Ⅲ)型循环水真空泵、KQ5200DB型数控超声波清洗器。
1.4 实验方法
准确称取一定质量的草酸于三口烧瓶中,向其中加入一定量的添加剂、去离子水,用水浴对反应体系加热,待其温度达到反应温度时,向其中滴加硫酸亚铁溶液,滴加完成后,继续搅拌5 min。之后将整个体系置于90℃的水浴中陈化一定时间。经离心、洗涤、干燥得到草酸亚铁产品。
1.5 草酸亚铁合成的工艺优化实验
1.5.1 单因素实验
通过改变添加剂的种类及添加量、硫酸亚铁质量分数、反应温度、陈化时间得到不同的草酸亚铁产品。
1.5.2 响应面优化实验
根据单因素实验的结论,利用数学分析软件Design-Expert 8.0.6 的 Box-Behnken 实验设计[5],选取乙二醇添加量、陈化时间、反应温度和硫酸亚铁质量分数4个因素,考察各因素间的交互作用对产品纯度和粒径的影响,以纯度为响应值1,粒径为响应值2,设计4因素3水平的响应面实验,因素水平见表1(添加剂种类为单因素确定的最适宜的添加剂,即乙二醇)。对响应面分析得到的预测最优条件进行实验验证,进行平行实验3次,分析产品纯度和测量产品粒径,并与预测值比较。
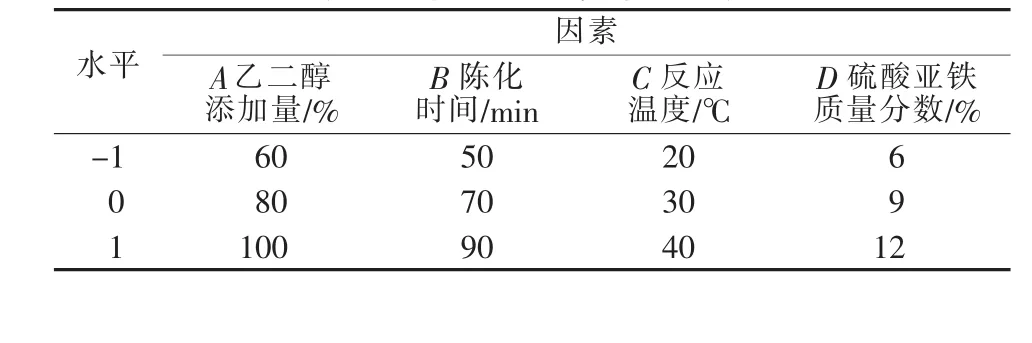
表1 响应面因素与水平表
2 实验结果与讨论
2.1 单因素实验
2.1.1 添加剂种类对产品纯度和粒径的影响
在硫酸亚铁质量分数为9%、反应温度为30℃、陈化时间为70 min的条件下,考察了添加剂种类对产品纯度和粒径的影响,结果如表2所示。
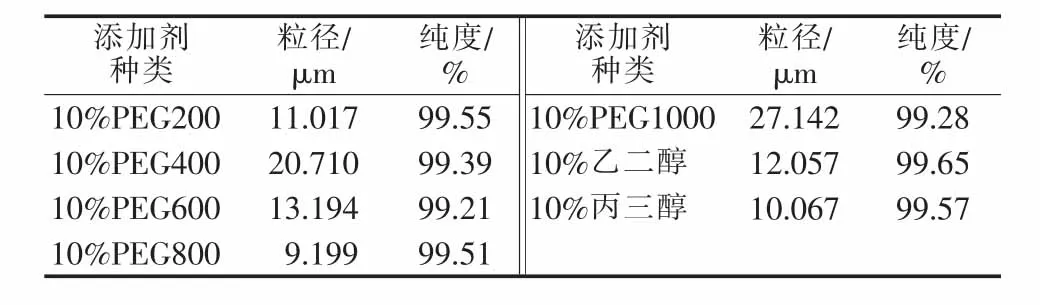
表2 添加剂种类对产品纯度、粒径的影响
综合考虑表 2的两个指标,选择 PEG200、PEG800、乙二醇和丙三醇作为表面活性剂进行下一轮的实验,结果如表3所示。由表3可知,当添加剂为100%乙二醇时,产品粒径可达1.956 μm,纯度为99.63%。故,本实验选用乙二醇作为添加剂。

表3 添加剂种类对产品纯度、粒径的影响
2.1.2 其他反应条件对产品纯度和粒径的影响
考察陈化时间、反应温度、乙二醇添加量和硫酸亚铁质量分数对产品纯度、粒径的影响,实验结果如图2所示。

图2 陈化时间(a)、反应温度(b)、乙二醇添加量(c)和硫酸亚铁质量分数(d)对产品纯度、粒径的影响
由图2a可知,随着陈化时间的增加,产品的纯度先逐渐增加后略微减小,70 min以后,随着陈化时间的增加,产品纯度有所减小,这可能是由于材料制备过程中,陈化作用可促进晶粒的生长和二次成核的发生,减小了比表面积,有助于减少由于共沉淀及表面吸附带来的杂质,从而增加了材料纯度,但是陈化时间过长,被氧化的可能性逐渐增加,导致产品纯度下降。而且由实验数据可知,随着陈化时间的增加,产品粒径先减小后增大,这可能是由于刚开始陈化的时候,产品还不稳定,导致产品粒径大小分布不均匀,随着陈化时间的增加产品逐渐形成稳定的晶形,产品粒径逐渐减小,但是随着陈化时间的继续增加,晶体开始聚集,二次成核等导致产品粒径增加。
由图2b可见,随着温度的增加纯度先增加后减小,这可能是由于温度的增加,Fe2+和C2O42-之间反应加快,减少了副反应的发生,草酸亚铁纯度增加,当温度升高到30℃以后,由于温度过高,加速了离子迁移和晶体生长,副反应的活化能同样被降低,导致副反应反而增加,草酸亚铁纯度下降。粒径随着反应温度的增加先增加后减小,这可能是由于温度的增加降低了离子反应扩散活化能,加快了化学反应速率与晶核生长速率,使得晶粒生长速率要强于形核速率,致使颗粒粒径增加,但是温度超过35℃,粒径呈现下降趋势。这可能是由于温度继续增加,使得分子运动碰撞加剧,在碰撞过程中使得晶体颗粒变小。
由图2c可知,随着乙二醇添加量的增加,产品纯度先减小后增加再减小,粒径基本呈现出减小趋势,在乙二醇添加量增加到80%后继续增加乙二醇添加量,粒径减小不明显而产品纯度却大幅下降。
由图2d可知,随着硫酸亚铁质量分数的增加,产品的纯度先增加后减小,这可能是由于较高浓度的硫酸亚铁会促进晶核的生长,使得晶体容错量增加,导致生成的草酸亚铁纯度偏低。而低浓度情况下草酸亚铁可能因为溶液量较大,Fe2+被氧化的几率增加,导致纯度下降。粒径在硫酸亚铁质量分数为9%~12%时快速增加,这可能是由于硫酸亚铁质量分数的增加促进了晶核的成长,但浓度比较低的时候影响不大,随着硫酸亚铁质量分数的继续增大,较高的浓度又开始抑制晶核的成长,所以颗粒变小。
2.2 响应面实验结果
2.2.1 实验结果
综合单因素实验结果选取硫酸亚铁质量分数、反应温度、陈化时间、乙二醇添加量这4个对产品纯度和粒径影响较大的因素,分析它们交互作用对产品纯度和粒径的影响。采用4因素3水平的响应面分析方法,选用Box-Behnken模型进行实验设计,响应面实验方案与结果见表4。表4中,第4、14、25、28、29号为中心(零点)实验,其余24组为析因实验。零点实验共计重复5次,用以计算实验随机误差。根据实验结果,利用Design-Expert 8.0.6软件对所得数据进行方差分析,结果见表5和表6。
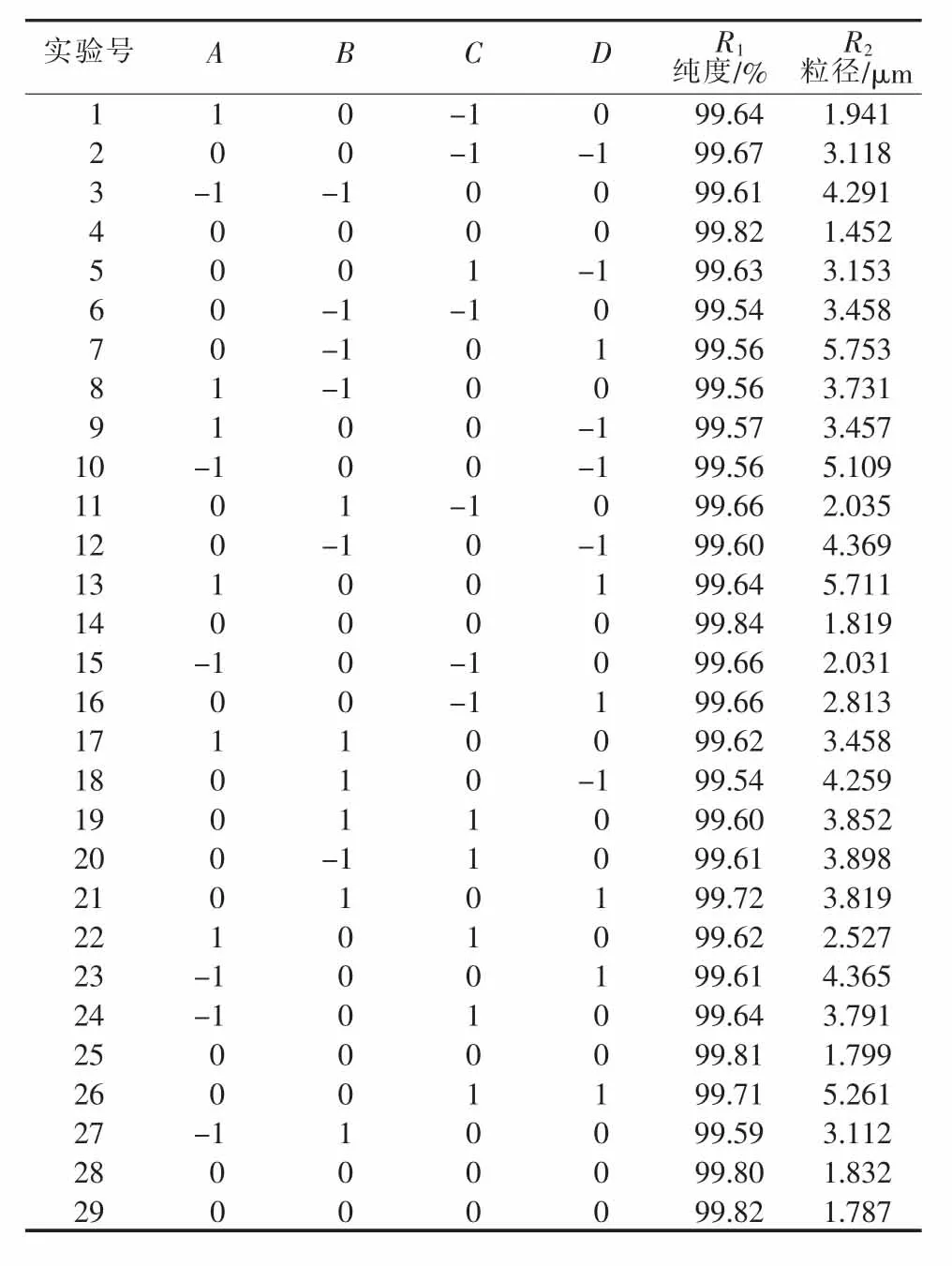
表4 响应面实验方案与结果
2.2.2 以纯度为导向的响应面分析
1)方差分析。响应面方差分析结果见表5。4个因素经过拟合得到R1(纯度)的二次多元回归方程为:
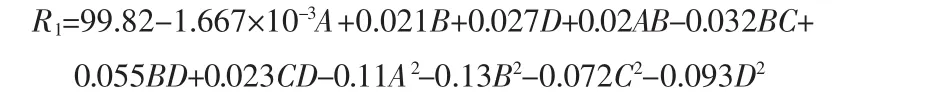
该二次多项式回归模型的F值为26.55,P<0.000 1,达到了极显著水平,证明该模型可以很好地描述各个变量与响应值之间的变化关系。相关系数R12=0.963 7,说明草酸亚铁纯度的实验值与利用该方程得到的预测值非常接近,拟合程度很高。同时方程的失拟项远未达到显著水平,因此可用该回归方程代替实验真实点对结果进行分析和预测[6]。从分析中还可看出一次项B、D差异均达到显著水平。在所确定的实验水平范围内,各因素对响应值的影响程度顺序为:D>B>A=C,即硫酸亚铁质量分数的影响>陈化时间的影响>乙二醇添加量的影响=反应温度的影响。4个因素中陈化时间和反应温度之间及陈化时间和硫酸亚铁质量分数之间有显著的交互作用。

表5 响应面方差分析
2)各因素交互的响应面分析。纯度为响应值的响应曲面图见图3。由图3可知,硫酸亚铁质量分数与陈化时间的交互作用对产品纯度的影响最为显著,体现为三维响应面图中曲面的弯曲程度较大、曲线较陡[7-8],三维图底部的等高线呈椭圆形;硫酸亚铁质量分数和乙二醇添加量、反应温度的交互作用次强;而乙二醇添加量与反应温度的交互作用最弱,表现为三维响应曲面较为平缓,底部等高线接近正圆形[7]。利用拟合方程确定最佳工艺条件的方法如下:对回归方程的各个因素均取一阶偏导数为0,联立即可求得产品纯度达到最高时所需的参数条件。最佳工艺条件为 A=0.8、B=72.52、C=29.88、D=0.095,即,乙二醇添加量为80%、陈化时间为72.52 min、反应温度为29.88℃、硫酸亚铁质量分数为9.5%,预测产品纯度达到99.82%。
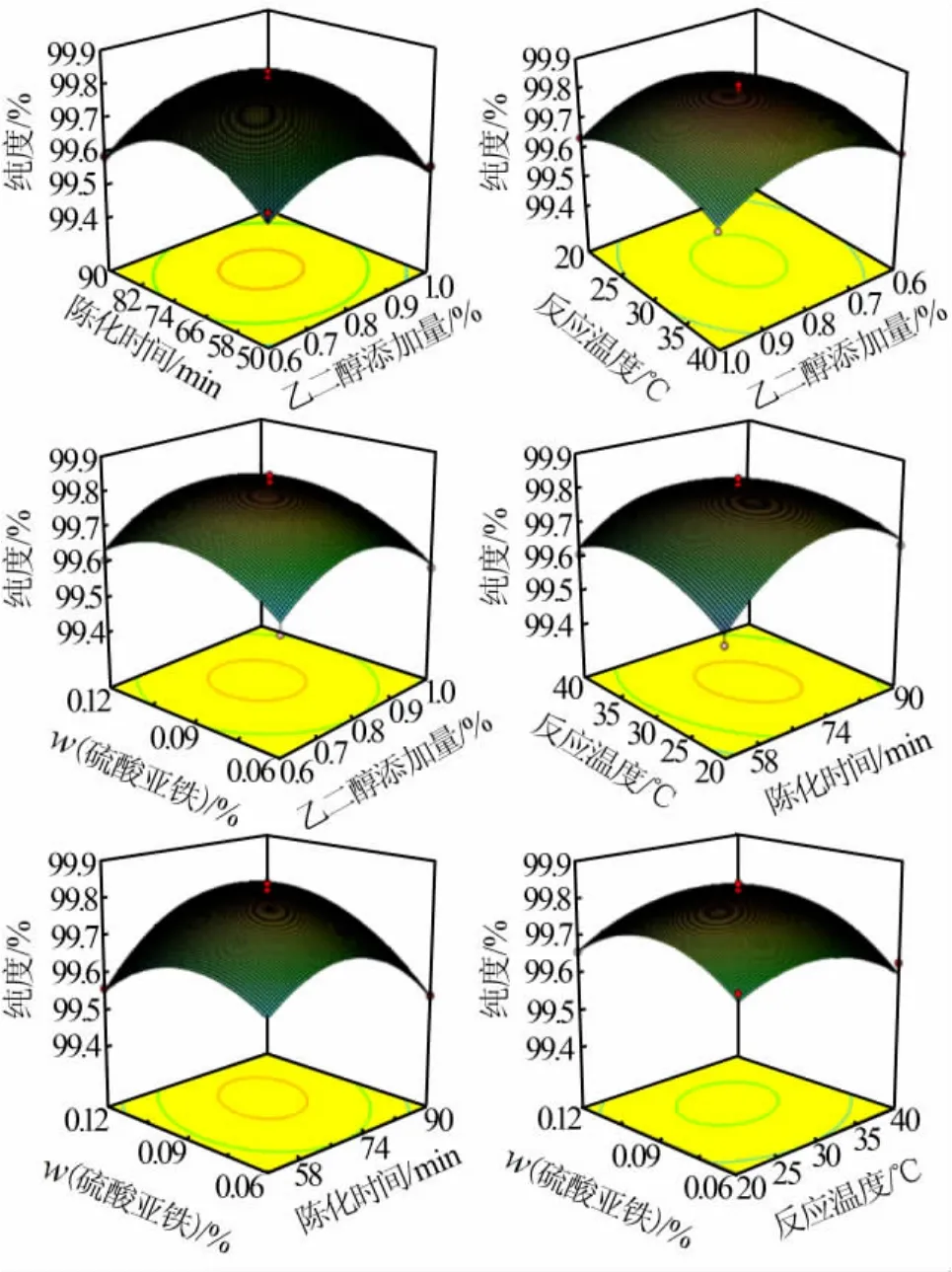
图3 纯度为响应值响应曲面图
2.2.3 以粒径为导向的响应面分析
1)方差分析。响应面方差分析结果见表6。同纯度分析,可得R2(粒径)的二次多元回归方程为:

并且可看出一次项C差异达到极显著水平,B、D达到显著水平。在所确定的实验水平范围内,各因素对响应值的影响程度顺序为:C>B>D>A,即反应温度>陈化时间>硫酸亚铁质量分数>乙二醇添加量。4个因素中硫酸亚铁质量分数和其他3个因素交互作用显著,反应温度和陈化时间交互作用显著。
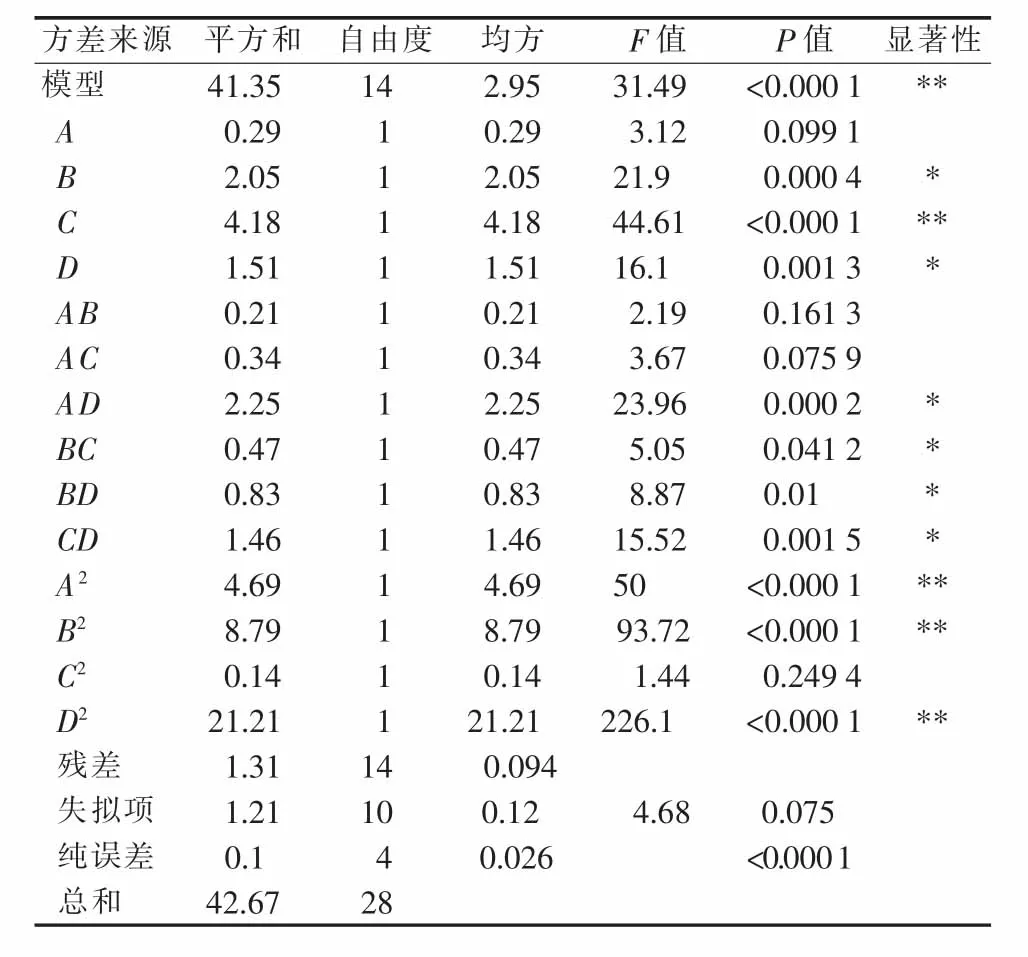
表6 响应面方差分析
2)各因素交互的响应面分析。各因素间的相互作用由图4可以看出。利用拟合方程确定最佳工艺条件的方法如下:对回归方程的各个因素均取一阶偏导数为0,联立即可求得产品粒径达到最小时所需的参数条件。最佳工艺条件为A=0.76、B=77.5、C=20、D=0.095,即,乙二醇添加量为76%、陈化时间为77.5 min、反应温度为20℃、硫酸亚铁质量分数为9.5%,预测产品粒径达到1.116 μm。
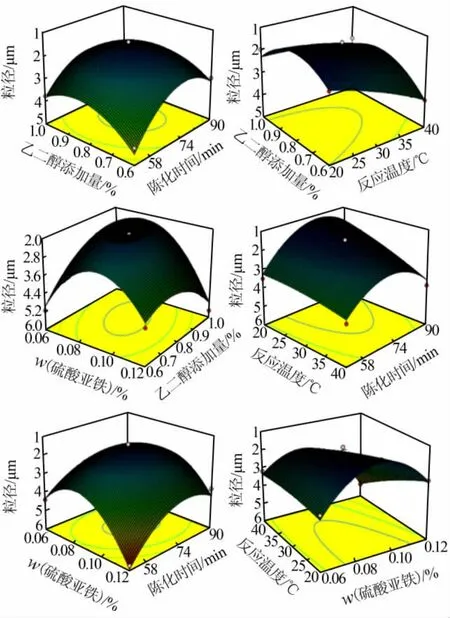
图4 粒径为响应值响应曲面图
2.2.4 实验结果的验证
由于产品要从两方面指标考虑,所以综合考虑两方面原因,所得到的工艺参数条件为A=0.8、B=73.47、C=26.88、D=0.092,即,乙二醇添加量为 80%、陈化时间为73.47 min、反应温度为26.88℃、硫酸亚铁质量分数为9.2%,预测产品的纯度为99.81%,粒径为1.523 μm。验证实验过程中,考虑到所用仪器设备所能达到的条件控制精度水平和操作方便,在验证实验中将参数条件修正为乙二醇添加量为80%、陈化时间为73 min、反应温度为27℃、硫酸亚铁质量分数为9%进行3次验证实验,实际测得产品平均纯度为99.80%,产品平均粒径为1.527 μm。由此可见,采用响应面法优化得到的合成草酸亚铁的参数准确可靠,具有一定应用价值。
2.3 产品的表征
2.3.1 TG-DSC和XRD表征
对响应面优化得到的最优条件下制得的产品进行分析,分析结果如图5所示。由图5a可知,产品为FeC2O4·2H2O,且产品失重分为两个阶段,第一阶段为二水合草酸亚铁失去两个结晶水,其反应方程式如式(2)所示,理论质量损失率为20%,实际质量损失率为20.19%,可以证明产品含有两个结晶水[9]。

第二阶段是草酸亚铁氧化分解,其反应方程式如式(3)所示,其理论质量损失率为35.57%,实际质量损失率为35.30%。
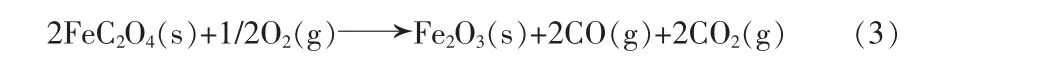
由图5a中的DSC曲线可知,在160~200℃时,草酸亚铁样品失去结晶水时吸收热量;在200~270℃时,草酸亚铁分解的第二阶段是放热过程。
XRD分析如图5b所示,乙醇(ET)和乙二醇(EG)作为添加剂制备的草酸亚铁,其衍射峰可与草酸亚铁标准卡JCPDS NO.72-1305对应,检测的峰强度大,证明草酸亚铁产品结晶良好,结晶度高;无杂质峰出现,证明产品纯度高[10]。并且可知,当乙二醇作为添加剂时,其峰强度大,证明其结晶度更高(与乙醇作为添加剂制得产品相比)。

图5 草酸亚铁的TG-DSC图(a)和XRD图(b)
2.3.2 ICP-AES分析
采用电感耦合等离子体发射光谱仪分析产品中杂质离子含量,其结果如表7所示。由表7可知,产品中杂质阳离子质量分数<0.05%[11]。

表7 杂质离子含量
2.3.3 样品的形态分析
图6a、b分别为草酸亚铁产品的SEM、TEM照片。由图6可见,产品为长棒状,表面较为光滑。

图6 草酸亚铁的SEM图(a)和TEM图(b)
3 结论
1)研究采用草酸和硫酸亚铁为原料,制备得到电池级草酸亚铁。该合成方法简单,操作简便,无废气排放。2)乙二醇作为添加剂可以有效降低草酸亚铁产品粒径。3)草酸亚铁制备的优化工艺条件为:乙二醇添加量为80%、陈化时间为73 min、反应温度为27℃、硫酸亚铁质量分数为9%。在这一条件下制备的草酸亚铁产品纯度为99.80%,粒径为1.523 μm,优于目前工业生产中的产品纯度和粒径。

