腹腔镜与开放手术治疗腹股沟嵌顿疝的比较研究
储修峰,徐妙军,吴志明,孟兴成,黄洪军
(1.绍兴市中心医院,浙江 绍兴,312030;2.绍兴市人民医院)
腹股沟嵌顿疝是外科常见的急腹症,手法还纳失败的患者需急诊手术治疗。由于腹股沟嵌顿疝的血运障碍、菌群移位,传统开放手术前入路手术区域容易被污染或感染,如行补片修补,存在较大风险,如发生补片感染,容易导致医疗纠纷,因此一度被认为是补片修补的相对禁忌证[1]。但不放置补片,术后复发率较高,常需二期行无张力修补术,同时部分患者麻醉后嵌顿疝内容物可自行还纳腹腔,无法更好地判断嵌顿内容物的生机,具有一定的漏/误诊率。鉴于腹腔镜技术在疝外科领域的广泛应用[2],越来越多的外科医师开始尝试采用腹腔镜技术治疗腹股沟嵌顿疝,目前临床报道逐渐增多,但尚存有一定争议[3]。本文通过回顾分析绍兴地区两家三级综合性医院采用腹腔镜及传统开放手术治疗115例腹股沟嵌顿疝的治疗经验,进一步探讨腹腔镜技术治疗腹股沟嵌顿疝的可行性、安全性及优势。
1 资料与方法
1.1 临床资料 回顾分析2012年4月至2017年12月绍兴市中心医院普通外科及绍兴市人民医院疝血管外科收治的115例腹股沟嵌顿疝患者的临床资料,根据手术方式将患者分为腔镜组与开放组。腔镜组入选标准:(1)无全麻及腹腔镜手术禁忌证;(2)嵌顿时间相对较短,术前无明显嵌顿疝内容物坏死及腹股沟区局部或腹腔内感染征象;(3)充分告知患者相关手术风险,尤其一期补片植入风险,患者及家属均同意行腹腔镜手术,并上报医院伦理委员会及医务科批准通过。腔镜组57例,28~75岁。开放组58例,35~79岁。两组患者性别构成、年龄及嵌顿时间差异无统计学意义,见表1。根据是否一期植入补片修补,另分为数个亚组,腔镜组中包括:(1)经腹腹膜前疝修补术(transabdominal preperitoneal,TAPP):顺利完成腹腔镜探查嵌顿松解及一期TAPP;部分麻醉后嵌顿疝复位成功的患者,可先行腹腔镜全腹膜外疝修补术(totally extraperitoneal,TEP),再入腹探查;(2)高位结扎组:完成腹腔镜探查嵌顿松解,联合脐下小切口切除坏死疝内容物,腔镜下单纯疝囊高位缝扎或仅行腹腔镜下嵌顿松解+疝囊高位缝扎;(3)TAPP修补+肠管切除:顺利完成腹腔镜探查嵌顿松解及一期TAPP,再次探查发现肠管生机异常,联合脐下方小切口切除坏死疝内容物。开放组:(1)一期修补组:传统开放嵌顿松解,污染较轻,行一期无张力修补;(2)高位结扎组:污染较重的患者,仅行嵌顿松解+疝囊高位结扎,必要时附加坏死疝内容物切除。
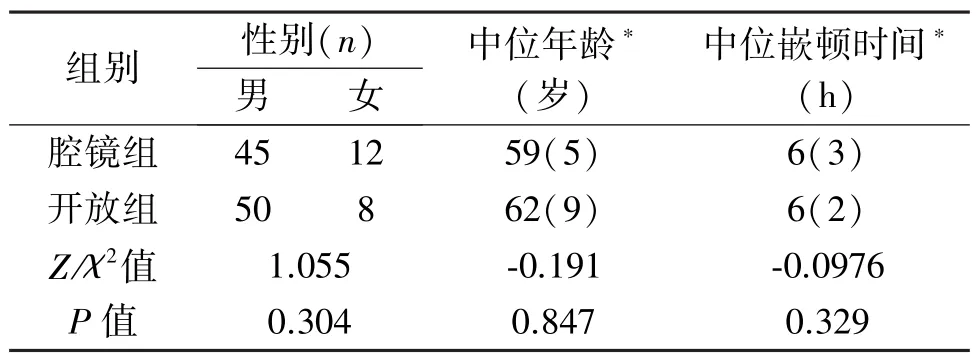
表1 两组患者临床资料的比较
(四分位数间距表示),检验采用非参数Mann-Whitney U检验
1.2 手术方法 腔镜组:全身麻醉,患者取头低脚高患侧偏高位。借助全麻的镇静与良好肌松,先对嵌顿疝内容物行手法复位。嵌顿复位成功且嵌顿时间较短的患者,行常规TEP,采用“中线位”三切口布局,分离腹膜外间隙,完整剥离疝囊,精索充分腹壁化,用大网孔补片完整覆盖耻骨肌孔区域修补(腔镜下修补网片均使用3D Max轻量网片),修补后腹腔镜自脐孔重新入腹,探查嵌顿疝内容物生机及有无对侧疝,如有肠管坏死,则辅助脐下方小切口行开放切除。未能复位的患者,脐孔下缘穿刺10 mm Trocar,建立气腹,分别于两侧腹直肌外侧缘穿刺5 mm Trocar。通过“内拉外推法”复位疝内容物(图1);嵌顿紧密,经上述操作仍不能还纳的患者,则需于内环口外侧(以免损伤腹壁下动脉)或股环的内侧(避免损伤股静脉)用电钩松解内环口,回纳嵌顿肠管。嵌顿肠管回纳后行腹腔探查,判断嵌顿肠管的生机,如肠管生机尚可,直接行TAPP,术毕再次探查肠管生机,盆腔内放置引流管一根,并借助患侧操作孔Trocar于皮下腹膜外潜行放置负压引流管;肠管已明确不可逆坏死的患者,则辅助脐下小切口切除肠管,镜下缝合内环口,不再行TAPP;对于肠管生机可疑者,肠管置于盆腔内,向盆腔内注入适量温生理盐水,浸泡嵌顿肠管15~20 min(图2),吸尽腹腔内液体,如仍有可疑,则辅助小切口切除肠管,腹腔镜下缝合内环口,不再行TAPP;如肠管生机较前有恢复迹象,则先行TAPP(图3),继续观察肠管生机,待术末再次探查观察肠管生机(图4),如肠管生机可,留置腹腔引流管及腹膜外引流管;如此时肠管生机仍感不佳,则经脐下辅助小切口开放切除坏死肠管,留置盆腔及腹膜外引流管。部分年老体弱或合并糖尿病,有化疗史、慢性肝病及长期口服激素等免疫力低下的患者,虽然肠管生机尚可,无需行肠管切除,仅行腹腔镜下内环口缝合,不再行TAPP。围手术期常规使用广谱抗生素。开放组:常规开放入路,松解嵌顿,探查肠管生机,如肠管生机可、污染轻,则行李金斯坦修补;部分年老体弱或合并糖尿病、免疫力低下的患者,虽经探查肠管生机尚可,无需行肠管切除,但为安全起见,亦单纯行内环口高位结扎,不再行无张力修补;对于肠管生机欠佳、经观察生机不可逆或明确坏死的患者,则行坏死肠管切除、内环口高位缝扎术。围手术期常规使用广谱抗生素。
1.3 统计学处理 采用SPSS 22.0软件进行数据分析。年龄、嵌顿时间不符合正态分布,采用中位数(四分位数间距表示),采用的Mann-Whitney U非参数检验。其他计量资料组间比较采用t检验。计数资料以百分率(%)表示,采用χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
2 结 果
腔镜组57例均顺利完成腹腔镜手术,部分需切除肠管者,行辅助小切口切除,其中TAPP组:38例顺利完成腹腔镜探查嵌顿松解及一期TAPP修补,5例麻醉后嵌顿疝复位成功的患者,先行TEP修补,再入腹探查;腔镜高位结扎组:17例先完成腹腔镜探查,2例经脐下方辅助小切口切除坏死疝内容物、腔镜下单纯疝囊高位缝扎,另15例仅行腹腔镜下嵌顿松解+疝囊高位结扎;TAPP修补+肠管切除组:2例顺利完成腹腔镜探查嵌顿松解及一期TAPP修补,再次探查肠管生机异常,经辅助小切口坏死肠管切除。开放组中一期修补组:30例行传统开放嵌顿松解,污染较轻,行一期李金斯坦式无张力修补;高位结扎组:28例先行传统开放嵌顿松解,6例内容物坏死或生机可疑,行坏死疝内容物切除,疝囊高位结扎;另22例行嵌顿松解+疝囊高位结扎。
腔镜组脐下方辅助切口感染1例;开放组漏诊误诊3例(其中肠坏死漏诊1例,合并股疝漏诊2例)。腔镜组补片植入率高于开放组,术后复发率低于开放组;切口感染率、补片感染率及漏诊/误诊率两组差异无统计学意义。见表2。
各亚组间相比,一期补片植入的患者中,腔镜组与开放组切口感染、补片感染、术后复发率、漏诊/误诊率差异无统计学意义;未采用一期补片植入的患者中,腔镜组与开放组切口感染率、肠切除率、术后复发率、漏诊/误诊率差异亦无统计学意义。见表3、表4。
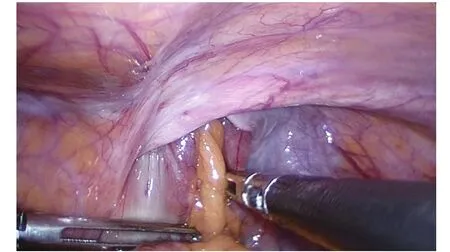
图1 “内拉外推法”复位疝内容物
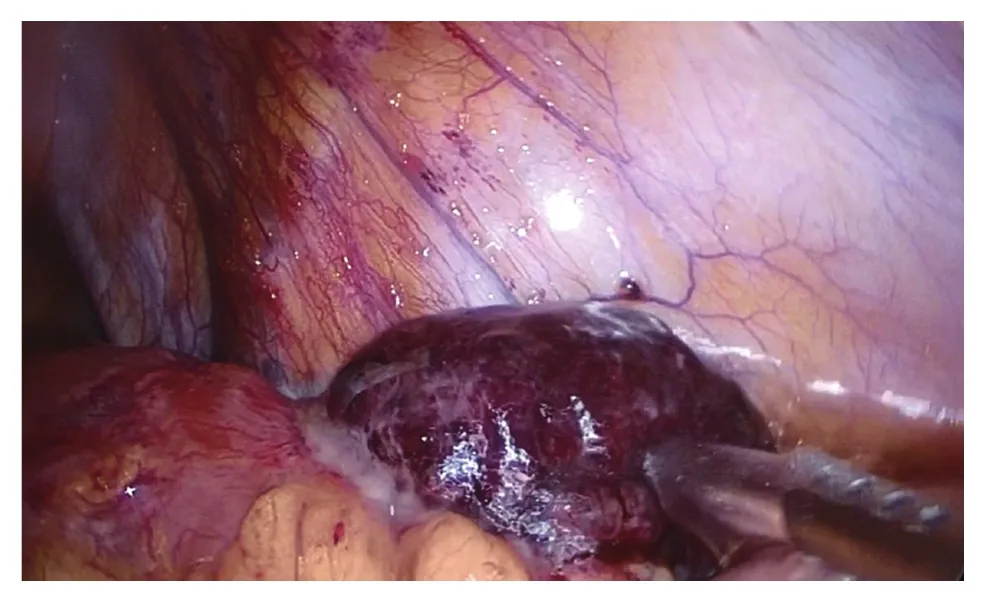
图2 温水浸泡观察肠管生机
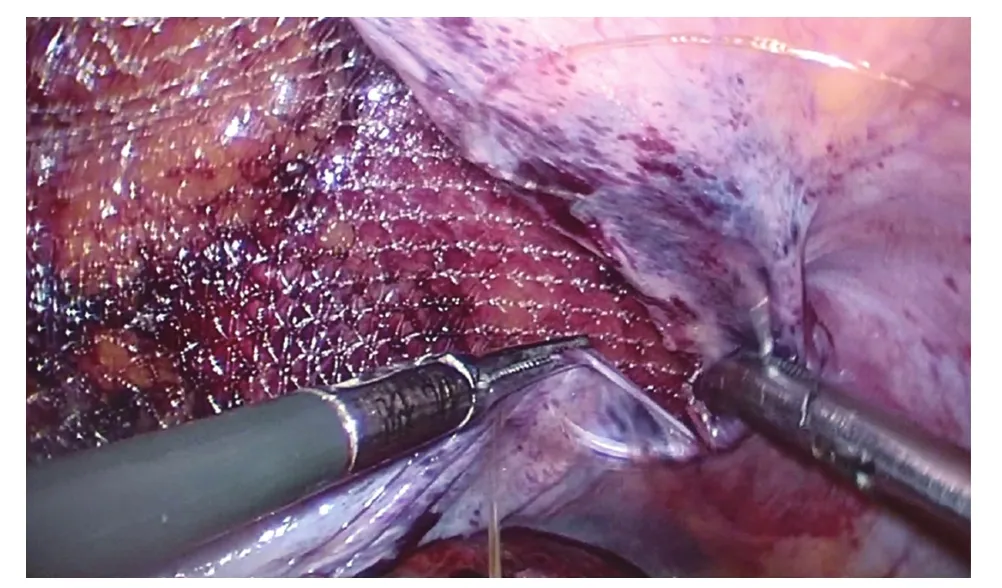
图3 TAPP修补
图4 TAPP术毕再次探查肠管生机
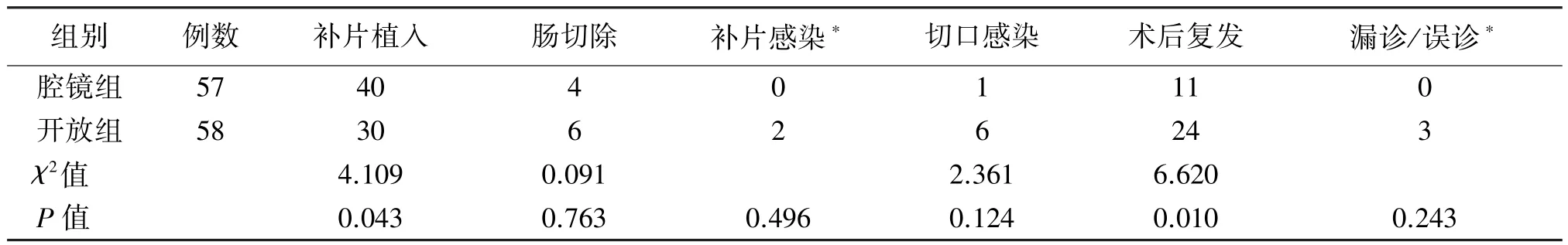
表2 两组患者手术相关指标的比较(n)
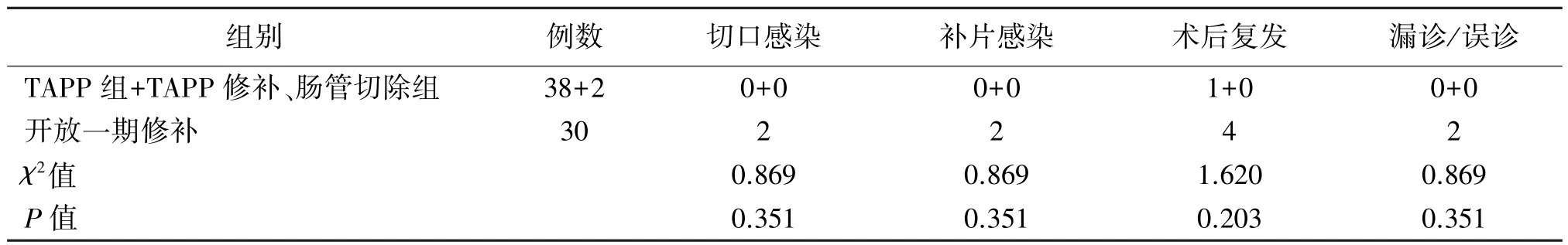
表3 补片植入患者亚组间手术相关指标的比较(n)
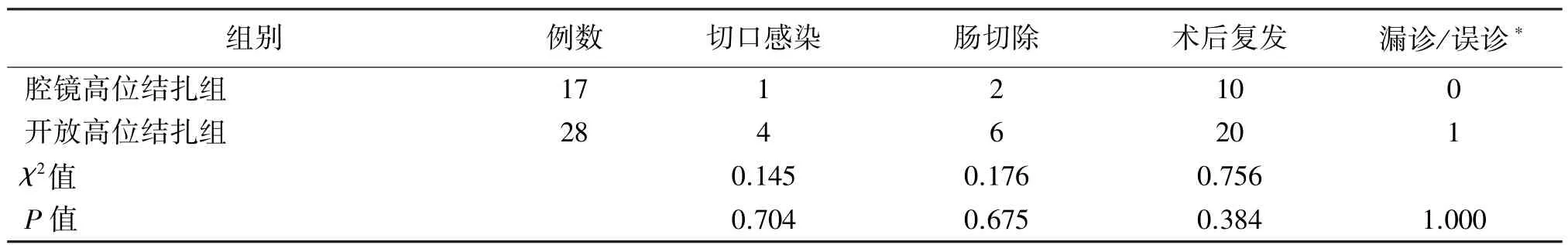
表4 未行补片植入的患者亚组间手术相关指标的比较(n)
3 讨 论
尽管我国《成人腹股沟疝诊疗指南(2014年版)》中明确指出:在污染的情况下不建议使用合成修补材料[1]。但近年越来越多的文献报道,在污染可控的情况下,使用一期补片修补安全可行,Elsebae等[4]报道了Lichtenstein术式与Bassini术式治疗腹股沟嵌顿疝的对比研究,二者术后切口感染、补片感染的发生率差异无统计学意义,但补片修补术具有复发率较低的优势。从临床实践角度分析,腹腔镜技术治疗腹股沟嵌顿疝,补片使用的指征明显较宽,目前国内外亦有越来越多的文献报道成功实施腹腔镜下一期补片修补治疗嵌顿疝[5-6]。Deeba等[7]对2009年报道的7篇关于LIHR治疗嵌顿疝的文献进行了Meta分析,共计报道328例患者,6例中转,17例行肠切除,结果表面嵌顿疝急诊腹腔镜手术在手术时间、并发症发生率及住院时间等方面均与开放手术差异无统计学意义。关于一期补片植入的安全性问题,支持的观点认为其可行的理由如下:(1)腹腔镜下修补术采用腹腔内入路,腹膜前补片放置的区域内没有切口,故无切口感染所导致的补片感染。(2)由于腹膜的隔离,对绝大部分嵌顿疝尚未绞窄坏死的患者,细菌尚未穿透腹膜,补片所在的腹膜前间隙基本处于无菌状态。(3)补片位于腹膜前间隙,位置较深,紧贴腹膜,术后即使存在炎症反应,也容易被腹膜吸收。故2013年欧洲内镜外科协会制定的《腹腔镜腹股沟疝手术共识》中提出:腹股沟嵌顿疝可以用腹腔镜手术治疗,即使须行肠管切除也可使用补片修补[8]。对于补片的选择,应首选大网孔[9]或具有耐受感染能力的生物补片[10]。
本研究中腔镜组共计57例,共植入补片40例,其中2例虽行肠切除,但均在补片修补后,另经脐下方辅助小切口行肠切除,术后无补片感染发生,故对肠管虽最终判断不可逆坏死,但腹腔内污染不明显者,先行TAPP修补后经切口行肠管切除,可大大降低补片感染风险。另17例均未植入补片,其中2例经腹腔镜探查肠管已不可逆坏死,经脐下方辅助小切口切除坏死疝内容物、腔镜下单纯疝囊高位缝扎,另15例因腹腔内污染稍明显或一般情况较差合并糖尿病,有化疗史、慢性肝病病史及长期口服激素等免疫力低下等高危因素,仅行腹腔镜下嵌顿松解+疝囊高位结扎。组间对比,腔镜组补片植入率高于开放组、术后复发率低于开放组;切口感染率、补片感染率及漏诊/误诊率两组间差异虽无统计学意义,但开放组发生补片感染2例、漏诊3例(其中肠坏死漏诊1例,合并股疝漏诊2例),腔镜组无一例补片感染及漏诊发生。亚组间对比,虽各个指标间差异亦无统计学意义,考虑系对手术适应证、无菌技术及手术操作技巧严格把握的结果。对于未植入补片组,腔镜高位结扎组术后复发率虽与开放高位结扎组差异无统计学意义,但由于前次腹腔镜手术未破坏腹股沟解剖,故复发后可选择局麻或半麻进行开放式修补,手术简单易行,或根据诊疗单位技术水平考虑再次选择腹腔镜手术修补。
腹腔镜用于嵌顿疝的治疗应充分利用其腹腔内探查的优势,疝修补前、后均需要探查,亦有学者行开放疝修补后,经疝囊进行腹腔镜探查[11],TAPP自腹腔内操作,利于还纳疝内容物,故从此角度,对于嵌顿时间较短、肠管生机尚可、腹腔内无明显污染的腹股沟嵌顿疝,治疗应首选TAPP。此外,对于腹腔内污染严重,需行肠管切除或合并糖尿病、免疫力低下等患者,虽经探查肠管生机尚可,无需行肠管切除,但为安全起见,宜仅行腹腔镜下内环口缝扎术。TAPP在治疗腹股沟嵌顿疝时,可待疝内容物还纳后,边修补边观察肠管活力,因其有足够的时间观察肠管活力,故理论上其肠切除的比例低于单纯开放手术,国外亦有相关文献证实[12]。腹股沟疝急性嵌顿时,可能发生肠道菌群移位、腹腔内细菌污染,TAPP过程中,腹膜被人为打开,因此不可避免地直接或间接使补片接触肠管及可能污染的区域,理论上会增加术后补片感染的风险。TEP由于不破坏腹膜的隔绝屏障,理论上可大大降低术后补片的污染。但TEP无法完成嵌顿疝内容物还纳及内容物的探查,虽有学者报道在施行短暂的腹腔镜探查+还纳后立刻转行TEP修补[13],但在腹腔镜探查及还纳过程中,同样难免有手术器械沾染所致的间接污染,同时TEP术后亦需再次进入腹腔内探查,操作较为繁琐。本研究中腔镜组有5例患者麻醉后嵌顿疝复位成功,且嵌顿时间较短,预判疝内容物生机可,故先行TEP修补,术后再进入腹腔探查,此方法可以实现理想状态下的腹膜隔绝。TEP术后虽需再次进入腹腔内探查,但相较TAPP,明显减少了腹腔内操作的程序及时间,大大降低了空腔脏器损伤的风险及术后腹腔粘连的发生率,同时先行TEP由于保持了耻骨肌孔周边区域腹膜的完整性,因此术前嵌顿时间较短、考虑肠管生机术后尚可、麻醉后可自行还纳的患者,可考虑先行TEP再进入腹腔探查,从降低补片感染风险角度分析,其具有一定优势性。Kurt等[14]认为嵌顿疝手术后感染虽与修补方式无关,但与是否行肠切除有关,无张力疝修补术用于不行肠切除的嵌顿疝是安全的。为慎重起见,对于腹腔镜探查明确肠管已不可逆坏死需切除、腹腔内污染严重者,应放弃进一步行TAPP,仅行腹腔镜下单纯疝囊高位结扎,必要时二期另行无张力修补术[15]。
对于术前无明确嵌顿疝内容物坏死及局部或腹腔感染征象、排除全麻及腹腔镜手术禁忌证的腹股沟嵌顿疝患者,优先考虑采用腹腔镜探查,根据术中探查结果结合患者全身情况、选择合适的腹腔镜手术方式及补片,结合围手术期抗生素的使用,与传统开放手术相比可大大提高嵌顿疝患者的一期无张力修补成功率,降低复发率。此外,对部分仅完成腹腔镜探查、内环口缝扎,无法一期无张力修补的术后复发患者,因前次手术未干扰腹股沟区,故二次开放手术修补的难度大大降低。综上所述,腹腔镜技术在腹股沟嵌顿疝的治疗中具有良好的应用价值。

