蒙脱土负载镍催化顺酐加氢制备丁二酸酐
毛 洁,王 清,王慢慢,朱世侦,周娅芬
(西华师范大学 a.化学化工学院,b.化学合成与污染控制四川省重点实验室,四川 南充 637009)
顺酐 (MA) 的催化加氢产物丁二酸酐 (SA)、γ-丁内酯、四氢呋喃和1,4-丁二醇等是重要的精细化工和医药中间体[1]。其中丁二酸酐广泛用于医药、农药、塑料、涂料以及食品添加剂等生产过程中[2-4]。如医药上,丁二酸酐可用于制造生胃酮、琥珀酰胺噻唑和琥珀酰氯亚胺等药物;农药上,丁二酸酐与偏二甲肼在乙腈中反应制得的N-二甲胺基琥珀酰胺(简称比久) 是一种低毒高效的植物生长抑制剂,可广泛用于花生、棉花、果树、蔬菜等经济作物。更重要的是,丁二酸酐的水解产物丁二酸与丁二醇缩聚可制得性能优异的生物可降解塑料―聚丁二酸丁二醇酯(PBS)[5-6]。随着白色污染问题的日趋严峻,生物可降解塑料PBS的市场前景十分广阔,这将极大地刺激和带动其上游产品丁二酸酐的市场需求。而目前我国丁二酸酐产能非常有限,限制了PBS产业的健康发展,成为P产业发展的瓶颈。为此,丁二酸酐产业已引起学术界的极大关注。
目前报道的顺酐加氢催化剂主要包括贵金属、镍基、铜基三种类型。贵金属催化剂可获得高的转化率和丁二酸酐选择性,但价格昂贵[7-9]。铜基催化剂存在着反应温度和压力高,催化剂负载量高、用量大,以及催化剂容易烧结、失活等问题[10]。近年来,一系列Al2O3、SiO2、TiO2、粘土等负载的Ni基催化剂被用于顺酐加氢反应[11-14],研究表明,载体的性质、种类及负载后催化活性物种在载体表面的存在状态对催化加氢反应性能有较大影响,在顺酐的液相加氢反应中表现出不同的丁二酸酐选择性。本文将蒙脱土负载镍催化剂用于顺酐加氢反应,考察催化剂还原方法和反应条件对加氢反应的影响。
1 实验部分
1.1 试剂与仪器
蒙脱土 (MMT)、氯化镍 (NiCl2·6H2O)、顺酐、氢氧化钠、乙醇、γ-丁内酯、乙酸酐均为分析纯,高纯氢气 (99.99 %),实验中用水为高纯水。高压反应釜 (GYF—60-2),气相色谱仪 (安捷伦7890A)。
1.2 催化剂的制备
采用沉积沉淀法制备Ni/MMT催化剂。室温下将一定量的蒙脱土分散于10 mL水中,不断搅拌下加入一定量的NiCl2·6H2O。10 min后,采用恒压滴液漏斗逐滴加入质量分数0.5 %的NaOH水溶液至溶液pH为10,继续搅拌6 h,过滤,用高纯水洗涤沉淀至中性且检测不到Cl-为止。60 ℃真空干燥12 h,即得到Ni/MMT催化剂。
1.3 催化剂活性测试
催化加氢反应在60 mL高压反应釜中进行。将所需量的催化剂、溶剂和顺酐加入到高压反应釜中。闭釜并用高纯氢气将釜中空气置换5次,充氢气至一定压力,升温至所需温度后,开启磁力搅拌并计时。反应结束后,冷却至室温,取出产物进行离心分离,取上层清液进行分析。
1.4 产物分析
利用气相色谱仪对加氢产物进行分析,氢火焰离子化检测器,HP-5弹性石英毛细管柱 (30×320×0.25 um)。采用程序升温法,柱温由60 ℃升至220 ℃;气化室温度250 ℃;检测器温度300 ℃。通过与标样色谱峰保留时间的对照和GC-MS定性分析各反应产物,采用峰面积归一化法计算百分含量。
2 结果与讨论
2.1 催化剂的表征
图1为Ni/MMT催化剂的XPS谱图。从图中可以看出,Ni 2p存在两组XPS双峰Ni 2p3/2和Ni 2p1/2,其中Ni 2p3/2的一组双峰的电子结合能分别为855.2 eV和861.3 eV,Ni 2p1/2的电子结合能分别为873.0 eV和879.4 eV,说明催化剂中的Ni以Ni(OH)2的形式存在[15]。
图2分别为使用前及用于催化顺酐加氢反应后的Ni/MMT催化剂的TEM图。从图中可以看出,反应前后该催化剂均呈现较薄的层状结构,催化剂中金属Ni在层状结构上分散均匀。

2.2 催化剂还原方法对加氢性能的影响
本实验中,分别采用H2、NaBH4和N2H4·H2O对沉积沉淀法制备的催化剂进行还原,对比考察了未经还原和还原后的催化剂对顺酐的加氢反应情况,结果如表1所示。从表中可以看出,H2还原的催化剂虽然顺酐的转化率高达99.4 %,但丁二酸酐的选择性只有34.9 %;未还原、NaBH4和N2H4·H2O还原的催化剂,丁二酸酐的选择性均为100 %,但顺酐的转化率却是未还原的催化剂的更高。采用未经还原的催化剂加氢效果较好,而且可简化催化剂的制备工序,降低成本,因此后面对顺酐加氢制备丁二酸酐反应条件的优化实验中,采用未经还原的催化剂。
2.3 溶剂种类的影响
本实验考察了四种溶剂对顺酐加氢制备丁二酸酐的影响,结果如表2所示。当反应溶剂为γ-丁内酯和乙酸酐时,丁二酸酐的选择性均为100 %,顺酐的转化率则是乙酸酐作溶剂时较高;以去离子水和无水乙醇作溶剂时,虽然顺酐的转化率比以乙酸酐作溶剂时的高,但丁二酸酐的选择性却仅有12.5 %和9.9 %。因此后续实验中,我们采用乙酸酐作为加氢反应的溶剂。
表1不同还原方法得到的Ni/MMT催化剂x对顺酐加氢的影响
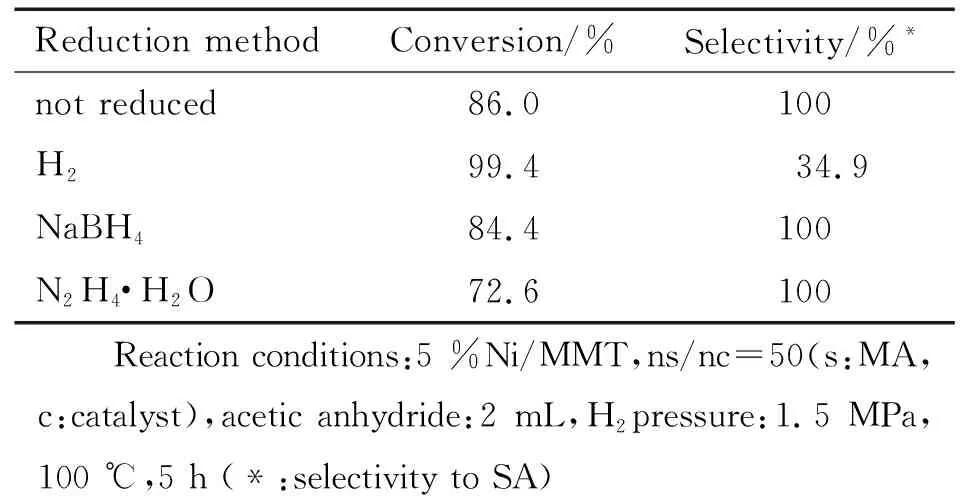
Reduction methodConversion/%Selectivity/%*not reduced86.0100H299.434.9NaBH484.4100N2H4·H2O72.6100 Reaction conditions:5 %Ni/MMT,ns/nc=50(s:MA,c:catalyst),acetic anhydride:2 mL,H2pressure:1.5 MPa,100 ℃,5 h (*:selectivity to SA)
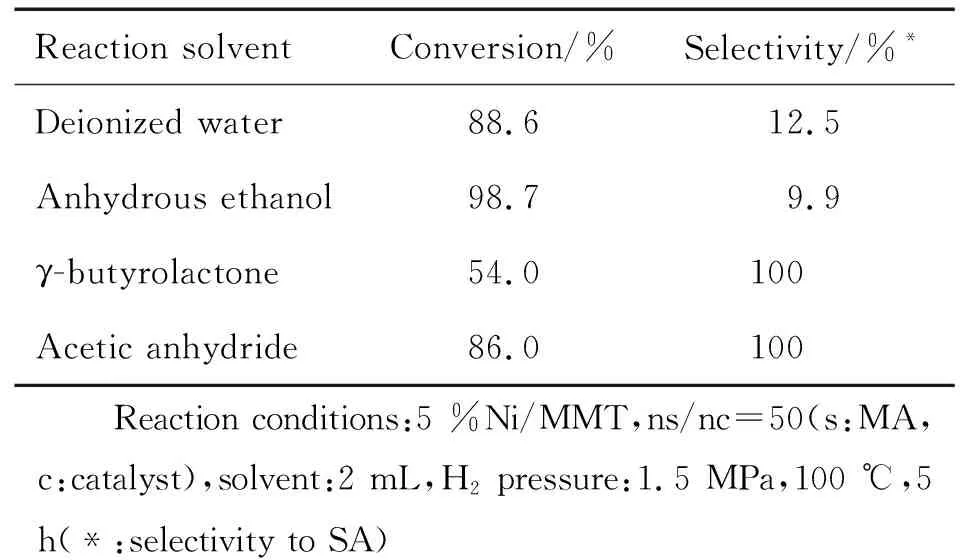
表2 反应溶剂对顺酐加氢的影响
2.4 反应温度的影响
从图3可以看出,反应温度对Ni/MMT催化顺酐加氢生成丁二酸酐的影响较大。在考察的温度范围内,丁二酸酐的选择性均能达到100 %,顺酐的转化率则随温度的变化而显著改变。反应温度从80 ℃升高到100 ℃的过程中,顺酐的转化率接近线性增加,到100 ℃时,顺酐的转化率达到86.0 %。当温度从100 ℃升高到120 ℃时,顺酐的转化率增加缓慢,120 ℃时顺酐转化率达到90.4 %。
2.5 氢气压力的影响
图4所示为氢气压力对Ni/MMT催化剂对顺酐加氢制备丁二酸酐反应的影响。从图中可以看出,氢气压力从0.5 MPa增加到2.0 MPa,丁二酸酐的选择性均为100 %,而顺酐的转化率几乎呈线性增加,在2.0 MPa处升至最大95.0 %,随着氢气压力的继续增大,在2.5 MPa处,顺酐的转化率和丁二酸酐的选择性都开始减小。当氢气压力超过2.0 MPa后,再增加氢气压力,顺酐的转化率及丁二酸酐的的选择性均开始降低,这与催化剂表面氢气吸附量过大有关,减少了催化剂与顺酐的接触,同时也与顺酐过度加氢有关。

2.6 反应时间的影响
顺酐的转化率和丁二酸酐的选择性随时间的变化情况,结果如图5所示。从图中可以看到,在所考察的时间范围内,顺酐的转化率随时间的变化呈现先增大后减小的趋势,而丁二酸酐的选择性均为100 %。反应1 h后,顺酐的转化率为59.3 %,随着反应时间的延长,顺酐的转化率在3 h内迅速升至95.0 %,3 h到4 h之间,顺酐的转化率变化不大,反应4 h后,丁二酸酐的选择性开始下降,这由于少量丁二酸酐进一步加氢成γ-丁内酯的结果。
2.7 催化剂的循环
催化剂循环实验按如下方法进行:每次催化加氢实验结束后,通过离心方法将催化剂从反应溶液分离,用去离子水反复洗涤后真空干燥,然后在相同的反应条件下继续使用。由图6可以看出,催化剂循环使用5次的过程中,顺酐的转化率维持在95.0 %~99.7 %,丁二酸酐的选择性一直保持在100 %,表明该催化剂具有很高的稳定性。

3 结 论
沉积沉淀法制备的蒙脱土负载镍催化剂,无需还原即对顺酐加氢表现高的催化活性和丁二酸酐选择性,催化剂制备工序更加简化。以乙酸酐作反应溶剂,反应温度100 ℃,氢气压力2 MPa,反应时间3 h,顺酐的转化率达到95.0 %,丁二酸酐选择性为100 %。催化剂经5次循环使用仍保持高的活性,稳定性好,具有一定的工业应用前景。

