体外循环心血管手术后苏醒延迟的危险因素分析
宋辛叶,栾 永
患者的麻醉苏醒情况不仅是手术后气管拔管的主要评估指标之一[1],也是对心血管手术后神经系统损伤早期诊断最便捷、最重要的观察指标之一[2]。苏醒延迟常导致患者机械通气时间和重症监护时间延长,增加其它系统并发症发病率,甚至导致患者死亡,也给患者及家属带来巨大经济负担。因此,明确影响患者苏醒延迟的危险因素,帮助及时觉醒对接受心脏手术的患者极为重要。近年来,越来越多的学者开始关注这一问题,但目前为止,导致心血管术后苏醒延迟的危险因素尚不明确。本研究对2014年1月至2015年12月间在本院接受体外循环(cardiopulmonary bypass,CPB)心血管手术患者进行回顾性分析,探讨麻醉苏醒延迟的发生率及危险因素,以期有助于心血管手术后麻醉苏醒延迟的预防及早期识别。
1 资料与方法
1.1 研究对象 回顾性研究2014年1月至2015年12月在本院心外科接受全身麻醉CPB心血管手术的成年患者,排除患有精神疾病的患者、术前意识状态不佳的患者、资料不全影响判断者。共637例。
1.2 研究方法 所有患者均实施心脏手术的常规监测,包括心电图、脉搏血氧饱和度、呼气末二氧化碳、桡动脉血压、中心静脉压、经食道超声心动图、心输出量等监测。诱导用药包括咪唑安定、舒芬太尼、依托咪酯和顺式阿曲库铵。麻醉维持用舒芬太尼、咪达唑仑、丙泊酚、顺式阿曲库铵和七氟烷。切口闭合后,停止输注维持用药。术后,所有患者均带气管插管转移到心脏ICU,机械通气支持,术后采用丙泊酚镇静至次日早晨。护士对患者的意识和神经系统状态进行定期记录。可以合作,并配合口头指令的患者被认为意识状态已经恢复。麻醉结束后12 h意识仍未恢复的病例被认为是苏醒延迟。各种术前和术中的变量收集如下:年龄、性别、身高、体重、体重指数(body mass index,BMI)、左心室射血分数(left ventricular ejection fraction, LVEF)、是否为二次手术、血红蛋白、血尿素氮(blood urea nitrogen,BUN)、肌酐(creatinine, Cr)、天冬氨酸转氨酶(as⁃partate aminotransferase, AST)、谷丙转氨酶(glutamic pyruvic transaminase, ALT)、CPB 时间、主动脉阻断(aortic crossclamp,ACC)时间、手术类型、血乳酸含量、CPB中最低鼻咽温度、手术时间、是否输血及二次开胸止血等。
1.3 统计学方法 采用SPSS 22.0版本统计软件进行数据处理,所有计量资料采用均数±标准差(±s)表示,计数资料采用百分率表示。计量资料的比较采用student-t检验,计数资料的比较采用X2检验或Fisher精确检验。采用Logistic回归分析影响因素。以P<0.05为差异有统计学意义。
2 结 果
2.1 本试验共纳入了637例病例,其中66例苏醒延迟,发生率为10.4%。表1比较了正常组(n=571)与苏醒延迟组(n=66)的术前临床资料,苏醒延迟组患者年龄偏大,且Cr和BUN平均水平均高于苏醒正常组患者,而性别、身高、体重、BMI、LVEF、乳酸两组相比无明显差异。见表1。
637例病例中接受冠状动脉旁路移植手术(cor⁃onary artery bypass grafting,CABG)的有118 例,接受瓣膜置换手术(valve replacement,VR)的有362例,同时接受CABG+VR的有16例,接受大血管手术的有73例,其中接受选择性脑灌的39例,深低温停循环的2例,接受其它手术的患者有68例:包括房间隔缺损修补术36例,室间隔缺损修补术11例,心房肿物切除术11例,法洛四联症矫治术3例,心内膜垫缺损修补术2例,动脉导管切断缝合术2例,左室流出道疏通术1例,右室流出道狭窄矫治术2例。苏醒延迟组中,接受其它手术的患者仅有1例,发生率为1.5%,远小于总体发生率(10.4%)。 见表2。
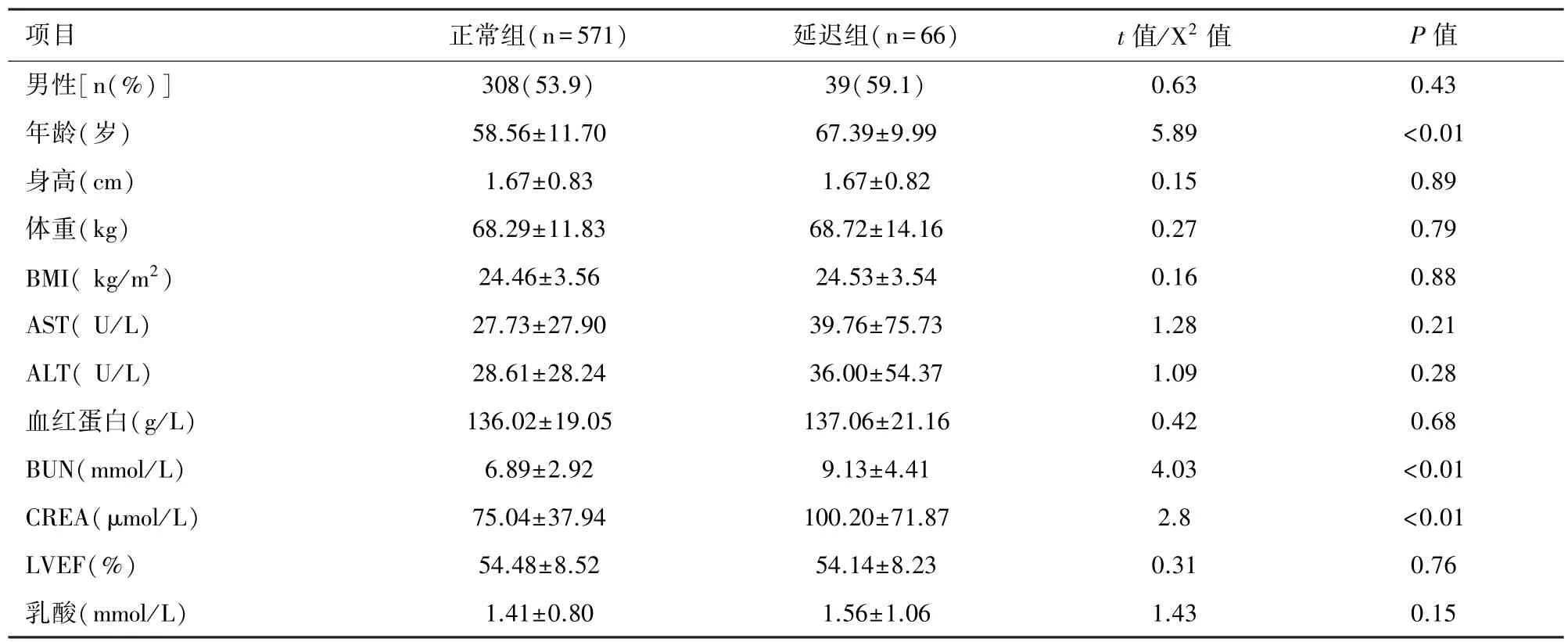
表1 术前两组患者的临床资料比较

表2 两组患者所经历的手术术式比较[n(%)]
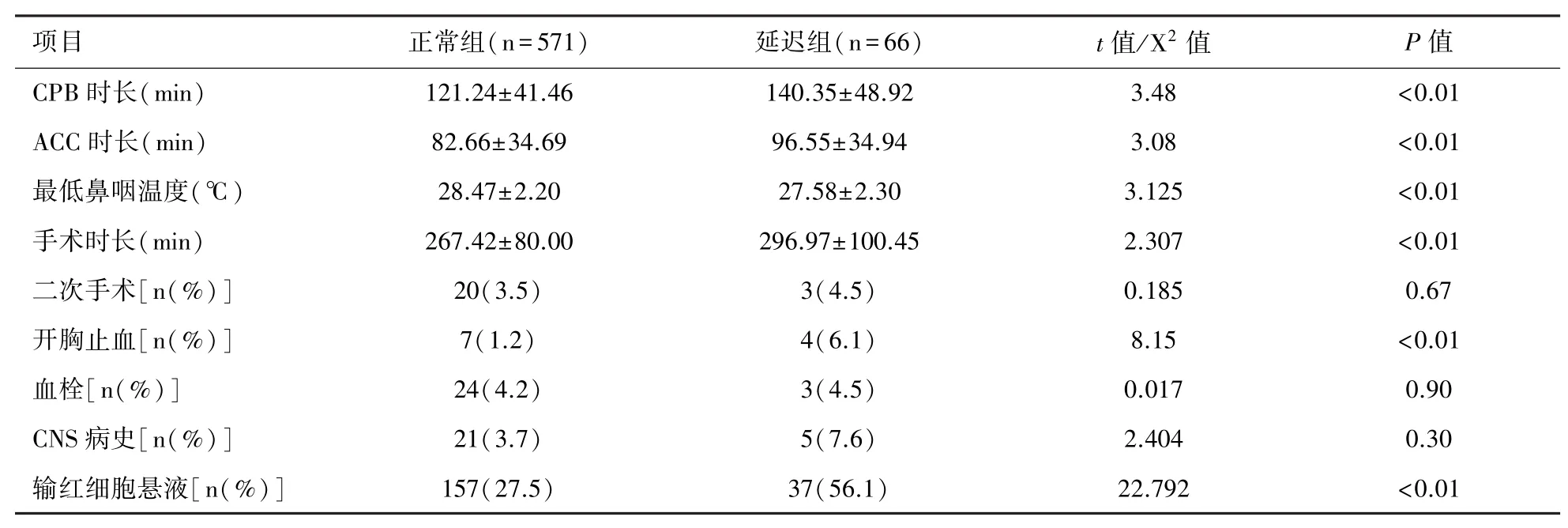
表3 手术相关因素的比较
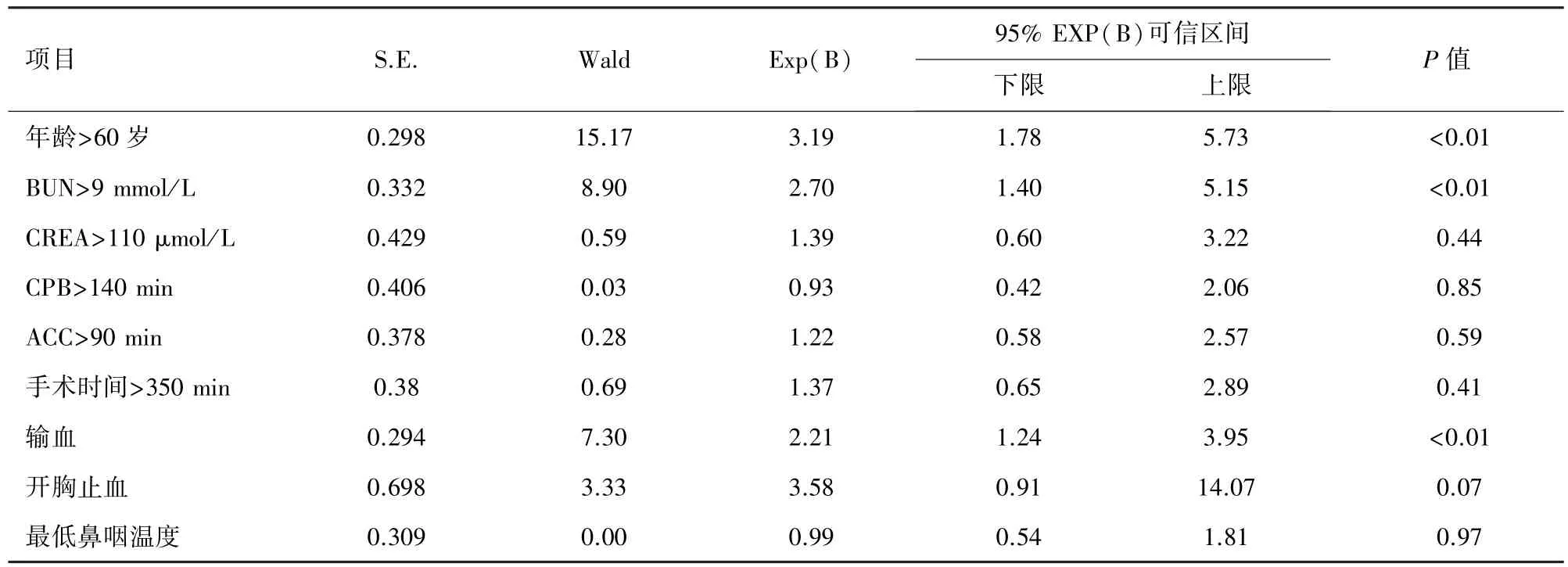
表4 心血管手术后发生苏醒延迟的多因素分析结果
年龄(P<0.01)、术前 BUN 水平(P<0.01)、Cr水平(P<0.01)、CPB 时间(P<0.01)、ACC 时间(P<0.01)、最低鼻咽温度(P<0.01)、手术时间(P=0.02)、二次开胸止血(P<0.01)、输血(P<0.01)是心血管手术后发生苏醒延迟的危险因素。见表1和表3。
Logistic回归模型的最终分析结果,Cr、ACC时间、最低鼻咽温度、手术时间、CPB时间、二次开胸止血和其它术式统计学上不再有显著性,最终年龄、BUN、是否输红细胞这3个变量被确定为显著影响苏醒延迟发生的独立危险因素。见表4。
3 讨 论
意识恢复是一个连续的过程,目前对全身麻醉后苏醒延迟并没有一个统一的定义。为尽量排除麻醉药物残留对苏醒延迟的同时尽量降低对灵敏度的影响,参考国内外相关资料[3-5],将麻醉结束后 12 h意识仍未恢复的病例认为是苏醒延迟。CPB心血管手术后苏醒延迟涉及因素较多,外科、麻醉、CPB及患者自身等都可能影响苏醒时间,其确切机制尚不明确。各种原因造成的脑组织损伤、麻醉药物代谢异常、机体内环境紊乱等则可能是引起患者苏醒延迟的直接原因。造成脑组织损伤的原因有很多,脑栓塞、内环境紊乱、高热、低氧血症、脑水肿致颅内高压等原因均能导致暂时性或永久性脑损伤。CPB过程中,炎症反应的发生能够引起脑组织水肿[6];滚压泵对人工管道的碾轧可能产生异物微栓、人工血管放置和拔除过程、复温时若水温与血温相差10℃以上也可能导致气栓的发生[7],可导致脑血管栓塞,对脑组织造成损伤。麻醉药物代谢异常的原因可能是患者的基础状况如年龄、性别、肝肾功能等因素导致其药代动力学的变化。老年患者一方面对阿片类、苯二氮卓类等全身麻醉药的敏感性增加,另一方面中枢神经系统功能进行性下降,意识恢复往往较为缓慢。机体内环境紊乱的原因可能是手术创伤及CPB本身和它所导致的炎症反应、内分泌变化、低温、血液稀释、人工材料及心脏停搏液的应用等所导致的强烈的应激。这项回顾性研究中,笔者尽量排除麻醉药物代谢的影响,重点讨论患者术前的基线资料与围手术期的治疗措施,发现年龄大、术前BUN水平较高、输红细胞是心脏手术后麻醉苏醒延迟的独立危险因素。
高龄(年龄>60岁)是苏醒延迟的独立危险因素,老年患者麻醉药物的表观分布容积、清除率、血浆蛋白结合率均有不同程度下降,导致药物在血浆中游离浓度增加[3],因此,与年轻人相比,要达到同样的麻醉深度,老年人需要的静脉或吸入麻醉药物的用量多有不同程度的下降[8]。随着年龄的增长,影响大脑意识恢复的区域解剖和功能上均会发生变化[9],老年人群不仅合并基础疾病多、器官功能减退,药代动力学特性和对麻醉药物反应也会发生改变[10],另外,老年人血管顺应性降低,对CPB中的平流灌注、低灌注耐受性差,同等条件下更容易出现神经系统损伤,这些因素均增加了苏醒延迟发生的风险。
尽管此前大部分研究认为男性苏醒延迟的风险要显著高于女性[3,11-12],本研究中性别在苏醒延迟上的差异并没有显著性。女性恢复更快可能与她们对麻醉药物的敏感性较低有关[3];雌性激素也被认为在两性麻醉恢复的差异中起到一定作用,故这种性别的差异可能主要体现在麻醉药物代谢上,而本研究中患者术后带气管插管转移到心脏ICU后,采用丙泊酚镇静至次日早晨停止镇静后12 h仍未苏醒的病例被定义为苏醒延迟,这个过程已尽可能排除麻醉药物的干扰,这可能是性别对本研究中苏醒延迟的发生率不具有显著影响的原因。
本研究结果提示与CREA相比,BUN检查可能对苏醒延迟有更强的预测作用,术前BUN>9 mmol/L为苏醒延迟的独立危险因素。最近有研究认为BUN检查对肾脏灌注、相关血流动力学变化和神经激素激活的敏感性更高,可能对心脏衰竭、急性心肌梗死患者的死亡风险有着较强的预测作用[13-14],相关研究发现,BUN水平升高也与主动脉和心脏手术后不良结局相关[15]。BUN虽然只是一种常规检查却能够反映出与患者心肾功能相关的临床状态,CPB中平流灌注、低温、低血压可能使术前已存在BUN水平异常的患者肾功能进一步降低,导致患者对麻醉药物的药效学、药代动力学发生变化,这也解释了为什么较高的BUN水平在一定程度上会导致心血管手术患者的麻醉苏醒延迟风险升高。
心血管手术涉及多种术式,不同术式间创伤大小、手术时程及患者病理生理基础均可能存在较大差别。就苏醒延迟而言,单因素检验结果提示仅“其它手术”组内存在统计学差异。可能与“其它手术”组的患者平均年龄较轻、手术操作相对简单、病程短、合并其它基础疾病少等因素有关。尽管主动脉弓部手术被认为有额外的增加脑部并发症的风险[4-5],但本研究并未发现主动脉弓部手术与其它术式在苏醒延迟的发生率上有统计学意义,尽管目前最佳脑保护方式仍存在争论[16],但分析其原因可能与行主动脉弓部手术时额外给予的脑保护措施(头部冰帽降温、CPB过程中给予甲泼尼龙、甘露醇等)有关。
本研究中单因素分析提示CPB时间(P<0.01)、ACC 时间(P<0.01)、最低鼻咽温度(P<0.01)、手术时间(P=0.02)、二次开胸止血(P<0.01)均与苏醒延迟相关,但Logistic多因素回归分析认为这些都不是导致苏醒延迟的独立危险因素。有研究认为发生脑部并发症的风险会随着CPB时间的延长而增加,这和炎性因子释放增多,血液破坏和有关器官缺血-再灌注损伤加剧有关[17]。 但也有研究[18]显示,目前并没有证据证明CPB及CPB时间的长短会对心脏手术后患者的意识恢复过程产生影响,CPB时间长对麻醉苏醒的影响可能来自于CPB期间给予患者的麻醉药物,而非CPB本身的影响。本研究中,CPB时间长的患者发生苏醒延迟的风险会增高,但CPB时间并非导致CPB心血管手术后苏醒延迟的独立危险因素。ACC时间长往往是由于手术操作较为复杂,这些患者往往病情重,手术操作复杂,需要更低的鼻咽温度、CPB时间、手术时间,这些因素交互在一起,并不具有独立意义。故本研究结果认为苏醒延迟组的CPB时间、ACC时间、手术时间,虽然都显著高于正常组,但却并非是苏醒延迟的独立危险因素的原因可能与患者的术前病变重,手术操作复杂,术前基础状态差,术中止血困难等因素有关。
本研究结果提示输红细胞是苏醒延迟的独立危险因素,而术前的血色素状况对苏醒延迟的发生没有统计学意义。分析其原因可能有以下两方面:一方面心血管手术的患者中,术前合并有充血性心力衰竭的患者较多,这些患者体液量较大,术中虽然有血液损失,但经过利尿、超滤后血红蛋白水平足以维持组织器官氧供,不需要输红细胞;另一方面与术前贫血相比,术中、术后持续的失血可能对苏醒延迟的发生影响更大。众所周知,输红细胞会对机体造成很大影响,输红细胞不只可以引发各种微栓子的形成,而且大量快速输血可导致内环境紊乱和中心体温降低,从而影响脑的供血及代谢,研究表明,术中输红细胞会对CABG手术患者的预后造成不利影响[19]。此外,围术期需要大量输血的往往是病变重、CPB时间长、术中出血多、创面广泛渗血、止血困难、术后引流多的患者。这些患者脑组织低灌注及栓子栓塞的机会较其它患者明显增加,易发生苏醒延迟。
综上所述,年龄、术前BUN水平,是否输红细胞可能是影响全身麻醉下心血管手术患者苏醒延迟的独立危险因素。那些年龄大,BUN水平升高,以及输红细胞的患者发生麻醉苏醒延迟的风险更大。CPB心血管手术后苏醒延迟的发生与多种因素相关,术前积极进行内科治疗,改善肾脏功能,选择适宜的手术方式及改进手术操作以缩短手术时间,减少术中出血等均是预防苏醒延迟的重要措施。

