克拉玛依九区原油中石油酸分子的表征
刘靖新,曹 青,修 远,马晨菲
(中国石油 石油化工研究院,北京 102206)
原油中酸性物质主要是石油酸,其组成复杂、结构多样[1-5]。Qian等[6]利用傅里叶变换离子回旋共振质谱仪成功鉴定出3 000多种石油酸。李恪等[7]使用FTIR、核磁共振波谱、质谱等多种表征手段对九区原油中的石油羧酸的组成和结构进行了研究,得到了各类型石油酸的结构模型。
液相色谱已广泛应用于石化分析领域,如行业标准NB/SH/T 0509—2010《石油沥青四组分测定法》[8]即采用了氧化铝柱色谱将石油沥青和渣油等试样分离成四组分,但可能是受到石油分子极性以及相对分子质量的影响,液相色谱技术用于石油酸试样表征方面的研究较少,Hsu等[9]认为液相色谱技术与常压化学电离源结合可有效表征石油酸的组成。田松柏[10]指出,复杂的质谱图解析工作难度较高,先采用气相色谱-质谱或液相色谱-质谱将石油酸分开,可极大程度地降低对质谱仪分辨率的要求及质谱图解谱的难度。Robson等[11]利用色谱技术结合对原油中的极性和非极性化合物进行分子剖析。
本工作采用高效液相色谱-飞行时间质谱联用法(HPLC-TOF MS),利用电喷雾电离源对九区原油中的石油酸进行了分析,对质谱直接进样法和HPLC-TOF MS法分析石油酸组成进行了比较,优化了溶剂、流动相等条件,并对九区原油中的石油酸组分进行了定性以及半定量分析。研究结果有助于加强对于新疆区块含酸原油分子层面的认知。
1 实验部分
1.1 试剂与仪器
ACQUITY UPLC H-Class型液相色谱仪、Synapt G2-Si型高分辨飞行时间质谱仪:Waters公司;Nicolet 6700型傅里叶变换红外光谱仪:Thermo公司;HSS T3C18型色谱柱:Waters公司;LabTech EV型旋转蒸发仪:莱伯泰科公司。
甲醇:质谱纯,Fisher公司;甲酸、甲酸铵:质谱纯,Sigma公司;环己烷、无水乙醇、NaOH、HCl(10%(w))、氨水(25%(w)):分析纯,北京化学试剂公司;九区原油:中国石油独山子石化公司。
1.2 实验条件
液相色谱:流动相主要采用甲醇体系洗脱,流速为0.3 mL/min,并对流动相添加剂(甲酸、甲酸铵、氨水)组成等进行优化。
质谱条件:采用ESI负离子电离模式,毛细管电压-2.5 kV,离子源温度120 ℃,脱溶剂温度280 ℃,脱溶剂流量800 L/h,锥孔气流速50 L/h。
HPLC-TOF MS分析:毛细管电压-2.5 kV,离子源温度150 ℃,脱溶剂温度450 ℃,脱溶剂流量800 L/h,锥孔气流速50 L/h。
红外光谱采集条件:扫描范围500~4 000 cm-1。
1.3 石油酸的分离与纯化
按文献[12]的方法对九区原油中的石油酸进行分离与纯化:1)称取20 g九区原油试样,加入140 g环己烷进行稀释,稀释后倒入清洁的分液漏斗中,用10 g环己烷洗净瓶中残油,转入分液漏斗中;2)另配制120 mL NaOH溶液(1%(w)),与120 mL无水乙醇混合均匀,取40 mL混合溶液加入到盛有原油的分液漏斗中,振荡3 min,静置1 h,等待分层,收集下层醇水溶液。共重复此操作6次;3)将步骤2中收集的醇水溶液加入清洁的分液漏斗中,加入10 mL环己烷,振荡、静置,除去有机相中的油污,重复操作,直至有机相溶液在滤纸上点样时不出现油渍;4)收集步骤3中的醇水溶液,加入HCl(10%(w))酸化至pH < 3,再用40 mL环己烷抽提,重复操作3次;5)收集有机相,弃水相,用高纯水洗涤有机相至水相pH约为7,将环己烷溶液转移至烧瓶中,旋蒸去除溶剂,即得石油酸试样。
1.4 石油酸组成的定性和半定量分析方法
采用ESI-MS分析石油酸组成时,得[M-H]-特征峰,进而获得石油酸的相对分子质量。石油酸主要组成为一元有机羧酸,其分子式可表达为CnH2n+zO2,其中,n为碳原子数,z为相对同碳数饱和脂肪酸氢原子数增量。根据高分辨质谱获得的精确相对分子质量可推测出相应元素组成。当石油酸浓度极低时,石油酸浓度与其分子的离子峰强度成正比,考虑羧酸结构的相似性及组成的复杂性,忽略质谱对不同羧酸的响应差异。通过归一化处理,可计算出不同类型羧酸化合物的相对百分含量。
2 结果与讨论
2.1 九区原油的基本性质
九区原油试样的主要性质见表1。从表1可知,九区原油属于低硫中间-环烷基原油,酸值4.92 mg,属于高酸原油,其中的石油酸主要以环烷酸为主。
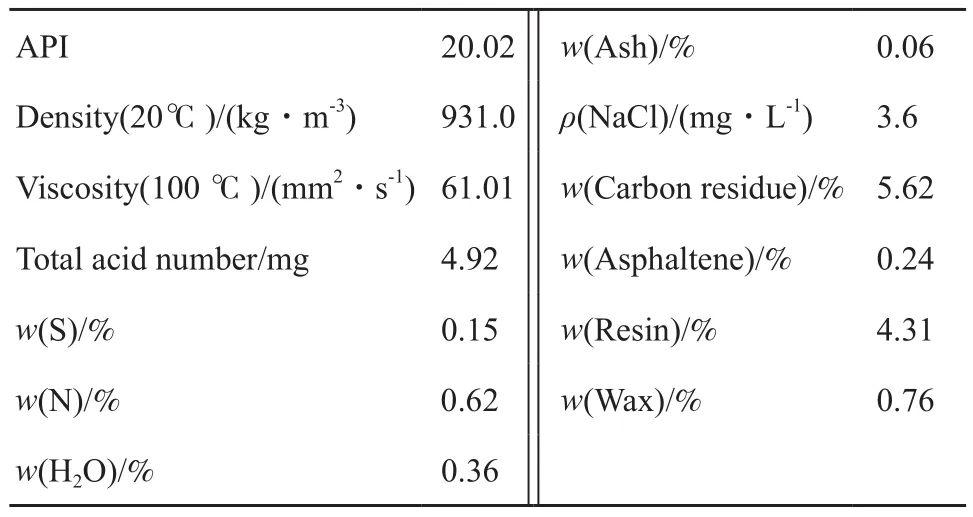
表1 克拉玛依九区原油主要性质Table 1 Main properties of Karamay district 9 curde oil
2.2 石油酸的红外光谱分析结果
图1为九区原油中石油酸的FTIR谱图。
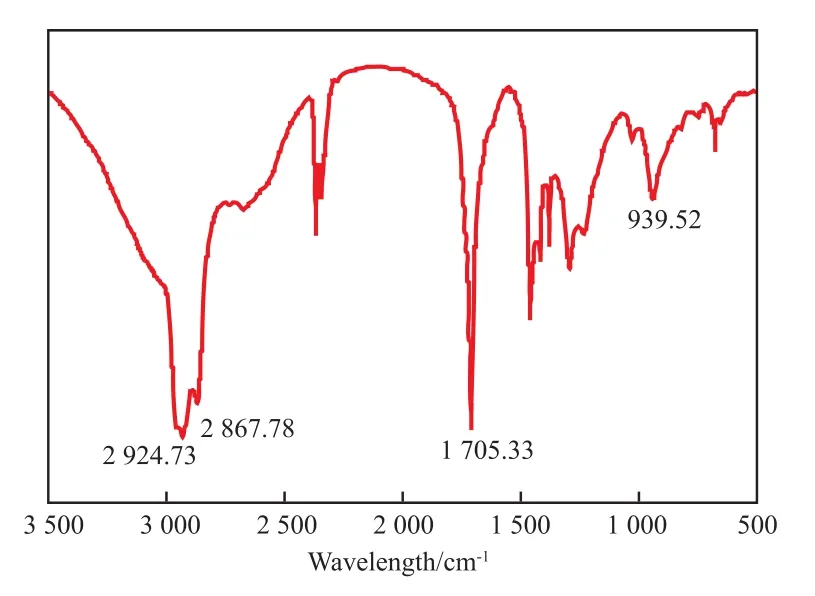
图1 九区原油中石油酸的FTIR谱图Fig.1 FTIR spectrum of petroleum carboxylic acids in district 9 crude oil.
从图1可看出,3 200~2 500 cm-1处为一组二聚体酸的特征吸收峰,1 705 cm-1处为二聚体酸羰基的特征吸收峰,939 cm-1处为二聚体酸羟基弯曲振动峰,因此,该试样具有典型环烷酸的结构特征。从羰基的峰形可看出,试样主要是一元酸。同时,根据文献[7]报道推测这些酸羰基主要是直接或通过较短的直链连接在五元或六元环上。由于722 cm-1附近无明显吸收,可知直链状结构(CH2)n中n> 4的结构体很少,说明正构脂肪酸含量少,环烷酸中包括烷基侧链在内多为较短支链取代基。
2.3 质谱直接进样条件的优化
首先,不经色谱分离,选择质谱直接进样分析,采用ESI负离子模式检测试样,结果见图2。从图2可看出,谱图呈现出2种质量分布状态,第一个分布在m/z=209~351之间,第二个分布在m/z=353~513之间。结合元素组成可知,第一个分布的分子组成为CnH2n+zO2,推测试样为一元羧酸,第二个分布的分子组成为CxHyO4,推测试样为羧酸二聚体。
二聚体的存在会影响石油酸定量的准确性。因此,需要将二聚体解聚。按文献优化结果[13],采用甲醇为主要溶剂对二聚体进行解体,实验对添加了不同浓度的甲酸铵、氨水的溶剂体系进行比较。通过比较,选择体积比为9∶1的甲醇/水溶液体系对二聚体进行解体,其中含有0.1%(φ)的氨水。甲醇/水/氨水溶液负离子ESI-MS法的石油酸平均质谱图见图3。
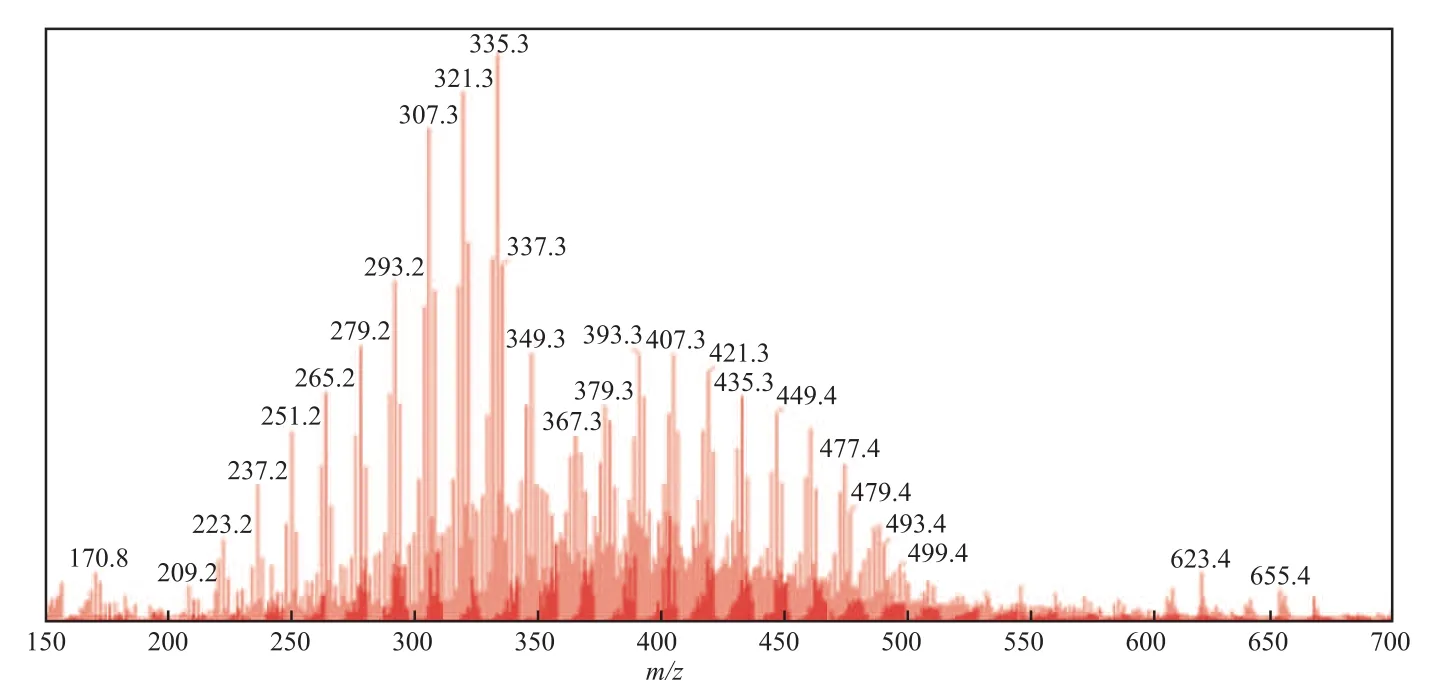
图2 纯甲醇溶液负离子ESI-MS法的石油酸质谱图Fig.2 Mass spectrum of petroleum carboxylic acids by negative ESI-MS using pure methanol.
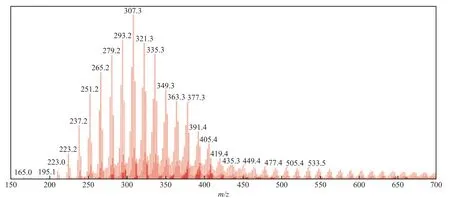
图3 甲醇/水/氨水溶液负离子ESI-MS法的石油酸质谱图Fig.3 Mass spectrum of petroleum carboxylic acids by negative ESI-MS using methanol/water/ammonia solution.
与图2相比,图3中低相对分子质量的一元羧酸的峰强度增加,质量分布向低相对分子质量方向移动。说明在此条件下,大多数二聚体解离。
2.4 液相色谱-质谱联用分离条件的优化
黄思棋等[14]对石油酸试样的分离条件进行优化,分别用甲醇(含0.1%(w)甲酸)-水(含0.1%(w)甲酸)体系、甲醇-0.1%(w)甲酸体系、甲醇-5 mmol/L甲酸铵体系、甲醇-0.1%(w)氨水体系4种流动相进行分析。
在使用甲醇(含0.1%(w)甲酸)-水(含0.1%(w)甲酸)体系梯度洗脱时,观测到大部分石油酸需要纯甲醇洗脱,推测由于石油酸结构中环烷基非极性较强所致。使用甲醇-0.1%(w)甲酸体系分析的质谱图见图4。从图4可看出,响应最强的质谱峰为m/z=435,经过元素组成分析,发现被检测到的石油酸多以二聚体形式存在。这可能与体系的pH有关,偏酸性条件有效地保护了氢键结构。使用甲醇-0.1%(w)氨水体系分析的质谱图见图5。从图5可看出,甲醇-0.1%(w)氨水体系既可满足色谱分离要求,又能兼顾质谱响应需要,得到m/z=209~671之间的质量分布。
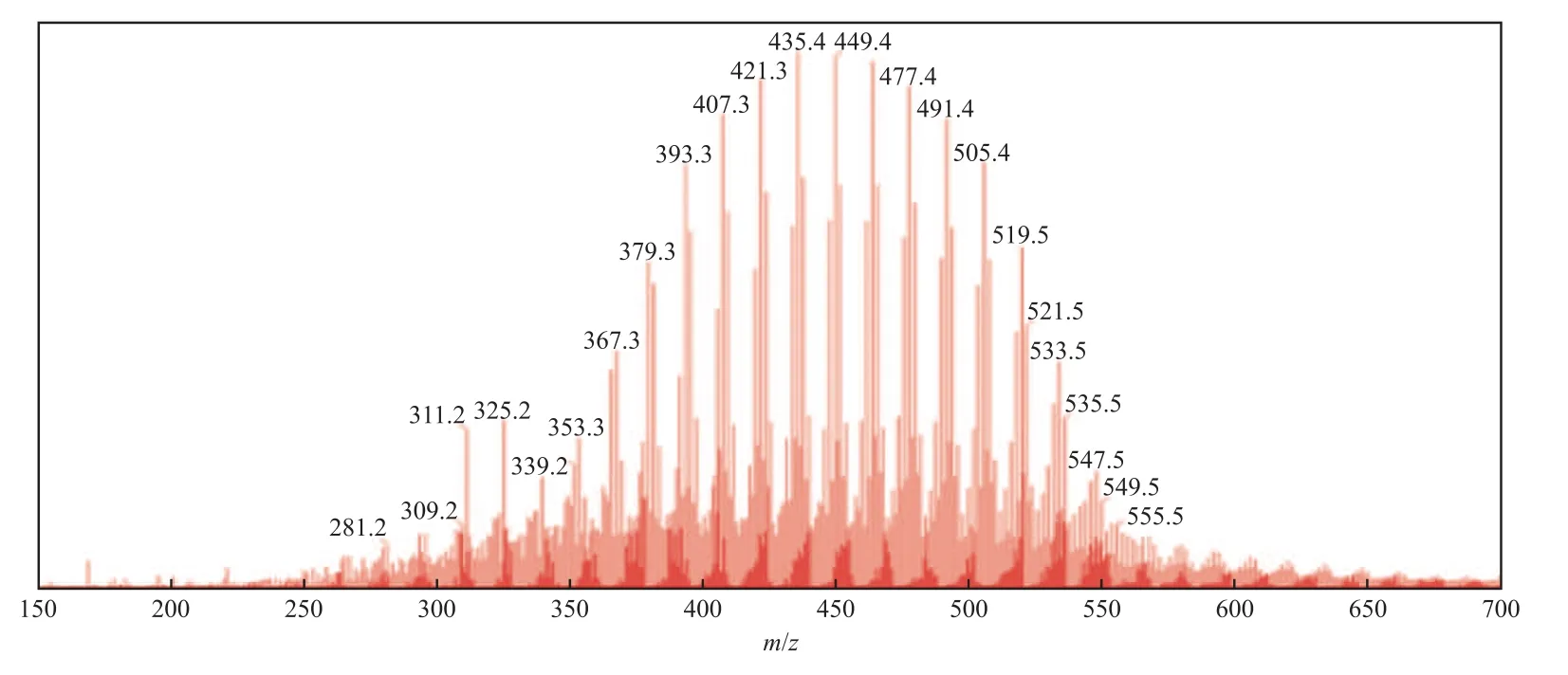
图4 HPLC-TOF MS分离的石油酸质谱图Fig.4 Mass spectrum of petroleum carboxylic acids by HPLC-TOF MS.Condition:methanol-0.1%(w)formate acid solution.
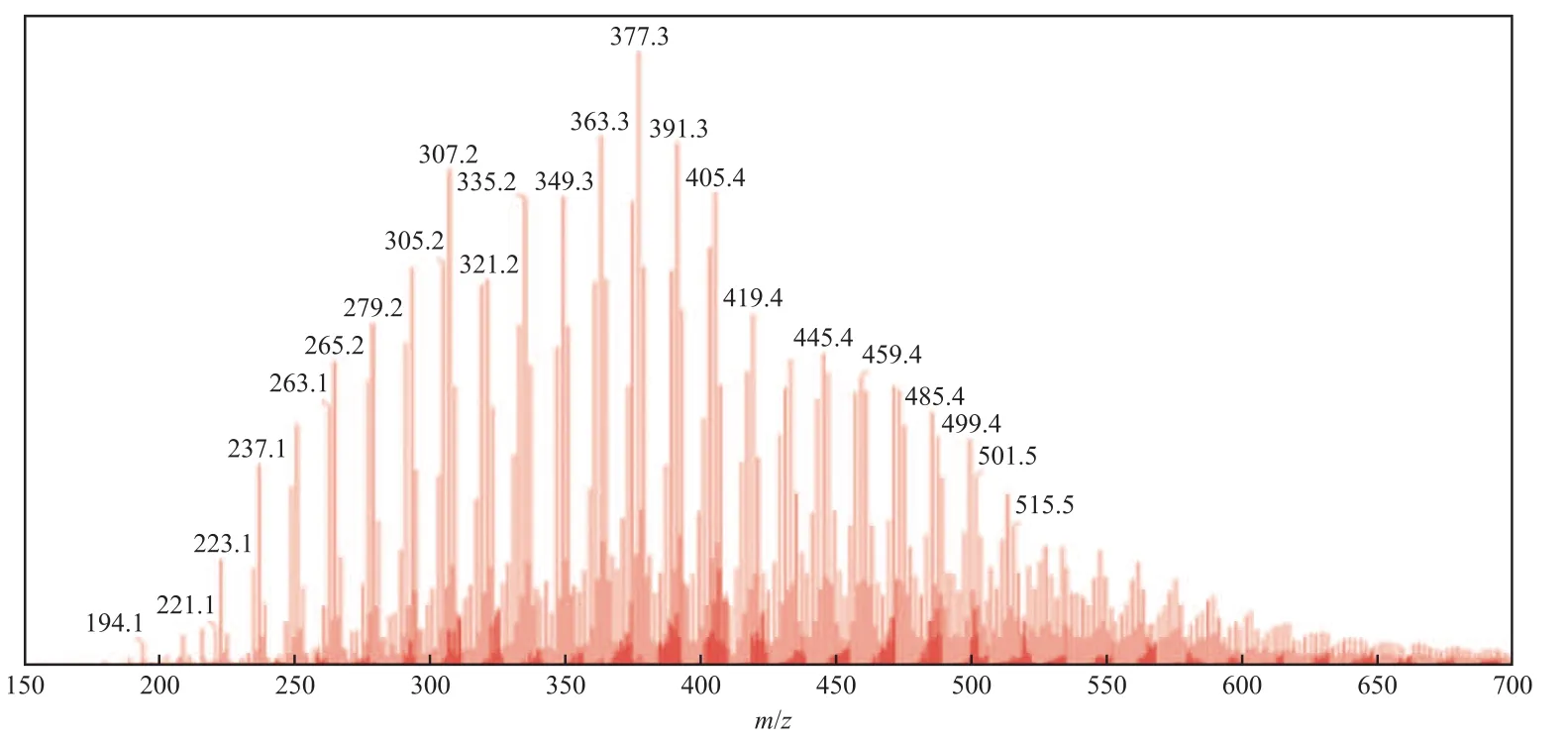
图5 HPLC-TOF MS分离的石油酸质谱图Fig.5 Mass spectrum of petroleum carboxylic acids by HPLC-TOF MS.Condition:methanol-0.1%(w) ammonia solution
2.5 九区原油中石油酸分布
2.5.1 质谱直接进样数据与HPLC-TOF MS数据比较
图3和图5给出了质谱直接进样和经HPLC分离后采集 的质谱图,对比可知,通过色谱分离获得的质谱图中,高质量端化合物响应(如m/z=377~515)明显强于直接进样方法的,且检测到了更多的酸性化合物。两种方法得到的质量数和强度分布均有差异,这是由于直接进样时,试样中各化合物间电喷雾电离会出现相互抑制的问题,导致直接进样分析得到的数据并不能较好地反映出石油酸的真实分布,从而影响定量分析。而通过HPLC分离,使不同类型的石油酸化合物分时到达质谱可较好地解决这一问题。
2.5.2 石油酸定性分析结果
通过HPLC分离,复杂的石油酸组分按照极性不同,流出顺序依次为烷基苯酸、羧酸二聚体和环烷酸。图6给出了烷基苯酸m/z=435和羧酸二聚体m/z=575及环烷酸m/z=377三个典型化合物的提取离子流谱图。从图6可看出,三种物质已基本实现分离。通过HPLC分离后进入质谱检测可有效地降低对质谱分辨率的要求和谱图解析的难度。
根据流出时间的差异,将质谱数据分割成三组进行处理,图7给出了三个馏分的质谱图。
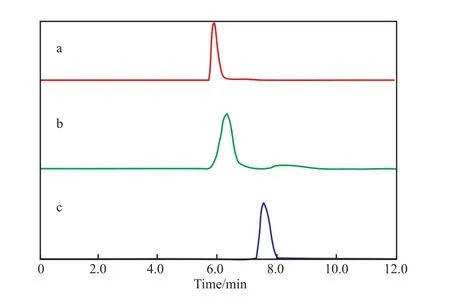
图6 三个典型石油酸化合物的提取离子流谱图Fig.6 Extracted ion chromatographs of three representative petroleum carboxylic acids.
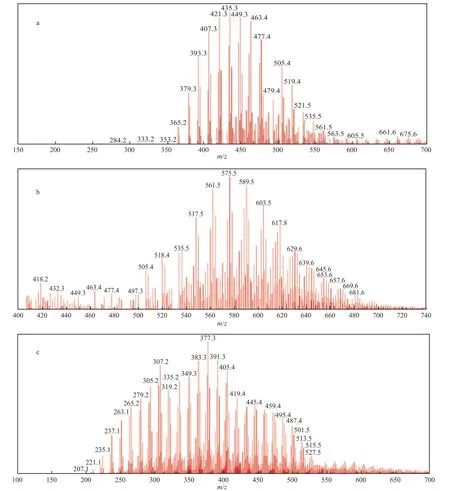
图7 经过色谱分离后得到的石油酸质谱图Fig.7 Mass spectra of petroleum carboxylic acids separated by HPLC.
图7a中质量分布m/z=353~481是碳数分布在24~33之间的烷基苯酸,其中,最高峰的m/z=435([M-H]-),绝对强度2.2×107,推断分子组成为C30H43O2。图7b中质量分布m/z=505~671是碳数分布在32~44之间的羧酸二聚体,最高峰m/z=575([M-H]-),绝对强度 1.4×107,推断分子组成为C37H67O4。图7c质量分布m/z=209~661是碳数分布在13~46之间的饱和脂肪酸和环烷酸,其中,最高峰m/z=377([M-H]-),绝对强度2.2×108,推断分子组成为C25H45O2,为二环环烷酸。
虽然不同结构化合物质的谱响应有差异,但比较谱峰强度差异后仍可得出:石油酸中的环烷酸含量较多,且二环环烷酸量最大,其次为一环和三环环烷酸。饱和脂肪酸、烷基苯酸和以二聚体形式存在的羧酸含量较低。除此以外,还发现了低含量含有O2S和O3S的酸性化合物存在[6]。综上可知,原油中石油酸的主要组成为脂肪酸、环烷酸和烷基苯酸,以及含有噻吩结构的一元有机羧酸,而不饱和脂肪酸和多元羧酸忽略不计。
2.5.3 石油酸半定量分析结果
通过归一化处理,可计算出不同类型羧酸化合物的相对百分含量具有相同的表达式CnH2n+zO2。图8a为质谱直接进样方法计算得到的石油酸分布,z=0为饱和脂肪酸,z=-18~-2为环烷酸,还包含烷基苯酸结构,但二者无法区分。由于液相色谱的分离作用,可以将不同类型石油酸分离并定量。图8b为HPLC-TOF MS方法得到的九区原油中石油酸分布。空心柱图代表饱和脂肪酸以及环烷酸类化合物的分布(z=-18~0);黑色实心柱图代表烷基苯酸类化合物的分布(z=-22~-12)。从图8可看出,两种方法检测到的石油酸分布趋势类似,但化合物类型与相对含量存在差异。九区原油中石油酸的饱和脂肪酸含量较少,二环环烷酸(z=-4)含量最多,其相对含量高达27%,其次为三环环烷酸(z=-6),再为一环环烷酸(z=-2)。z=-16的石油酸由多环环烷酸和烷基苯酸共存,且分布中烷基苯酸含量最高(图b)。但由于电喷雾电离的离子抑制效应,质谱直接进样的方法(图a)得到的石油酸种类较少,并没有检测到z=-20,-21的结构。且与图b相比,其主要羧酸的相对含量差异较大(如二、三环环烷酸含量等)。
李恪等[7]早期使用红外、核磁和质谱等方法对九区原油中石油酸的类型进行分析,证实链状羧酸含量在10%以下,环烷酸中以一至四环酸为主,尤以二、三环酸居多。这与本工作的定量结果相符。本工作采用原油直接萃取石油酸方法,利用HPLC的分离作用,使烷基苯酸类化合物分开定量,使不同类型石油酸化合物的定量分析结果更加准确。对于不同原油,Wu等[12]对于辽河重油的石油酸分析表明,石油酸中也以环烷酸居多,且二环环烷酸相对含量高达20%。
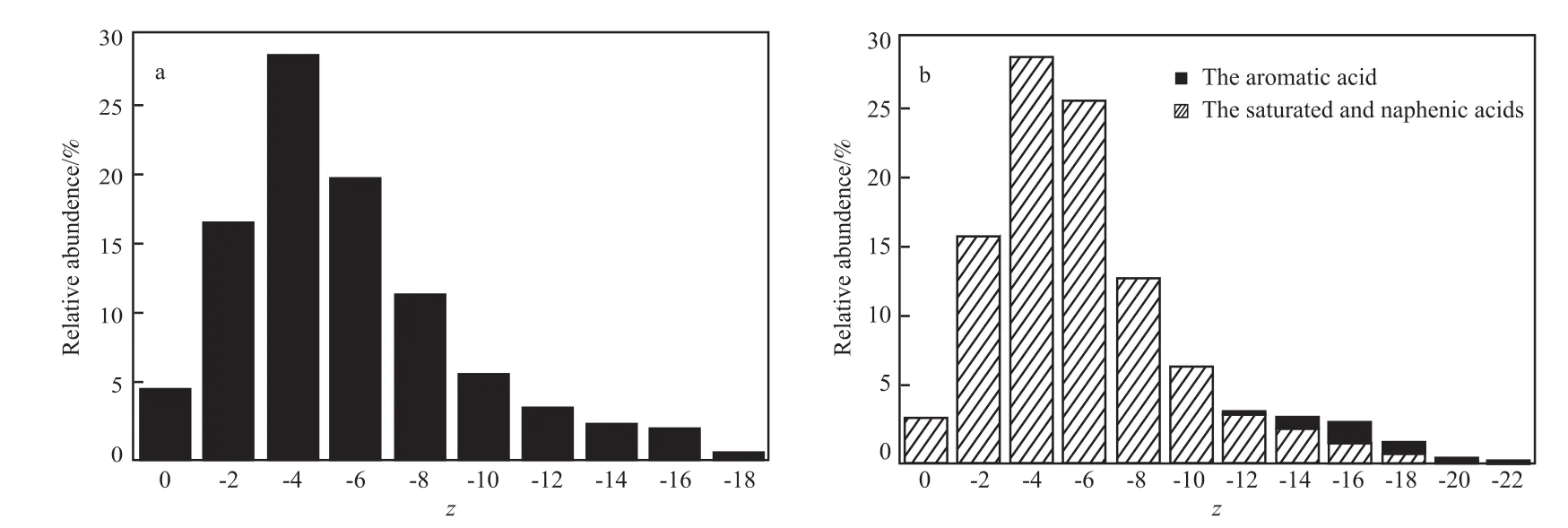
图8 质谱直接进样(a)和HPLC-TOF MS(b)两种方法得到的石油酸分布Fig.8 Acid distributions by direct MS(a) and HPLC-TOF MS(b).
3 结论
1)采用HPLC-TOF MS技术,结合负离子电喷雾电离方式,可将烷基苯酸、与饱和脂肪酸和环烷酸分离,有助于获得最接近真实分布的石油酸组成。
2)采用原油直接萃取石油酸方法,利用HPLC的分离作用,使不同类型石油酸化合物的定量分析结果更加准确。
3)九区原油总的石油酸主要由环烷酸构成,且二环环烷酸含量最高;另含有少量饱和脂肪酸、烷基苯酸、羧酸二聚体,以及低含量含有O2S和O3S的酸性化合物。

