石墨烯对改性大豆蛋白胶性能的影响
杨 光,王睿聪,杨 波,李 琴,袁少飞
(1.上海理工大学 医疗器械与食品学院,上海 200093;
2.浙江省林业科学研究院 浙江省竹类研究重点实验室,浙江 杭州 310023)
大豆蛋白胶作为一种新型胶黏剂,原料来自大豆蛋白,加工过程中不加入任何甲醛成分,因而完全没有甲醛隐患;但与传统胶黏剂相比,大豆蛋白胶具有黏度高、流动性差、机械强度差、耐水性不好等问题,故大豆蛋白胶的改性研究备受关注[1]。
石墨烯是一种由单层碳原子sp2杂化堆积成的具有二维蜂窝状晶体结构的碳质材料[2],具有优异的强度、柔韧性、导电性、导热性和光学特性[3]。由于石墨烯优异的性能,因此广泛用于生产高能效材料、印刷电子、透明导体、耐用飞机材料、纳米复合材料以及催化剂等方面[4]。石墨烯和石墨烯基材料也广泛用于独特的生物医学领域[5]。石墨烯具有高比表面积,可附着各种生物分子,这种性能有助于官能化和表面修饰的简易化,因此石墨烯成为现代药物递送系统的潜在候选者[6]。基本的生物分子相互作用(如核酸相互作用、脂质和蛋白质相互作用、氧化反应和生物降解等[7])也可促进石墨烯在药物递送中的利用。迄今为止,石墨烯及其衍生物在基因转移、生物传感、光疗、抗菌应用、细胞培养和组织工程等领域有广泛研究[7]。研究发现,石墨烯即使在经历外界剧烈的化学作用后仍然能保持较好的二维平整结构,进而延续其优异的摩擦润滑特性,相关成果有助于推动二维材料在微纳摩擦与润滑领域的应用[8]。
本工作在改性大豆蛋白胶中加入石墨烯,采用SEM,DSC,FTIR等表征手段研究了石墨烯的加入对改性大豆蛋白胶性能及结构的影响,以期石墨烯的润滑及强韧特性可以对大豆蛋白胶进行降黏的同时提升胶合强度,旨在为石墨烯的应用提供一种新途径。
1 实验部分
1.1 原料与试剂
大豆蛋白粉:蛋白质含量为90.54%(w),旺鑫生物科技有限公司;盐酸胍:分析纯,国药集团化学试剂有限公司;石墨烯:工业级,苏州恒球石墨烯科技有限公司;杨木单板:250.0 mm×250.0 mm×1.2 mm,含水率为8.731%(w)。
1.2 仪器与设备
FA2104型电子天平:上海舜宇恒平科学仪器有限公司;JB-2型恒温磁力搅拌器:上海雷磁仪器有限公司;DHG-9203A型鼓风干燥箱:上海一恒科技有限公司;150T型全自动热压机:苏州新协力有限公司;MWD-W50型人造板万能力学试验机:济南机械材料厂;Q2000型差示扫描量热仪:德国Netzsgh公司;Quanta FEG 450型扫描电子显微镜:美国FEI公司;Nicolet iS10型傅里叶变换红外光谱仪、DYY-2C型电泳仪:Thermo Fisher公司;DYCZ-24DN型电泳槽:北京市六一仪器厂;LGJ-10D型冷冻干燥机:北京四环科学仪器厂。
1.3 改性大豆蛋白胶的制备
称取大豆蛋白粉10 g,加入1.5 mol/L的盐酸胍100 mL,在40 ℃的条件下充分搅拌5 h,制得改性大豆蛋白胶。
1.4 测试与表征
大豆蛋白粉中蛋白质含量用凯氏定氮法测定[9]。
重量法测单板含水率:将干燥前的单板称重,在103 ℃左右烘至绝干后称重,用两次的质量差,求出单板的含水率。
胶合强度的测定:将杨木单板在热压温度130 ℃,热压时间10 min,双面涂胶量400 g/m2的热压条件压制胶合板。按GB/T 17657—2013 人造板及饰面人造板理化性能试验方法锯制试件测胶合强度[10]。
DSC分析:将冻干后的改性大豆蛋白胶与加入石墨烯的改性大豆蛋白胶研磨成粉末状,取2~5 mg放入铝皿中,氮气气氛,温度20~220 ℃,升温速率10 ℃/min,分析试样在升温过程中的吸放热情况。
十二烷基硫酸钠聚丙酰胺凝胶电泳实验(SDS-PAGE):取改性大豆蛋白胶及加入石墨烯的改性大豆蛋白胶进行电泳分析,并以大豆蛋白的水溶液作对照,分析改性过程中蛋白质的变化及石墨烯对改性大豆蛋白胶的影响。
取适量大豆蛋白粉与冻干后的两种大豆蛋白胶,进行镀金处理,采用SEM在10 kV的加速电压下观察试样形貌。将大豆蛋白粉与冻干后的两种大豆蛋白胶分别制成粉末,进行FTIR分析。KBr压片,波数400~4 000 cm-1。
2 结果与讨论
2.1 石墨烯加入量的确定
石墨烯加入量对大豆蛋白胶初黏度的影响见图1。由图1可见,随石墨烯加入量的增多,大豆蛋白胶的初黏度逐渐降低。这是因为石墨烯的水不溶性和团聚效应[11]及相应的润滑性所致。石墨烯的加入量越多,包裹在大豆蛋白胶颗粒外的石墨烯颗粒越多,致使溶液的初黏度逐渐下降;且石墨烯的加入量越多,大豆蛋白胶的颜色越深,由黄褐色逐渐变为黑色。
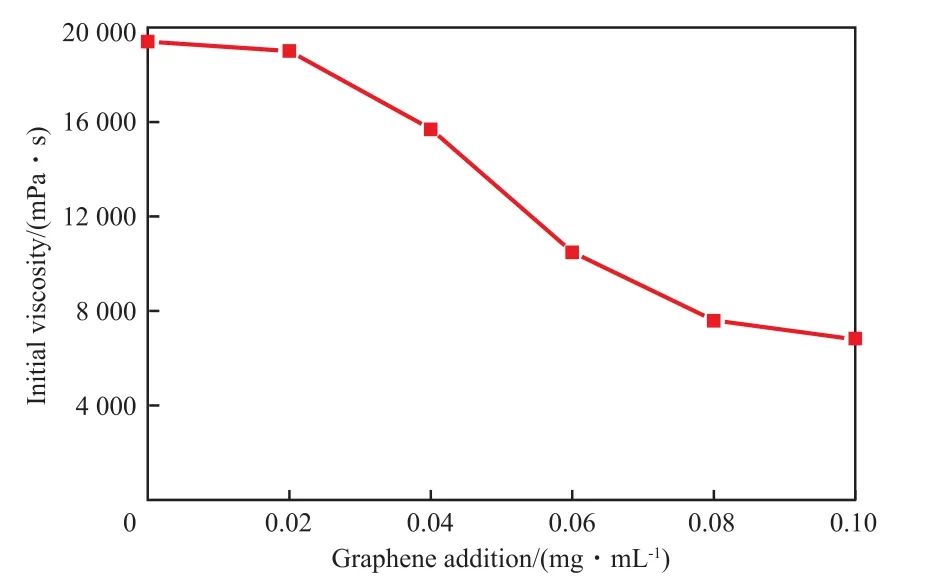
图1 石墨烯加入量对大豆蛋白胶初黏度的影响Fig.1 Effects of graphene addition amount on initial viscosity of soy protein adhesive.
石墨烯加入量对大豆蛋白胶胶合强度的影响见图2。由图2可见,随石墨烯加入量的增多,大豆蛋白胶的胶合强度逐渐增高后持平。这是因为,加入石墨烯后,改性大豆蛋白胶的黏度下降,在黏结胶合板的过程中更利于施胶的均匀性。同时石墨烯是一种新型纳米材料,具有非常高的韧性[12],将它加入到大豆蛋白胶中,在胶合板的热压过程中随着胶黏剂逐渐分散到杨木单板,致使大豆蛋白胶的胶合强度有所提高。而当石墨烯的加入量超过0.04 mg/mL后,大豆蛋白胶的黏度过低,包裹在胶黏剂颗粒外的石墨烯颗粒也会发生相互排斥作用,致使胶合强度持平后还略有降低。综上,石墨烯的最佳加入量为0.04 mg/mL,此时改性大豆蛋白胶的干状剪切强度为1.577 MPa,湿状剪切强度为0.746 MPa。

图2 石墨烯加入量对大豆蛋白胶胶合强度的影响Fig.2 Effects of graphene addition amount on bonding strength of soy protein adhesive.
2.2 SEM分析结果
大豆蛋白粉水溶液冻干后的SEM照片见图3。

图3 大豆蛋白粉水溶液冻干后的SEM照片Fig.3 SEM image of soybean protein powder aqueous solution after freeze-drying.
由图3可见,大豆蛋白粉表面比较粗糙,结构比较紧实,这是因为本实验用的大豆蛋白粉中大豆蛋白的含量为90.54%(w),蛋白质中的氨基酸由肽链折叠弯曲成各种空间结构,分子中还有维持蛋白质构象的氢键、离子键、范德华力及共价键,其他如二硫键等也对蛋白质结构有一定的维持作用,未经过改性处理,各种构成蛋白质结构的价键未遭到破坏,构成功能结构的官能团未遭暴露,故蛋白粉颗粒的结构粗糙且紧实,这种结构不利于在黏结胶合板时发生交联反应。
改性大豆蛋白胶冻干后的SEM照片见图4。由图4可见,与大豆蛋白粉相比,未加入石墨烯的改性大豆蛋白胶表面比较光滑,有很多空隙,结构相对较松散。这说明大豆蛋白经过盐酸胍改性后,部分氢键断裂,蛋白质分子中发挥胶黏作用的官能团暴露。由盐酸胍改性蛋白质的机制可知,蛋白质分子中某些非共价键断裂,与盐酸胍形成复合物致使空间结构遭到破坏,相对应的理化性质发生改变,微结构也发生变化。改性大豆蛋白胶中松散的结构与缝隙的存在有利于交联反应的发生,在黏结胶合板的过程中可以增大与被黏物的接触面积。

图4 未加入石墨烯的改性大豆蛋白胶冻干后的SEM照片Fig.4 SEM image of modified soybean protein adhesive without graphene after freeze-drying.
加入石墨烯的改性大豆蛋白胶冻干后的SEM照片见图5。由图5可见,与未加入石墨烯的改性大豆蛋白胶相比,加入石墨烯的改性大豆蛋白胶结构更松散,缝隙较多,呈现多孔网状结构。石墨烯是一种新型纳米材料,不溶于水且有独特的强韧性及良好的润滑性能[13],还有一定的团簇效应,在大豆蛋白胶的改性过程中加入石墨烯,蛋白质分子的各种价键及空间结构被盐酸胍破坏,而石墨烯附着在这些被破坏的分子表面形成团簇,致使加入石墨烯的改性大豆蛋白胶的表面较为粗糙且缝隙较多,更利于在黏结胶合板过程中与单板发生交联反应,这可能也是加入石墨烯使大豆蛋白胶黏度降低的原因。

图5 加入石墨烯的改性大豆蛋白胶冻干后的SEM照片Fig.5 SEM image of modified soybean protein adhesive with graphene after freeze-drying.
2.3 DSC分析结果
2.3.1 未加入石墨烯的改性大豆蛋白胶的DSC分析结果
大豆蛋白经改性制得大豆蛋白胶,在改性过程中,大豆蛋白的结构官能团及肽链都会发生一定的变化。未加入石墨烯的改性大豆蛋白胶的DSC曲线见图6。
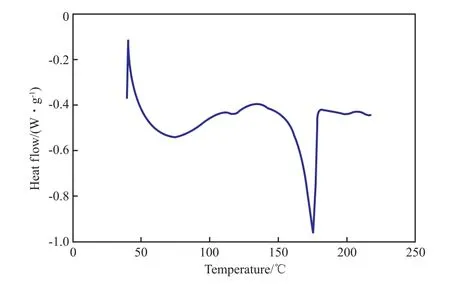
图6 未加入石墨烯的改性大豆蛋白胶的DSC曲线Fig.6 DSC curve of modified soy protein adhesive without grapheme.
由图6可见,未加入石墨烯的改性大豆蛋白胶出现两个吸热峰,第一个吸热峰从50.00 ℃开始,在温度升高到73.06 ℃时达到顶峰,到100.00 ℃时第一个峰趋于平缓,通过面积积分可知第一个吸热峰吸收的热量是46.76 J/g,通过温度区间可以判断这个吸热峰是水分的吸热峰。第二个吸热峰在164.67 ℃时出现,在175.57 ℃时达到顶峰,到180.00 ℃结束,该吸热峰吸收的热量是37.62 J/g,由吸热峰的温度范围可以判定第二个吸热峰是未加入石墨烯的改性大豆蛋白胶的吸热峰。从图6还可以看出,冻干后的未加入石墨烯的改性大豆蛋白胶的固化温度在175.57 ℃左右。
2.3.2 加入石墨烯的改性大豆蛋白胶的DSC分析结果
加入石墨烯的改性大豆蛋白胶的DSC曲线见图7。由图7可见,加入石墨烯的改性大豆蛋白胶也有两个吸热峰,第一个热吸热峰出现在45.94 ℃,在71.91 ℃时达到顶峰,到100.00 ℃左右时该曲线趋于平缓,该吸热峰吸收的热量为53.16 J/g,为大豆蛋白胶中水分的吸热峰,与图6相比,水分吸热峰峰值温度略微降低,吸热量从46.76 J/g增加到53.16 J/g,增加了12.04%,这可能与样品冻干后的含水率有关。第二个吸热峰峰值温度为130.00~180.00 ℃,从169.29 ℃开始吸热,在174.68 ℃时达到顶峰,到180.00 ℃结束,该吸收峰吸收的热量是38.77 J/g。加入石墨烯的改性大豆蛋白胶的固化温度也在175.00 ℃左右,与未加入石墨烯的改性大豆蛋白胶的固化温度差别不大,说明加入石墨烯对改性大豆蛋白胶的固化温度无影响。在改性过程中石墨烯颗粒包裹在大豆蛋白胶颗粒外,降低了改性大豆蛋白胶的黏度,除了石墨烯的强韧性之外,一定情况下,大豆蛋白胶黏度的降低更有利于与木板纤维发生交联反应。

图7 加入石墨烯的改性大豆蛋白胶的DSC曲线Fig.7 DSC curve of modified soy protein adhesive with grapheme.
2.4 SDS-PAGE实验
大豆蛋白主要是球蛋白,约占85%(w);根据沉降系数的不同,主要有7S,11S两种[14]。大豆蛋白粉、未加入石墨烯的改性大豆蛋白胶及加入石墨烯的改性大豆蛋白胶分子中的蛋白质分布见图8。由图8可见,3种试样的蛋白质都是分布在15~75 kDa的大分子蛋白。3种试样的蛋白质的相对分子质量分布基本相同,说明盐酸胍在改性大豆蛋白粉制备大豆蛋白胶的过程中,盐酸胍与蛋白质的反应并未引起蛋白质中的氨基酸肽链的断裂,改性机理是盐酸胍附着在蛋白质分子表面形成复合物从而使蛋白质改性,所以相对分子质量分布没有发生变化。加入石墨烯后,谱线的条带也没发生显著变化,说明石墨烯没有直接参与到改性反应中,其存在方式可能是黏附在蛋白胶颗粒表面,而吸附在表面的石墨烯颗粒之间的相互润滑作用引起了改性大豆蛋白胶黏度的降低。

图8 3种试样的SDS-PAGE实验Fig.8 SDS-PAGE analysis of three samples.
2.5 FTIR分析结果
蛋白质的谱线一般分为几组特征吸收谱带。酰胺Ⅰ,酰胺Ⅱ,酰胺Ⅲ的波长分别对应1 600~1 700,1 530~1 550,1 200~1 300 cm-1[15]。大豆蛋白粉与两种改性大豆蛋白胶的FTIR谱图见图9。由图9可见,3种试样中都含有蛋白质的典型酰胺吸收光谱带,2 700~3 500 cm-1处是H化学键的伸缩振动峰。其中,3 100~3 500 cm-1处是O—H和N—H 的伸缩振动吸收峰,2 940~2 980 cm-1处是甲基中C—H的伸缩振动吸收峰;1 644 cm-1处是酰胺键中C==O 的吸收峰;1 535 cm-1处是酰胺键中C==C的吸收峰;1 240 cm-1处为酰胺Ⅲ中CN的伸缩振动和NH的面内变形振动峰,1 100 cm-1处是伯醇中C—O伸缩振动吸收峰。两种改性大豆蛋白胶在3 400~3 500 cm-1处有伸缩振动吸收峰,且两种蛋白胶的吸收峰宽度相比于大豆蛋白粉右移且变宽,表明大豆蛋白的羟基与羟基、氨基与氨基、羟基与氨基之间极有可能存在分子间氢键,而经过改性后大豆蛋白中的这些氢键被暴露出来,可能存在交联反应。与大豆蛋白粉相比,两种改性大豆蛋白胶的胶酰胺Ⅱ和酰胺Ⅲ的吸收谱带稍微减弱,这表明在盐酸胍改性大豆蛋白的过程中可能存在C==C打开与盐酸胍形成复合物,而—NH2相对减少。这些官能团的变化是大豆蛋白胶黏结性形成的化学基础[16]。两种改性大豆蛋白胶曲线走向基本相似,说明石墨烯的加入没有影响蛋白胶的改性过程,与SDS-PAGE结果相一致,也进一步说明石墨烯引起改性大豆蛋白胶的降黏效果是物理作用。

图9 大豆蛋白粉与两种改性大豆蛋白胶的FTIR谱图Fig.9 FTIR spectra of soy protein and two modified soy protein adhesives.
3 结论
1)石墨烯的最佳加入量为0.04 mg/mL。石墨烯的加入对大豆蛋白胶有一定的降黏作用,使改性大豆蛋白胶在黏结胶合板时胶合强度有一定的提升,是由于降黏作用还是石墨烯的强韧性,有待进一步探索研究。
2)大豆蛋白粉结构紧实,表面粗糙,这种结构不利于发生交联反应;未加入石墨烯的改性大豆蛋白胶表面出现空隙,这种结构更有利于发生交联反应;加入石墨烯的改性大豆蛋白胶结构呈现疏松多孔状,空隙更加密集。
3)石墨烯对大豆蛋白胶的固化温度,蛋白质相对分子质量分布及官能团的变化没有影响,说明石墨烯的加入没有影响大豆蛋白胶的改性过程,对改性大豆蛋白胶的降黏是物理作用。

