帕金森病的发病机制、诊断标准及治疗策略
梁建庆
1817年,英国医生James Parkinson最早发表了关于震颤麻痹的论文,首次描述了帕金森病(Parkinson's disease,PD)的概念、病程和临床症状。令人遗憾的是,该著作发表后少有人问津。1877年,法国医生Jean Martin Charcot将这种病命名为PD,随后受到人们的广泛关注[1]。PD是一种好发于中老年人的常见的神经系统退行性疾病,我国65岁以上人群患病率为1700/10万,且随年龄增长逐渐升高,给家庭和社会带来了沉重的负担[2]。医学界最初认识PD距今已近200年,人们对PD的认识脚步并未放缓,研究成果及远期前景令人鼓舞。
1 PD的发病机制
PD的主要病理特征是中脑黑质致密部多巴胺能神经元变性缺失,退变神经元内有特征性的路易小体(Lewy body)。本病病因迄今未明,发病机制十分复杂,与众多因素有关[3]。α-突触核蛋白(α-syn)是一种可溶性蛋白质,是路易小体的主要组成部分,α-syn基因突变与遗传性PD的发生有关[4]。大脑中暴露于α-syn的细胞伴有趋化因子和促炎症因子上调,神经胶质细胞活化,神经毒性增加,可抑制酪氨酸羟化酶(tyrosine hydroxylase,TH)的表达,导致多巴胺能神经元减少。当α-syn过表达或发生突变时,蛋白质结构易出现错误折叠,积聚为有神经毒性的寡聚物,并能吸引正常结构的α-syn聚集。同时PD患者的血脑屏障滤过率发生改变,脑对α-syn的摄取量增加,使其在中枢神经系统内堆积,损伤多巴胺能神经元,导致PD发生[5]。多巴胺能神经元含有神经递质多巴胺(DA),后者在代谢过程中会产生氧自由基(OFR),使多巴胺能神经元处于氧化应激状态,造成氧化损伤[6-7]。DNA甲基化是表观遗传学的重要组成部分,是在DNA甲基化转移酶(DNMTs)的作用下使CpG二核苷酸5'-端的胞嘧啶(C)转变为5'-甲基胞嘧啶(5mC)的过程。DNA甲基化可关闭某些基因的活性,去甲基化则诱导了基因的重新活化及表达。DNA甲基化能引起染色质结构、DNA构象、DNA稳定性及DNA与蛋白质相互作用方式的改变,从而控制基因表达。Lee等[8]和Charlton等[9]发现,将内源性甲基供体S2腺苷蛋氨酸(SAM)注入啮齿类动物脑内可导致PD样改变,提示过度甲基化可能为PD的诱发因素。Obeid等[10]发现PD患者外周血中SAM相对含量下降;Pieper等[11]发现,PD患者黑质致密部细胞中的TNF-α启动子甲基化水平降低,SNCA内含子1甲基化水平降低,提示低甲基化可能与PD的发病相关。目前,DNA甲基化与PD发病机制关系的研究已经起步,但研究成果不多,结果存在矛盾之处,因此,仍须进一步研究。
神经营养因子(neurotrophic factors,NTFs)是一类由神经元的靶组织、神经元自身,以及神经胶质细胞合成分泌的可溶性多肽或蛋白质,可以调节神经元的存活、分化,神经突起的生长及突触的可塑性,维持成年动物神经系统结构、功能的稳定,参与损伤后神经再生过程等。研究发现,补充脑源性神经营养因子(BDNF)和胶质细胞源性神经营养因子(GDNF)可上调TH的转录表达,阻止多巴胺能神经元凋亡,促进其功能恢复[12]。目前,有研究发现PD致病因素如α-syn、PTEN诱导的蛋白激酶1(PTEN induced putative kinase 1,PINK1)基因等与细胞自噬密切相关[13-14]。PINK1活化异常,线粒体修复不足等,均可促进线粒体自噬,细胞发生凋亡,从而形成PD。因此,PINK1活化是线粒体修复及线粒体损伤后依赖泛素化清除的关键,可直接促使多聚泛肽链磷酸化而介导线粒体修复及Parkin蛋白的活化[13-14],后者可加速多巴胺能神经元变性死亡及胞质内路易小体的形成。PD的发病还与神经递质(单胺类、氨基酸类)、神经炎症、miRNA、钙的细胞毒作用、免疫学异常、细胞凋亡等有关。目前普遍认为PD并非单一因素致病,可能有多种因素参与。此外,遗传因素可使PD患病易感性增加,在环境因素及年龄老化的共同作用下,通过α-syn、氧化应激、DNA甲基化、神经营养因子、线粒体自噬、神经递质、神经炎症、miRNA、钙的细胞毒作用、免疫学异常、细胞凋亡等机制引起黑质多巴胺能神经元变性,导致PD发病。
2 PD的诊断标准
PD的临床症状和体征有一定特点,如震颤、强直、少动(运动徐缓)、姿势异常和姿势反射障碍等,若症状典型、体征明确,则诊断不难。但由于PD进展缓慢,早期症状较轻,何时出现首发症状并不明确,而且各种症状并不按固定次序出现,因此容易漏诊、误诊[15]。1984年,全国锥体外系疾病讨论会曾提出PD及帕金森综合征的诊断标准和鉴别诊断[16],其中原发性PD的诊断标准为:①至少具备4个典型的症状和体征(静止性震颤、少动、僵直和位置性障碍)中的2个;②是否存在不支持诊断原发性PD的不典型症状和体征如锥体束征、失用性步态障碍、小脑症状、意向性震颤、凝视麻痹、严重的自主神经功能障碍、明显的痴呆伴有轻度锥体外系症状;③脑脊液中高香草酸减少,对确诊早期PD,以及特发性震颤、药物性帕金森综合征与PD的鉴别均有帮助。这是国内最早的PD官方权威诊断标准。2002年,刘焯霖[17]提出了PD的诊断标准,较1984年的标准有所改进和完善。2006年,蒋雨平等[18]也提出了原发性PD的诊断标准,具体诊断标准更加细化。为了达到早期诊断的目的,PD的诊断标准处于不断更新的状态,在英国脑库PD临床诊断标准的基础之上,《2016中国PD诊断标准》[19]参考了2015年国际运动障碍病学会(MDS)推出的PD临床诊断新标准,结合我国国情,对中国2006年发布的PD诊断标准进行了更新。帕金森综合征的核心症状去掉了姿势平衡障碍。新的诊断标准分成临床确诊和临床可能两个层级,支持标准精简为4项,增加了辅助检查和非运动症状作为支持标准之一。此外,将缺乏非运动症状也作为警示标准之一[20],具体内容见图1。目前,PD的诊断依然是经验性诊断,尽管国内外每年都有对PD诊断指南的解读与更新[21],但临床表现、各种检查、对多巴胺能药物的反应,以及后期运动症状波动仍是诊断的基石。放眼未来,寻找诊断PD的客观标志物,制订诊断PD的金标准,仍然有很多工作要做。但只要我们坚持实践-理论-实践的科研指导思想,坚信实践是理论之源,必然催生PD诊断的新标准、新思想及新理论。
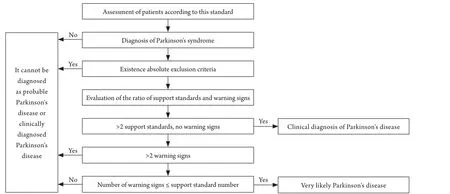
图1 帕金森病诊断流程图Fig.1 Diagnostic flow chart for Parkinson's disease
3 PD的现代治疗策略
PD的临床治疗进展较快。从20世纪60年代开始,DA制剂就已经用于临床并使广大PD患者受益,此后又相继出现了DA制剂增效剂、多巴胺能受体激动剂、单胺氧化酶B抑制剂。80%的患者对DA制剂有良好的治疗反应。为了减少患者的外周反应及长期服药后的症状波动,近年来,一些新型DA制剂,如贴剂、肠道胶或者超长效制剂陆续上市。作为药物治疗的补充,深部脑刺激(DBS)治疗的应用越来越广泛,对于患者的震颤、运动波动有非常明显的改善作用[22]。除上述方法外,其他如运动疗法、职业疗法、音乐疗法等均可辅助治疗PD,其中太极拳疗法获得了广泛关注[23]。2014年,中华医学会神经病学分会PD及运动障碍学组制订发布了《中国PD治疗指南(第三版)》[24](由上海交通大学附属瑞金医院陈生弟教授执笔),该学组在2006年和2009年分别制订了第一、二版中国PD治疗指南,对规范和优化我国PD的治疗行为和提高治疗效果均起到了重要的作用。近年来,国内外在该治疗领域又有了一些治疗理念的更新和治疗方法的进步。为了更好地适应其发展,更好地指导临床实践,指南制订组对中国PD治疗指南第二版进行了必要的修改和更新。新版指南明确提出,对PD的运动症状和非运动症状应采取全面综合治疗的理念,同时强调了“早诊断、早治疗”的用药原则[25]。陈生弟教授呼吁:“广大神经科医生须在临床实践中参考新指南,以控制PD症状、延缓疾病进展为治疗目标,使患者生活质量得到长期改善。”PD的治疗没有绝对的固定模式,但必须强调“个体化、精准化”治疗。不同患者之间的症状可能会存在区别,对治疗的敏感度也存在一定差异,不同患者对治疗的需求存在差异,同一患者在不同病情阶段对治疗的需求也不尽相同。因此,2014版指南可能适用于一般规律,在临床实际应用时,须注意详细了解患者的病情(疾病严重程度、症状类型等)、治疗反应情况(是否有效、起效时间、作用维持时间、“开期”延长和“关期”缩短时间、有无不良反应或并发症)等,结合医师自己的治疗经验,既遵循指南,又体现灵活性原则,以期达到更为理想的治疗效果。具体内容见图2-4,分别描述了早期PD的治疗方法、患者症状波动期的处理措施、出现并发症如异动症的处理原则等,内容翔实,可操作性强。
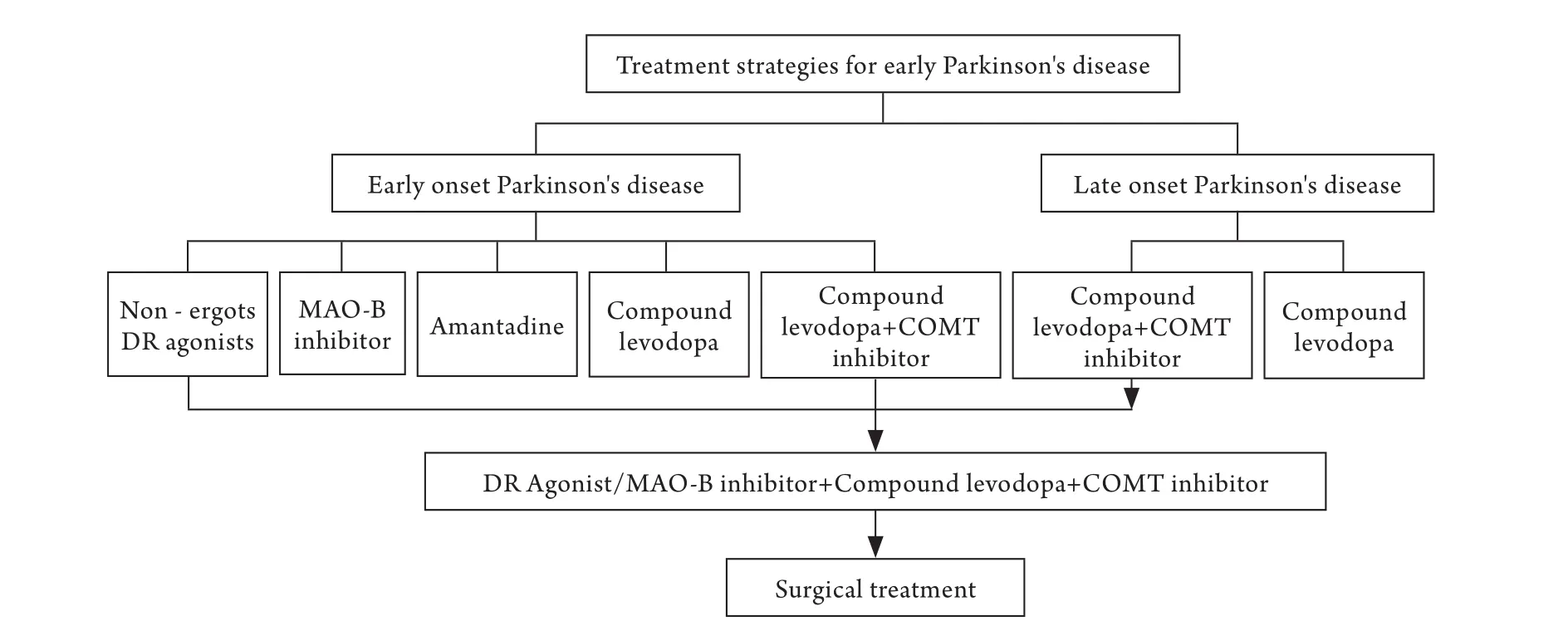
图2 早期帕金森病的治疗策略Fig.2 Treatment strategies for early Parkinson's diseaseDR.Dopamine receptors; MAO-B.Monoamine oxidase B; COMT.Catechol-o-methyl transferase
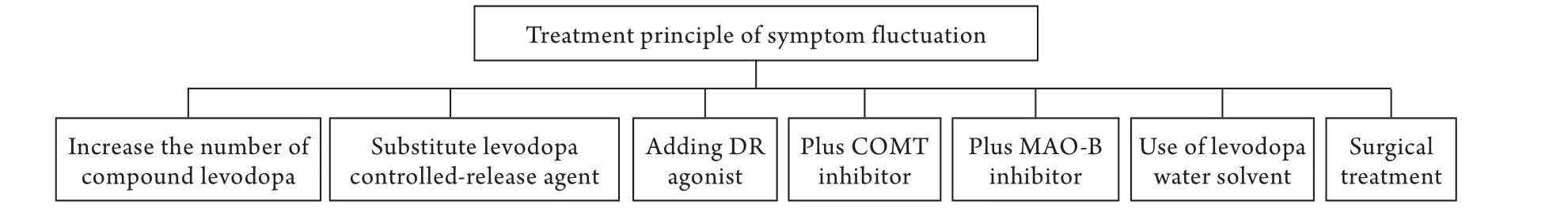
图3 症状波动的处理原则Fig.3 Principle of treatment of symptom fluctuationDR.Dopamine receptors; MAO-B.Monoamine oxidase B; COMT.Catechol-o-methyl transferase

图4 异动症的处理原则Fig.4 Treatment principle of dyskinesiaDR.Dopamine receptors; COMT.Catechol-o-methyl transferase
4 小 结
基于PD具有慢性病程、患病率高和致残率高等特点,目前已成为老龄化社会中受到高度关注的重要医学和社会问题。因此,PD的发病机制、早期诊断和治疗研究成为热点和焦点[26]。尽管近200年来,PD的相关研究取得了一定的成果,但我们要清醒地认识到,PD发病机制的神秘面纱仍然没有被彻底揭开。因此,临床实践中仍存在诸多困惑,如PD缺乏准确的早期客观化诊断指标,也无预防和阻止疾病进展的有效方法。未来PD的研究任务依然任重而道远,值得科研工作者深思和探讨的未知领域很多,但只要科研思路正确、科研方法得当,PD的研究定会出现“山重水复疑无路,柳暗花明又一村”的景象。

