提锂技术进展
朱加乾 徐宝金 宋学文 陈 波
(1.福州大学紫金矿业学院,福建福州350108;2.安徽马钢罗河矿业有限责任公司,安徽巢湖231562)
锂是最轻的碱金属,被誉为21世纪“推动世界进步的重要能源元素”之一,锂及其化合物性质优良,应用范围遍及电池、医学、航天、化工以及国防等多个领域。随着国民节能环保意识的增强以及新能源市场的崛起,锂及其化合物作为清洁能源受到了广泛关注。但是,新型锂材料的研发速度却远远满足不了市场上急速增长的锂需求量,因此,提高国内工业提锂技术水平(尤其是卤水提锂技术)迫在眉睫。合理地开发利用我国丰富的锂资源,不但能使我国逐渐摆脱锂资源(锂辉石矿)进口的困境,并且能够在锂资源市场上占据一定的优势地位。
1 锂矿资源现状
世界上锂矿资源储量丰富,截止当前已探明的锂矿资源(金属量)储量约为4 300万t,主要锂资源国的金属锂产量、储量和各自的占比情况如图1和图2所示。
由图1可以看出:玻利维亚已探明的锂资源储量位居世界第一,总储量约为1 020万t,其次是美国,约为992万t,而中国的锂资源储量也比较丰富,位居世界第三位,约为710万t,加上智利和阿根廷2个国家,储量前5位国家目前已探明的锂资源储量总和约占全球锂资源的93.6%,其中南美洲“锂三角”(玻利维亚、智利、阿根廷)占据了全球约54%的锂矿资源[1-2]。

由图2可以看出:澳大利亚是全球最大的锂生产国,产量占比高达40.51%,尽管其锂资源储量并不是最大,约为66万t,但是其锂辉石矿储量却极其丰富,是目前世界上最大的锂辉石矿出口国;第二大锂生产国的国家是智利,产量占比达到33.99%,二者的锂生产量总和约占全球的74.50%。我国锂产量位居世界第4位,约为2 000 t,但是,同时我国也是全球最大的锂资源消费国,目前仍需进口大量的锂矿资源,其中大部分的锂矿资源(锂辉石矿约占66%)来自澳大利亚[3]。
2 锂矿床类型及矿物种类
锂在自然界中主要赋存于固体矿石和盐湖卤水中。在地球岩石圈中含量排名第35位,总量达918万亿t,但是地球岩石圈厚度高达150 km,实际能被勘探并开采利用的锂矿资源非常少[4]。金属锂主要存在于伟晶岩及花岗岩矿床、卤水矿床、含锂黏土矿床和含锂沸石矿床等4大类矿床中,其占比分别约为26%、64%、7%、3%[5],其中伟晶岩及花岗岩矿床、卤水矿床这2类含锂矿床最具经济开发价值。锂辉石、透锂长石、锂云母、磷锂辉石等是应用于工业提锂的主要含锂矿物,其中锂辉石是伟晶岩中提锂最常见的矿石,常与绿柱石、石英以及钽铌铁矿伴生,占每年锂产品生产原料的30%。目前,针对自然界存在的最具经济价值的2大类含锂矿床,提锂技术可以分为2大类:卤水提锂技术和矿石提锂技术。
3 卤水提锂
我国锂资源丰富,尤其是卤水锂资源。国内卤水锂资源主要集中分布在湖北、新疆、青海、西藏等中部和西部地区,其储量约占全国总储量的89.8%[6-7]。
卤水提锂大多利用太阳能作为主要能源,具有生产工艺流程简单、成本低等优点,已成为提锂(工业级碳酸锂)的主要方法[8-9],也是国内外矿业企业开发和工业锂盐生产的主要途径。但是,国内大多数含锂盐湖卤水中的镁锂比高达40~1 800,不但开发条件恶劣而且锂浓度偏低[10],因此与国外相比,国内含锂盐湖卤水开采难度要大得多。卤水提锂技术一般分为沉淀法、溶剂萃取法和离子交换吸附法等。
3.1 沉淀法
沉淀法提锂是利用太阳能使蒸发池中的含Li+卤水蒸发并浓缩,当[Li+]达到一定值时,再利用石灰脱除Ca2+、Mg2+,最后利用碳酸盐或者铝酸盐使Li+以Li2CO3形式析出[11],沉淀法根据沉淀剂种类的不同,可分为碳酸盐沉淀法和铝盐沉淀法,其中碳酸盐沉淀法工艺最为成熟。
3.1.1 碳酸盐沉淀法
碳酸盐沉淀法提锂适宜处理[Mg2+]/[Li+]值低且不含或仅含少量碱金属的盐湖卤水。当卤水中[Mg2+]/[Li+]偏高时,卤水经浓缩后,溶液中的氯化镁浓度增大,加入碳酸钠后,镁便会与碳酸钠形成碳酸镁沉淀。因此,在锂以碳酸锂沉淀形式析出之前大量的碳酸钠就已经被消耗掉[12]。但是随着提锂技术的发展,在一定试验条件下,碳酸盐沉淀法也可应用于高[Mg2+]/[Li+]的盐湖卤水提锂。王日公等[13]将温度范围控制在40~100℃,使高[Mg2+]/[Li+]的盐湖卤水处于过饱和状态,并在保温状态下迅速将其抽到带搅拌器的振荡分离塔中,再加入Na2CO3并搅拌、振荡5~10 min,将溶液静置分层,当MgCO3和Li2CO3有明显的分界面时,立刻分离出MgCO3和Li2CO3,接着将离心机中的Li2CO3悬浮物进行脱水,再对Li2CO3粗品进行精制,得到的Li2CO3产品纯度≥99.5%。该项发明分离步骤简单、快速、可降低生产成本,能够在盐湖区实现直接一步分离出Li2CO3。Hamzaoui等[14]利用Na2CO3沉淀盐湖卤水中的Mg2+,当搅拌时间为20 min、碳酸根与镁离子的物质的量比为0.91时,镁离子沉淀效果最好,镁离子的去除率为98%,并保留了大部分锂离子在溶液中,但碳酸根与镁离子的物质的量比低于0.61时,耗碱量大且工艺复杂。Boryta等[15]在盐湖卤水中加入氧化钙和碳酸钠去除镁离子,经过滤后,将滤液的pH调节到10,再利用离子交换柱去除滤液中的M2+和M3+阳离子,然后将pH调整到7,最后利用结晶器分离出氯化锂。
3.1.2 铝酸盐沉淀法
铝酸盐沉淀法是利用二氧化碳碳化分解铝酸盐后,得到活性Al(OH)3,使其与盐湖卤水中的Li+作用形成锂铝化合物进行提锂。铝酸钠碳化沉淀法提锂是一种重要的铝酸盐沉淀法,其工艺流程为:先用浓度为40%的CO2来碳化分解10%的铝酸钠(NaAlO2),得到无定形的Al(OH)3,其对溶液中Li+具有很好的选择性,将得到的无定形Al(OH)3加入提硼后含锂0.13%的卤水中,经沉锂除镁后,锂、镁的分离率可达95%以上;控制焙烧温度为350℃,将获得的锂铝沉淀物焙烧30 min,常温下用水浸取,使Al3+与Li+分离;用CaO去除浸取液中Mg2+、Ca2+等杂质后,蒸发并浓缩;控制溶液温度为95℃,加入浓度为20%的Na2CO3溶液反应生成Li2CO3;最后经过洗涤、烘干,得到Li2CO3产品,其质量可达工业一级品标准(纯度≥99%)。黄师强等[16]将含Li+卤水脱硼后,母液利用铝酸钠碳化沉淀提锂方法提取Li2CO3,Li+的沉淀率和Mg2+的分离率均超过95%,制得的Li2CO3的纯度超过98%,Li+的回收率超过87%,试验过程发现无定形Al(OH)3溶液对锂具有很好的选择性且与制备工艺无关。A.H.Hamzaoui等[17]在强碱性条件下制备的Al(OH)3凝胶能够吸附Li+,并通过探索试验得出吸附Li+的最佳试验条件。
与碳酸盐沉淀法相比,采用铝盐沉淀法获得的Li2CO3的回收率和纯度均较高,但其生产工序复杂,碳酸钠和淡水消耗量大、碳化液和焙烧浸取液蒸发能耗大,目前依旧无法工业化生产。
3.1.3 其它沉淀法
近些年来,为了更好地开发利用盐湖卤水资源,研究者们进行了大量的试验研究,得出了一些针对不同种类盐湖卤水的新沉淀法。
徐徽等[18]采用氨和碳酸氢铵两段沉镁提锂法处理高[Mg2+]/[Li+]的盐湖卤水。实验结果表明:在25℃下,用氢氧化钠调节溶液pH值到12,控制加料(ρ(Mg2+)=23 g/L、ρ(Li+)=20 g/L、氯化铵饱和,快速搅拌)速度为0.3~0.5mL/min的条件下,反应时间为20~30 min,母液中Mg2+的去除率可达98%,在该条件下制备碳酸锂,不但锂的回收率高且产品纯度较高。Jerome[19]处理Atacama盐湖卤水时先采用水合硫酸锂结晶沉淀法处理,再经蒸发并浓缩,获得Mg2+、Li+、SO42-含量分别为4.7%~6%、0.8%~1.2%、1.2%~4.2%和Mg2+、Li+、SO42-含量分别为2.5%~6%、<6%、<0.12%的2种不同组成的卤水,混合后卤水中的Li2SO4过饱和,最后经沉淀、过滤处理,获得一水硫酸锂晶体,其纯度为98.97%,锂的总回收率为73.3%。该方法的优势在于不需额外添加化学原料,比较适合处理低[Mg2+]/[Li+]的盐湖卤水,其技术关键在于获得上述2种不同组成的卤水。
硼、镁共沉淀法[20]是将已析出K+、Mg2+的盐田卤水加入沉淀剂除去Mg2+、B3+,母液加氢氧化钠再次除Mg2+,再加入 Na2CO3,Li+最终以 Li2CO3沉淀的形式析出。采用硼、镁共沉淀法可以使锂的回收率达到80%以上,其工艺流程简单、分离效率高,但由于沉淀物多是胶体,过滤困难,因此导致锂离子损失率高达15%以上,而且利用该方法硼的回收难度较大,工业化很难实现。
硼、锂共沉淀法[21]。首先将卤水进行析出钾盐和钠盐、脱SO42-处理;再利用太阳能使其蒸发浓缩,沉淀除去Mg2+,使Li+得到富集;在一定的温度、压力、pH值的条件下使Li+和B3+共沉淀;然后用水洗涤硼、锂共沉淀物,锂以Li+的形式进入溶液,残存固体即是硼酸;接着向洗液中加入氢氧化物使Mg2+和Ca2+以沉淀形式去除,最后向溶液中加入过量的Na2CO3,Li+以Li2CO3沉淀析出。硼、锂共沉淀法更适合处理高镁锂比的硫酸镁亚型盐湖卤水,其成本低廉,锂的回收率可达到75%以上,且获得的碳酸锂可达工业一级或特级标准。
3.2 溶剂萃取法
溶剂萃取法的基本原理是:向含有锂离子的溶液中加入与之不相溶的有机相,且该有机相对锂离子有更大的溶解度,利用锂离子在两相中的溶解度不同,从而达到锂离子转相富集的目的[22]。国内外学者在盐湖卤水特别是高MgCl2盐湖卤水体系萃取剂方面进行了大量的试验研究,按照使用萃取剂体系的不同主要可分为含磷有机萃取剂体系、胺类萃取剂体系、冠醚混合萃取剂体系和双酮、酮、醇萃取剂体系[23]。磷酸三丁酯(TBP)萃取提锂法在国内研究最为深入,而且该方法特别适合用于高[Mg2+]/[Li+]的卤水处理,是一项十分有前景的提锂技术。
孙锡良等[24]以青海盐湖含锂卤水为研究对象,采用200#溶剂汽油为稀释剂、TBP为萃取剂、氯化铁(FeCl3·6H2O)为共萃取剂萃取卤水中的锂。结果表明:在萃取过程中,水相中H+浓度是影响萃取指标的重要因素,维持溶液的pH值在一定范围内,既能保证Li+进入有机相并减少H+与有机溶剂的络合,又能保证溶液中的Fe3+不发生水解。当TBP的质量分数为 60%、有机相与水相的体积比为 1.5、n(Fe3+)/n(Li+)=1.3、c(OH-)=0.05 mol/L时,含锂卤水中锂的回收效果最好,此条件下锂的萃取率达到80%。但上述方法反萃酸度高,对设备腐蚀严重。
高洁等[25]设计了以TBP-BA-FeCl3-溶剂油为协同萃取剂的溶剂萃取法,该方法能有效降低反萃取酸度,解决设备腐蚀问题。该工艺利用协同萃取剂进行三级萃取,HCl(0.5~2 mol/L)作为洗涤液对有机相进行三级洗涤,维持有机相与反萃剂体积比在1~50范围内,以HCl(1~6 mol/L)作为反萃剂进行三级反萃,单级反萃时间为2~20 min,最终获得氯化锂溶液,锂的总回收率达90%以上。当对原料卤水中含锂浓度要求不高时,加入BA(乙酸丁酯)和溶剂油能有效降低反萃酸度,对设备危害小,同时反萃后的有机相可循环使用,绿色经济环保。
3.3 离子交换吸附法
离子交换吸附法基本原理是将有选择性且含吸附阳离子的物质作为交换剂,与卤水中的锂离子进行交换,从而使锂离子得到富集。离子交换剂分为有机离子交换剂和无机离子交换剂2大类。当前国内外研究最多的无机离子吸附剂分为离子筛型氧化物吸附剂、铝盐吸附剂、无定型氢氧化物吸附剂等[26-28]。离子交换吸附法更适用于高镁锂比和低品位的含锂卤水的处理,应用前景好。
3.3.1 离子筛型氧化物吸附法
离子筛型氧化物吸附剂受到研究者们较多的关注,特别是以二氧化锰离子筛作为锂吸附剂,因其具有吸附选择性好、循环利用率高和生产成本相对较低等优点[29],引起了研究者的关注。刘骆峰等[]通过水热法制备锂离子筛吸附剂,通过实验发现,原料氢氧化锂和氯化锰中锂、锰的物质的量之比为4∶1,加入氧化剂95 mL,水热合成温度为360℃并恒温反应24 h,温度控制误差不超过±1℃时,合成的离子筛对Li+有较高吸附量,最高吸附量为41.02 mg/g。该吸附剂能有效降低锰溶损,锰溶损率仅为3.06%,具有良好的工业化前景。为探索高[Mg2+]/[Li+]的盐湖卤水处理方法,孟庆伟等[30]选用陶瓷膜和锰系离子筛进行耦合,通过水热合成法制得了吸附性能优良的锂离子筛(H1.6Mn1.6O4),当使用该离子筛处理察尔汗盐湖卤水时,锂离子的吸附容量达到31.44 mg/g,而且陶瓷膜(r孔径=50 nm)对离子筛的截留率为100%,膜渗透通量超过150 L/(m2·h),陶瓷膜耦合后的锰系离子筛对Li+回收率大于97%,锂离子筛经HCl和H2O2清洗后,又能有效恢复膜渗透通量。
3.3.2 铝盐吸附法
铝盐吸附法是以铝盐沉淀法为基础发展而来的提锂新方法。20世纪70年代初,科研者在该吸附剂的合成与制备方面进行了大量的试验研究[32]。20世纪90年代后,张绍成[33]在处理高镁锂比的卤水时,利用醋酸丁酸纤维素造粒制备铝盐吸附剂(Li-Cl·2Al(OH)3·nH2O),然后将其装入吸附—解吸装置中进行Li+的吸附,吸附的Li+用水解吸,解吸液再经过精制和浓缩后,得到的含Li+富液可成为制备Li2CO3或LiCl的原材料。董茜等[34]在实验室使用Al(OH)3和Li(OH)制备铝盐吸附剂并对其吸附效果进行研究。结果表明:控制n(Al(OH)3):n(Li(OH))=2.0、酸(pH=5.8)洗3~4 h,即可得到铝盐吸附剂,该吸附剂在Li+的选择性和吸附方面都有较好的效果,并且对碱金属杂质离子(如Mg2+、Na+、K+等)基本不吸附。
3.4 卤水提锂技术小结
沉淀法提锂工艺存在着耗能高、工艺流程复杂、成本高等缺点,对高镁锂比卤水提锂还需进行技术革新。在所有沉淀法提锂中,碳酸盐沉淀法是现阶段较为成熟的工艺,已经应用于工业生产。近年来新出现的硼镁、硼锂共沉淀法等还需进行大量的工艺优化研究才能实现工业化生产。
溶剂萃取法能够有效地分离碱金属和碱土金属,是从高镁锂比卤水中提锂最为有效、成本较低、能耗较少、工艺简单、绿色环保的一种提锂方法,具有很好的工业应用前景。但是该方法存在的氯化铁易乳化、萃取剂的萃取率和盐酸的循环利用率低以及设备腐蚀等问题亟待解决。
离子交换吸附法是目前最具应用前景并能很快实现工业化应用的提锂方法。其生产工艺流程简单、回收率高、选择性好,尤其适用于处理高[Mg2+]/[Li+]的卤水。实验室研究的无机离子交换剂的吸附效果好,却多为粉末状,溶损率高。因此,开发合成离子筛的新技术、联合纳米材料进行造粒等是未来的研究热点。例如,在合成离子筛时加入高价态金属离子和非金属离子进行改性研究,以降低有机物的使用量,提高离子筛的循环使用率、降低溶损率。
4 矿石提锂
矿石提锂指以锂辉石、锂云母等为原料来生产相关的锂产品。该技术依旧是目前生产高品质电池级碳酸锂的主要技术。因其技术相对成熟且适应性较强,国内外相关锂生产商仍然采用此技术进行高品质锂产品的生产。矿石提锂方法可以分为以下5种:石灰烧结法、硫酸盐法、硫酸法、氯化焙烧法和纯碱压煮法,硫酸法是目前应用最为广泛的生产方法[35]。
4.1 石灰烧结法
石灰烧结法[36]最早出现于1935年,是最早的矿石提锂方法。该方法工艺过程发生的主要化学反应为,

将锂辉石与石灰按一定比例混合,并将混合料置于转窑中进行焙烧(T=800~900℃),烧结产品再经湿磨、浸出、过滤、洗涤后可得氢氧化锂溶液,最后经蒸发、浓缩、沉淀等操作制得碳酸锂和氢氧化锂产品。该方法能处理各类品位不同的锂矿石,生产成本较低,但对石灰质量要求较高,且耗能大、回收率低、浸出的矿泥易凝聚,设备维护困难,并且随着硫酸盐法、硫酸法、氯化焙烧、纯碱压煮法等一些较先进的方法的不断出现已经面临淘汰。
4.2 硫酸盐法
硫酸盐法[37]主要用于处理含锂硅酸盐类矿物和磷酸盐矿物,其工艺过程为K2SO4与锂矿物混合,混合后的物料经造球、焙烧,使矿石中的锂转变为硫酸锂,发生的化学反应是:

反应生成的熟料经稀H2SO4浸出,使Li+从矿石中进入溶液中,进入溶液中的Li+经净化、沉淀后便可获得Li2CO3。但该反应过程为可逆反应,为了获得更多的硫酸锂,加入的硫酸钾必须过量。利用该方法提锂时,几乎所有的含锂矿石都能被分解。但由于硫酸钾价格昂贵,使得生产成本增加,而且钾盐回收困难;若使用硫酸钠全部取代硫酸钾则极可能生成锂辉石玻璃,后续的硫酸浸出工序会受到很大的影响,同时烧结过程温度必须严格控制(因焙烧温度接近锂盐熔融温度),使其生产上受到一定限制。为了降低K2SO4的用量,湖南有色金属研究所使用铝厂产出的副产物——CaSO4替代K2SO4与锂云母精矿焙烧,获得了较好的指标并使副产物得到了较好的回收利用。Luong等[38]控制焙烧温度为850℃条件下,选择FeSO4和CaO与锂云母矿混合焙烧1.5 h,最终锂的回收率为85%。
4.3 硫酸法
硫酸法[39]仍是目前国内外矿石提锂主要的工业生产方法。其不但可用于处理锂辉石、锂云母、磷铝锂石,也可处理低品位含锂矿石(Li2O含量为1.0~1.5%)。该工艺流程为:将锂辉石于高温(T=950℃~1 100℃)下焙烧,锂辉石的晶型由单斜晶系变成四方晶系(β-锂辉石),化学活性增强;接着将浓H2SO4与β-锂辉石混合后,控制焙烧温度为250~300℃进行焙烧,发生如下置换反应:

生成的焙烧产物在搅拌槽中用稀硫酸浸出,净化除去大量Ca2+、Mg2+、Fe3+、Al3+等杂质,再用Na2CO3进一步除去Ca2+、Mg2+,得到纯净的Li2SO4;再将溶液蒸发和浓缩,加入Na2CO3与Li2SO4反应生成Li2CO3;沉淀物经洗涤、干燥即可获得纯净的Li2CO3,锂的回收率可达90%。该方法具有能耗低、生产效率高、锂和钾回收率高等优点。但硫酸法存在浸出液杂质含量高、硫酸和纯碱消耗量大、对设备腐蚀大等问题。
4.4 氯化焙烧法
氯化焙烧[45]是利用氯化剂与锂云母作用,将碱金属和有价金属转化成氯化物,从而与杂质分离,可以分成高温氯化焙烧和中温氯化焙烧2种。中温氯化法是控制一定焙烧温度(低于碱金属氯化物沸点的温度)焙烧制得烧结块,烧结块溶出后,与杂质分离;高温氯化法是控制一定焙烧温度(高于碱金属氯化物沸点的温度)进行焙烧反应,使氯化物气化后,与杂质分离。化学反应方程式为,
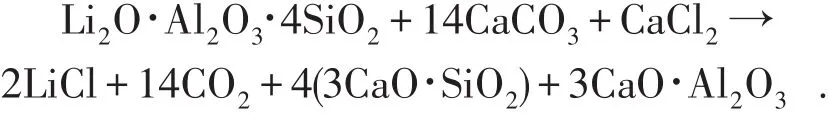
该方法工艺流程简单、锂的回收率可达90%以上,且能耗低、焙烧时间短,但生产成本较高、设备防腐要求高,且高温氯化产生的气态产物LiCl难以收集。伍习飞等[40]氯化焙烧锂云母矿时,采用氯气作为氯化剂。研究结果表明:控制反应温度T=800~900℃,Li、K等碱金属极易被氯化,而二氧化硅和三氧化二铝不会被氯化。最终Li+的回收率大于92%,K的回收率大于72%。
4.5 纯碱压煮法
纯碱压煮法[41]主要用于处理锂云母矿。其工艺流程与硫酸法提锂相似,均需预先对锂矿石进行转型或脱氟焙烧,然后将焙烧产物与纯碱均匀混合,控制反应温度为200℃、压强在0.2~2 MPa,利用纯碱中的钠置换锂,化学反应方程式为,

压煮后的料浆实现碳酸锂与残渣有效分离的方法有2种。一种是将二氧化碳通入料浆中,将锂转变成碳酸氢锂,分离残渣后并加热溶液,锂以碳酸锂结晶析出;另一种是将石灰加入料浆中,使锂转变成氢氧化锂进入溶液,经过滤、蒸发并浓缩得到LiOH·H2O产品,通入二氧化碳后,得到碳酸锂产品。该方法的优点在于生产成本低、工艺流程简单、对设备腐蚀性小、不耗硫酸、没有大量副产品Na2SO4生成、生产效率高、产品碳酸锂可达电池级标准、压煮浸出时间短等,但其对生产工艺条件及生产原料的要求较为苛刻。据报道[42]江西赣锋锂业已经成功应用压煮法处理锂云母,锂回收率可达到75%~92%。
4.6 矿石提锂技术小结
石灰烧结法由于其耗能大、回收率低及对石灰的质量要求高等缺点,随着硫酸盐法、硫酸法、氯化焙烧等一些较先进的方法的不断出现已经面临淘汰;硫酸盐法几乎能处理所有的含锂矿石,但是烧结过程温度必须严格控制,且硫酸钾的价格昂贵使其生产上受到一定限制;硫酸法仍是目前国内外矿石提锂主要的工业生产方法,其不但可用于处理锂辉石、锂云母、磷铝锂石,也可处理低品位含锂矿石(Li2O含量为1.0~1.5%),但硫酸法存在浸出液杂质含量高、硫酸和纯碱消耗量大、对设备腐蚀大等问题;氯化焙烧法具有工艺流程简单、锂的回收率可达90%以上、能耗低等优点,但也存在生产成本较高且高温氯化产生的气态产物LiCl难以收集等不足;纯碱压煮法提锂工艺过程与硫酸法提锂类似,但其解决了硫酸法对设备腐蚀严重的问题,具有生产成本低、生产效率高等优点,但其对生产工艺条件及生产原料的要求较为苛刻。
5 展望
(1)卤水提锂技术主要分为沉淀法提锂、溶剂萃取法提锂和离子交换吸附法提锂3种,其中最具有发展前景的提锂方法为离子交换吸附法提锂。离子交换吸附法解决了沉淀吸附法工艺复杂、生产成本相对较高的问题以及溶剂萃取法对设备腐蚀的问题,并且离子交换吸附法具有回收率高、选择性好等优点,但是应加快解决无机离子交换剂溶损问题。可以考虑联合纳米等新型材料开发新的无机离子交换剂,以解决溶损问题,早日实现卤水提锂技术工业化、规模化应用。矿石提锂技术主要有石灰烧结法、硫酸盐法、硫酸法、氯化焙烧法、纯碱压煮法,其中纯碱压煮法是具有较好前景的提锂方法。纯碱压煮法不但解决了硫酸盐法和硫酸法对设备腐蚀严重等问题,而且避免了氯化焙烧法提锂过程中产生的气态产物LiCl难以收集的问题。同时纯碱压煮法具有生产效率高、产品碳酸锂可达电池级标准等优势,今后应该注意改进纯碱压煮法使其适应性更强。
(2)卤水提锂技术主要应用于工业级碳酸锂的生产,其工艺简单、生产成本较低,但是生产条件恶劣。矿石提锂技术主要用于生产高质量电池级碳酸锂,生产工艺成熟,但生产成本较高,对设备要求高。2种提锂技术各有优势,二者在国内将长期保持互补关系,需要根据目前国内的生产现状及时作出相关政策调整,适应当前国际锂产业的飞速发展。

