右美托咪定在左半肝切除术中对肝缺血再灌注损伤作用的分析
丁海涛,刘紫琪,贾晓鹏,郝建华
解放军总医院第一附属医院 麻醉科,北京 100037
我国肝炎患者众多,每年新发原发性肝癌患者占全球的55%[1]。肝切除术是目前治疗原发性肝癌的最有效策略,随着人们对肝解剖结构认知的加深,以肝段为基础的肝切除术能有效改善患者的远期预后[2]。但同时大范围的肝切除术也增加了患者术后肝功能衰竭的风险,因此如何降低肝缺血再灌注损伤是肝切除术围术期管理研究的重点之一[3]。右美托咪定是一种α2肾上腺素受体激动剂,具有镇静、镇痛、抗焦虑、抑制交感神经等作用,临床可作为麻醉过程中辅助用药。研究表明,右美托咪定可以通过降低交感神经节纤维神经递质的释放减少相关炎性因子的产生,达到保护器官功能的作用[4-5]。本研究探讨右美托咪定对肝缺血再灌注损伤的作用,为肝切除术中的麻醉用药方案提供参考。
对象和方法
1 研究对象 选取本院2016年1月- 2017年12月60例行左半肝切除术患者。纳入标准:1)术前诊断为原发性肝癌且符合肝切除手术适应证;2)术前麻醉评估可耐受半肝切除术;3)在我院行开腹左半肝切除术且术中采用Pringle手法进行全肝门阻断;4)对治疗策略知情同意,并通过我院伦理委员会审批。
2 分组及麻醉方法 纳入患者采用随机种子数法分为实验组(30例)和对照组(30例)。实验组患者在麻醉诱导前给予右美托咪定,以1μg/(kg·h)的速度静脉泵入10 min,然后以0.5μg/(kg·h)的速度静脉持续泵入至手术结束。对照组患者予以同等剂量的0.9%氯化钠注射液静脉泵入。两组均采用静-吸复合麻醉方式。入室后建立静脉通路,常规心电监测,桡动脉置管监测动脉血压,麻醉诱导方法:咪达唑仑0.04 mg/kg,舒芬太尼0.5μg/kg,罗库溴铵0.6 mg/kg。气管插管后连接呼吸机辅助通气。麻醉维持方法:丙泊酚6 mg(kg·h),舒芬太尼 0.3μg/(kg·h),罗库溴铵 0.3 mg/(kg·h),吸入七氟醚(呼气末浓度为1%)。并依据患者的血流动力学情况调整麻醉药物和液体用量。两组术中均采用Pringle手法行全肝门阻断方式切除左半肝,即肝门阻断带同时阻断肝动脉和门静脉主干。
3 检测指标 分别于肝门阻断前(T0)、肝门开放后(T1)、关腹前(T2)和术后第1天(T3)抽取患者静脉血送检,检测患者的肝功能[谷丙转氨酶(alanine aminotransferase,ALT)、 谷 草 转 氨 酶 (aspartate aminotransferase,AST)、碱性磷酸酶(alkaline phosphatase,ALP)、总胆红素 (total bilirubin,TB)]和相关细胞因子水平[白细胞介素-6(interleukin-6,IL-6)、IL-10、 丙 二 醛 (malondialdehyde,MDA)、超氧化物歧化酶(superoxide dismutase,SOD)]。人IL-6 ELISA(KLC006)和 IL-10 ELISA(KLC009)试剂盒均购自上海康朗生物科技有限公司。
4 统计学分析 应用SPSS18.0统计软件进行统计学分析,符合正态分布计量资料以-x±s表示,两组之间比较采用t检验;不同时间点不同组间比较采用两因素重复测量方差分析。计数资料组间比较采用χ2检验。P<0.05为差异有统计学意义。
结 果
1 两组基线资料比较 实验组男性23例,女性7例,年龄平均(56.6±13.3)岁,其中乙肝患者28例,丙肝患者2例,术前Child分级,A级23例,B级7例,肿瘤直径平均(7.1±1.7) cm。对照组男性21例,女性9例,年龄平均(54.6±11.4)岁,其中乙肝患者25例,丙肝患者5例,术前Child分级,A级26例,B级4例,肿瘤直径平均(7.5±2.2) cm。两组患者之间基线资料无统计学差异,具有可比性。见表1。

表1 两组一般资料比较Tab. 1 Comparison of clinical data about patients in two groups
2 围术期指标比较 所有患者均顺利完成手术,无术中死亡。实验组平均手术时间(243.6±59.1) min,平均肝门阻断时间(24.7±10.3) min,平均术中出血量(464.8±126.2) ml,5例患者术中输血,输血率为16.7%,平均术中液体总入量(2 853.4±637.1) ml,平均尿量(1 843.8±372.3) ml。对照组平均手术时间(223.3±56.2) min,平均肝门阻断时间(26.9±8.7) min,平均术中出血量(402.1±153.1) ml,6例患者术中输血,输血率为20.0%,平均术中液体总入量(2 631.6±532.8) ml,平均尿量 (1 704.7±315.8) ml。两组间围术期指标差异无统计学意义。见表1。

表2 两组不同时间段肝功能指标的比较Tab. 2 Comparison of liver function between two groups at different time points
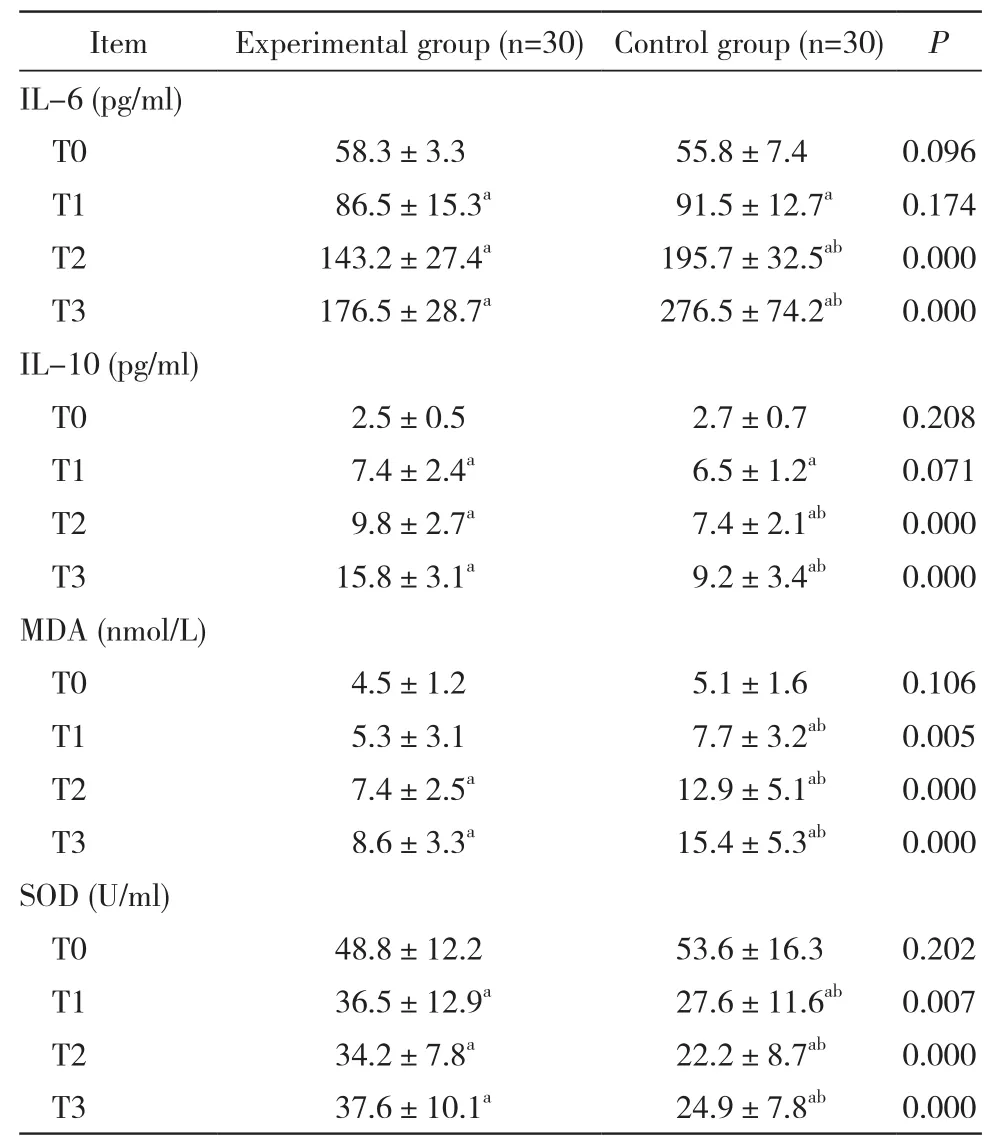
表3 两组不同时间段细胞因子水平的比较Tab. 3 Comparison of cytokines between two groups at different time points
3 两组肝功能指标比较 肝门阻断后两组肝功能各项指标较阻断前均明显升高(P均<0.05),实验组肝功能的升高幅度小于对照组(P均<0.05),见表2。
4 两组细胞因子水平比较 两组IL-6、IL-10、MDA水平在肝门阻断后较阻断前逐渐上升,SOD逐渐下降(P均<0.05)。实验组IL-6、MDA水平升高幅度和SOD下降幅度均小于对照组,而IL-10的升高幅度大于对照组(P均<0.05)。见表3。
讨 论
肝缺血再灌注损伤是指由各种原因导致肝血流中断后,经再次血液流通灌注,肝功能障碍和结构损伤反而加重的现象[6]。如果不能有效控制,甚至可能导致患者出现肝功能衰竭。因此如何有效地减少肝缺血再灌注损伤是减少肝手术患者术后并发症、改善预后的关键因素之一[7]。
我国原发性肝癌患者大多术前存在肝炎、肝硬化情况,一方面肝拥有动脉和门脉两套血供系统,另一方面肝硬化本身会引起肝血窦高压,因此肝切除术中出血情况常难以控制。Pringle手法用于临床肝切除术已经有近半个世纪的历史,其通过对肝动脉和门静脉进行阻断后再实施肝切除术,对于伴有肝硬化的患者,每次全肝门阻断时间应<15 min。由于肝血供的完全阻断,从而大大减少了术中出血量,保障了大范围肝切除手术的安全性。但同时因肝血流阻断后再通,难免造成肝缺血再灌注损伤。肝缺血再灌注损伤的具体机制目前尚不完全明确,研究认为主要与氧自由基、炎性因子和细胞因子的产生有关[8-9]。肝缺血因术中的肝门阻断,再灌注开始于肝门血流的复通,因此如何在术中改善肝细胞功能,减少相关细胞因子的产生,对于降低肝缺血再灌注损伤有着重要意义。
氧自由基产生和脂质过氧化物反应增强是肝缺血再灌注损伤的重要机制之一[10]。肝缺血后,氧自由基会在短时间内大量产生,进而引起肝细胞膜、线粒体膜和溶酶体膜的脂质过氧化,破坏生物膜的完整性,最终引起肝细胞坏死[11]。因此,脂质过氧化的产物丙二醛和抗氧化剂的超氧化物歧化酶是评估机体氧自由基产生和清除能力的重要指标。肝细胞坏死后,库普弗细胞会释放大量的促炎性因子,进而激活中性粒细胞释放大量炎性因子,导致肝微循环障碍,引起肝细胞坏死[12]。IL-6和IL-10是常见的反应机体炎症情况的细胞因子。本实验结果显示,肝血流阻断复通后,肝功能指标和相关细胞因子水平较肝门阻断前明显升高(P<0.05)。这说明肝经历缺血并再次灌注后,肝细胞会产生一定程度的损伤,其机制可能与炎性细胞因子释放有关。
右美托咪定是新一代的高选择性α2肾上腺素受体激动剂,输注后主要在肝代谢,最终90%以上的代谢产物经肾排出,目前临床主要用于麻醉和监护室的镇静与镇痛作用[13-14]。右美托咪定主要通过作用于蓝斑的α2受体发挥镇静作用,因而对呼吸功能影响较小,同时也可以作用于周围神经的α2受体抑制交感神经的活性,引起低血压和心动过缓[15-16]。大量基础研究表明,右美托咪定对多种脏器具有保护作用,其具体机制可能与减少细胞因子产生有关[17]。Sahin等[16]研究表明,对大鼠实施肝缺血再灌注模型前腹腔注射右美托咪定预处理,大鼠体内的SOD含量明显高于对照组,由此考虑右美托咪定的肝保护保护功能可能与清除过量的氧自由基有关。郭友祥等[18]研究表明,对于肝硬化患者术中应用右美托咪定能显著降低术后患者的IL-6和TNF-α浓度,从而降低机体的应激反应。本实验结果显示,实验组肝功能、IL-6、MDA水平升高幅度和SOD下降幅度均小于对照组患者,而IL-10的升高幅度大于对照组患者(P<0.05)。这说明应用右美托咪定能一定程度上减少炎性细胞因子的产生,改善肝功能。但本研究病例资料有限,尚需多中心大样本研究进一步证实。
综上所述,右美托咪定应用于肝切除术,能有效抑制氧自由基的形成,减少促炎性细胞因子的产生[19-20],从而改善肝功能,说明其对肝缺血再灌注损伤具有一定的保护作用[21]。

