纳米载药系统靶向肿瘤微环境治疗策略
宋 柯,潘 昊,韩嘉艺,陈立江
(辽宁大学药学院,沈阳 110036)
在治疗肿瘤过程中,手术、放疗和化疗被称为肿瘤的三大治疗手段,从手术切除到化疗药物的问世,再到放射治疗,都是以直接切除、杀伤或灭活肿瘤细胞为主,这些手段在治疗恶性肿瘤中取得了较好疗效,但并不是对所有肿瘤都有效;此外,化疗药物难以分辨肿瘤细胞和正常细胞,产生明显的不良反应。分子生物学的发展促进了癌变分子的识别,分子靶向药物的成功应用(如甲磺酸伊马替尼、曲妥珠单抗等)是肿瘤生物治疗的重大进展,同时人们认识到,肿瘤的发生是一个连续的基因改变的累积过程[1]。但是分子靶向药物依然存在着水溶性低和毒性大等缺点,因大多数临床使用的传统药物都是低相对分子质量的化合物,通过扩散渗透到肿瘤细胞和正常细胞中,并不能完全排除全身毒性,较短的半衰期也迫使大多数低相对分子质量的抗癌药物在最大耐受剂量下使用。纳米技术的出现和迅速发展使多种治疗方法和制剂的联合使用成为可能,纳米载体不仅可以通过肿瘤有高渗透长滞留效应(enhanced permeability and retention effect,EPR效应)来优先递送药物,还由于其粒径、形状、表面特性等可控,可以用来提高生物利用度、控制药物释放、减少药物不良反应、提供病人更好的剂量时间表等。在此领域科学家也进行了非常深入的探讨[2-4]。此外,纳米载体也可通过特定的靶向配体进行表面修饰,用来靶向肿瘤和其他基质成分。在过去20多年里,已有20多种纳米制剂被批准用于临床[5],其中以脂质体纳米粒和聚合物-药物结合物为主。然而虽然这些纳米制剂在减少不良反应和诱导肿瘤消退上有极大的成效,但仅限于少数几种肿瘤,肿瘤耐药性和不能根治依然是极大的问题。其中,肿瘤微环境是阻碍纳米系统治疗的重要原因,这是由于肿瘤细胞和微环境的双向交流(类似正常细胞间的交流,可以促进正常组织的发育和功能),肿瘤细胞间以及和微环境的相互作用能决定并且改变肿瘤的表型,因此造成治疗的困难[6-7]。此外,大量证据表明,涉及肿瘤微环境的机制也会影响肿瘤耐药性,如美国布罗德研究所的研究人员[8]曾在试管中模拟了肿瘤微环境,将癌细胞和健康细胞共培养,再加入抗肿瘤药物,结果显示原本抗肿瘤效果较好的药物效果大为减弱,表明肿瘤细胞或能够利用周围环境中的健康细胞来抵抗抗肿瘤药物。
因此,而深入认识肿瘤微环境、了解其构成及对免疫调节的影响、复杂的信号通路和特殊生理特性等可以为未来治疗肿瘤提供新的手段并为研制新的抗肿瘤药物提供依据,同时优化纳米载药系统的设计,可以克服一些传统疗法所不能解决的问题,这也为多靶点治疗、联合用药等治疗方法提供策略。
1 肿瘤细胞和微环境间的相互交流
肿瘤细胞与其微环境间的相互交流如图1所示,以上皮-间质转换来源为例,基底膜被破坏,肿瘤细胞通过分泌一些生长因子和蛋白酶来激活基质环境,如血管内皮生长因子(vascular endothelial growth factor,VEGF)可以促进肿瘤血管生成,基质金属蛋白酶(matrix metalloprotease,MMP)可以直接或间接降解细胞外基质(extracellular matrix,ECM)的多种成分。这些酶可以以自分泌和旁分泌的方式发挥作用,同时,它们特异性迁移并侵袭ECM,同时影响蛋白酶及抑制剂的表达。细胞外基质原本是不断降解和重建的平衡,但肿瘤细胞的出现打破了这种平衡,这些分子和肿瘤细胞过表达的生长因子促进肿瘤新生血管生成、激活基质炎症细胞和肿瘤相关成纤维细胞(tumor-associated fibroblast,TAF),TAF分泌更多的生长因子和蛋白酶,在级联中扩增这些信号,从而促进恶性肿瘤生长的活化基质的重建[9]。这些活化基质重建后流动性低,如一些胶原成分会抑制肿瘤的迁移,但肿瘤细胞又会分泌生长因子和蛋白酶来降解基质,帮助自己迁移,因此肿瘤微环境和肿瘤细胞是相互促进又相互抵抗的矛盾体。
2 纳米载药系统
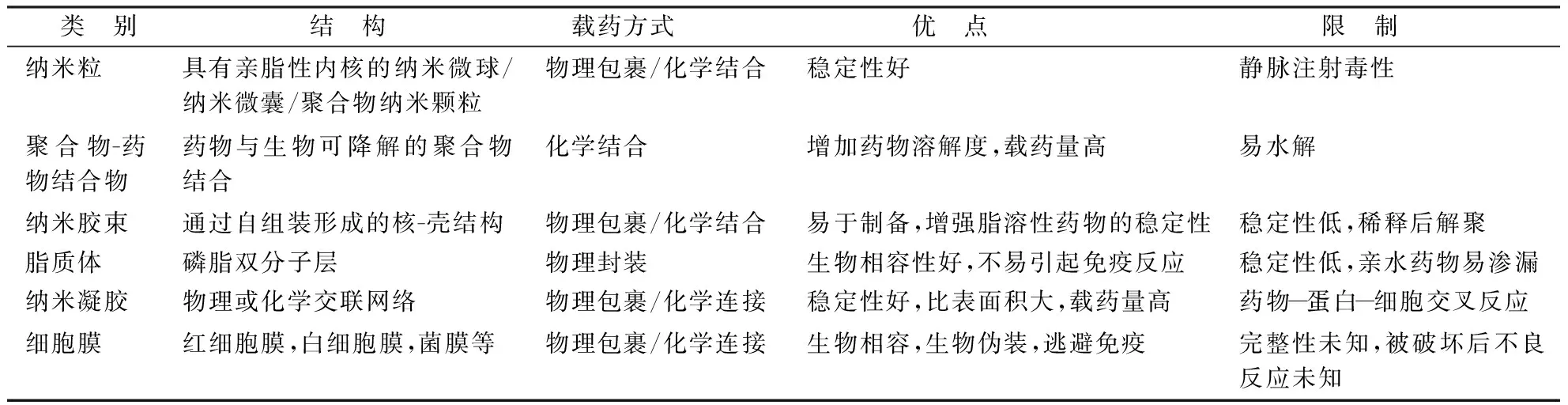
纳米载药系统按作用原理不同可分为主动靶向传递系统和被动靶向传递系统。按组成不同可分为纳米粒、聚合物-药物结合物、纳米胶束、脂质体、纳米凝胶和一些新型纳米载药系统如细胞膜载体(如表1所示)。按环境敏感类型的不同可分为pH敏感型、酶敏感型、温度敏感型、还原性敏感型和光敏性纳米载药系统等。主动靶向指纳米系统表面修饰特定的分子与肿瘤部位某些受体特异性结合,被动靶向是依靠肿瘤部位特有的生理和病理环境以及纳米系统自身的性质来实现制剂或药物的蓄积,通过EPR效应以及对纳米系统粒径和电荷智能化控制来设计传递系统。

图1肿瘤细胞和其微环境间的相互交流
表1不同组成的纳米载药系统
类 别结 构载药方式优 点限 制纳米粒具有亲脂性内核的纳米微球/纳米微囊/聚合物纳米颗粒物理包裹/化学结合稳定性好静脉注射毒性聚合物-药物结合物药物与生物可降解的聚合物结合化学结合增加药物溶解度,载药量高易水解纳米胶束通过自组装形成的核-壳结构物理包裹/化学结合易于制备,增强脂溶性药物的稳定性稳定性低,稀释后解聚脂质体磷脂双分子层物理封装生物相容性好,不易引起免疫反应稳定性低,亲水药物易渗漏纳米凝胶物理或化学交联网络物理包裹/化学连接稳定性好,比表面积大,载药量高药物-蛋白-细胞交叉反应细胞膜红细胞膜,白细胞膜,菌膜等物理包裹/化学连接生物相容,生物伪装,逃避免疫完整性未知,被破坏后不良反应未知
目前有很多纳米制剂已经被应用于临床治疗,如Doxil[10](聚乙二醇多柔比星脂质体,FDA批准的第1个纳米制剂)以及Abraxane[11](紫杉醇白蛋白纳米粒),Marqibo[12](硫酸长春新碱脂质体)等,能改善治疗性能和减少不良反应,但是研究发现,这些纳米颗粒主要聚集于微血管和肿瘤组织的周围,无法穿透肿瘤组织,存活的肿瘤细胞会继续生长繁殖,还可能会自我更新产生耐药性[13]。
3 纳米载药系统靶向肿瘤微环境治疗策略
根据纳米载药系统靶向肿瘤微环境的靶点不同,可将其主要分为靶向肿瘤血管、靶向肿瘤细胞间液及细胞外基质、靶向肿瘤基质细胞、靶向肿瘤相关树状突触细胞和靶向肿瘤干细胞。根据这些不同的靶点,以及肿瘤微环境的异常化,可以设计不同类型的纳米载药系统来传递药物、实现靶向治疗。如因肿瘤细胞在有氧和无氧条件下均有高的糖酵解率,导致肿瘤基质的pH范围在6.2~6.9[14],低于正常组织的pH水平(7.4),而且肿瘤细胞核内体和溶酶体有着更低的pH,可以利用酸不稳定基团(如缩醛、腙、亚胺、酯等)构建pH响应性的传递系统。如根据肿瘤微环境中存在过度表达的蛋白酶和细胞因子等物质,可构建被蛋白酶特异性水解或与细胞因子特异性结合的传递系统[15]。如根据肿瘤部位对高热造成的损伤敏感,构建温敏材料在肿瘤微环境或肿瘤细胞内发生相转变,还可以结合肿瘤热疗等[16],以及其他的一些治疗策略。
3.1 靶向肿瘤血管
肿瘤血管的生成是肿瘤细胞获取更多营养物质、迁移和侵袭的必要途径,促血管生长因子主要有VEGF家族、成纤维细胞生长因子(fibroblast growth factor,FGF)、血小板衍生生长因子(platelet derived growth factor,PDGF)家族和血管生成素(angiopoietin,ANG)。肿瘤血管生成抑制剂主要作用于肿瘤血管基底膜,通过特异性抑制肿瘤血管内皮细胞增殖,拮抗促血管生成因子。由于突变的肿瘤细胞可以生成其他一些促血管生成蛋白来进行补偿,因而相对于肿瘤细胞,血管内皮细胞被认为是基因组相对稳定的[17]。此外,纳米粒进入肿瘤血管时,首先被内皮细胞层内化,故很多研究者将其作为抗血管生成药物的靶点和疗效评估的标志物。但是抗血管生成治疗并没有想象中的乐观,Pàezribes等[18]研究表明,抗血管生成治疗会增加恶性肿瘤的进展、促进肿瘤的侵袭和转移,这可能是因为肿瘤多种形式的逃避抵抗,导致疾病的复发。故而有研究者试图通过抑制肿瘤新生血管生成、肿瘤细胞生长的双重靶向来提高治疗效果。
Gu等[19]利用纤维黏连蛋白可变剪切片段(extra domain B,EDB)在胶质瘤新生血管内皮细胞与胶质瘤细胞中都过表达的特点,制备了用EDB靶向肽APTEDB修饰的聚乙二醇-聚乳酸(polyethylene glycol-polylactic acid,PEG-PLA)纳米粒运载紫杉醇(PTX),实现肿瘤血管、肿瘤细胞双重靶向,并比较了未用EDB修饰的纳米粒(NP-PTX)和修饰后纳米粒(APT-NP-PTX)的特性。二者的粒径、载药量及包封率都很相似,而APT-NP-PTX对HUVEC细胞和U87MG细胞均显示出剂量依赖毒性,且各剂量和NP-PTX相比,毒性均有显著提高(P<0.05)。体内近红外成像和体内分布研究表明,APT-NP-PTX显示更好的肿瘤靶向性和较高的肿瘤内积累,并且有较低的伴随毒性。
夫马吉欣(TNP-470)是烟曲霉素类似物,Ingber等[20]于1990年首次发现其具有抗血管生成作用,临床实验证明其具有抗肿瘤活性[21],但是随后人们发现TNP-470在最优抗肿瘤剂量下有神经毒性[22]。Segal等[23]将N-(2-羟丙基)甲基丙烯酰胺[N-(2-hydroxypropyl)methyl acrylamide,HPMA]聚合物和阿仑唑奈(alendronate,ALN)以及TNP-470共聚形成HPMA聚合物-ALN-TNP-470(图2),实现同时靶向骨转移瘤上皮和内皮间质、联合治疗癌症相关骨病。ALN和TNP-400都是通过Gly-Gly-Pro-Nle肽键连接,在体内可以被组织蛋白酶K水解。由于循环血管内皮细胞(circulating endothelial cell,CEC)可作为测量抗血管生成活性的生物标志物[24-26],在非荷瘤小鼠中,相比ALN与TNP-470单独给药组,ALN和TNP-470联合用药显著诱导CEC凋亡,表现出对正常血管的毒性,而纳米系统组无显著影响,但是在给药K7M2荷瘤小鼠实验中,纳米系统组中凋亡的CEC水平是对照组的4倍,表明此种治疗方法靶向性良好、对正常血管的毒性低。此外,HPMA作为优良的生物可降解材料,并无PEG长循环带来的累积毒性,有替代PEG的生物前景。
尽管纳米载药系统具有很多优点,靶向肿瘤血管治疗还有很多难题要解决,如肿瘤抵抗血管生成药物的现象和如何能更好地使肿瘤血管正常化等问题。
在最近对肿瘤血管的研究中,Navarro等[27]发现一类抗血管生成药物——多激酶抑制剂(TKIs)可以改善乳腺癌和肺癌小鼠模型的低氧状态。研究者指出,即使肿瘤部位含氧量正常,肿瘤细胞也会关闭糖酵解途径转而依赖线粒体代谢,这是肿瘤生存的必要条件。研究者将TKls与苯乙双胍等线粒体抑制药物联合使用,协同效果良好,这一发现揭示了肿瘤抵抗抗血管生成药物的可能机制,为其临床应用提供了新策略。Lin等[28]对肿瘤患者体内的CEC和循环肿瘤细胞(circulating tumor cell,CTC)进行了系统的检测、鉴别和比较,首次发现肿瘤患者体内存在染色体异倍体CEC,此次研究让人们清晰认识到异倍体CTC和异倍体CEC是两类不同的细胞,有助于人们进一步了解CEC在肿瘤血管生成以及肿瘤的生长、转移中的相关性。
3.2 靶向细胞间液及细胞外基质
细胞外基质是基质细胞分泌到细胞外间质中的大分子物质,由上皮和内皮细胞产生。研究表明致密的细胞外基质会减缓大分子的渗透和扩散,如纤维状胶原会限制粒径大于50 nm的粒子运动[29],此外还会形成高压环境,造成肿瘤治疗的困难,粒径智能化调节的纳米系统是提高药物穿透性一种策略。
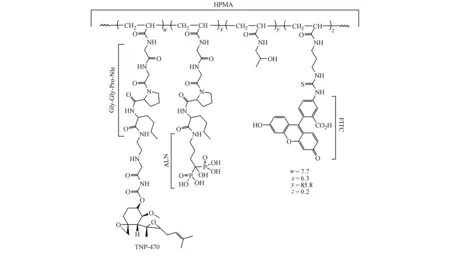
图2HPMA共聚物-ALN-TNP-470化学结构
Wang等[30]用热引发自由基聚合的方法将聚乙二醇单甲醚-聚乳酸-衣康酸[methoxyl poly (ethylene glycol)-poly(lactic acid)-itaconic acid,PLE-AC]制备成一种pH响应的水凝胶[P(LE-IA-MEG)],一分子衣康酸有两个羧基基团,具有良好的pH响应性能。研究表明,与pH 1.2的条件相比,在pH 6.8时,该水凝胶体积明显增大,横截面变得松散,有利于药物的释放。而较大的凝胶颗粒在肿瘤组织外可以实现长循环,进入肿瘤后,纳米药物粒径变小,利于穿透。体外细胞毒性试验和溶血试验表明,PLE-AC不会导致溶血、细胞毒性低,是安全的药物载体候选材料。
细胞外基质的Ⅰ型胶原网络会阻碍药物进入肿瘤内部,Zhang等[31]先给药氯沙坦,降低Ⅰ型胶原的水平,然后静脉注射pH敏感的紫杉醇脂质体,该脂质体用R8肽修饰,当其通过EPR效应到达细胞间液时,低pH的环境使腙键断裂、暴露出R8肽,继而被肿瘤细胞摄取,发挥药效。体内实验表明,该脂质体有良好的靶向性,同时研究表明氯沙坦的联合治疗不仅显著提高了抗肿瘤活性(P<0.05)、增加了纳米系统在肿瘤部位的积聚,还降低了肿瘤间质压力、提高了氧含量。但是氯沙坦作为一种血管紧张素Ⅱ受体拮抗剂,可能会导致肿瘤血管扩张,促进肿瘤细胞迁移,故而控制给药剂量是重要因素。
由于肿瘤部位的谷胱甘肽(glutathione,GSH)浓度高于正常组织,本课题组[32]设计了一种基于谷胱甘肽还原响应性的接枝共聚物胶束(图3),该胶束以胱胺二盐酸盐为桥链将聚丙烯酸和维生素E琥珀酸酯通过二硫键连接,用来提高索拉非尼(sorafenib,SFN)的水溶性并控制其释放,同时减少了索拉非尼毒性,体外释放结果显示,该胶束在低浓度GSH下稳定,在高浓度GSH存在下,二硫键断裂,紫杉醇48 h累积释放量高达85%。
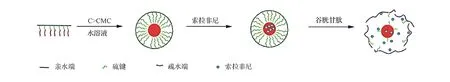
图3索拉非尼封装胶束及响应性释放[29]
3.3 靶向肿瘤基质细胞
肿瘤微环境内的基质细胞会通过细胞黏附或分泌因子介导的旁分泌方式支持肿瘤生长,如内皮细胞、炎症细胞、TAF等都被认为是抗肿瘤治疗的潜在靶点。上述提到,相比肿瘤血管,内皮细胞被认为是相对生理稳定的,一些内皮细胞标志物也存在于肿瘤上,故有研究者设计靶向内皮细胞的纳米系统来减少氧气及营养供应,达到“饿死肿瘤”的目的,同时可以实现双重靶向。
肿瘤相关巨噬细胞表面甘露糖受体大量表达,故甘露糖被用作靶向巨噬细胞的纳米系统靶向配体[33],许多纳米系统也被设计为巨噬细胞成像用于诊断治疗[34]。以前巨噬细胞被认为是免疫系统分泌用来攻击消除肿瘤的细胞,但M2型巨噬细胞可以通过多种途径参与肿瘤血管生成,此外大量的研究表明,M1型巨噬细胞有抗肿瘤特性[35],目前的焦点在于如何调节M1/M2型巨噬细胞的比例或调节其表型变化以改善治疗。
TAF的作用很多,如合成分泌ECM、通过TGF-β介导的VEGF-A来激活血管生成、分泌细胞因子来间接帮助肿瘤转移[36]。Zhang等[37]指出,在富含基质的膀胱癌模型中,TAF水平高,肿瘤生长加快。将吉西他滨和顺铂纳米粒联合给药,多次注射后α-SMA阳性成纤维细胞的生成减少了87%以上(免疫荧光),相比联合给药组(游离药物),经复合纳米粒治疗,肿瘤组织的通透性提高2.75倍。
3.4 靶向肿瘤相关树突状细胞
随着肿瘤恶化,肿瘤间质会产生一个抑制免疫系统的微环境,导致免疫系统产生对肿瘤的免疫耐受,肿瘤细胞抗原性减弱,难以被免疫系统识别和清除[38]。帮助肿瘤细胞逃避免疫最为重要的因子为程序性死亡受体及配体(PD-1/PD-L1)和细胞毒性T淋巴细胞相关抗原(CTLA-4)[39],相关靶向治疗的药物有如Nivolumab和Pembrolizumab[40]。其中,树突状细胞(dendritic cells,DCs)是已知最具有潜力的抗原呈递细胞,肿瘤相关树突状细胞(tumor-associated dendritic cells,TADCs)疫苗被认为是最具潜力的肿瘤免疫治疗方法,原因在于其可刺激宿主免疫系统产生特异性抗肿瘤免疫应答、诱导细胞毒性肿瘤T细胞来杀伤肿瘤细胞。
与传统的肿瘤疫苗相比,“纳米疫苗”具有明显的优势,因为它们能够保护抗原免受蛋白质降解、优化体内树突状细胞特异性传递,并允许多种抗原、免疫刺激抗体、细胞因子和寡核苷酸的组合传递,可以促进免疫细胞活化、提高肿瘤疫苗作用甚至代替肿瘤疫苗。
与正常的DC相比,TADCs对TLR刺激反应响应性较差,会造成肿瘤疫苗的作用障碍,这一现象与STAT3信号通路过度激活相关。Luo等[41]制备了一种多肽类胶束,用来共封装poly IC、STAT3 siRNA和OVA抗原。结果显示,体内和体外试验中,STAT3在TADCs中的表达均减少了50%以上,CD86、CD40和IL-12表达升高,表明该纳米载药系统可以有效诱导TADC的成熟和活化。该纳米载药系统通过调节肿瘤的微环境和激发有效的抗肿瘤免疫反应,增加成熟的CDs和减少免疫抑制细胞,从而使肿瘤得到显著的抑制。
Reddy等[42]经皮内注射不同粒径的纳米粒,发现肿瘤间质液可以高效地将超小纳米颗粒(25 nm)传递到毛细淋巴管及引流淋巴结,可以靶向近半淋巴滞留处的树突状细胞,而粒径在100 nm的纳米粒传递效率仅为10%,表明纳米粒的粒径大小可直接影响其进入TADCs。这些纳米粒的表面化学特性可以激活补体级联反应,可在原位有效激活TADCs并成像。
在最近的研究中,Sagiv-Barfi等[43]用“原位接种”的方法研制出了一种新型肿瘤疫苗,注射到肿瘤部位后引发T细胞免疫应答,全身攻击肿瘤细胞,该免疫刺激剂可治疗多种肿瘤,并且效果显著,目前已进入临床研究。
3.5 靶向肿瘤干细胞
越来越多的研究证明肿瘤干细胞(cancer stem cells,CSCs)与肿瘤复发和耐药性有着直接原因[44-45],也有人将其称为具有干细胞表型的肿瘤细胞。肿瘤干细胞相比普通肿瘤细胞,有着多种高表达的标志物,如CD44、CD133和EPCAM等。目前关于肿瘤干细胞的来源争论不一,主要有两种观点,一种认为肿瘤干细胞由正常干细胞转变而来,另一种认为肿瘤细胞中只有小部分细胞具有形成并维持肿瘤生长和异质性的能力,被认为是肿瘤的起始。
Fiorillo等[45]研究表明将氧化石墨烯纳米化,能有效抑制多种肿瘤细胞系的形成,其可以选择性靶向CSC,而不是仅仅简单地作为药物传递系统。对MCF7 CSCs研究表明,氧化石墨烯对抑制肿瘤球形成表现出剂量依赖性,更为重要的是,氧化石墨烯不影响MCF7细胞系非肿瘤干细胞的生存能力,显示出良好的选择性。随后他们对其他5种肿瘤细胞模型(SKOV3、PC3、MIA-PaCa-2、A549、U87MG细胞系)进行了试验,同时研究了氧化石墨烯对已知CSCs信号通路的影响,发现其对其他5种肿瘤细胞模型的CSCs有相似的抑制作用,并发现氧化石墨烯主要抑制Wnt、Notch、STAT1/3和NRF-2信号转导通路。有趣的现象在于研究者发现氧化石墨烯可能通过诱导CSCs分化成为非肿瘤干细胞来实现抑制作用此外,Justilien等[46]首次发现MMP-10是极其重要的肺癌干细胞基因和新靶点。Ames等[47]通过多个临床前模型研究表明活化的自然杀伤细胞优先靶向具有肿瘤干细胞表型的肿瘤细胞,将免疫疗法和细胞毒性治疗相结合,有助于克服肿瘤耐药性。
4 结 语
如上所述,肿瘤微环境中存在了大量可以影响肿瘤生长的因素:如肿瘤血管非正常化、高密度的细胞外基质限制了纳米粒的穿透、肿瘤细胞与间质的交流,促进其生长等。目前纳米载药系统靶向策略主要为:①肿瘤血管、内皮细胞双重靶向,以达到肿瘤血管正常化或“饿死肿瘤”的目的;②降低肿瘤间质压力、改善肿瘤基质中的缺氧环境,提高纳米载体及药物的穿透性;③靶向基质细胞,降低或阻断肿瘤细胞与基质细胞间的交流,同时也会影响免疫相关微环境;④靶向肿瘤相关树突状细胞,增强诱导细胞毒性肿瘤T细胞来杀伤肿瘤、减弱肿瘤的免疫抑制;⑤靶向肿瘤干细胞,以期找到一种根源治疗的方法。
目前纳米载药系统靶向肿瘤微环境主要存在的问题是:①环境敏感型纳米载药系统的响应性不够好;②纳米载药系统容易被免疫系统清除或自身累积产生毒性;③肿瘤组织的高度异质性会带来纳米粒分布的异质性,从而产生耐药性。如今面临的挑战是如何正确认识肿瘤微环境,认识到其异质性而不是把不同类型的肿瘤同一而论,即便是同一类型肿瘤,组织间也存在着差别;如何设计响应性好、选择性高并且释放动力学优良的纳米载药系统;如何设计逃避免疫的生物相容性材料并能被有效清除,如Gao等[48]建立了红细胞膜包裹pH响应的纳米粒载药系统;如何设计多功能的纳米载药系统,使其能够同时靶向肿瘤细胞及间质细胞,又能阻断肿瘤细胞与细胞间质之间的交流,如Swami等[49]将骨髓瘤和骨转移微环境作为靶点;以及如何开发更加复杂、贴近真实的离体数学模型和临床相关的体内模型、更准确的影像来充分探究肿瘤微环境。

