不阻断肾蒂机器人辅助腹腔镜肾部分切除术初步体会
肖建军,周晓晨,张亿达,郭 炬,傅 斌,孙 庭,王共先,曹润福
(1.遂川县人民医院,江西遂川 343900;2.南昌大学第一附属医院泌尿外科,江西南昌 330000)
近年无症状肾癌的检出率日渐增高,手术切除仍然是局限性肾癌的首选治疗方法,欧美及国内泌尿外科等各大诊治指南推荐肾癌肿瘤TNM(tumor node metastasis,TNM)分期中的T1a期肾癌首选肾部分切除术,甚至对于合适的T1b期肾癌也可考虑肾部分切除术[1-2]。随着手术经验的积累和手术器械的进步,尤其是机器人手术技术的出现,手术方式发生了巨大的变化。为确保手术安全性,我们在开展机器人辅助腹腔镜肾部分切除术初期采用阻断技术实施手术。随着经验的积累,我们逐步尝试对位置表浅、体积较小的外生性为主的T1a期肾肿瘤采用不阻断技术。现就本研究治疗的40例病例资料进行分析,初步探讨不阻断肾蒂机器人辅助腹腔镜肾部分切除术的可行性及临床疗效。
1 资料与方法
1.1临床资料本文选取2016年04月至2017年10月间南昌大学第一附属医院泌尿外科收治的40例局限性肾癌行机器人辅助肾部分切除术患者的临床资料,不阻断组18例;阻断组22例。阻断组中位于腹侧(A)的有5例(5/22),不阻断组腹侧(A)有2例(2/18)。两组患者的年龄、体重指数、ASA评分、肿瘤大小、R.E.N.A.L评分、术前的患侧肾小球滤过率(glomerular filtration rate,GFR)等比较差异均无统计学意义。所有患者术前均行双肾动静脉计算机断层扫描(computed tomography,CT)血管成像、腹部彩超、胸片等检查明确诊断及排除远处转移。
1.2手术设备及方法气管插管全身静脉复合麻醉后取健侧卧位,并留置导尿管。两组均经后腹腔入路,以右侧肿瘤切除为例,患者取左侧卧位,选取腋中线髂嵴上2 cm作为镜头通道,腋前线肋缘与髂嵴连线中点偏腹侧2 cm处为1号操作臂通道,腋后线平1号臂水平为2号操作臂位置,1号臂穿刺点与镜头穿刺点连线中点下方8 cm为助手通道。任意两个端口之间的距离大于8 cm,机器人两操作臂穿刺通道点与镜头操作通道连线成角大于120°。建立腹膜后操作通道后,清理腹膜后脂肪,辨认腰大肌、腹膜折返和肾周筋膜等标志,在腹膜折返的内侧纵行剪开肾周筋膜,切开肾周脂肪,于腰肌前间隙寻找肾动脉,开展手术初期术中常规充分游离出肾动脉并用小儿导尿管悬吊标记(图1A),置入“bulldog”血管夹,暂不阻断肾动脉以备需要时及时改为阻断(最近有2例患者因为肿瘤直径小、外凸明显、未游离肾动脉直接切除肿瘤)。电剪距肿瘤边缘正常肾实质表面0.2 cm处标记边缘,在助手吸引器帮助保持清晰视野下,采用边推边切边凝的交替钝锐性薄层切除。切除肿瘤后用双极或电剪再次行肿瘤基底创面止血,如有集合系统损伤使用可吸收缝线修补,取20 cm长2-0带CT-1针倒刺线尾打结后夹持Hem-o-lok夹进行肾脏创面连续缝合重建,每针收紧缝线后紧贴肾脏表面夹持Hem-o-lok夹免打结进行肾实质切口缝合后生理盐水冲洗创面,观察无明显活动性出血后,将肿瘤置入专用标本收集袋从助手孔取出。术后常规留置肾旁引流管。肾蒂阻断(图1B)组除行肾动脉阻断外其他操作同不阻断组。
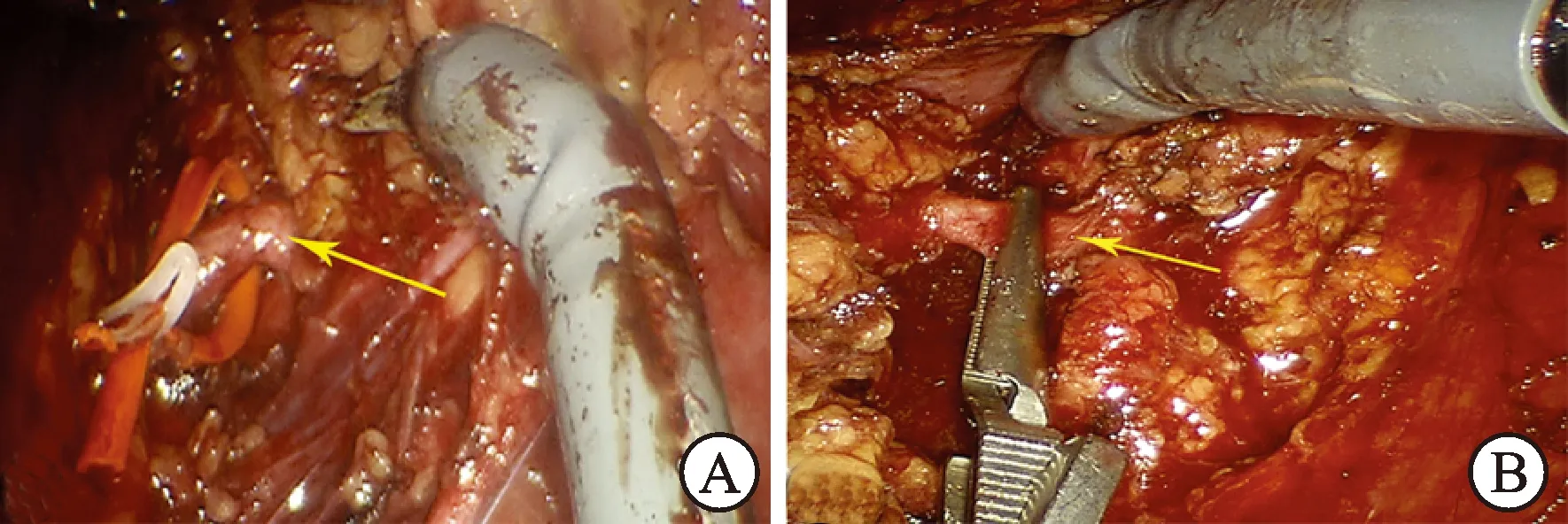
图1 术中肾动脉的处理情况
A: 不阻断肾动脉,黄色箭头示肾动脉;B: 阻断肾动脉,黄色箭头示肾动脉。
1.3统计学方法使用SPSS 18.0统计软件处理数据,样本均数比较采用独立样本t检验,计量资料以均数±标准差表示,以P<0.05为差异有统计学意义。
2 结 果
两组手术均顺利完成,无中转开放、无输血病例,出现围手术期Clavien分级3级以上并发症。不阻断组相比阻断组平均手术时间无明显增加,患侧GFR下降率更低,但术中出血量增多。术后病理切缘均阴性,其中透明细胞癌32例;肾乳头状腺癌6例;肾嫌色细胞癌2例(表1)。术后随访3~18月未发现有肿瘤复发病例。
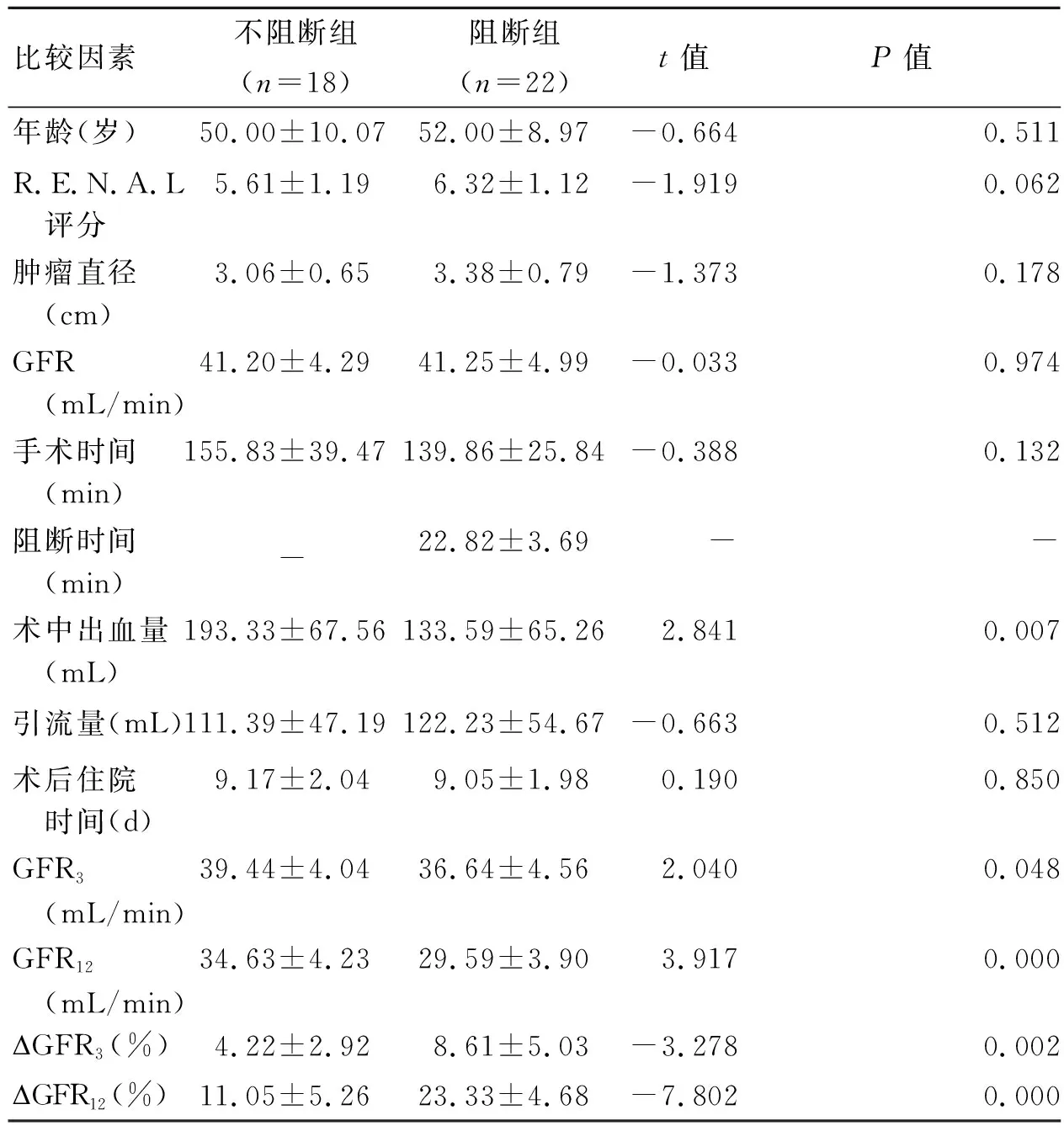
表1 不阻断组与阻断组临床参数比较(n=40)
GFR:术前患侧肾脏肾小球滤过率;GFR3:术后3月患侧肾脏GFR;GFR12:术后12月患侧肾脏GFR;GFR3、GFR12:术后3月、12月患侧肾脏GFR下降率;GFR3=(1-GFR3/GFR)×100%;GFR12=(1-GFR12/GFR)×100%。
3 讨 论
近年肾癌发病率逐年升高、影像学技术的发展及健康体检的日益普及,无症状肾癌的检出率日渐增高。手术切除仍然是局限性肾癌的首选治疗方法,随着手术经验的积累和手术器械的进步,尤其是机器人手术技术的出现,手术方式发生了巨大的变化。欧美及国内泌尿外科等各大诊治指南推荐肾癌TNM分期中的T1a期肾癌首选肾部分切除术,甚至对于合适的T1b期肾癌也可考虑肾部分切除术[1-2]。多项回顾性研究肯定了肾部分切除术在肿瘤控制方面的有效性和肾功能的保护作用[3-5]。1993年WINFIELD等[6]首次报导了腹腔镜肾部分切术,传统的腹腔镜肾部分切除术常采取阻断肾蒂的办法,可以更好的控制术中出血及保持相对清晰的手术视野。传统观点认为小于30 min的热缺血时间对于术后肾功能的损害是一过性或可逆的,甚至有动物试验报道肾脏最大能够耐受90 min的热缺血时间[7]。有文献报导不阻断肾动脉肿瘤切除过程中必然出血较阻断组多,影响手术视野,为了保证切缘阴性,术者潜意识下容易过多的切除正常肾实质,所以短时间(<20 min)的肾动脉阻断可能更加有利于术后肾功能的保护。最近一项研究根据50例阻断病例的术前资料,从143例不阻断病例中筛选出50例,与其一一配对;对比术后指标显示,不阻断技术对患者术后短期的肾功能似乎不具备明显优势[8];近期另一项包含351例病例的多中心回顾研究也指出不阻断技术对双肾功能完好的患者,不阻断技术似乎并不能带来显著的肾功能获益[9]。但THOMPSON等[10]认为每增加1 min的热缺血时间术后最终进展为肾功能不全Ⅳ期(尿毒症期)的风险将增加6%,具体到每一个患者肾脏的热缺血时间都是不一样的,年龄、基础的肾脏功能和并存的其他疾病都是影响因素。多种如选择性阻断[11]或控制性降压或低温灌注[12]最大限度减少热缺血的方法和技术使用以更好的保护肾功能,但实际操作难度较大,目前仍然缺乏多中心大样本的报告结果。
从GUILLONNEAU等[13]于2003年率先报道了不阻断肾动脉、初步实现了肾部分切除的真正“零缺血”起,该技术已有长足进步。尤其是机器人辅助腹腔镜技术的出现,利用其机械臂灵活、稳定、自动滤颤及高清的纵深视野更加提高了手术效率及安全性[14]。早期已经有多中心报导介绍了不阻断肾蒂机器人辅助肾部分切除术[15-16],甚至对于复杂的肾脏肿瘤采取不阻断机器人辅助肾部分切除也是可行的[17]。最近CACCIAMANI等[18]报道了一项包括987例机器人肾部分切除术的回顾性荟萃分析,结果提示避免阻断肾动脉主干对肾功能的保护具有显著优势,而各项围手术期指标和肿瘤控制效果与阻断技术相当。但不阻断技术可能伴随着更高的出血风险,出血严重而无法控制者可能导致最终切除患肾[19]。
多数文献采用总体GFR变化研究术后肾功能的损害,但术后肾功能的损害可能被对侧正常肾脏部分代偿所掩盖[20],所以本研究采用患侧肾脏的GFR的变化来进行对比分析。有文献报道不阻断肾蒂显著增加了术中出血量,而术中出血量(>400 mL)是术后进展为慢性肾功能不全的危险因素[21]。本研究不阻断组的出血量也是显著高于阻断组,但选择合适的病例,出血量是可控的,没有输血病例,不阻断肾蒂由于避免了肾脏热缺血,术后3月及12月的患侧GFR下降率明显小于阻断组,进一步说明了不阻断肾蒂对于术后肾功能的保护作用。
本文为回顾性研究,比较不阻断组与阻断组手术效果、术后肾功能的保护等,均选取的是经后腹腔入路的病例进行分析可以避免经腹腔入路病例资料的干扰。我们团队积累了较丰富的经后腹腔入路腹腔镜肾部分切除术的手术经验,熟练掌握经该入路实施T1a-T1b期肾肿瘤的腹腔镜肾部分切除术,其中包括位于腹侧的肿瘤。经过初步探索,我们发现采用机器人腹腔镜技术,仍可采用经后腹腔入路安全、有效地完成绝大多数保留肾单位肾肿瘤切除手术。因此在本研究中,所有患者均采用经后腹腔入路机器人辅助腹腔镜技术。
我们开展手术初期选取位置表浅、体积较小的外生性为主的T1a期肾肿瘤有助于手术的顺利开展。所有患者术前均行双肾动静脉CT血管成像,了解肿瘤与肾门集合系统及肾动静脉分支间的关系,术者做到心中有数,必要时术中借助超声定位准确判断肿瘤轮廓。术中常规充分游离出肾动脉并用小儿导尿管悬吊标记,置入“bulldog”血管夹,以备术中发生难以控制的出血时能够及时行肾蒂阻断,这对于开展手术初期显得更为重要。随着手术经验的积累,有2例患者因为肿瘤直径小、外凸明显,未游离肾动脉直接切除肿瘤。电剪距肿瘤边缘正常肾实质表面0.2 cm处标记边缘,在助手吸引器帮助保持视野下沿标记切开肾实质后找到一个合适平面后慢慢的采用边推边切边凝的交替钝锐性薄层切除,完整切除肿瘤的前提下尽可能保留多的正常肾实质。只要肿瘤边缘包膜完整,术中不必行快速冰冻病理检查,边缘的厚度也不影响肿瘤的复发率[22]。电凝止血不满意还可以采用边推边凝边缝合方法或使用Hem-o-lok夹子。不阻断肾蒂没有了时间的紧迫感,让术者在肾脏创面缝合重建的过程中能够更加的从容细致。倒刺线与Hem-o-lok夹子的交替配合使用在肾实质的连续缝合起到了很重要的作用,不仅缩短了手术时间,还可以避免缝线打结对肾实质的撕裂,严密缝合肾实质的前提下尽可能的薄层缝合。
采用机器人辅助技术,利用其灵活、稳定、高清的三维视野优势,选择合适的病例进行不阻断肾蒂机器人辅助腹腔镜肾部分切除术,可避免热缺血对肾功能的影响,不增加手术时间,术中出血量稍增加,围手术期并发症无增加,该技术是安全可行的。本研究局限于回顾性研究,病例数较少,患者选择上可能存在偏倚,随访时间短,还需要更多的病例数及长期的随访来观察肿瘤控制及肾功能的变化指标。

