螺旋CT血管成像胃血管检查对胃癌根治术的指导意义
郭剑华,易海玲,汤培荣
(广东医学院附属惠东医院放射科,广东 惠东 516300)
胃癌是临床发病率和死亡率较高的常见恶性肿瘤,根据临床统计资料,在低于35岁人群中,胃癌发病率高达3.0%~5.0%,我国每年新发胃癌患者约有40万例,每年因为胃癌死亡的人数达到了30万左右[1]。随着各类诊断仪器设备的应用以及人们健康意识的提升,早期胃癌的诊断率相对于先前明显提升,为胃癌的早期治疗奠定了基础[2]。在早期胃癌手术治疗中,胃癌根治术已经逐渐成为标准术式,在具体胃癌根治术过程中需要将携带病灶的组织和器官进行切除,清扫淋巴结,除此之外,部分病灶侵犯部位与血管较近,部分血管出现变异,增加了手术操作难度以及术后出血风险,术前对变异性血管的检出可为手术操作奠定基础[3]。为进一步提高胃癌根治术治疗效果,降低手术风险,减少对术中血管的损伤。本文收集75例胃癌患者资料,总结螺旋CT血管成像检查对胃癌根治术的临床指导意义。
1 资料与方法
1.1 一般资料 研究对象为本院2013年8月至2017年7月间收治的胃癌患者75例,均通过胃镜检查确诊。其中男性46例、女性29例,最小年龄37岁、最大74岁,平均年龄(63.8±5.1)岁,所有患者符合胃癌根治术的适应症和禁忌症,患者及其家属在了解手术及麻醉须知后签署知情同意书,各项检查、诊断以及手术治疗资料完整。
1.2 CT检查方法 应用飞利浦Ingenuity Core 128层螺旋CT,检查前禁食4~6 h;向患者及其家属进行CT检查过程的完整说明,呼吸训练,要求患者在扫描时按照语音提示作屛气配合。扫描参数:管电压120 kV,管电流250 mA,矩阵512×512,螺距53,层厚0.5 mm,层距0.3 mm;扫描范围膈顶至髂前上棘水平。
所有患者均作CT平扫加血管成像检查,平扫前肌肉注射20 mg盐酸山莨菪碱,口服6 g产气粉,当患者有胃腔膨胀感后,进行仰卧位CT平扫。然后嘱咐患者口服500 mL饮用水,再次水充盈CT平扫。之后通过Stellant 双管高压注射器经肘中静脉以4.0 mL/s注射速率注入造影剂欧乃派克(350 mg/mL)80 mL,并追加20 mL生理盐水;动脉早期采用SureStart智能阈值触发扫描,感兴趣区(region of interest ROI)放置于腹主动脉腔干水平,延时8 s后采用低剂量(120 kV,50 mA)对ROI行同层动态监测扫描,每隔1 s扫描1次,当ROICT值达到180 Hu时自动触发动脉早期扫描;延时30 s触发门脉期扫描;得到动脉早期,门静脉期CT血管成像增强图像。
Michels分型标准主要有:Ⅰ型:正常型,即肝总动脉(CHA)起源于腹腔动脉干(CA),发出肝固有动脉(PHA)及胃十二指肠动脉(GDA),前者继续分出胃右动脉(RGA)及肝左右动脉(L/RHA)。Ⅱ型:胃左动脉梯度肝左动脉;Ⅲ型:肠系膜上动脉替代肝右动脉;Ⅳ型:胃左动脉替代肝左动脉(rLHA),肠系膜上动脉替代肝右动脉(rRHA);Ⅴ型:胃左动脉副肝左动脉;Ⅳ型:肠系膜上动脉代替副肝右动脉。
1.3 图像后处理 将扫描获得的数据进行薄层重建,层厚1.0 mm,应用飞利浦星云工作站对动脉早期图像数据进行多平面重建(multi-planner reformation,MPR)、最大密度投影(maximal intensity projection,MIP)、容积重建(volume renering,VR),显示各组胃供血动脉,由两名高年资医师盲法分别对影像作出判断,结果不一致时,聘请第3位医师评判。
1.4 观察指标 不同CT后处理技术对胃血管解剖类型显示情况;患者胃左动脉、胃右动脉、胃网膜右动脉以及胃网膜左动脉等血管显示情况;正常以及解剖变异胃供血血管检出情况。
1.5 统计学分析 数据均采用统计学软件SPSS19.0进行处理,用百分率(%)表示,采用χ2检验。
2 结 果
本组75例,胃供血动脉成像质量均较佳,动脉血供丰富,均来源于腹腔动脉。发自腹腔动脉干的胃左动脉和来自肝固有动脉的胃右动脉形成胃小弯动脉弓供血胃小弯。来自胃十二指肠动脉的胃网膜右动脉和来自脾动脉的胃网膜左动脉形成胃大弯动脉弓供血胃大弯。来自脾动脉的数支胃短动脉供应胃底。胃后动脉可以是1支或2支,起自脾动脉的中1/3段,见图1。
2.1 CT与手术对胃血管解剖类型比较 以术中分型为标准,按照Michels分型标准,本组75例,Ⅰ型70例,占93.3%,Ⅱ型2例,占2.7%;Ⅳ型1例,占1.3%;Ⅵ型2例,占2.7%;CT血管成像将1例Ⅵ误判为Ⅳ型,诊断符合率为98.7%(74/75),组间比较差异无统计学意义,χ2=0.000,P>0.05,见表1。
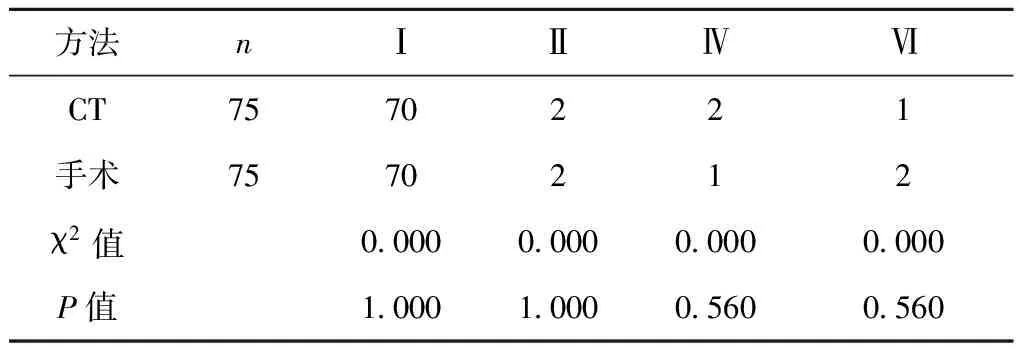
表1 患者术前螺旋CT血管成像与术中病理分型比较
2.2 CT与手术对不同部位胃血管显示比较 在不同部位血管显示情况方面,螺旋CT血管成像检查中对1例患者胃右动脉没有显示出来,其余各部位的血管显示与手术保持一致,差异无统计学意义。1例患者胃右动脉没有显示出来,主要是因为该患者的胃右动脉较为狭窄,影响到显示效果,见表2。
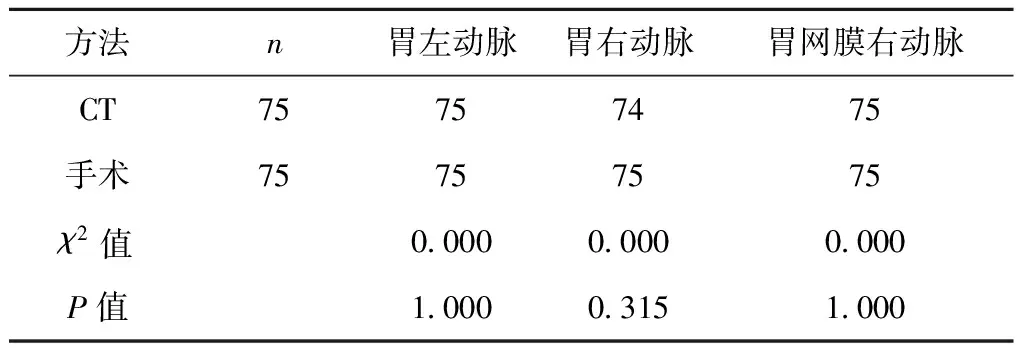
表2 患者术前螺旋CT血管成像对不同部位血管显示情况
2.3 CT与手术对不同部位解剖变异检出对比 患者术前螺旋CT血管成像对血管解剖异常率检出情况见表3,以手术诊断为依据,其中供胃血管正常70例,占93.3%,解剖变异5例,占6.7%。在解剖变异、供胃血管正常诊断方面,螺旋CT血管成像和手术证实完全一致,差异无统计学意义。在胃右动脉变异方面,其中2例患者起始于胃十二指肠动脉,2例患者起始于肝右动脉、1例患者起源于肝中动脉。
3 讨 论
胃癌属于常见恶性肿瘤,在各类恶性肿瘤中处于第3位,而在消化道恶性肿瘤中则居于首位[4-8]。临床统计资料显示,胃癌在胃部恶性肿瘤中占到了95.0%,患者以中老年人群为主,近年来呈现出年轻化发展趋势[9-10]。随着临床研究的深入,现阶段认为多种因素都能引发胃癌,比如不良生活习惯、幽门螺旋杆菌感染、慢性萎缩性胃炎、遗传因素等[11]。长期以来,由于我国大多数人群没有定期体检的习惯,因而大多数确诊的胃癌患者基本已经处于中晚期,此时手术治疗已经无法发挥作用[12]。
随着全社会对恶性肿瘤的关注,越来越多的人群开始重视健康体检,加之腹部超声检查、胃镜、X线钡餐以及螺旋CT等多种诊断方法的应用,早期胃癌诊断率有所上升[13]。早期胃癌检出率为手术方法治疗胃癌奠定了基础,常用的手术有姑息性手术以及根治性手术。临床文献报道中指出胃癌根治术有效地提高了早期胃癌患者的治疗效果,延长患者生存质量以及生存质量[14]。在常规早期胃癌开腹根治术的基础上,腹腔镜技术发展也在胃癌早期治疗中得到了应用[15]。
采用胃癌根治术治疗胃癌期间,不仅需要保证局部病灶切除彻底、淋巴结清扫完整,同时还需要注意手术操作难点,比如解剖层面较为复杂、胃周围血管分布着一定的淋巴结,操作过程中很容易引发血管损伤,造成术中或者术后出血,增加手术治疗风险,基于此,对胃癌患者实施胃癌根治术前需要尽可能明确血管分布以及血管解剖异常情况,从而避免手术操作的盲目性,提高手术操作的安全性[16-18]。
本组对行胃癌根治术患者在术前通过螺旋CT血管成像技术进行全面检查,通过检查了解不同患者的胃部血管分布、血管解剖异常以及对应的血管分型等,在血管分型方面,螺旋CT血管成像与手术病理分型符合率为98.7%,螺旋CT血管成像在胃左动脉、胃短动脉以及胃网膜左、右动脉的诊断与手术病理符合率为100.0%,与胃右动脉手术病理符合率为98.7%,1例患者胃右动脉无法显示是因为患者的动脉较细。在血管解剖变异检出率方面,螺旋CT血管成像检查方法与手术病理诊断方法证实具有高度一致性,综合上述几点,表明螺旋CT血管成像能够较好的显示胃癌患者主要血管以及血管解剖变异,为患者采用胃癌根治术治疗提供了更多的资料信息。有学者在文献报道中指出,对胃癌患者在术前采用螺旋CT血管成像,能够明确患者病灶血管分布情况、血管周边淋巴结分布情况以及病灶周边存在的主要血管等,这些信息都可以作为患者术中保护血管的关键,避免手术中造成的血管损伤[19-20]。
对于胃癌患者实施螺旋CT血管成像检查过程中应注意以下几点:(1)根据患者螺旋CT血管成像检查情况,确定患者是否需要再进行血管造影检查,对于螺旋CT检查后相关血管显示清晰的,可避免使用血管造影,减少对患者的伤害,根据检查结果做好患者的沟通工作,尤其是出现血管畸形或者血管钙化患者;(2)不同患者在增强扫描过程中会因为个体差异性造成不同增强扫描时间存在差异性,而动脉早期采用Sure Start智能阈值触发扫描可以根据监控到造影剂填充情况自动触发启动扫描,可以成功铺抓到动脉早期图像;(3)术前做好全面检查,对于造影剂过敏、严重肝肾心肺功能不全、家属不予配合患者,应避免使用螺旋CT血管成像;(4)重视各类图像重建技术的应用,依靠图像重建技术以及处理措施能够提高影像资料的清晰度,保证影像资料满足临床需求,为胃癌根治术手术操作奠定基础。
综上所述,对胃癌患者在术前实施螺旋CT血管成像检查,能够较好的显示出患者胃部不同血管,明确胃部血管解剖正常或者异常,并为胃癌根治术的治疗提供重要参考,提高手术操作的安全性,值得推广应用。
(此文图1见封三)
文见第95-97页
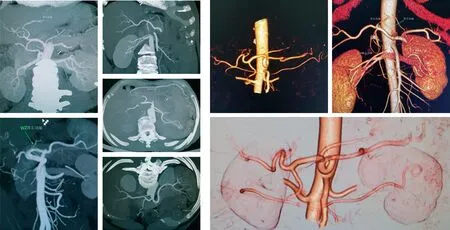
图1 胃癌患者图像后处理胃供血动脉显示情况

