妊娠期蜕膜息肉切除术的安全性探讨
李 嘉 杨 艳 杨 蕊 宋雪凌 马彩虹
(北京大学第三医院妇产科生殖医学中心 国家妇产疾病临床医学研究中心,北京 100191)
蜕膜息肉(decidual polyps)也称蜕膜脱垂,即子宫蜕膜增生、水肿并脱垂至宫颈口外。典型的蜕膜息肉仅见于妊娠妇女[1],少数不典型蜕膜反应息肉见于非孕期但长期接受孕激素治疗者[2],考虑本病可能与高孕激素水平有关。该病患病率低,国内外相关文献资料极少,仅见个案报告及小样本病例分析[2]。近年来,妊娠合并蜕膜息肉的患者逐渐增多,在需要大量使用孕激素的体外受精-胚胎移植(in vitro fertilization and embryo transfer,IVF-ET)患者中尤为明显,引起了临床医生的重视。蜕膜息肉贯穿整个宫颈管,破坏了宫颈的天然屏障,且极易出血坏死,使流产风险大大增加。目前对于妊娠期蜕膜息肉的处理尚无统一的推荐。本文总结2010年1月~2016年12月我院行蜕膜息肉切除术54例的妊娠结局,其中宫腔镜手术28例,探讨蜕膜息肉切除术的安全性。
1 临床资料与方法
1.1 一般资料
本组54例,年龄27~42岁,(32.2±3.65)岁。自然妊娠24例,辅助生育技术助孕30例。初产妇42例,经产妇12例。手术孕周5.3~24.3周,(11.8±5.7)周。75.9%(41/54)有阴道出血,出现症状到手术间隔时间6 h~3个月;分泌物增多1例;无症状常规检查发现12例。30例术前行超声检查,均提示宫颈内口上方低回声,延续至宫颈外口(图1)。阴道检查可见宫颈外口赘生物(图2),息肉直径0.8~8cm,(2.93±1.60)cm,其中>3 cm 28例。息肉表面有脓苔10例。
经门诊检查初步诊断为妊娠合并蜕膜息肉,当存在以下三种情况之一时建议手术治疗:①有阴道出血或分泌物增多症状;②息肉直径≥3 cm;③息肉表面覆有脓苔。充分知情同意并愿意接受手术者收入院,术前行宫颈分泌物培养,如结果为阴性,则行手术;如培养为阳性,则使用敏感抗生素治疗后手术。
1.2 方法
1.2.1 术式选择 根据发现息肉的孕周不同,早孕期选择宫腔镜手术,中孕期选择常规手术。双极电凝术为过渡术式。
1.2.2 治疗方法 ①常规手术为弯钳钳夹、套扎等不使用能量器械的方法,切除息肉后如创面渗血,予阴道内填塞纱布压迫止血,术后1日取出。②双极电凝术为经阴道直视下于宫颈外口水平双极电凝切除息肉。③宫腔镜手术为我们探索的新方法,具体步骤如下:无需麻醉,取臀低头高的膀胱截石位,不使用膨宫机及有压力的水源,术中仅依靠重力作用,从而尽量避免手术操作过程中生理盐水进入宫腔,降低感染风险。电切镜外鞘型号A42021A。按宫腔镜手术常规消毒,铺无菌巾。术前不导尿,术中经腹部超声监测。无需扩宫棒扩张宫颈口。宫腔镜直视下将镜体自宫颈外口置入宫颈管内,腹部超声监测下于距宫颈内口下方1 cm处以双极电切环电切息肉蒂部(电切功率40 W),如电切过程中出血,随时电凝创面止血(电凝功率40 W),蒂部离断后退出宫腔镜,取出息肉同时更换双极电珠,再次将宫腔镜置入宫颈管内,双极电珠电凝创面止血(电凝功率40 W)。确定止血彻底后结束手术。如息肉过大导致宫腔镜电切困难,可于宫颈外口水平先以常规术式摘除息肉,再行蒂部电切。但须警惕息肉蒂部回缩至内口上方导致止血困难。故超声监测下进行手术,电切点距宫颈内口≥1 cm。
2 结果
常规手术24例,宫腔镜手术28例,双极电凝术2例,结果见表1,术后病理诊断蜕膜息肉(图3)。
常规手术24例中自然流产率8.3%(2/24),1例术后4天流产,手术孕周15.6周,术前可见息肉表面脓苔;1例术后2周流产且明确为感染性流产(病理提示重度绒毛膜羊膜炎),术前间断阴道出血3个月,手术孕周18.7周。2例均为单胎妊娠且未合并宫颈机能不全等高危因素,术前宫颈分泌物培养均为阴性。早产率16.7%(4/24),其中1例34周前分娩,该患者术前宫颈分泌物培养为大肠埃希菌,予敏感抗生素治疗,孕32周因感染中毒性休克行剖宫产分娩,宫颈分泌物培养仍提示大肠埃希菌;3例34~37周分娩。
双极电凝术2例手术孕周分别为7.7周和16.3周,术后均有阴道出血,均于术后1周内自然流产。
宫腔镜手术28例中2例因胎儿异常引产(1例唐氏综合征,1例脊柱裂)。自然流产率17.9%(5/28),流产孕周12.4~21周,(18.3±3.5)周,流产时间均在术后6周以上。5例自然流产中2例合并宫颈机能不全,未行宫颈环扎术,其中1例术前宫颈分泌物培养为白假丝酵母菌,抗真菌治疗后手术;2例双胎妊娠,术前均可见息肉表面脓苔;1例无明显高危因素。早产率10.7%(3/28),其中2例34~37周分娩,1例34周前分娩,该患者既往曾行宫颈锥切术,孕30周因早产胎膜早破剖宫产分娩,术前宫颈分泌物培养阴性。
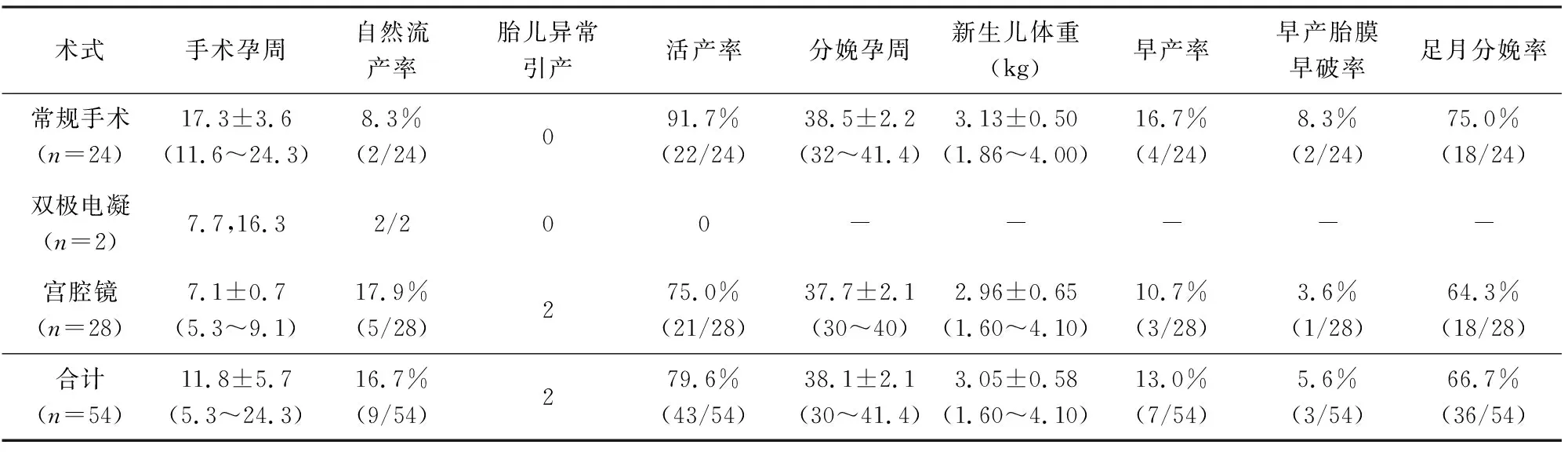
表1 不同术式蜕膜息肉切除术后妊娠结局

图1 妊娠7周合并蜕膜息肉超声图像,显示息肉贯穿整个宫颈管 图2 肉眼见蜕膜息肉外观充血明显,蒂宽,局部可见脓苔覆盖 图3 镜下见蜕膜细胞镶嵌状排列,胞浆丰富淡染或空泡状,核位于细胞中央(HE染色 ×100)
3 讨论
蜕膜息肉患病率较低,相关内容在文献中很少提到。近年来,蜕膜息肉的检出率较前有所增加,可能与辅助生育技术治疗的推广和随之而来的大剂量黄体支持药物应用以及病理科医生对于该疾病的认识提升有关。妊娠合并蜕膜息肉与妊娠合并宫颈息肉类似,常见症状为无痛性阴道出血,因此孕早期阴道流血不能仅仅诊断为先兆流产或难免流产,需行阴道检查明确诊断[3]。蜕膜息肉与宫颈息肉相比赘生物质地更加糟脆,更易发生接触性出血,息肉表面常见脓苔覆盖。另外,孕期超声可提示[4],蜕膜息肉自宫腔向下延伸,贯穿宫颈管(图1)。诊断最终需要病理结果明确。蜕膜息肉恶变可能极小,我们未见报道。
妊娠合并蜕膜息肉的处理并无相关规范和指南,结合疾病特点,可以参考妊娠合并宫颈息肉的处理办法。相对于观察和保守治疗,多数医院倾向于选择息肉切除术[5]。可能由于考虑到以下因素:宫颈息肉引起的反复阴道出血增加了感染几率;宫颈息肉相关的局部炎症可能导致绒毛膜羊膜炎。孕期行息肉切除术后绒毛膜羊膜炎发生率低于未行息肉切除者[6]。更重要的是,息肉切除术有助于除外恶性病变,尽管恶性的几率很低[7]。对于中晚期妊娠合并宫颈息肉,除上述因素外,宫颈息肉的存在可能影响对阴道出血原因的判断,延误治疗的最佳时机。同样,蜕膜息肉也引起反复阴道出血,且蜕膜息肉由于发源于蜕膜,贯穿整个宫颈管,破坏了宫颈黏液的天然屏障,使宫内感染的几率更高。组织糟脆、血运丰富也增加了感染风险。也正因为如此,对于蜕膜息肉的处理需要更加谨慎的评估和选择。
在本研究中,我们筛选了增加感染风险的几项指标作为手术指征。在妇产科多种疾病中,阴道出血增加感染风险是十分明确的,并且出血时间越长,感染风险越高;息肉大小一定程度上体现宫颈管扩张程度,因此认为息肉越大,感染风险越高;脓苔的存在除了提示感染存在,还可能与息肉组织坏死有关,这也是增加感染风险的因素。因此,对于有以上情况的蜕膜息肉,我们建议手术切除。然而,同期并没有很好的对照研究来观察保守治疗的结局。文献提出蜕膜息肉发生的高峰期是妊娠8~12周,此后随着hCG水平的下降,蜕膜息肉将逐渐消失,无需处理。但本研究中手术孕周最大的为24.3周,提示未处理的蜕膜息肉可能会持续存在。流产患者中手术孕周最大的为18.7周,该患者术前已经间断阴道出血3个月,如能尽早处理降低感染风险,有可能改变妊娠结局。综合考虑,在感染高危因素单独或同时存在时,手术切除蜕膜息肉是合理的考虑。
参考妊娠合并宫颈息肉的处理方法,对于常规手术的患者,我们采用弯钳、剪刀或套扎的方式切除蜕膜息肉。本研究结果显示常规手术后流产率较低,可能与中孕期胎儿发育等相对稳定有关。尽管流产率低,但2例流产中1例明确诊断感染性流产,另1例术后4天流产,高度提示与感染有关。可能与常规手术仅能从宫颈外口水平切除蜕膜息肉,剩余息肉仍占据宫颈管内有关。
双极电凝术由于明显不良的妊娠结局,在探索过程中被摒弃。在对该术式的观察中发现。使用能量器械并没有改善术后阴道出血的情况。可能因为蜕膜息肉的蒂较宽,双极钳较小,分次处理息肉过程中止血不彻底,或焦痂脱落后再次出血有关。同时,与常规手术相似,双极电凝术也仅能从宫颈外口水平处理息肉,无法解决宫颈管扩张的问题。
宫腔镜手术是对新方法的尝试,本组28例,宫腔镜下蜕膜息肉切除术后行超声监测,可以观察到宫颈管闭合,这是前两种手术方式无法做到的。同时,宫腔镜下放大倍数的观察也避免可能存在的止血不彻底的问题。尽管观察到的结果显示流产率略高,但流产的5例均在早孕期接受手术,中孕期发生流产,手术和流产间隔时间较长,有直接因果关系的可能降低。且其中4例合并双胎、宫颈机能不全这种极易在中孕期发生流产的因素。在综合了以上不利因素后,宫腔镜术后流产率与IVF助孕后总体的流产率(13~20%)[8]相近。提示宫腔镜蜕膜息肉切除手术本身对妊娠的影响较小。
宫腔镜蜕膜息肉手术无需扩宫棒扩张宫颈口,不进入宫腔,因此与常规宫腔镜相关的子宫穿孔、液体过载等并发症均未发生。
从本研究的妊娠结局可以推测,妊娠合并蜕膜息肉患者术后不良妊娠结局的发生主要与感染有关。对于术前宫颈分泌物培养阳性者,我们针对培养的结果应用敏感的抗生素后进行手术,术后患者可继续妊娠至足月分娩。因此,需重视术前宫颈分泌物培养的结果以及围手术期的抗生素应用,对提高手术安全性起到十分重要的作用。此外,出血时间、息肉大小及是否有脓苔覆盖均可能增加流产风险,但这些因素作为手术指征更精确的量值还需要进一步的观察和总结。
总之,蜕膜息肉由于生长方式及环境的特殊性,增加了流产风险,但手术切除也可能带来风险。如果未引起大量阴道出血,能够除外恶性可能,也许保守治疗能够带来更好的结局。但事实上,需要病理诊断才能明确息肉类型。因此,在无法除外恶性疾病时,切除息肉可能仍然是主要的选择。但妊娠期蜕膜息肉切除存在风险,需慎重评估。如果决定手术,宫腔镜下蜕膜息肉切除术是一种新的、安全、有效的手术方式,根据目前结果认为其对妊娠结局的不良影响并不高于常规手术,但仍需谨慎把握手术指征并向患者充分告知风险,并在抗生素治疗等方面加强应用以进一步降低感染性流产的发生。对于蜕膜息肉的最佳处理方案,需要进一步的前瞻性病例对照研究。手术时机的选择取决于发现息肉的时间,因此,应重视对早孕期阴道出血、分泌物增多患者的阴道检查,特别是辅助生育技术治疗的患者,以免延误诊治。

