早期二甲双胍治疗对糖尿病前期合并短暂局灶脑缺血后长期认知功能的影响
黎洁洁,彭玉晶,王拥军
既往的流行病学数据表明卒中和糖尿病可增加阿尔茨海默病(Alzheimer disease,AD)的发病风险[1-3]。本课题组前期使用短暂局灶脑缺血或2型糖尿病动物模型的研究结果发现这些动物具有AD样改变,包括认知功能障碍,脑内Aβ或磷酸化tau蛋白的增加[4-5]。糖尿病作为卒中的独立危险因素,可加剧卒中引起的认知功能障碍[6]。糖尿病前期包括空腹血糖受损和糖耐量异常[7]。卒中患者中,约1/3合并糖尿病前期[8]。糖尿病前期同样可导致认知功能障碍[9]。虽如此,糖尿病前期对卒中后认知功能的影响仍不清楚。二甲双胍被推荐用于糖尿病前期患者预防糖尿病的发生[7]。本课题组前期研究表明,二甲双胍可减轻糖尿病鼠颅内AD样的病理改变[5],而本次研究将分析二甲双胍对糖尿病前期合并短暂局灶脑缺血大鼠认知功能的影响。
1 研究对象与方法
1.1 实验动物及饮食 6周龄雄性Wistar大鼠接受高脂饮食(60%脂肪,20%碳水化合物,20%蛋白质,货号D12492i,美国Research Diet公司)制作糖尿病前期模型,或与高脂饮食的胆固醇/糖含量匹配的正常对照饮食(10%脂肪,70%碳水化合物,20%蛋白质,美国Research Diet公司)。首都医科大学动物关怀委员会同意所有实验操作。
1.2 腹腔糖耐量实验 分别在10周龄和14周龄时通过腹腔糖耐量实验的方法评估是否出现糖尿病前期[9]。大鼠禁食12 h后,腹腔注射葡萄糖(2 g/kg),2 h后尾静脉采血,通过血糖检测试纸(拜耳)检测血糖值。
1.3 短暂大脑中动脉闭塞(transient middle cerebral artery occlusion,MCAO) MCAO方法如前所述[4],腹腔注射10%水合氯醛(3 ml/kg)麻醉14周龄的雄性Wistar大鼠。通过电加热毯将动物体温控制在(37±0.5)℃。将尼龙线插入颈内动脉,至稍有阻力时停止,90 min后拔除拴线。
1.4 二甲双胍治疗和生化指标检测 高脂饮食喂养4周后将动物随机分成二甲双胍治疗组[200 mg/(kg·d),腹腔注射[5]]和生理盐水治疗对照组。每2周称量动物体重以调整药物治疗剂量。22周龄时通过血糖检测试纸(拜耳)进行空腹血糖检测;14周龄和22周龄时通过ELISA的方法检测血清空腹胰岛素浓度(货号EZRMI-13K,Millipore公司)。
1.5 Rotarod旋转棒实验 分别在15、20周龄时进行Rotarod旋转棒实验评估运动功能。如前所述[4],让动物站在转轴上1 min以熟悉滚动轴装置及周围环境。然后开始训练动物在转轴上学习行走:设定转轴为加速运动,5 min内速度从4 rpm匀速加速到40 rpm,当动物从转轴上掉落下来之后停止实验。每天连续3次,每次间隔15 min,持续2 d。第3天开始正式测试。同样设定转轴5 min内速度从让动物接受转速4 rpm匀速加速到40 rpm。记录动物从转轴上掉下来时的时间和转轴的速度。速度-时间指数=时间(s)×速度(rpm)。
1.6 Morris水迷宫 动物在21周龄时进行Morris水迷宫实验评估认知功能[10]。参照迷宫(直径160 cm,高度50 cm)的中心将水迷宫分为四个象限。整个实验分为平台不可视实验和探索实验。在平台不可视实验中,逃离平台(直径12 cm,高度28 cm)固定置于第四象限中央,距离水面2 cm。平台不可视实验包括连续5 d的训练期。在训练期中,每天接受3次训练,每次间隔15 min。每次训练的时候,动物依次顺时针从四个象限放入水池,动物到达平台后当次训练结束,如果时间超过2 min无法到达平台,当次训练终止,将动物引导到逃离平台,并让动物在平台逗留30 s,随后擦干放入笼中。所有训练期结束后的第2天进行探索实验。整个探索实验持续2 min。在探索实验中,第四象限的平台将被撤离,同时记录动物在第四象限逗留的时间。通过水迷宫上方的摄像头和迷宫软件(上海济良软件技术公司)记录分析动物游泳路线和时间。实验人员将进行盲法操作。
2 结果
2.1 高脂饮食可诱导糖尿病前期 持续4周的高脂饮食即可引起糖耐量异常和体重增加,持续到8周时,这种改变更加明显,同时还出现血清胰岛素含量增加(表1),说明高脂饮食可诱导糖尿病前期的发生。
2.2 糖尿病前期对卒中后运动和认知功能的影响和正常饮食组相比,糖尿病前期大鼠的运动功能受损。糖尿病前期合并MCAO后,长期运动功能变差,但和正常饮食组相比,糖尿病前期并没有影响MCAO术后短期的运动功能(表2)。在认知功能方面,所有动物随着训练次数增加,到达平台时间逐渐缩短。然而,MCAO大鼠到达平台时间多于对照组,这与探索实验结果相似(表3)。同时,在探索实验中,无MCAO的动物逗留在第四象限的时间更多(表4)。而与MCAO组相比,糖尿病前期合并MCAO的大鼠在第四象限逗留的时间更短(表4),提示这些动物空间记忆能力受损。另外,如表3所示,在到达平台速度方面,有或无MCAO大鼠结果类似。
2.3 二甲双胍治疗对糖尿病前期合并MCAO的认知功能的影响 所有动物同样具有空间学习记忆能力。二甲双胍治疗组找到平台的时间更短(表5)。
但在探索实验中,两组动物逗留在第四象限的时间比较,差异无统计学意义(表6)。两组动物到达平台速度无差异(表5)。
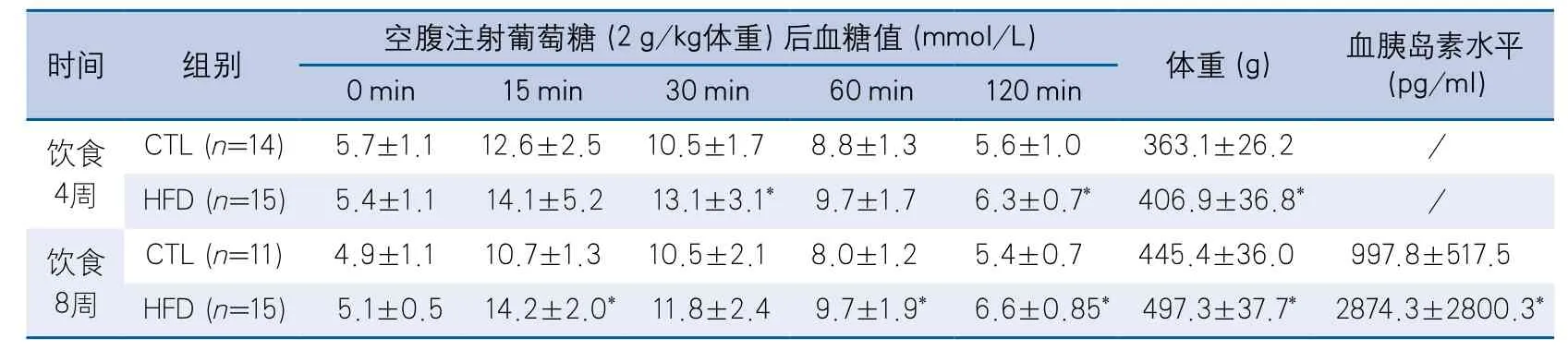
表1 高脂饮食对生化指标的影响
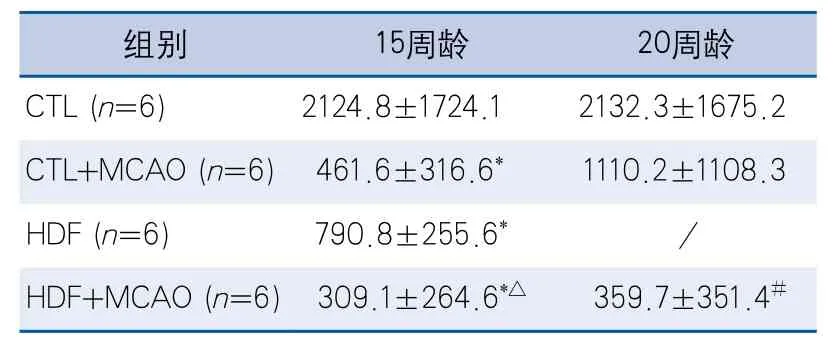
表2 Rotarod旋转棒实验各组速度-时间指数
2.4 二甲双胍对生化指标的影响 二甲双胍治疗可降低空腹血糖,并且有降低空腹胰岛素水平的趋势(表7),提示二甲双胍治疗改善认知功能可能与改善糖尿病前期状态有关。
3 讨论
卒中后认知功能障碍是临床中常见的问题。糖尿病是缺血性脑血管病最常见的合并症之一,并且和认知功能相关[11]。糖尿病前期是介于正常糖代谢和糖尿病之间的中间状态,提示发生糖尿病的风险增加[12-13]。既往流行病学研究表明,约1/3无糖尿病史的缺血性脑血管病患者合并糖尿病前期[14]。更重要的是,糖尿病前期患者不仅是发生糖尿病和卒中的高危人群,也更容易发生认知功能障碍[15-17]。本研究通过高脂饮食成功建立糖尿病前期的动物模型,表现为糖耐量异常、肥胖和胰岛素水平增加。和本课题组既往研究结果一致,短暂局灶脑缺血损害了认知功能[4]。而本研究进一步发现,高脂饮食引起的糖尿病前期加剧了缺血性卒中引起的长期认知功能障碍。
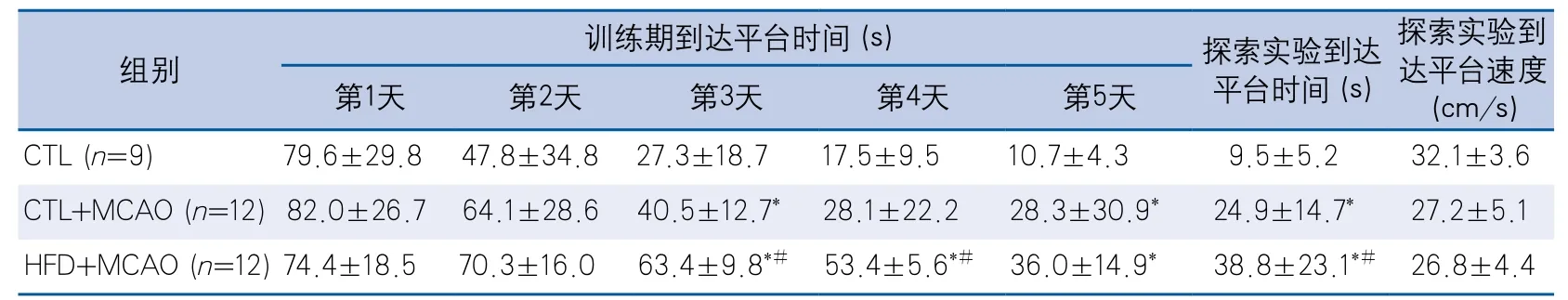
表3 Morris水迷宫实验
虽然所有动物找到平台的时间逐渐缩短,说明不管是否有糖尿病前期或MCAO,所有动物都具有空间学习记忆能力,然而不管在训练期还是探索实验中,糖尿病前期合并MCAO大鼠找到平台时间更长,说明其空间学习记忆能力受损。临床数据表明,糖尿病前期是卒中不良结局的危险因素[14],MCAO术后运动功能障碍可能影响水迷宫实验结果。但本研究结果表明,无论有无MCAO的大鼠,其到达平台速度无明显差异,提示水迷碍[20],而其他研究却发现接受二甲双胍治疗的糖尿病患者其痴呆风险明显降低[21-22]。尸检的结果也间接证实了二甲双胍治疗可以改善AD相关的神经病理改变[23]。研究人群差异,研究设计不同和糖尿病的严重程度差异可能是上述临床研究结论不同的原因。在实验室研究方面,既往研究表明,二甲双胍可通过促进神经再生改善空间学习记忆能力[24]。本课题组前期研究同样表明,二甲双胍可改善糖尿病大鼠颅内AD样的病理改变[5]。在本研究中,在糖尿病前期之后以及卒中发生前使用二甲双胍,模拟了临床常见的患者状态,结果发现二甲双胍能改善糖尿病前期合并缺血性卒中后认知功能障碍。糖-能量代谢状态和Aβ蛋白,tau蛋白以及神经再生有关[25],本研究检测了相关生化指标,发宫实验观察到的空间学习记忆能力差异并不是由运动功能受损导致的。
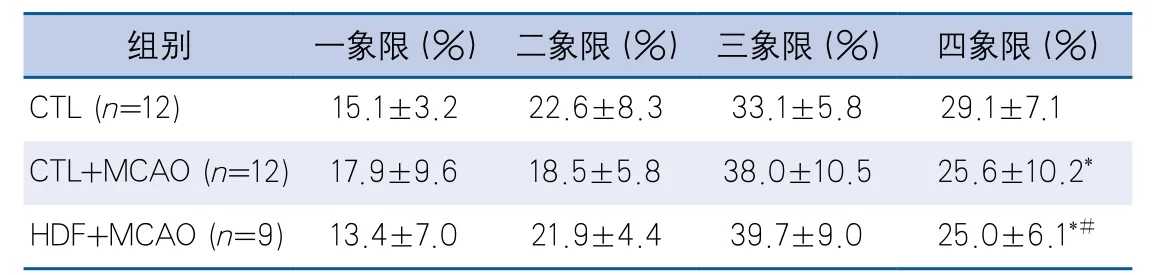
表4 Morris水迷宫探索实验平台所在各象限逗留时间占总时间比例
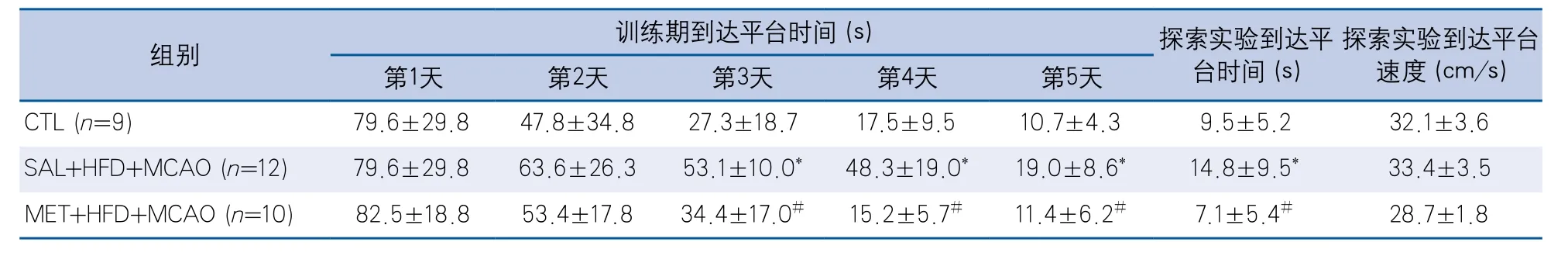
表5 二甲双胍治疗对Morris水迷宫的影响
改善卒中后认知功能障碍的治疗手段非常有限。近来的研究结果表明早期预防糖尿病可以降低认知功能障碍的风险[17]。生活方式干预和二甲双胍治疗被推荐用于糖尿病前期患者以预防糖尿病的发生[18]。与生活方式干预相比,二甲双胍成本更低,并且不受患者活动能力的影响[19]。然而,二甲双胍对认知功能的作用,目前仍存在争议。有临床研究发现二甲双胍可导致认知功能障现二甲双胍可降低空腹血糖。另一方面,临床研究表明二甲双胍可改善卒中结局[26-27],而基础研究表明二甲双胍可减小梗死体积[28-30]。因此,本研究所观察到的二甲双胍对认知功能的影响可能与降低血糖、保护脑组织有关,这还需要后续的研究加以证实。
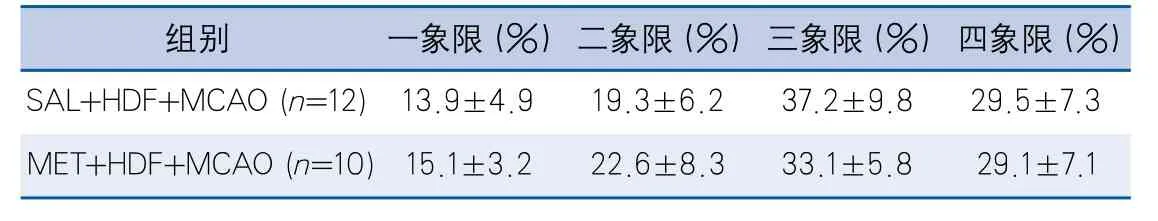
表6 二甲双胍治疗对Morris水迷宫探索实验平台所在各象限逗留时间占总时间比例的影响
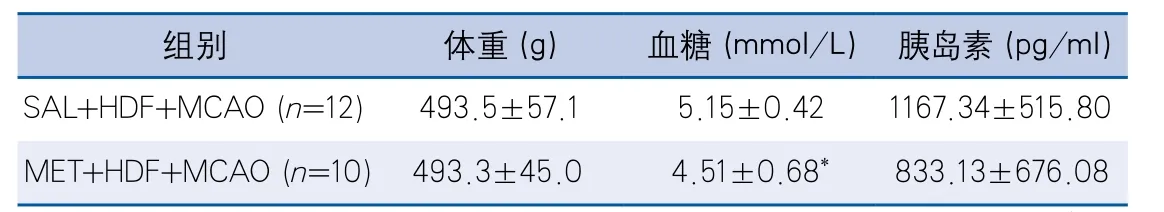
表7 二甲双胍对生化指标的影响
本研究存在以下局限性:首先,为了减少动物的死亡率,本研究采用缺血90 min的MCAO模型,这只能模拟一部分的临床卒中患者;其次,二甲双胍对缺血的基底节区或者远端和记忆有关的海马区的组织病理改变有何影响,本研究并没有涉及,需要后续研究进一步阐述。
【点睛】约1/3卒中合并糖尿病前期,本研究为改善糖尿病前期合并卒中后长期认知功能障碍提供治疗依据。

