Nur77慢病毒表达载体的构建及在鼻咽癌CNE-2Z细胞中的稳定表达
王 建
在世界大部分地区,鼻咽癌(nasopharyngeal carcinoma)是1种罕见的恶性肿瘤,但是在东南亚、北非和我国南方(尤其是广东省)其发病率显著增高,国内称之为“广东癌”[1]。鼻咽癌恶性程度较高,易于转移且预后不良[2]。Nur77是1个孤儿核受体家族成员,参与调控多种恶性肿瘤的发生发展[3]。我们的前期研究发现微管相关蛋白与肿瘤的侵袭转移密切相关[4]。为了探讨Nur77在鼻咽癌转移过程中的作用及机制,本研究构建绿色荧光蛋白标记的Nur77基因慢病毒表达载体并稳定转染鼻咽癌CNE-2Z细胞,为后续实验奠定基础。
1 材料与方法
1.1 主要试剂
限制性内切酶(Thermo);T4 DNA连接酶(Thermo);DNA回收试剂盒(Magen);KOD Plus DNA聚合酶(TOYOBO);cloneez无缝重组试剂盒(金斯瑞);质粒抽提试剂盒(康为);LipofectaminTM3000(Invitrogen);FItran:慢病毒包装专用转染试剂(辉骏生物);Trypsin-EDTA(MP);Polybrene(辉骏生物);Pyrex®cloning cylinder(Sigma)。
1.2 质粒及细胞株
XL1-BLUE MRF'感受态细胞(辉骏生物);慢病毒表达载体:pCDH-EGFP-G4S-MCS(辉骏生物);慢病毒包装质粒:pMD2.G、psPAX2(辉骏生物);HEK293T及CNE-2Z细胞。
1.3 方法
1.3.1 制备目的基因片段 根据人Nur77全长序列设计引物,上游引物为:5'-AATGAATTCGAATGCCCTGTATCCAAGCCCAA -3',含EcoRI酶切位点;下游引物为:5'-AATGGATCCTCAGAAGGGCAGCGTGTCCATG-3',含BamHI酶切位点。PCR反应体系如下:上下游引物各1 μl(10 μmol/L)、模板cDNA 1 μl、KOD Plus DNA聚合酶0.5 μl、10×聚合酶buffer 2 μl、ddH2O 12.5 μl、dNTP 2 μl。反应条件:94 ℃ 5 min;94 ℃ 30 s,60 ℃ 30 s,68 ℃ 2 min,共25个循环;68 ℃ 5 min。扩增后,经1%琼脂糖凝胶电泳后回收目的片段。
1.3.2 构建重组表达载体 用EcoRI和BamHI酶切载体和片段,反应体系如下:10×buffer 6 μl、载体/基因片段10 μl、EcoRI酶 1 μl、BamHI酶1 μl、ddH2O 42 μl,于37 ℃酶切3 h,回收酶切后的质粒和基因片段;线性化质粒和基因连接,反应如下:基因片段2 μl、线性化载体3 μl、T4连接酶1 μl、10× T4 Buffer 2 μl、ddH2O 12 μl,16 ℃连接过夜。
1.3.3 转化感受态细胞及菌落检测 感受态细胞加入10 μl DNA混匀,冰浴30 min;转化管于42 ℃循环水浴锅中热激90 s后冰浴3 min;每管加入500 μl SOC液体培养基,37 ℃振荡培养1 h,使细菌复苏;菌液涂抹培养基于37 ℃培养过夜;挑取单菌落置于液体培养基中,37 ℃摇菌;做菌落PCR检测阳性克隆;挑取单菌落摇菌后抽提质粒,酶切验证是否得到阳性克隆;阳性克隆送测序验证。
1.3.4 慢病毒包装及滴度测定 20 μl包装质粒和4μg慢病毒表达质粒在400 μl 0.9%(w/v)生理盐水中混合,并加入50 μl转染试剂,室温孵育20 min后加入到培养293T细胞的100 mm皿中;转染后48 h和72 h分别收集上清,3 000 rpm 4 ℃离心10 min,取上清用0.45 μm微孔滤器过滤;离心管底铺上2~4 ml 20%(w/v)蔗糖-PBS溶液,缓慢加入慢病毒上清液,50 000 g超速离心浓缩2 h,用250~500 μl PBS重溶;逐孔稀释法进行慢病毒滴度测定。
1.3.5 建立稳定转染细胞株 CNE-2Z细胞以2×104/孔接种至24孔板;取两孔细胞分别加入25 μl的pCDH-EGFP-G4S-Nur77病毒液和pCDH-EGFP-G4S-MCS对照病毒液;感染48h后,于荧光显微镜下观察感染效果;在6孔板中按20、50、100、200、500、1000接种感染细胞,培养7~12天后观察克隆形成情况;镜下将发光细胞群找到,用记号笔在培养皿底部划定范围做记号;用sigma公司克隆环套住记号笔画圈范围的克隆,向克隆环中加60~70 μl胰酶消化,传到新的96孔板培养孔中培养;一周后观察并标记单克隆孔;当单克隆孔长至孔面积的1/5时,选择均为阳性(通过荧光判断)的单克隆孔,消化再培养,长满后移到24孔中继续培养;Western blot进行稳定转染细胞株的Nur77蛋白表达水平检测。
2 结果
2.1 pCDH-EGFP-G4S-Nur77过表达载体的构建
以CNE-2Z细胞cDNA为模板的PCR产物行1%琼脂糖凝胶电泳鉴定,可见大小约为1 700 bp的特异性扩增条带,与预期一致(图1)。菌落PCR及酶切鉴定选出阳性克隆,将以阳性克隆为模板扩增出的基因片段进行测序,目标基因序列进行同源性分析对比,同源性100%,表明重组质粒构建成功。
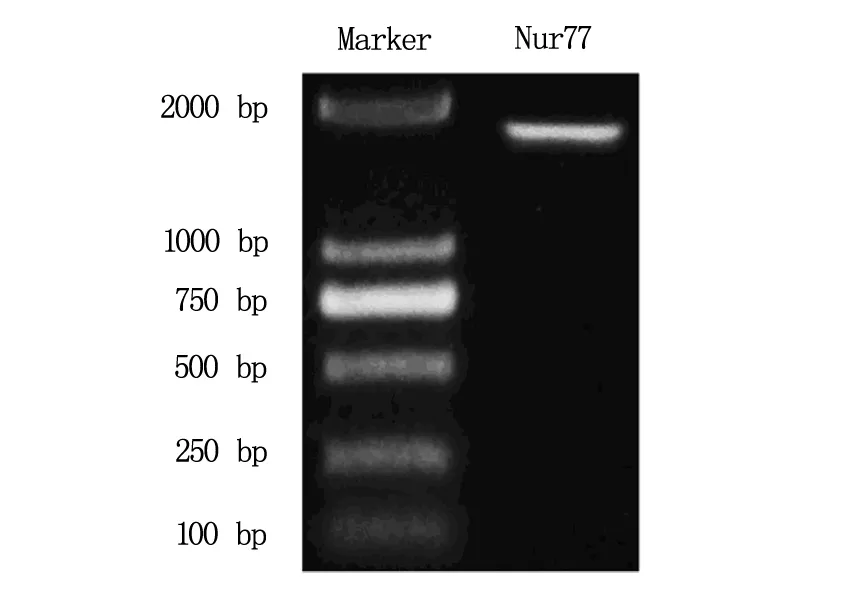
图1 Nur77基因PCR扩增产物琼脂糖凝胶电泳图
2.2 慢病毒滴度测定
接种病毒48 h后观察荧光表达情况,病毒原液的滴度值=荧光细胞个数/稀释后的病毒量。实验和对照病毒滴度均超过1×10-8Tu/ml。
2.3 过表达Nur77的稳转CNE-2Z细胞株的建立及蛋白表达检测
通过病毒感染及荧光筛选,获得了稳定表达Nur77的细胞株。荧光显微镜观察可见,发荧光的细胞与明场视野下细胞相一致(图2)。Western blot结果显示(图3),与转染空载体组相比较,本底Nur77的蛋白水平无显著差异,而融合蛋白在空载体组无表达而在Nur77组高表达,提示Nur77成功稳定转染CNE-2Z细胞株。
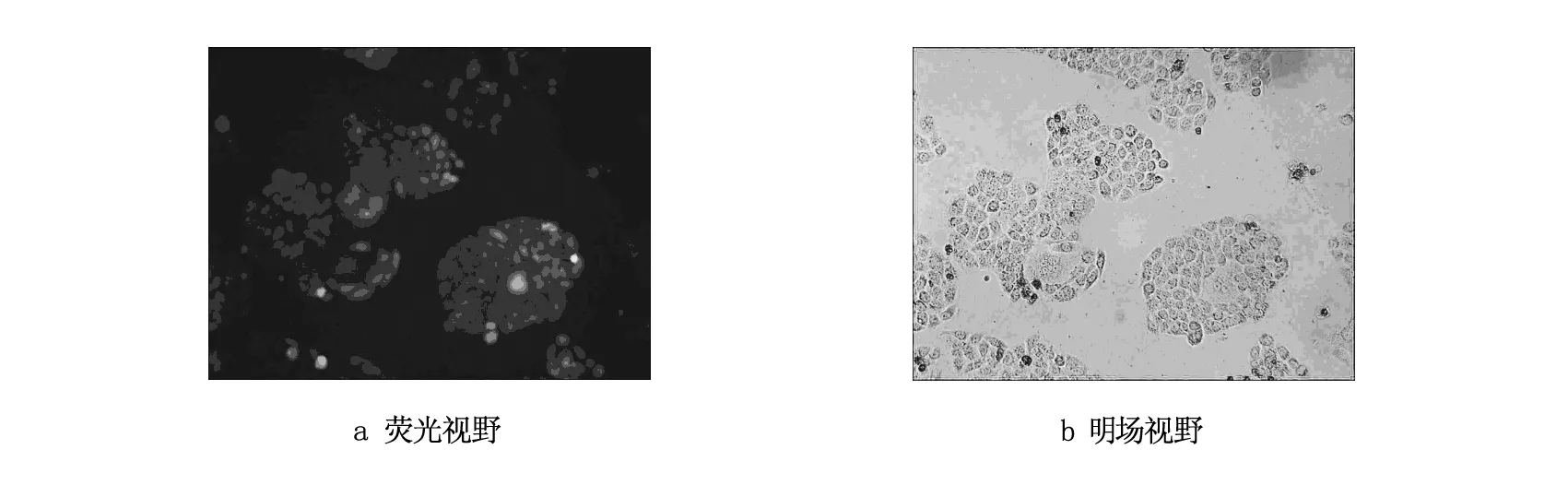
图2 稳定转染细胞株的荧光显微镜观察
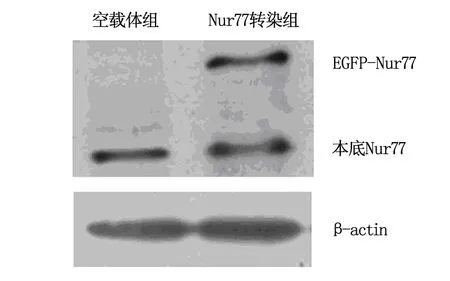
图3 转染的CNE-Z细胞Western blot检测
3 讨论
Nur77是1个核转录因子,在细胞增殖、凋亡、迁移等多种生物学过程中发挥重要影响[5]。在肿瘤发生发展中,Nur77具有双重作用。一方面,作为转录因子,其能上调多种基因表达促进细胞的增殖与迁移,抵抗凋亡;另一方面,其蛋白本身的亚细胞定位变化如定位到线粒体可诱导凋亡[6]。而我们的研究方向,是探讨Nur77通过作用于微管蛋白调节鼻咽癌细胞迁移、侵袭的分子机制。因此,构建Nur77与荧光蛋白融合表达质粒稳定转染鼻咽癌细胞株能更好的反映目的蛋白的亚细胞定位及与相关蛋白的相互作用。
质粒瞬时转染的效率虽然高,但转染后目的基因很少能整合进入基因组,因此不适合稳定株的筛选[7]。慢病毒载体是以人类免疫缺陷I型病毒(HIV-1)为基础发展起来的基因载体。它是1种逆转录病毒,能使外源基因整合入宿主基因组并稳定、长期表达,但却比一般的逆转录病毒具有更高的滴度和更广的宿主范围。携带外源基因的慢病毒载体与包装载体同时转染包装细胞,即可进行病毒的包装,而后经收集和浓缩的慢病毒液可以直接用于感染宿主细胞[8]。本研究成功构建了绿色荧光蛋白标记的Nur77慢病毒表达载体并稳定转染CNE-2Z细胞,为进一步研究Nur77亚细胞定位改变及对微管功能的调控奠定了前期实验基础。

