重组人血管内皮抑素联合mFOLFOX4方案治疗晚期原发性肝癌的临床观察
薛 李 田 宏 王丽霞
原发性肝癌是恶性程度极高的肿瘤之一,患者确诊时大部分已到晚期,失去了手术治疗的时机。临床数据显示,原发性肝癌患者中,仅约25%的患者符合手术治疗的指征,75%的患者需要通过放疗、化疗、介入治疗、中医药、生物治疗等方式进行合理组合治疗,其目的在于延长患者的生存时间、降低患者治疗期间的不良反应、提升患者生存期间的生活质量[1]。重组人血管内皮抑素是近年来开发的一种治疗恶性肿瘤的药物,其通过抑制为肿瘤细胞提供营养的血管内皮细胞的新陈代谢,达到截断肿瘤细胞营养而杀灭肿瘤细胞的目的[2-3]。mFOLFOX4化疗方案是《2009年原发性肝癌规范化诊治专家共识》指南中推荐的治疗晚期原发性肝癌的一种化疗方案,是具有临床较高认可度的治疗原发性肝癌的化疗方案[4-5]。本文将2种治疗方案联合用于治疗晚期原发性肝癌患者,以期寻找更适合晚期原发性肝癌患者治疗的方案。现报告如下。
1 资料与方法
1.1 临床资料
选择2013年1月至2014年3月我院收治的晚期原发性肝癌患者84例作为研究对象,纳入标准:①年龄18~60岁;②符合《2009年原发性肝癌规范化诊治专家共识》中对原发性肝癌的诊断和晚期标准;③有可测量病灶;④不符合肝动脉栓塞化疗指征者;⑤发生肝外转移或者合并门静脉主干癌栓者或者肝功能C级者;⑥预估生存时间>6个月;⑦患者及家属了解参加此次研究利弊,并签署知情同意书,愿意配合各项研究工作。排除标准:①不符合上述纳入条件者;②妊娠或哺乳期妇女;③未同意参与本次研究,或未签署知情同意书者。将其按照就诊顺序编号随机分为对照组与观察组,每组42例。2组患者性别、年龄、治疗史、入组前目标病灶基线直径、肿瘤灶数量、肿瘤转移器官比较,差异无统计学意义(P>0.05)。见表1。
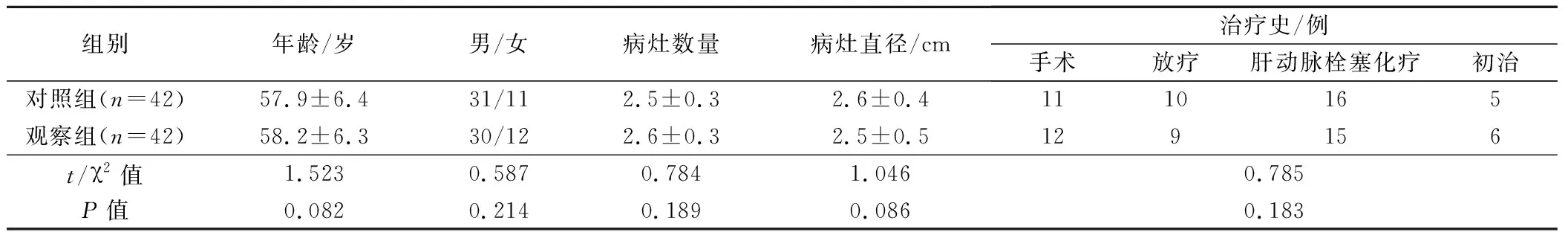
表1 2组患者临床基线资料比较
1.2 方法
2组患者入组后均根据患者情况选择中药制剂如华蟾素注射液、康莱特注射液、生物制剂如α-干扰素等治疗以改善患者癌症相关症状和患者生活质量。对照组患者在上述治疗的基础上采用以mFOLFOX4系统化疗方案:甲基强的松龙40 mg溶解于100 ml生理盐水中静脉滴注(第1、2天),西咪替丁0.4 g溶解于100 ml生理盐水中静脉滴注(第1、2天),5%的葡萄糖注射液静脉滴注(第1天),奥沙利铂(85~100 mg/m2)溶解于250 ml 5%的葡萄糖注射液中静脉滴注(第1天),30 ml丹参注射液溶解于250 mL 5%的葡萄糖注射液中静脉滴注(第1、2天),亚叶酸钙(200 mg/m2)溶解于250 ml生理盐水中静脉滴注(第1、2天),5-氟尿嘧啶 (400 mg/m2)溶解于100 ml生理盐水中静脉推注(第1、2天,1次/天),5-氟尿嘧啶(400 mg/m2)溶解于250 ml生理盐水中静脉滴注(第1、2天,1次/天,滴注6 h以上或者24 h持续滴注)(第1、2天),胃复安10 mg/次,肌注(第1、2天,1次/天)。每2周重复一次,共6周,当患者出现病情进展或出现3级以上不良反应时应停止化疗。观察组在对照组治疗基础上,再予以重组人血管内皮抑素注射液(山东先声麦得津生物制药有限公司生产,国药准字S20050088,规格:15 mg/2.4×105U/3 ml/支)静注治疗,每天15 mg,于化疗第1天开始给药,连续给药14天。2组患者均行6个周期治疗。在治疗过程中严密观察患者急性、亚急性不良反应,当患者出现3级及以上的不良反应时,应停止化疗,退出研究。
1.3 观察指标
比较2组患者治疗前、完成治疗后1周内、6个月、3年目标肿瘤的直径,评价2组患者治疗后的近、远期疗效。收集患者治疗过程中的不良反应并比较。比较2组患者1年期、2年期、3年期生存率。
1.3.1 临床疗效判定 采用实体瘤疗效评价标准(RECIST),选择患者可测量病灶作为目标病灶,采用CT测量患者入组前、完成治疗后1周、治疗后6个月、3年的目标病灶直径变化,按照如下标准判断临床近期、远期疗效。完全缓解(CR):所有目标病灶消失;部分缓解(PR):目标病灶基线直径之和至少降低30%;疾病稳定(SD):目标病灶基线直径之和有下降,但未达到PR,或者增加但未达到PD的程度;病变进展(PD):目标病灶基线直径之和增加至少20%或出现新病灶。临床总有效率= (CR+ PR+ SD)/总例数×100%。
1.3.2 不良反应观察 每周期全身治疗前、后均进行血常规、肝肾功能和心电图等检查,治疗期间收集患者的不良反应症状,注意关注患者是否出现mFOLFOX4的不良反应如:食欲下降、恶心、神经毒性如四肢末端异常、遇冷疼痛等、中性粒细胞减少、腹泻。
1.4 统计学处理
采用SPSS 18.0对数据进行统计学分析。计数资料采用χ2检验,等级计数资料采用秩和检验,计量资料采用t检验,P<0.05 表示差异有统计学意义。
2 结果
2.1 2组患者近远期临床疗效比较
2组患者均完成6个周期化疗疗程。完成治疗后6个月、3年对照组患者临床总有效率分别为35.71%、4.76%,观察组分别为47.62%、9.52%;观察组近远期临床疗效均明显高于对照组(P<0.05)。见表2。
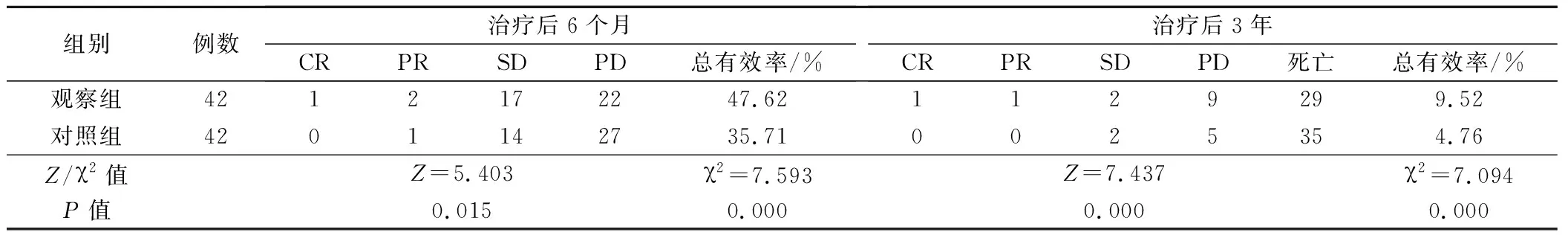
表2 2组患者近远期临床疗效比较/例
2.2 2组患者生存率比较
2组患者1年、2年生存率差异无统计学意义,但观察组患者3年生存率明显高于对照组,见表3。
2.3 不良反应
治疗期间2组患者不良反应发生率差异无统计学意义(P>0.05)。见表4。

表3 2组患者生存率比较(例,%)

表4 2组患者急性和亚急性不良反应比较(例,%)
3 讨论
原发性肝癌是临床恶性程度极高的恶性肿瘤之一,被临床称为“癌中之王”,患者预后较差。原发性肝癌是我国的高发恶性肿瘤,其发病人数和死亡人数占到世界原发性肝癌的50%[6]。目前手术仍然是根治原发性肝癌的主要方法,但临床大部分患者在确诊时已为中晚期,符合手术指征并成功实施手术治疗者少之又少。大部分患者需要以延长生存期、改善临床症状、提升生活质量为目的的综合治疗方案。目前非手术治疗原发性肝癌的手段主要有:介入治疗、消融治疗、放疗、放化疗结合、系统性化疗、中医药治疗、生物治疗等方式[7-8],其中肝动脉介入栓塞术是指南推荐对于不能手术患者首选的治疗方案。但是肝动脉化疗栓塞术治疗方案也对患者有较高的要求,对于肝功能受损严重的患者、有大量肝腹水的患者、全身多器官衰竭者、白细胞和血小板明显降低患者、凝血机能严重退化、感染、肿瘤发生远处转移者而言,肝动脉栓塞术和肝动脉化疗均是禁忌证。而原发性肝癌的发病机制复杂,晚期患者中具有上述禁忌证的患者不在少数。因此,对于大部分晚期原发性肝癌患者而言,以化疗为主的综合治疗方案仍然是临床主要治疗手段。众多临床研究显示,对于原发性肝癌患者系统性化疗方案明显优于一般性支持治疗[9-10]。从20世纪50年代开始,临床所用的化疗药物均在原发性肝癌患者治疗中进行了研究,如阿霉素、氟尿嘧啶、顺铂、丝裂霉素,但单药化疗的临床疗效并不理想。而且,单药化疗过程中的不良反应也限制了其的临床应用,完成单药化疗的患者在生存时间和生存质量改善方面并未获得可接受的临床效益。随着新一代化疗药物奥沙利铂、吉西他滨、伊立替康等在临床的成功应用,肝癌系统性化疗的选择余地大为增加。FOLFOX4是临床治疗大多数恶性肿瘤的经典化疗方案,其通过采用甲基强地龙和西咪替丁对胃肠道进行保护,减轻奥沙利铂对胃肠道的刺激作用,奥沙利铂作为靶向作用的部位,其中的铂原子与肿瘤细胞的DNA发生交联,阻断肿瘤细胞的复制和转录过程,达到杀灭肿瘤细胞的目的[11-12]。5-Fu通过参与核苷酸的合成,阻断肿瘤细胞核苷酸的正常转化,达到抑制肿瘤细胞DNA和RNA合成的目的,其在处方中具有协同奥沙利铂的抗癌作用。亚叶酸钙可增强5-Fu的体内作用。改良FOLFOX4化疗处方通过调整奥沙利铂的给药剂量和时间,在保证总量的同时,使奥沙利铂发挥作用的过程更适合肿瘤细胞的增殖周期,达到更强的抗癌效果[13]。
重组人血管内皮抑素是血管生成抑制类新生物制品,其作用机理是通过抑制形成血管的内皮细胞迁移来达到抑制肿瘤新生血管的生成,阻断了肿瘤细胞的营养供给,从而达到抑制肿瘤增殖或转移目的[14-15]。
本研究采用重组人血管内皮抑素联合mFOLFOX4化疗方案对晚期原发性肝癌患者进行治疗,结果显示,较之于仅采用mFOLFOX4化疗的患者,联合治疗患者的生存期有较大的提高,说明该治疗方案提升了晚期肝癌患者的生存质量。
综上所述,重组人血管内皮抑素联合mFOLFOX4化疗方案治疗晚期原发性肝癌患者可明显提高临床疗效,提高患者的3年生存率,且并不增加患者的不良反应,对此类患者具有较高的临床价值。

