肌肉减少症的发病机制及诊治研究进展
王晓乐,白 洁
1 概念及流行病学
人体骨骼肌共有600余块,分布广,约占体重的40%,每块骨骼肌不论大小、位置如何,都有一定的形态、结构和辅助装置,并有丰富的血管和淋巴管分布,受一定的神经支配。因此,每块骨骼肌都可以看作一个器官。成年人肌肉质量在30岁左右达峰,此后每年以1%~2%的速度开始下降,随着年龄增加,骨骼肌流失速度加快[1]。有文献指出,肌肉减少症(肌少症)患者半数以上为老年人群,尤其是80岁以上老年人[2],由此造成的功能失调、慢性心肺疾病、吞咽功能障碍甚至是跌倒、骨折、致残乃至死亡的风险大大增加,在一定程度上影响老年人的生命质量,加重家庭和社会负担。一项国外的调查预测,到 2050 年全球肌少症患者将达到 5 亿[3,4]。 我国2009年一项全国性疾病监测死亡调查指出,“跌倒”在老年人死亡率中已占一定比例[5]。因此对肌少症的研究意义重大。
肌肉减少症(Sarcopenia,Sp),来源于希腊语,其中,sar意为肌肉,penia意为流失,1989年,此名词由美国塔夫茨大学的Irwin Rosenberg首先提出[6],并最初将其定义为:泛指增龄性的骨骼肌质量减少、肌力下降。1998年,Delmolnic等利用双能X线测定人体骨骼肌质量,将低于健康成年人2个标准差者定义为肌少症[7]。随着研究的深入,欧洲老年肌少症工作组(European Working Group on Sarcopenia in Older People,EWGSOP)于2010年发表了肌少症共识[8],并与国际肌少症工作组(International Working Group on Sarcopenia,IWGS)在 2011 年达成共识[6],将其定义为:与增龄相关的进行性的全身肌量较少、肌强度下降或肌肉生理功能减退。然而肌肉减少应该被定义为正常的生理功能减退还是病理变化,目前国际仍未明确划分。
Sp流行病学:由于地区、种族差异、生活方式的多样化、所使用的指标评价工具和标准不同,肌肉减少症患病率存在差异。美国人群中肌少症发病率分别为男7%,女10%;英国社区老年人男女肌少症患病率分别为4.6%和7.9%。而我国肌少症患病率调查主要来自中国台湾和香港地区,男性患病率约6.7%~8.4%,明显高于女性(0.4%~2.6%)[9,10]。 有报道指出,>60岁的中国社区老年人的肌少症发病率达 10.4%[11]。
2 发病机制
Sp作为一种增龄性疾病,其发病机制复杂多样,可能有运动、中枢及外周神经,激素、营养、免疫、遗传等多种因素参与。
2.1 神经-肌肉机制 α运动神经元退化和丢失是肌肉质量及功能下降原因之一[12,13]。肌纤维的存活有赖于神经元的正常功能。人体骨骼肌含有两种纤维,Ⅰ型即慢肌纤维,其周围有丰富的血管、神经,但肌质网不发达,摄Ca+能力较弱;Ⅱ型即快肌纤维,肌质网发达,摄Ca+能力强,收缩能力强,一般由大运动神经元支配。此外,老年时星状细胞数量和募集能力下降,均致Ⅱ型纤维比Ⅰ型纤维下降显著。目前的研究显示,运动神经元分化过程受到某种影响后发生退行性病变,使得损伤后修复过程异常易致肌少症[14]。
2.2 内分泌机制 多数研究显示,睾酮水平降低与肌少症的发生有关,补充睾酮可增加老年人的肌肉质量和功能。体外试验揭露睾酮减少引起肌少症的机制为睾酮可促进星形细胞的数量,且为主要的调控因子[15]。有调查显示,绝经期妇女发生肌少症的概率明显增加,这提示雌激素与肌少症的发生或有关系,但其对肌少症的作用证据不一,可能主要影响肌肉强度。
韩国学者Kim等研究发现,与健康老年人群相比,血糖高的老年人群发生肌少症可能性明显增高[16],Morley JE 的研究则显示, 年龄>80岁的老年糖尿病患者,肌少症的发病率最高可达50%[17]。而一项来自于Kalyani和Ji的前瞻性研究得出以下结论:糖化血红蛋白(HbA1c%)≥8%的老年T2DM患者骨骼肌质量明显下降且发生跌倒风险亦明显增加[18,19],其可能的机制是:胰岛素能够促进骨骼肌对葡萄糖的摄取,促进蛋白质合成,抑制蛋白质分解。
糖尿病患者体内持续高血糖造成一种慢性炎症状态,使白介素6(IL-6)、肿瘤坏死因子α(TNF-α)、C反应蛋白等炎症细胞因子浓度增加,肌肉质量和肌肉力量呈下降趋势。已经有研究证实,IL-6可以通过促进骨骼肌分解代谢使得肌肉量减少,TNF-α则可以直接引起肌肉蛋白的减少,两者相互促进,促进肌少症发生[20]。
此外,糖尿病病程对肌少症发生亦有重要影响。一项针对日本人群群体跟踪研究显示,糖尿病病程越长,糖基化终末产物 (Advanced Glycation End Products,AGEs)积累越多,而组织中 AGEs含量与四肢骨骼肌质量呈负相关[21];同时,糖尿病病程越长,其神经系统并发症出现可能性大大增加,机体会处于相对少运动状态,运动神经元数量减少,发生肌肉质量减少以及肌肉功能减退[22]。一项调查显示,在糖尿病患者中,并发肌肉减少症往往预后不良[23]。
Notch通路是一种高度保守的跨膜受体,在肌肉生长以及肌肉再生过程中起着重要作用[24]。一方面,维生素D的缺乏可以阻止Notch通路,从而导致肌肉萎缩、肌肉质量下降,这在动物试验中已经得到证实[25];而Seo等的研究中,增加每日钙摄入量能明显减少肌少症的发生[26];另一方面,机体持续高血糖状态也会对该通路造成影响,阻碍肌肉血管生成,进而影响肌肉血液及营养供应,增加骨骼肌萎缩甚至跌倒、骨折等不良事件发生风险。
骨骼可通过旁分泌影响肌肉。骨钙素可能通过激酶途径以及影响代谢来调节肌量、影响功能[27,28];硬骨素通过调控Wnt信号通路调节肌肉分化[29];目前尚未证实成纤维细胞生长因子-23对肌肉有直接调节功能,但其可通过抑制肾小管重吸收磷致低磷血症,降低1α羟化酶致活性维生素D减少来影响肌肉的质量和功能[30]。
2.3 氧化应激与线粒体功能紊乱 氧化应激是由自由基在体内产生的一种负面作用,并被认为是导致衰老和疾病的一个重要因素。适量的活性氧簇(Reactive Oxygen Species,ROS)可通过激活核因子κB(Nuclear Factor-λ-gene Binding,NF-λB)、丝裂原活化蛋白激酶(Mitogen-activated Protein Kinase,MAPK)等多条信号转导途径使体内抗氧化物水平和功能提高,以此抵抗ROS的过度增加。老年人骨骼肌进入衰老进程,不断产生大量ROS,导致体内氧化与抗氧化失衡,损伤肌细胞结构和功能,进而影响钙离子转运,由此造成肌肉组织的损害。
线粒体功能紊乱在促进人体衰老中有重要影响。线粒体DNA(mtDNA)缺乏保护性蛋白,并且其自我修复能力较差,使其易受到氧化而发生损伤,加之线粒体基因组一旦发生突变,其缺乏内含子的特点使得线粒体难以保持基因的完整性,蛋白质合成及电子传递通路受损,影响正常的氧化磷酸化,ATP合成减少,促进骨骼肌衰老进程,同时衰老骨骼肌产生大量ROS,促进肌少症的发生[31]。
2.4 遗传因素 最近有研究发现一些基因的甲基化与肌量变异有关[32]。但目前关于遗传因素的研究较少,主要方向集中在与肌少症表型相关的一些候选基因,目前尚不能得到大范围人群的证实。
2.5 其他相关疾病 随着年龄增长,心脑血管系统等全身脏器老化,功能减退,甚至是慢性消耗性疾病或者恶性肿瘤的发生,使老年人活动力下降,营养不良,蛋白质消耗增加,相对摄入量不足,从而导致肌肉质量和力量下降、肌肉功能减退,增加跌倒率、致残率、死亡率。
3 诊断
目前国际上尚缺乏统一的肌肉减少症诊断标准,这与不同地区、不同人种、不同基因、饮食及生活习惯的干预有很大关系。起初由Delmonica于1988年提出,运用双能X线吸收法 (Dual energy X-ray absorptiometry,DXA)测定四肢骨骼肌质量,再除以身高的平方(即四肢骨骼肌指数 SMI)低于健康成年人2个标准差定义为肌少症,这仅仅将关注点放在骨骼肌质量方面。然而,正如2011国际肌少症共识指出的,肌肉减少症同样也包括肌肉力量下降以及肌肉功能减退。2013年亚洲肌少症工作组(Asian Working Group for Sarcopenia,AWGS)综合了多份来自于亚洲不同国家和地区关于肌少症的研究报道,推荐:运用DXA测定四肢骨骼肌质量除以身高的平方作为肌肉力量诊断标准,若男性<7.0 kg/m2,女性<5.4 kg/m2则考虑存在肌肉质量减少;而运用生物电阻抗 (Bioelectrical Impedance Analysis,BIA)测定肌肉质量减少的切点为男性<7.0 kg/m2,女性<5.7 kg/m2;推荐步速为步行6 m试验中速度<0.8 m/s为肌肉功能减退;握力男性<26 kg、女性<18 kg为肌肉力量下降诊断切点[33]。这与EWGSOP提出的诊断标准相似。综合国内外标准及研究,目前推荐采用图1筛查标准。
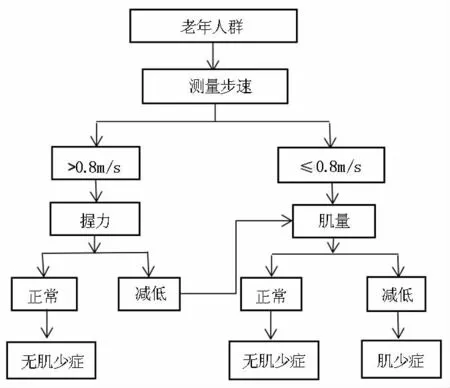
图1 肌少症筛查流程图
3.1 肌肉质量测定 目前常用的肌肉质量测定方法有DXA、CT/MRI计算机体层扫描、BIA。DXA可以很好地将骨骼、肌肉及脂肪组织区分开来,但不能准确分辨出肌肉组织中的脂肪含量,同时存在射线辐射等问题,因此在肥胖人群测量中,其测量数值往往比正常值偏高。CT/MRI能比DXA评估肌肉质量更优,但其产生的辐射较DXA更高,此外费用问题也限制了其在肌肉质量评估中的应用。目前国际较为流行的测定方法为BIA法,即利用生物电阻抗原理,利用电极在体表记录不同组织产生的电阻抗,精确测量骨骼肌质量。再根据骨骼肌指数计算判定是否存在骨骼肌质量减少。
3.2 肌肉力量测定 目前国际上使用最广泛的肌肉力量测量方法为握力测定,JAMAR握力计由于其价格低廉、便于携带的特点,是目前应用范围最广、可信度最高的握力测定仪,美国手治疗协会(American Society of Hand Therapists,ASHT)推荐测定方法为受试者双足自然放于地面,屈髋屈膝90°,取坐姿,肩内收中立并屈肘90°,双上臂与胸平贴,伸腕0~30°并保持切点尺偏,左右手分别测量三次握力取最大值。来自一项分析总结多达四万多名受试者的荟萃分析显示,握力增加,死亡风险呈现下降趋势,肌肉力量测定有着重要的位置。韩国一项研究指出,肌肉力量测定较肌肉质量测定能更好地预测老年人群机体活动能力以及5年死亡率[34]。
3.3 肌肉功能测定 肌肉功能评定方法较多,包括日常步速评估法,其是将步速<0.8 m/s判定为肌肉功能下降,能较好地反映肌肉功能,也是目前常用的肌少症筛查诊断方法之一。此外,简易机体功能评估 (Short Physical Performance Battery,SPPB)是临床应用最广泛的方法,它包括日常步速测定、前后位坐立站起时间以及站立平衡试验,每项评定记分0~4分,低于1分则为肌肉功能下降。
AWGS在2016年发布的关于肌少症的更新中指出,尽管这项诊断准则被广泛接受,但仍可能需要进一步修订,从而更好地推进亚洲地区肌少症的研究进展[35]。
4 防治
肌少症目前的防治主要集中在三个方面,即适当运动锻炼、营养支持(尤其是蛋白质、维生素D的摄入)以及合理的药物治疗。
适当的主动和被动运动对于肌少症的发生有一定的延缓作用。多项研究证实适当的渐进性的抗阻训练能够增加骨骼肌蛋白质的合成,提高肌量、肌力,在一定程度上减少骨折、跌倒等事件的发生[36,37],长期规律训练更能持续的获益[38]。但是训练的强度和时间尚未得到统一的认识。
蛋白质,尤其是支链氨基酸的摄入可促进骨骼肌蛋白质的合成,抑制其降解,从而在一定程度上达到防治肌少症的目的。Bauer等美国学者建议老年人群蛋白质每天摄入量应达到1.2 g/kg·d,慢性消耗性疾病蛋白质摄入量应该更高[39]。适量补充维生素D对于改善肌萎缩、增加肌肉量有明显帮助。2011年一项Meta分析显示,25(OH)D高于25 nmol/L者,补充维生素D后肌肉质量与功能无明显改善,然而低于25 nmol/L者补充维生素D后臀部肌力改善明显[40],随后一项 Meta 分析显示,25(OH)D低于30 nmol/L的老年人,补充维生素D可以提高肌力[41],同样,临床试验证实12周的抗阻训练的健康男性在补充维生素D后肌力也有明显提高[42]。
目前,市场上尚缺乏专门针对肌少症的药物。一些药物因其具有增加、调节蛋白质和激素的作用而用于治疗肌少症,虽有一些疗效,但效果并不理想。不管对于男性还是女性,睾酮能增加其肌量和肌力,并且不会增加老年人的病死率,但有研究也表明睾酮也会带来如过敏反应、心脏事件、肿瘤等不良反应。选择性雄性受体激动剂目前尚在临床研究中,其优点为在体内不会被代谢为二氢睾酮或雌激素,但其整体疗效尚需进一步证实。生长激素可促进骨骼和肌肉的生长,与睾酮联用可明显的增加肌量和肌力,但其安全性尚未证实。一些因子如胰岛素样生长因子-1、胃饥饿素可增加生长激素水平,有一定的临床价值。作为β-2受体激动剂,Espindolol是一种吲哚洛尔对映体,2期临床研究提示其可增加肌量、握力和降低脂肪量[43]。有研究发现血管紧张素转换酶抑制剂(Angiotensin Converting Enzyme Inhabitors,ACEI)能够通过增强血管内皮功能改善骨骼肌血流,推测其可以用来对抗肌肉减少,但目前ACEI类药物治疗肌少症仍存在很大争议,仍需要大样本试验探究。除ACEI类药物外,银杏叶提取物、他汀类药物、血管扩张剂等心血管药物也有益于肌肉减少的延缓,但上述药物用于治疗肌少症为目的时,其安全性和不良反应有待于更多研究才能明确。肌酸,是人体内自然产生的一种氨基酸衍生物,它可以快速增加肌肉力量,促进新肌增长,加速疲劳恢复,提高爆发力。肌酸在人体内储存越多,力量及运动能力也越强。因此成为体育界提升竞技水平的运动增强剂。老年人适当的抗阻训练配合肌酸补充可以显著提高受试者肌力和肌肉质量[44],但对于慢性肾功能不全患者来说,大剂量的肌酸可以引起液体潴留甚至引发肾炎。
根据肌少症发生的可能的神经-肌肉机制,营养神经药物可能会在一定程度上减少肌少症的发生、缓解肌少症的症状,但目前关于此项研究较少。
肌肉减少症日益成为一项全球化健康问题,虽然目前对肌少症的研究取得了一定的进展,但其具体的发生机制、诊断标准与治疗方案仍需更进一步的系统的研究。

