以智能下降为首发症状合并松果体区肿瘤的Rasmussen脑炎1例并文献复习
Rasmussen脑炎(Rasmussen encephalitis,RE)又称Rasmussen综合征(Rasmussen syndrome,RS),是一种罕见的后天获得性进展性慢性炎症性脑疾病,以一侧大脑半球损害引起的难治性癫痫、进行性偏瘫和智能减退为主要临床特征[1]。典型RE通常以癫痫为首发临床表现,以难治性部分发作性癫痫(包括癫痫持续状态,Epilepsia partialis continua,EPC)为主要特征[2]。然而,也有极少数病例出现癫痫症状缺失或延迟的情况[3~7]。我们对1例12岁(现16岁)非典型RE患儿进行了4 y的随访。本例患儿以智能减退为首发症状,起病2 y内无癫痫症状,期间并发松果体肿瘤,最终被确诊为RE。我们通过总结临床表现、视频脑电图、磁共振(magnetic resonance,MR)及正发射断层显象术(positron emission tomography,PET)图像、文献复习探讨非典型RE的特点,提高对该类疾病的认识。
1 病例资料
患儿男,右利手,足月顺产,起病前生长、发育正常,智力、精神正常。10岁时(2010年)起病,逐渐出现动作迟缓、记忆力减退、学习能力下降、情绪不稳定以及社交退缩,查头部CT(2010年10月29日)未见明显异常,未做处理。
2012年5月18日开始反复出现发作性右上肢抖动,遂于2012年6月15日就诊。入院查体:意识清楚,远事记忆力、计算能力、理解能力减退,MMSE评分18分;右侧鼻唇沟浅;四肢肌张力正常,肌力5级,右侧肢体轻偏瘫试验阳性,可见右上肢不自主抖动;全身深浅感觉正常;右侧跟腱反射亢进,Babinski(+),左侧正常。辅助检查:常规指标(血常规、尿常规、大便常规、肝肾功能、电解质、血糖、血脂)、感染指标(超敏C反应蛋白、结核PPD试验、弓形虫抗体、巨细胞病毒抗体、风疹病毒抗体、弓形虫抗体)、自身免疫指标(ANA、抗-ds-DNA、ANCA、抗心磷脂组合、狼疮抗体)、遗传代谢病指标(血乳酸、血铜蓝蛋白)无异常;脑脊液检查(常规、生化、蛋白、感染相关指标)无异常;头部MR(2012年6月21日)见左侧大脑半球沟回加深、脑室扩张、大脑脚缩小、血管显影减少(见图1);脑电图提示左侧占优势的阵发性、短程高波幅尖慢、棘慢复合波(见图2)。具体病因不明,考虑为“先天性大脑半球发育障碍”,给予安定片可暂时减少肢体抖动发作,但对智能情况无明显改善。
2012年12月25日复查MR发现松果体区类圆形异常信号,边界清楚,增强扫描明显强化,考虑松果体区生殖细胞瘤。行放化疗后肿块完全消失,但放化疗后患儿近似于痴呆表现,生活不能自理,经数月康复治疗后恢复到放化疗前水平。然而,患儿的智能水平在随后数年中仍呈进行性下降趋势。
2014年1月,患儿癫痫发作频率增加,表现为频繁右上肢抖动、摸索动作、流涎,遂于2014年3月19日再次住院治疗。查体:意识清楚,情绪欣快,言语字数少,近、远期记忆力减退,计算力、理解能力差,MMSE评分12分,MoCA评分12分;右侧鼻唇沟浅;步态异常,行走时右膝关节弯曲差,右侧腕关节肌张力高,四肢肌力5级,右侧轻偏瘫试验阳性,右下肢膝反射、跟腱反射亢进,右侧Babinski(+),左侧正常。辅助检查:颅脑MR(2014年3月15日)提示松果体区未见肿块,左侧大脑半球进一步萎缩(见图1);长程视频脑电图监测到左侧占优多发痫样放电,同步视频可见有癫痫发作(见图2)。考虑“症状性癫痫 复杂部分性发作”,高度怀疑“Rasmussen脑炎”。给予奥卡西平、左乙拉西坦抗癫痫治疗。

A:MR(2012年6月21日)左侧额叶为主的皮支、壳核萎缩,右则大脑半球无异常;B:MR(2012年12月25日)松果体区类圆形异常信号,边界清梦,增强扫描明显强化;C、D:MR(2014年3月15日)左侧额、颞叶、壳核萎缩加重,半脑室扩张积水,松果体区无异常信号
图1 多次头部MR 提示左侧大脑半球进行性萎缩,并发现松果体区肿瘤,经放、化疗后肿瘤消失
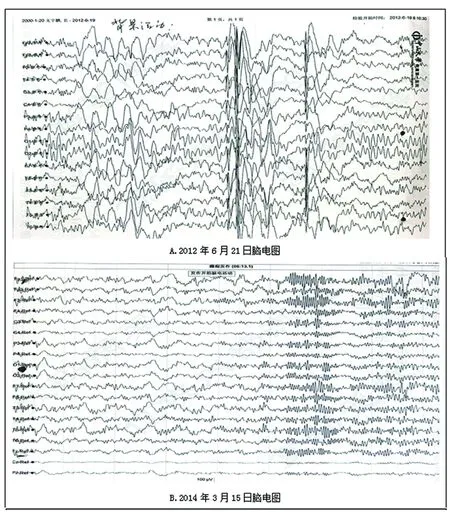
A:较多左侧占优势的阵发性、短程高波幅尖慢、棘慢复合波;B:不对称脑电活动,左侧占优,局灶慢活动,多发痫样放电
图2 EEG明显左侧占优势的异常脑电图波,痫样放电逐渐增多
2014年5月7日在静脉注射18F-FDG后行脑PET-CT断层显像,提示左侧大脑半球、脑干萎缩,左侧大脑半球、基底节弥漫性代谢减低(见图3)。在之后的随访过程中,多次PET检查和长程视频脑电图提示患儿左侧大脑半球进行性萎缩、代谢减低,反复癫痫发作、痫样放电。
目前患儿语言功能减退,少语,反应迟钝,记忆力、计算能力差,每日癫痫发作数次,均表现为右上肢抽搐,伴呼吸急促、面色发紫,“奥卡西平 300 mg TID、左乙拉西坦 0.5 g BID”治疗效果差。但家属始终拒绝行脑组织活检和手术治疗。
患儿以智能下降起病,并进行性加重,起病2 y后出现难治性部分发作性癫痫伴神经功能受损症状,多次EEG提示与临床症状相符的左侧大脑半球异常电活动,头部MR、PET-CT提示进行性弥漫性左侧大脑半球萎缩、代谢减低,在排除血管性、感染性、遗传代谢性等病因后被确诊为RE。

图3 可见PET-CT示左侧大脑半球弥漫性低代谢

表1 文献资料
MRI 磁共振成像(magnetic resonance image),EEG 脑电图(electroencephalography),PET 正发射断层显象术(positron emission tomography,PET)
2 讨 论
目前RE的诊断主要依据2005年Bien提出的诊断标准[8],包括A、B两个部分。A部分:(1)局灶性癫痫(有或无持续性局灶性癫痫);(2)脑电图示一侧大脑半球慢波伴或不伴癫痫样放电;(3)MRI示一侧大脑半球皮质萎缩伴至少下列之一:灰质或白质T2/FLAIR高信号,同侧尾状核头高信号或萎缩。B 部分:(1)持续性局灶性癫痫或进行性一侧皮质损害;(2)MRI示进行性一侧半球灶性萎缩;(3)组织病理学检查示脑组织T 细胞和小胶质细胞浸润(如果脑组织中出现较多的巨噬细胞、B 细胞性和浆细胞或病毒包涵体则可排除RE). 满足A部分3点或B部分2点即可诊断为RE。其中A部分用于诊断典型RE并不困难;而B部分则是考虑了部分非典型RE,并在无癫痫表现的情况下强调病理学诊断,但对于MRI证据却强调“进行性”,缺乏早期诊断的效能。Olsen等[9]对82例患者进行回顾性研究后证明上述诊断标准的敏感度可达到81%,但其4例假阴性结果中便有1例是因为缺乏癫痫症状。关于无癫痫或癫痫延迟的非典型RE,国内暂无专门报道,仅费凌霞等[3]在收集的9例患者中提到有2例缺乏癫痫症状的患儿(见表1)。而国外也仅有4篇报道[4~7],包括11个病例(见表1)。
本病例的独特之处主要包括两个方面:(1)RE特征性进行性单侧大脑半球萎缩,智能减退为首发,癫痫症状在2 y后出现;(2)RE病程中并发松果体肿瘤。对于无或迟发癫痫症状的非典型患者,RE的诊断很可能被忽视。而智能下降临床病因繁多,很难作为RE诊断的参考依据[1]。在缺乏组织病理学支持的情况下,这类患者很可能因诊断困难而延误治疗。在既往被报道过的非典型RE,癫痫可在起病0.5~2.5 y后出现,首发症状包括智能减退和单侧运动功能障碍[3~7]。非典型RE患者的病情进展情况与典型RE患者相同,甚至前者的脑萎缩进展率更高于后者[5],因此,早期诊断是有效治疗的必要条件。多次颅脑MR提示单侧大脑半球进行性萎缩即应高度怀疑为RE,但确诊仍有赖于脑组织活检[8]。而相较脑组织活检,非创伤性的检查更能得到患者及家属的理解。单侧弥漫性半球性低代谢改变是RE的特征性PET表现[10]。研究证明F-脱氧葡萄糖(F-FDG) PET显示的低代谢区域与MR、组织病理学提示的异常区域有一致性[10,11]。在部分MR阴性的病例中,PET检查也能发现脑部的异常改变[12]。相较MR,PET对于RE患者颅内变化更敏感,可作为早期诊断RE的依据。
据我们所知,这是第1例被报道的RE病程中并发松果体区生殖细胞瘤的病例。颅内生殖细胞瘤非常罕见,常位于松果体和蝶鞍上区域,发病高峰年龄为10~12岁[13],与本病例相符。既往病例报道了在干扰素γ受体-1缺陷患儿颅内发现有松果体区生殖细胞瘤[14]。而更多关于颅外生殖细胞瘤的病例报道提示该类疾病可能与免疫缺陷有关[15~17]。有意思的是,在本例患者身上的这两种疾病可能的发病机制是相互矛盾的。探索二者之间的关系可能需要在遗传和免疫方面的更进一步检查,而明确这一关系可能对探索这两种疾病的发病机制有一定意义。
目前已有的资料提示RE的发病机制跟大脑免疫反应有关[1]。炎症反应和神经元凋亡可引起癫痫的发生,而后者本身即可引起血脑屏障破坏、神经元凋亡继而加重脑组织损伤,形成恶性循环[6]。但其中具体的病理生理学过程尚不清楚。与以往癫痫首发的典型RE病例不同,本例癫痫症状延迟的病例提示RE的发生及神经受损症状可以在时间上与癫痫症状相独立,应当引起关于RE发病机制新的思考。

