黄芩素室温磷光传感器的构建及应用
郭艳霞,王媛媛,李淑娴,王文科*
(山西师范大学 生命科学学院,山西 临汾 041000)
黄芩是一种传统的中药材,可用于治疗温湿、暑湿、胸闷呕恶和胎动不安等症状[1],其主要成分为黄芩苷(Baicalin)和黄芩素(Baicalein,BAI)[2]。黄芩素在我国临床上主要用于抗炎[3]、抗病毒[4-5]和抗癌[6-9],药效远优于黄芩苷。目前用于BAI检测的方法有高效液相色谱法(HPLC)[10-13]、紫外分光光度法(UV-Vis)[14]和毛细管区带电泳-电化学检测法(CE-ED)[15]。上述方法准确高效,但存在预处理复杂、耗时长、检出限高的不足。所以建立高效、灵敏和操作简单的BAI的测定方法具有重要意义。
近年来,量子点[16-19](Quantum dots,QDs)的研究逐渐深入,可通过与一些物质进行特异性结合,实现对其表面的修饰和加工,从而形成掺杂型量子点[20],进而改变或增强量子点的原有性能。研究表明:室温磷光(Room-temperature phosphorscence,RTP)量子点具有发光寿命长、线性范围宽、能够避免体系背景荧光和散射光干扰的优点,是一种测定药物含量的新方法[21-22]。
目前,基于室温磷光法检测黄芩素的研究尚未见报道。本研究以水相共沉淀法合成了表面带有正电荷的聚乙烯亚胺(PEI)包覆的锰掺杂硫化锌量子点(PEI-Mn/ZnS QDs),基于该量子点可与黄芩素之间发生电子转移,从而使得PEI-Mn/ZnS QDs室温磷光猝灭的现象,建立了一种可在室温下灵敏、快速测定黄芩素含量的磷光方法。该方法为药品的含量标定和快速检测提供了新途径。
1 实验部分
1.1 仪器与试剂
JEM-2100透射电子显微镜(日本电子株式会社),Rigaku D/max-2500 X-射线衍射仪(日本Rigaku公司),Cary Eclipse荧光分光光度计(美国瓦里安公司),PHS-3C型pH酸度计(雷磁公司)。
高纯水(18.2 MΩ·cm)采用WaterPro水纯化系统(美国Labconco公司)制备;Zn(Ac)2·2H2O、Mn(Ac)2·4H2O、Na2S·9H2O(分析纯,天津科密欧化学试剂有限公司);BAI标准品(纯度>98.0%,合肥博美生物技术有限责任公司);聚乙烯亚胺(MW=1 800,纯度99.0%,广州翔博生物技术有限公司);黄芩饮片(北京同仁堂)和血清(服用黄芩水煎液的健康志愿者)。
1.2 实验方法
1.2.1PEI包覆的Mn掺杂ZnS量子点的合成量子点根据文献[23-24]方法略加改进合成:于100 mL三口烧瓶中,分别加入5 mL Zn(Ac)2·2H2O(1 mmol/L)、2 mL Mn(Ac)2·4H2O(0.04 mmol/L)和PEI(0.75 g)并溶于20 mL高纯水中。混匀后,用1 mol/L HCl调至pH 11.0,通氩气搅拌10 min后将溶液加热至80 ℃,回流30 min。迅速加入2.5 mL 0.4 mol/L的Na2S溶液,继续搅拌回流1 h后停止加热,待冷却至50 ℃后用1 mol/L HCl调至pH 8.0。将得到的PEI-Mn/ZnS QDs溶液于空气中50 ℃陈化2 h。溶液冷却至室温后,采用等体积的无水乙醇洗涤使量子点沉降,离心收集沉淀(洗涤、沉淀重复3次),真空干燥24 h即得预制备的PEI-Mn/ZnS QDs固体。图1分别为PEI-Mn/ZnS QDs对BAI的检测示意图、PEI-Mn/ZnS QDs及BAI的结构示意图。
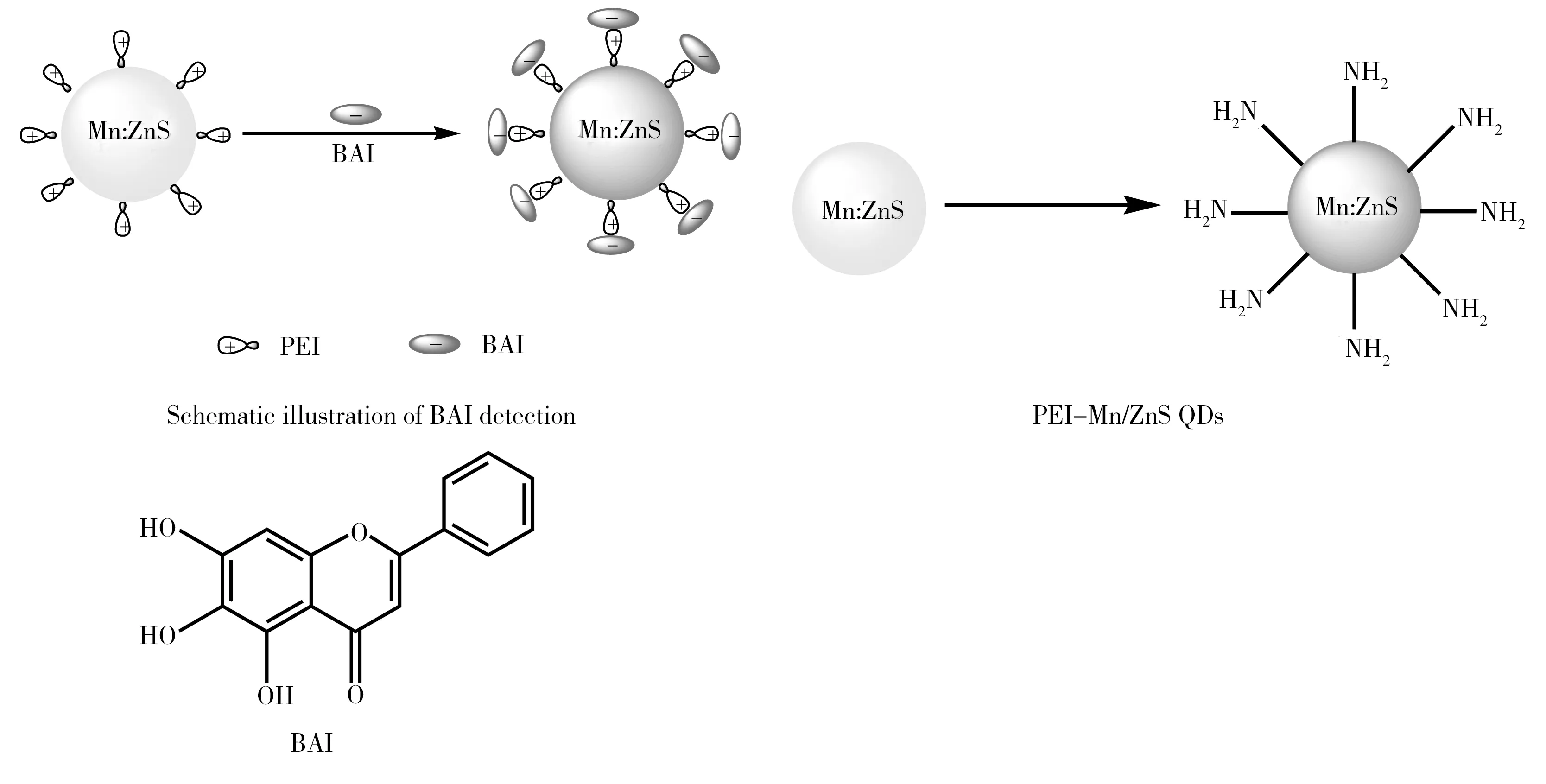
图1 BAI的检测示意图(A)、PEI-Mn/ZnS QDs(B)及黄芩素的结构示意图(C)Fig.1 Schematic illustration for BAI detection(A),structures of PEI-Mn/ZnS QDs(B) and BAI(C)
1.2.2测定方法在一系列10 mL比色管中,加入500 μL PBS缓冲液(0.2 mol/L,pH 8.0)、50 μL PEI-Mn/ZnS QDs溶液(1 mg·mL-1)和不同体积的BAI标准溶液,用高纯水定容至5 mL,摇匀,静置10 min后进行磷光分析(参数设置:选择磷光模式;激发波长为295 nm;波长扫描范围为500~700 nm;激发与发射波长的狭缝宽度均设为10 nm)。
1.2.3实际样品的处理黄芩素实际样品来自黄芩饮片,以60%的乙醇水溶液为萃取剂,将黄芩饮片于50 ℃萃取30 min即得黄芩素的检测液。将500 μL PBS缓冲液(0.2 mol/L,pH 8.0)、50 μL PEI-Mn/ZnS QDs溶液(1 mg·mL-1)、50 μL BAI检测液加入10 mL具塞比色管中,高纯水定容至5 mL,摇匀,室温下反应10 min后进行分析,参数同上。血清样品采自健康志愿者服用黄芩水煎液3 h后的血清,用高纯水稀释100倍,直接检测。
2 结果与讨论
2.1 PEI-Mn/ZnS QDs的表征
将PEI-Mn/ZnS QDs粉末分散于水中,超声30 min,取数滴样品分散于铜网上,充分干燥后采用JEM-2100透射电镜在200 kV高速电压下扫描,结果发现,量子点呈粒径3 ~5 nm的均一球形(图2A)。图2B为PEI-Mn/ZnS QDs的粒径分布图,可观察到PEI-Mn/ZnS QDs的分散效果良好,主要分布在4 nm附近。图2C为PEI-Mn/ZnS QDs粉末的X射线衍射光谱(XRD),(111)、(220)及(311) 3个晶面的衍射显示PEI-Mn/ZnS QDs具有典型的立方型闪锌矿结构,未观察到其他衍射峰,表明合成的量子点较为纯净。图2D为PEI-Mn/ZnS QDs的紫外光谱和磷光光谱。该量子点的激发峰和最大发射峰分别为295 nm和585 nm,与文献结果完全吻合[25],即蓝色发射带为Mn2+4T1-6A1跃迁产生。以上表征结果说明量子点已成功合成。
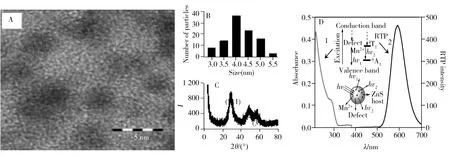
图2 PEI-Mn/ZnS QDs的TEM图(A)、粒径分布图(B)、XRD光谱(C)和紫外吸收光谱(曲线1)及磷光光谱图(曲线2)(D)Fig.2 TEM image(A),the size distribution histogram(B),XRD image(C) and UV absorption(curve 1) and phosphorescence(curve 2) spectra(D) of PEI-Mn/ZnS QDs
2.2 BAI检测条件的优化
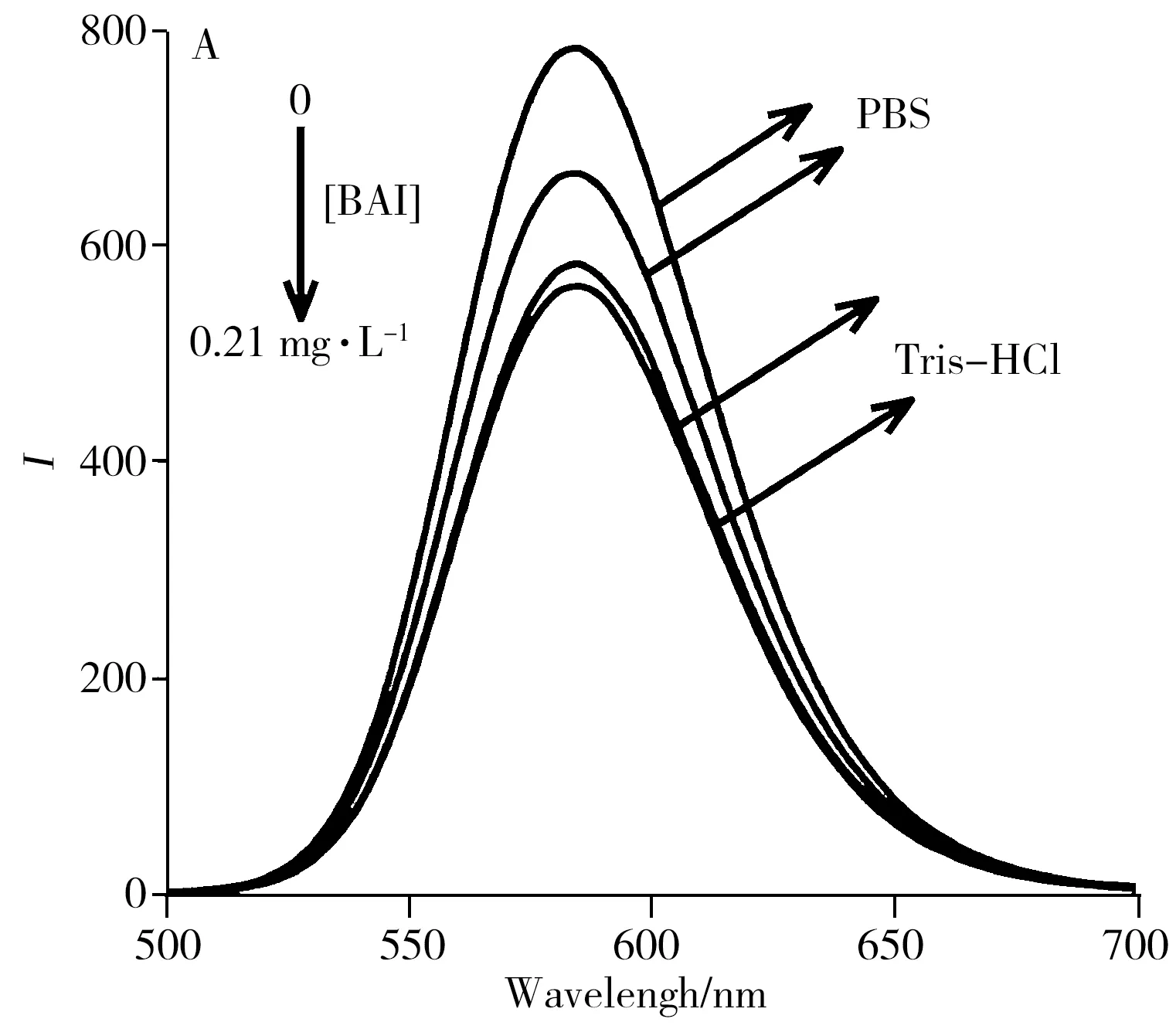
PEI-Mn/ZnS QDs的灵敏度和稳定性与缓冲液体系、缓冲液pH值、反应时间和盐浓度有关,因此对以上因素进行了优化。考察了浓度和pH值相同的Tris-HCl与PBS缓冲液对反应体系的影响(图3A),发现在Tris-HCl缓冲液中PEI-Mn/ZnS QDs的磷光强度弱于PBS缓冲液,且BAI猝灭量子点的磷光强度效果不灵敏。因此,实验选择PBS缓冲液为最佳介质。pH值对PEI-Mn/ZnS QDs的影响如图3B所示:PBS缓冲液的pH值为6.0~7.0时,量子点的RTP强度随着pH值的增大而增强,当pH值为7.0~8.5时,RTP强度较为平稳。由于黄芩素在碱性溶液中的溶解度较好,所以选择pH 8.0为最佳缓冲液pH值。实验还考察了反应时间对PEI-Mn/ZnS QDs稳定性的影响,结果显示,PEI-Mn/ZnS QDs在60 min内很稳定,为便于快速测定,选择反应时间为10 min。当PBS缓冲液的pH值为8.0,反应时间为10 min时,考察了PEI-Mn/ZnS QDs在不同NaCl浓度(0~0.1 mol/L)范围内的磷光强度。结果显示,在0~0.1 mol/L NaCl浓度范围内,PEI-Mn/ZnS QDs的磷光强度信号较稳定,所以在实际操作中无需考虑NaCl对反应体系的影响。
2.3 工作曲线与检出限
实验首先探究了BAI对 PEI-Mn/ZnS QDs磷光发射光谱的影响。图4A显示,PEI-Mn/ZnS QDs的RTP信号强度随BAI质量浓度的增加而减小,说明BAI猝灭了PEI-Mn/ZnS QDs的磷光。在最优检测条件下,PEI-Mn/ZnS QDs的磷光猝灭程度(P0/P)与BAI质量浓度在0.07~0.60 mg·L-1范围内呈良好的线性关系(图4A插图),标准曲线方程为P0/P=3.677 9CBAI(mg·L-1)+0.488 3,相关系数(r)为0.997。以11次平行测定的标准偏差的3倍除以标准曲线的斜率计算,得到检出限(3σ)为0.039 mg·L-1。对不含BAI和含有0.2 mg·L-1BAI的PBS缓冲液(0.2 mol/L,pH 8.0)+PEI-Mn/ZnS QDs(1 mg·mL-1)检测体系连续11次平行测定的相对标准偏差(RSD)为4.1%。图4B为PEI-Mn/ZnS QDs与BAI的共振光散射谱图,在未加BAI时,单独量子点的共振光散射较弱,随着BAI的加入,共振光散射强度随之增加。由于量子点最外层带有阳离子,BAI最外层带有阴离子,两者之间可通过静电引力的作用形成疏水性较强的化合物,在疏水作用与分子间作用力下,PEI-Mn/ZnS QDs与BAI聚集形成纳米复合物,致使体系的共振光散射显著增强。与已有方法相比,此方法灵敏度高、快速简单,对比结果见表1。
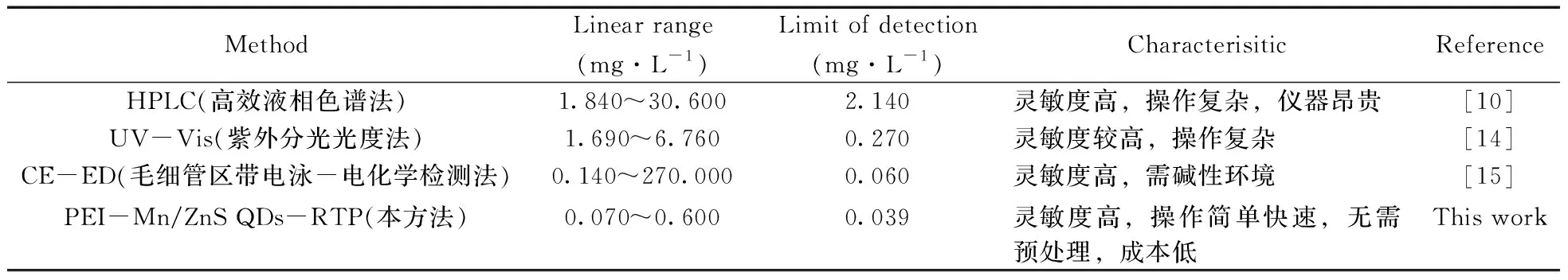
MethodLinear range(mg·L-1)Limit of detection(mg·L-1)CharacterisiticReferenceHPLC(高效液相色谱法)1.840~30.600 2.140灵敏度高,操作复杂,仪器昂贵[10]UV-Vis(紫外分光光度法)1.690~6.760 0.270灵敏度较高,操作复杂[14]CE-ED(毛细管区带电泳-电化学检测法)0.140~270.0000.060灵敏度高,需碱性环境[15]PEI-Mn/ZnS QDs-RTP(本方法)0.070~0.6000.039灵敏度高,操作简单快速,无需预处理,成本低This work
2.4 共存物质的影响
考察了常见离子和物质对PEI-Mn/ZnS QDs检测黄芩素含量的影响。检测了1 000倍的Mg2+,500倍的甘氨酸、Na+、K+,300倍的葡萄糖、蔗糖、L-脯氨酸,150倍的Ca2+、谷氨酸、精氨酸,50倍的草酸和10倍黄芩苷对0.5 mg ·L-1黄芩素测定的影响。结果表明:以上物质对PEI-Mn/ZnS QDs的室温磷光强度影响不大,相对误差均在5%以内。说明PEI-Mn/ZnS QDs可对BAI进行检测。
2.5 实际样品的测定
按“1.2.3”方法对黄芩饮片和血清进行处理后,进行2个浓度水平(1.00、2.00 mg·L-1)的加标回收实验。结果显示,黄芩饮片的加标回收率分别为97.2%和100.7%;血清的加标回收率分别为96.0%和98.0%。在相同实验条件下,对黄芩饮片和血清中黄芩素在24 h内每隔3 h测定1次,连续测定8次,日内RSD分别为2.8%和3.4%;将黄芩饮片和血清中黄芩素溶液密封室温保存7 d,每天测量1次,得日间RSD分别为3.3%和4.7%,说明该检测体系具有较好的精密度。
2.6 BAI与PEI-Mn/ZnS QDs的作用机制研究

图5 磷光猝灭的Stern-Volmer方程和Lineweaver-Burk双倒数函数曲线Fig.5 Stern-Volmer plot and Lineweaver-Burk plot of phosphorescence quenching
BAI可以猝灭磷光,表明PEI-Mn/ZnS QDs与BAI之间发生了相互作用。磷光猝灭过程分为动态猝灭和静态猝灭。动态猝灭过程遵循Stern-Volmer方程:P0/P=1+KSVCq;静态猝灭遵循Lineweaver-Burk双倒数函数曲线:1/(P0-P)=1/P0+KLB/(P0Cq)。式中,P0为磷光体的磷光强度;P为加入磷光猝灭剂后体系的磷光强度;Cq为猝灭剂浓度;KSV为Stern-Volmer常数;KLB为静态猝灭结合常数。图5为拟合的Stern-Volmer方程和Lineweaver-Burk双倒数函数曲线,P0/P与BAI的浓度呈明显的线性关系,符合Stern-Volmer方程,即猝灭机制为动态猝灭。
可以推测PEI-Mn/ZnS QDs与BAI的反应机理为:在溶液中,BAI为一种电子受体,带负电荷,而PEI-Mn/ZnS QDs带正电荷,BAI可通过静电作用与PEI-Mn/ZnS QDs产生电子转移,致使PEI-Mn/ZnS QDs的磷光猝灭(如图6)。

图6 PEI-Mn/ZnS QDs检测黄芩素的原理Fig.6 Principle of PEI-Mn/ZnS QDs for detection of BAI
3 结 论
本文基于BAI对PEI-Mn/ZnS QDs的室温磷光猝灭机制,建立了BAI浓度的检测方法,其检出限低至0.039 mg·L-1,线性范围为0.07~0.60 mg·L-1。基于量子点的RTP检测方法无需复杂预处理,且能够避免中药提取液以及生物自身体液背景荧光和散射光的干扰,该方法可用于中药材及生物体液中黄芩素含量的检测。

