基于荷移反应的高效液相色谱法测定氨基丁醇
邵梅琪, 陈 艳, 彭 青, 柳鹏福,2, 吴杰群,2, 储消和,2*
(1. 浙江工业大学绿色制药协同创新中心, 浙江 杭州 310014; 2. 浙江省长三角生物医药产业技术研究园, 浙江 德清 313200)
氨基丁醇,在有机合成和药物生产中有着广泛的用途,是抗结核药物盐酸乙胺丁醇青霉烯类抗生素的重要中间体[1],其中R-3-氨基丁醇更是抗艾滋新药不可缺少的手性源中间体[2]。
氨基丁醇没有紫外吸收,目前关于此类氨基醇类物质的检测方法主要有气相色谱法、HPLC-衍生化法、1H NMR和13C NMR等[3,4],如利用三氟乙酸酐衍生-气相色谱法以及HPLC-衍生化法检测氨基醇类的含量,但这些方法中衍生试剂的使用对色谱柱损伤较大[5,6];利用1H NMR、13C NMR和IR测定β-氨基醇的结构和含量,对检测设备要求较高[7]。因此建立一种采用常规试剂和常用检测设备(如高效液相色谱-紫外检测器)测定氨基丁醇含量的方法具有重要意义。
自1952年Mulliken提出电荷传递理论(charge transfer theory)以来[8],荷移反应引起了广大科研人员的研究探索。荷移反应是基于电子供体和电子受体间的电荷转移从而形成荷移络合物的一种反应,其络合物往往具有颜色。利用荷移反应,可以调节药物水溶性,增强药物稳定性[9]。在检测方面,由于荷移络合物的形成能使吸收光谱发生较大幅度的红移,并且在紫外或可见光区域具有较大的特定吸收峰,所以利用这个特性可以避开其他物质的干扰,提高检测方法的选择性[10]。
荷移反应一般利用待测物质作为电子供体,荷移试剂作为电子受体,如利用荷移-分光光度法来检测马来酸曲美布汀、卡维地洛、左氧氟沙星等含量[11,12];利用荷移-液相色谱法准确快速测定硫酸西索米星以及硫酸胍基丁胺等无紫外吸收的物质[13]。
目前用荷移-液相色谱测定氨基丁醇含量的方法尚未见报道。氨基丁醇上氮原子存在孤对电子,能与缺电子的荷移试剂四氯苯醌(TCBQ)发生荷移络合,本文研究了氨基丁醇和四氯苯醌的荷移反应,确定了检测氨基丁醇的反应条件以及色谱条件,建立了高效液相色谱法-紫外检测器检测氨基丁醇含量的方法。该法简便快捷,试剂稳定,且重复性好,适用于氨基丁醇含量的快速检测。
1 实验部分
1.1 仪器、试剂与材料
LC-2030C高效液相色谱仪(日本岛津公司); UV2800紫外可见分光光度计(中国上海舜宇恒平科学仪器有限公司); Mutiskan go DQ083酶标仪(美国Thermo公司); ME54精密分析天平(梅特勒-托利多仪器上海有限公司)。
氨基丁醇(分析纯,阿拉丁试剂上海有限公司);甲醇(色谱纯,美国Tedia公司);四氯苯醌、四硼酸钠、硼酸和三乙胺(分析纯,国药集团化学试剂有限公司)。
1.2 溶液的配制
精密称取氨基丁醇0.1 g,置于100 mL容量瓶中,用蒸馏水稀释至刻度,配制质量浓度为1 g/L的氨基丁醇标准溶液。精密称取四氯苯醌0.049 2 g,置于100 mL容量瓶中,用无水乙醇稀释至刻度,配制浓度为0.002 mol/L的四氯苯醌溶液。
称取硼砂1.907 g,加水至100 mL,配制成0.05 mol/L的硼砂溶液;称取硼酸1.237 g,加水至100 mL,配制成0.2 mol/L的硼酸溶液。以体积比45∶55将硼砂溶液和硼酸溶液混合,配制成pH 8.4的硼酸-硼砂缓冲液。
1.3 荷移反应条件
量取氨基丁醇标准溶液1 mL、四氯苯醌溶液5 mL和pH 8.4硼酸-硼砂缓冲液1 mL,置于10 mL具塞试管内,加水至刻度,于60 ℃水浴中反应60 min,用水冷却至室温,于350 nm处检测吸光度值。
1.4 分析条件
色谱柱:Agilent Extend C18色谱柱(250 mm×4.6 mm, 5 μm);柱温:25 ℃;流动相:A为0.001%(体积分数)三乙胺水溶液,B为甲醇;流速:0.8 mL/min。梯度洗脱程序:0~4 min, 5%B; 4~6 min, 5%B~50%B; 6~11 min, 50%B~5%B; 11~20 min, 5%B。进样体积:10 μL。
2 结果与讨论
2.1 络合物组成和反应机理
分光光度法可以用来测定络合物组成,且测定方法简便有效[14]。本实验采用等摩尔连续变化法测定络合物组成及表观稳定常数。固定氨基丁醇和四氯苯醌物质的量之和不变,连续改变二者物质的量之比,进行络合反应[15]。结果表明,氨基丁醇和四氯苯醌的配位比为1∶1,稳定常数(K)为3.75×104。
氨基丁醇分子中有一个N原子,具有一对孤对电子,可以作为n-电子供体,四氯苯醌作为π-电子受体,两者可形成n-π型络合物,根据两者的配位比推测氨基丁醇和四氯苯醌的荷移络合物的形成机理,具体见图1。
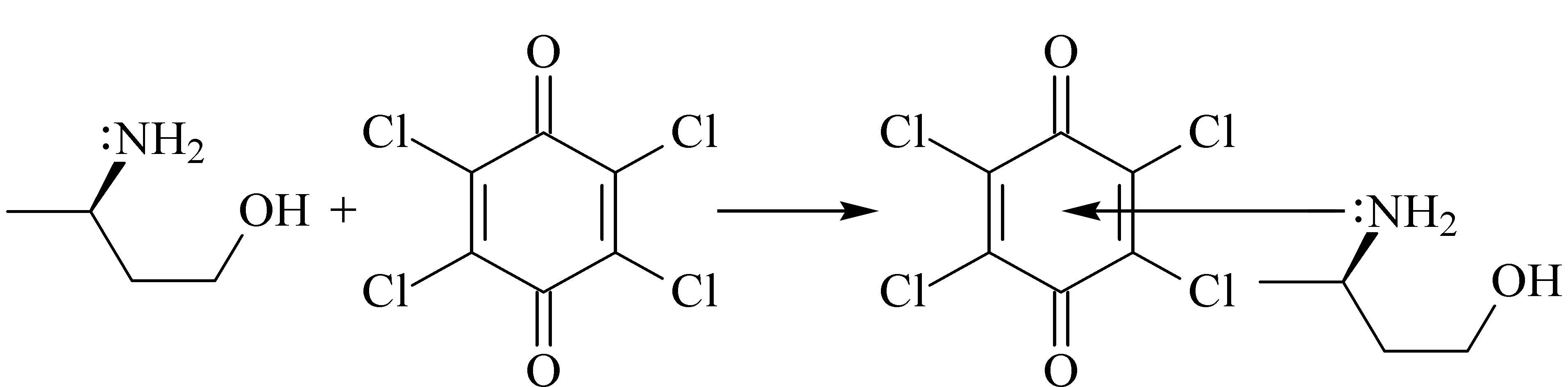
图 1 氨基丁醇和四氯苯醌的荷移反应机理Fig. 1 Charge transfer mechanism of aminobutanol and tetra-chloro-benzoquinone (TCBQ)
2.2 荷移反应条件的优化
2.2.1检测波长的选择
为确认氨基丁醇与四氯苯醌荷移络合物特定吸收峰的波长,本文按1.3节方法配制标准溶液并进行荷移反应,以氨基丁醇和四氯苯醌标准溶液为参比,绘制吸收光谱图(见图2)。结果发现,氨基丁醇在190~400 nm范围内无紫外吸收,四氯苯醌在215 nm和290 nm处有2个吸收峰,两者形成的络合物在215 nm和350 nm处有2个吸收峰,络合物的吸收光谱发生了红移。因此本文选择350 nm作为检测波长。
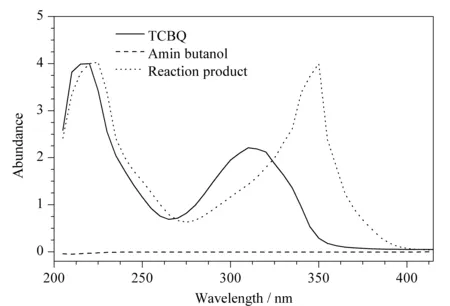
图 2 氨基丁醇、四氯苯醌和反应产物的紫外光谱图Fig. 2 Ultraviolet spectra of aminobutanol, tetra-chloro- benzoquinone and reaction product
2.2.2反应介质选择
为考察反应介质对荷移反应的影响,本文选择水、甲醇、乙醇、丙酮和乙腈5种反应介质进行试验。结果表明,氨基丁醇和四氯苯醌在丙酮和乙腈中反应时会产生浑浊现象,在水、甲醇和乙醇等介质中反应时,反应液澄清透明,吸光度值分别为0.225、0.209和0.227,相差不大。因此根据实用性和简便性,本实验在水中进行反应。
2.2.3缓冲液pH值的选择
为考察反应体系的pH值对荷移反应的影响,本文通过加入pH 4.0、5.0、6.0、6.6、7.0、7.4的磷酸氢二钠-柠檬酸缓冲液,7.8、8.0、8.4、8.7、9.0的硼砂-硼酸缓冲液和9.5、9.9、10.3、10.8的碳酸钠-碳酸氢钠缓冲液进行试验(见图3a)。氨基丁醇和四氯苯醌在酸性条件下基本不发生反应;在中性和碱性条件下,两者发生荷移络合反应。反应在pH 8.0~9.5范围内灵敏度较高,当pH>9.5时,络合物吸光度值随pH值的增大而下降。综合考虑,选用pH 8.4的硼砂-硼酸缓冲液进行反应。
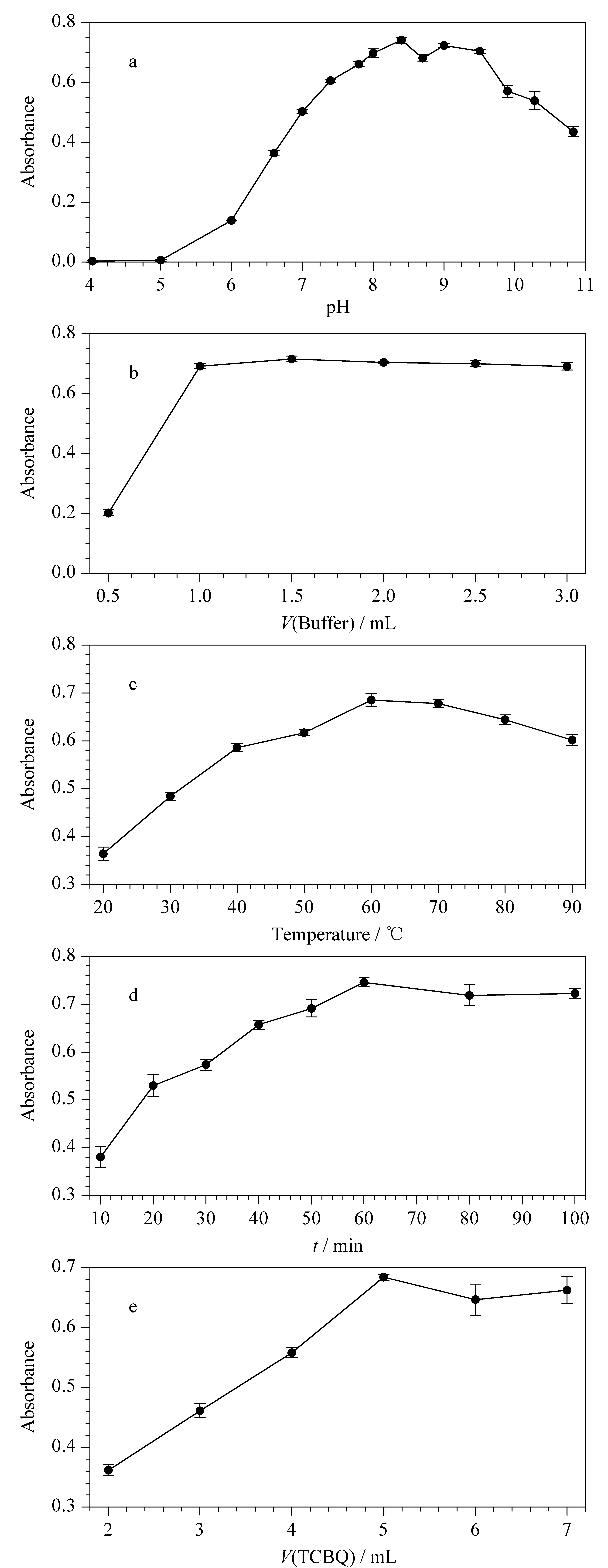
图 3 (a)缓冲液pH值、(b)缓冲液用量、(c)反应温度、(d)反应 时间和(e)TCBQ用量对反应产物吸光度值的影响(n=3)Fig. 3 Effect of (a) pH value of buffer, (b) the amount of buffer, (c) reaction temperature, (d) reaction time and (e) the amount of TCBQ on the absorbance of the reaction product (n=3)
2.2.4缓冲液用量的选择
为考察缓冲液用量对荷移反应的影响,分别加入pH 8.4的硼砂-硼酸缓冲液0.5、1、1.5、2.0、2.5和3.0 mL,按1.4节描述进行试验。结果表明,当缓冲液用量大于1 mL时,其用量对实验结果几乎无影响(见图3b)。因此本实验最终采用硼砂-硼酸缓冲液1 mL。
2.2.5反应温度和时间的选择
本文考察了反应温度(20、30、40、50、60、70、80和90 ℃)对荷移反应的影响(见图3c)。当反应温度为60 ℃时,氨基丁醇和四氯苯醌的反应已基本完全;反应温度大于80 ℃时,反应产物的吸光度值有所降低。因此反应温度选择60 ℃。
在60 ℃反应温度下分别反应10、20、30、40、50、60、80、100 min,进行反应时间的考察(见图3d)。当反应时间大于60 min时,氨基丁醇与四氯苯醌反应完全。因此选择的反应时间为60 min。
2.2.6荷移试剂用量的选择
为考察荷移试剂用量对反应的影响,在1.4节描述的实验体系中分别加入0.002 mol/L四氯苯醌2、3、4、5、6和7 mL进行试验(见图3e)。结果表明,在用量2~5 mL时,荷移络合物的吸光度值随四氯苯醌用量的增大而增大;当用量大于5 mL时,吸光度值基本不变。因此,本实验选择0.002 mol/L的四氯苯醌5 mL作为荷移试剂用量。
2.3 色谱条件的优化
氨基丁醇本身无紫外吸收,与荷移试剂TCBQ反应络合后形成的络合产物在350 nm处有吸收峰,可用于高效液相色谱检测。本实验选择Agilent Extend C18色谱柱(250 mm×4.6 mm, 5 μm)进行分离,该色谱柱pH适用范围宽(2.0~11.5),适用于大多数化合物的分析。色谱条件的选择必须考虑以下要求:分离度(R)>1.5;理论塔板数不低于2 000;含量测定的RSD≤2% ;峰形窄而尖;分离时间短。
2.3.1流动相的选择
本文通过参考相关文献[13],选择以甲醇和水作为流动相,并通过优化梯度洗脱程序,使荷移络合物的色谱峰峰形较好且与空白溶剂分开。但荷移络合物的峰形有一定拖尾现象,因此在水相中加入不同体积分数(0.001% 、0.005% 、0.010% 、0.015%和0.020% )的三乙胺,比较出峰情况。综合考虑分离度、拖尾因子、理论塔板数以及色谱柱损耗等因素,最后选择三乙胺的体积分数为0.001% 。
2.3.2流速和柱温的选择
在上述条件下改变流动相的流速(0.4、0.6、0.8、1.0和1.2 mL/min)以及柱温(15、20、25、30和35 ℃),考察其对峰形的影响。根据分离度和峰形,本文选择流速为1.0 mL/min,柱温为25 ℃。
在最优色谱条件下,对氨基丁酸标准溶液荷移反应后的产物进行分析,其色谱图见图4
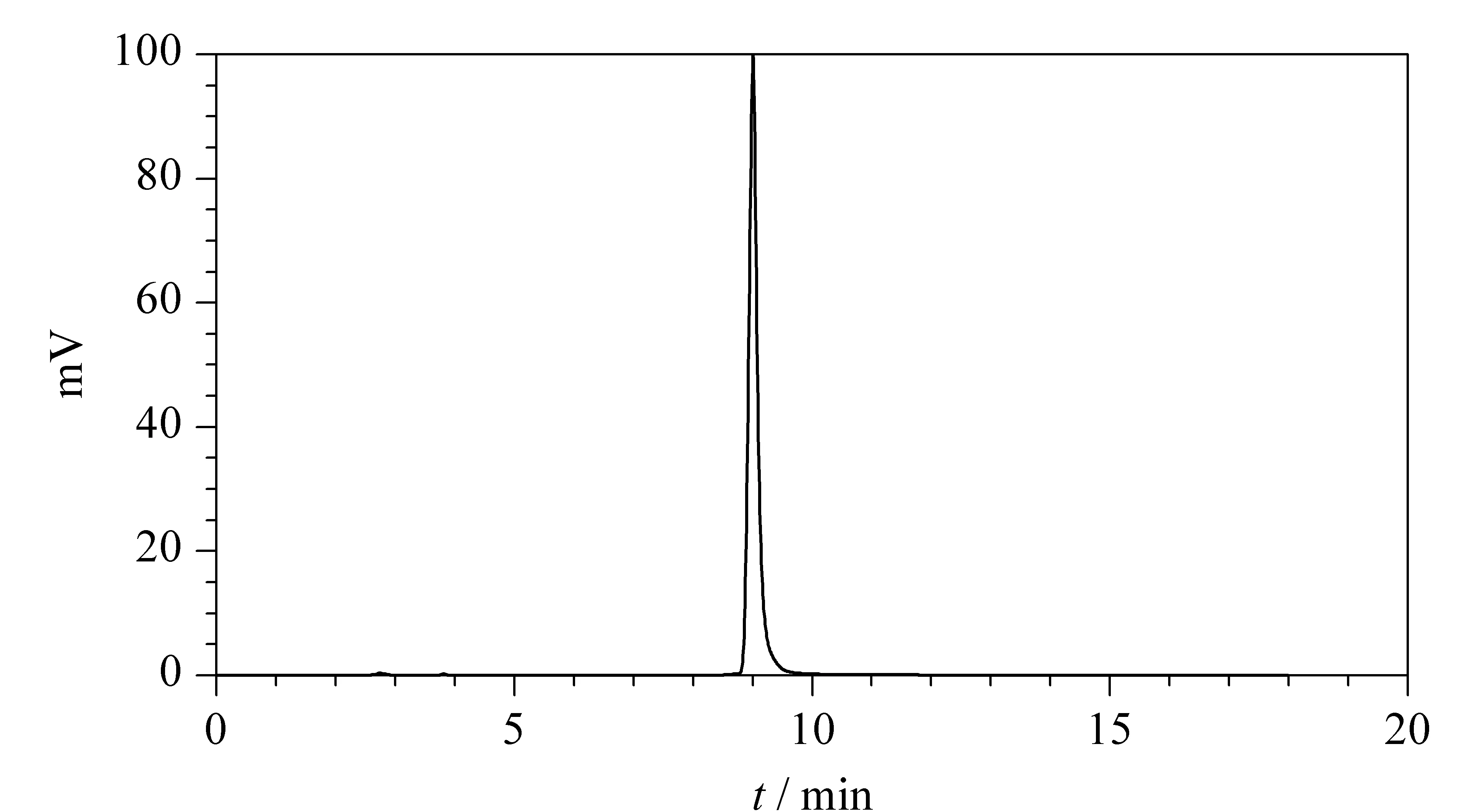
图 4 氨基丁醇标准溶液荷移反应后反应产物的色谱图Fig. 4 Chromatogram of the reaction product after charge transfer reaction of aminobutanol standard solution
2.4 方法学考察
2.4.1标准曲线
配制0.1、0.2、0.4、0.5和0.6 g/L的系列氨基丁醇标准溶液,在1.3节条件下进行荷移反应,在1.4节条件下进行检测。结果表明,氨基丁醇的峰面积(Y)与对应的质量浓度(X, g/L)在0.1~0.6 g/L范围内呈良好的线性关系,线性方程为Y=8.870×106X+1.463×106,相关系数(R2)为0.999 4。按信噪比3∶1和10∶1确定方法的检出限和定量限,分别为0.003 g/L和0.010 g/L。
2.4.2回收率和精密度
在0.2 g/L的氨基丁醇样品中分别加入3个水平(0.2、0.25和0.35 g/L)的氨基丁醇标准溶液进行加标回收试验,每个添加水平做6个平行样品,验证方法的重复性。结果表明,氨基丁醇的加标回收率为98.3% ~103.6% , RSD为0.9% ~1.6% (见表1),证明该方法重复性好,数据准确可靠。
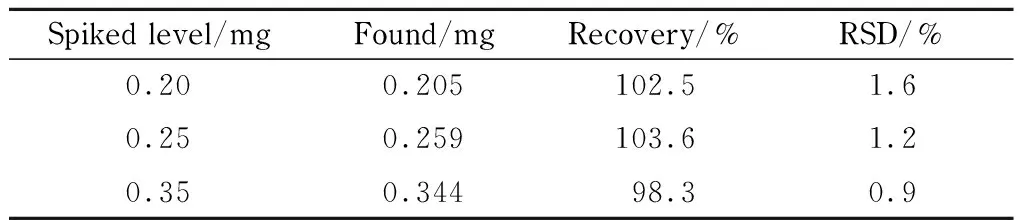
表 1 氨基丁醇的加标回收率和精密度(n=6)Table 1 Recoveries and precisions of aminobutanol (n=6)
Background: 0.2 g/L.
2.4.3稳定性
氨基丁酸标准溶液和TCBQ在1.3节条件下进行反应后,分别放置0、1、2、3、4和5 h,测定荷移络合物的吸光度值,其结果的相对标准偏差为0.83%(n=5)。证明氨基丁醇和四氯苯醌的荷移络合物稳定性良好。
2.4.4实际样品测定
采用本文描述的方法分析氨基丁醇样品,将其与四氯苯醌进行荷移反应,最后通过高效液相色谱进行含量检测。结果表明,氨基丁醇的含量为6.084 g/L,其色谱谱图见图5。

图 5 实际样品荷移反应后反应产物的色谱图Fig. 5 Chromatogram of the reaction product after charge transfer reaction of the real sample
3 结论
本研究建立了一种利用荷移反应和高效液相色谱-紫外检测器快速检测氨基丁醇的方法。该方法只需常规的紫外检测器就可实现氨基丁醇的含量分析,具有操作简便、分析快速准确、稳定性好等特点,满足日常检测要求,适用于氨基丁醇含量的快速定性定量检测。该方法可进一步开发测定其他无紫外吸收脂肪族氨基醇类的含量。
- 色谱的其它文章
- 全二维气相色谱-质谱分析煤油基吸热型碳氢燃料烃族组成
- QuEChERS-超高效液相色谱-串联质谱法测定不同植被类型土壤中11种甲氧基丙烯酸酯类杀菌剂
- 离子液体分散液液微萃取-超高效液相色谱-串联质谱法测定食品接触材料中全氟辛酸和全氟辛烷磺酸的迁移量
- 超高效液相色谱-串联质谱法快速测定鸡蛋中氟虫腈及其代谢物残留
- 固相萃取-高效液相色谱-串联质谱法同时测定牛奶和羊奶中莫奈太尔及其代谢产物残留
- Determination of 11 synthetic musks in imported seafood by solid phase extraction and gas chromatography-mass spectrometry

