胃癌患者微创全胃切除的手术效果研究
冯志刚,杨雨民
(内蒙古民族大学附属医院 普外科,内蒙古 通辽 028000)
胃癌是临床常见的消化道癌,近年来随着人们生活方式的变化和生活水平的提高,其发病率和病死率逐年升高,已经对我国人民生命健康产生了严重威胁[1-2]。临床外科中主要通过根治性全胃切除术对胃癌患者进行治疗,胃癌根治手术也从传统手术进展到腹腔镜辅助根治性全胃切除术,近年来又出现了完全腹腔镜根治性全胃切除术,手术方式、细节和入路方式均发生较大变化[3]。完全腹腔镜和腹腔镜辅助根治性全胃切除术在区域淋巴结清扫和病灶切除方面无显著差异,但在消化道重建方面存在差异[4]。已有研究指出[5]完全腹腔镜根治性全胃切除术的临床疗效能够达到与开腹手术相同的根治效果,也有研究指出患者术后生活质量较差。因此,本研究对完全腹腔镜和腹腔镜辅助根治性全胃切除术的手术效果进行了比较,以期能为后期临床治疗提供参考。现报道如下:
1 资料与方法
1.1 一般资料
选取2015年1月-2018年1月我院收治的132例腹腔镜根治性全胃切除术胃癌患者为研究对象,依据1∶1比例将患者随机分为对照组(n=66)和观察组(n=66),本研究已通过医院伦理委员会的批准。观察组中,男43例,女23例,年龄18~87岁,平均(54.39±9.20)岁,体质指数(body mass index,BMI)为(23.19±3.22)kg/m2,肿瘤最大直径为(3.91±1.72)cm。对照组中,男47例,女19例,年龄19~88岁,平均(55.23±9.41)岁,BMI为(22.97±3.04)kg/m2,肿瘤最大直径为(4.05±1.88)cm。两组患者的一般资料比较差异无统计学意义(P>0.05),具有可比性。
纳入标准:①经临床诊断为胃癌的患者;②年龄≥18周岁的患者;③符合腹腔镜手术指征的患者;④无其他脏器和远处转移的患者;⑤凝血功能正常的患者;⑥自愿参加本项研究并已经签署知情同意书的患者。
排除标准:①姑息性手术治疗患者;②合并心、肝、肾、肺功能障碍而无法耐受手术的患者;③合并急慢性疾病或免疫系统疾病的患者;④严重的精神疾病或认知障碍患者。
1.2 方法
观察组患者给予完全腹腔镜根治性全胃切除术治疗,对照组患者给予腹腔镜辅助根治性全胃切除术治疗。
1.2.1 腹腔镜辅助根治性全胃切除术 患者采取仰卧位,采用气管插管全身麻醉。在脐孔上做一10 mm小口穿刺10 mm Trocar,建立二氧化碳CO2人工气腹,确保压力为12~14 mmHg,左侧和右侧腹部做1 cm切口置入腹腔镜器械,主操作孔为左锁骨中线肋下2 cm处,由此置入腹腔镜并对腹腔情况进行全面探查,确定病灶的位置、大小及周围情况等。沿横结肠使用超声大游离大网膜至十二指肠球部,由左至脾下级,对N4组淋巴结进行清扫。将结肠系膜前叶和胰包膜掀起,上提胃大弯,横断胃短血管,并对胃大弯侧进行充分游离。解剖胃结肠静脉干,使用钛夹夹闭并离断静脉,对根部N6组淋巴结进行清扫。解剖胃网膜右动脉,使用钛夹夹闭并横断右动脉,解剖胃十二指肠动脉、肝总动脉和肝固有动脉,对N8和N5组淋巴结进行清扫。使用钛夹夹闭并切断胃右血管,顺着肝总动脉向左清扫N7和N9组淋巴结,使用钛夹夹闭并离断胃左血管。下拉胃,沿左肝向下打开肝胃韧带,进入小网膜囊后对肝十二指肠韧带进行游离,对N12组淋巴结进行清扫。沿着胃小弯侧对胃周网膜组织进行清扫,对N1和N3组淋巴结进行清扫。在上腹正中位置做一个5 cm切口,置入切口保护器将胃提出切口外以完成食管空肠吻合,重建消化道,留置引流管,缝合切口。
1.2.2 完全腹腔镜根治性全胃切除术 患者采取仰卧位,采用气管插管全身麻醉。脐孔下方约1 cm处做一个1 cm的切口,建立CO2人工气腹,确保压力为12~14 mmHg,使用套管针(直径为10 mm)进行穿刺,置入腹腔镜并对腹腔情况进行全面探查,确定病灶的位置、大小及周围情况等。在右腋和左腋前线肋缘下2 cm位置分别置入1个套管针(直径为5 mm)作牵引孔,在左侧腹直肌外缘脐上2 cm水平线位置置入1个套管针(直径为5 mm)作为牵引孔,右侧对称位置置入1个12 mm套管针作为主操作孔。提起大网膜并使用超声刀切除结肠大网膜,剥离结肠系膜前叶,将肠系膜上静脉充分暴露,进行淋巴结清扫。将双侧胃网膜血管切断,然后切除病灶,取出标本放入保护袋内送检。使用直线切割吻合器将空肠离断,在食管残端左侧做一个切口行空肠吻合,重建消化道,留置引流管,缝合切口。
1.3 观察指标
记录并比较两组患者术中情况、术后情况和并发症发生情况。①术中情况:包括切口长度、近端切缘、远端切缘、食管空肠吻合时间、淋巴结清扫数目、术中出血量、总手术时间和网膜切除程度;②术后情况:包括镇痛时间、肛门首次排气时间、首次进食流质食物、首次进食半流质食物、引流管拔除时间和住院时间;③并发症:包括吻合口漏、吻合口狭窄、吻合口漏出血、腹腔出血、切口感染、肠梗阻、肺部感染、恶心/呕吐。
1.4 统计学方法
采用SPSS 20.0软件包进行统计学分析,计量资料用均数±标准差(±s)表示,采用t检验,计数资料采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组术中情况比较
观察组患者的切口长度短于对照组患者,远端切缘、食管空肠吻合时间和总手术时间长于对照组患者,差异有统计学意义(P<0.05)。见表1。
2.2 两组术后情况比较
观察组患者术后镇痛时间短于对照组患者,差异有统计学意义(P<0.05)。两组患者的肛门首次排气时间、首次进食流质食物、首次进食半流质食物、引流管拔除时间和住院时间比较差异无统计学意义(P>0.05)。见表 2。
2.3 两组并发症情况比较
观察组和对照组患者的并发症总发生率分别为21.19%和28.76%,观察组明显低于对照组,差异有统计学意义(P<0.05)。见表 3。
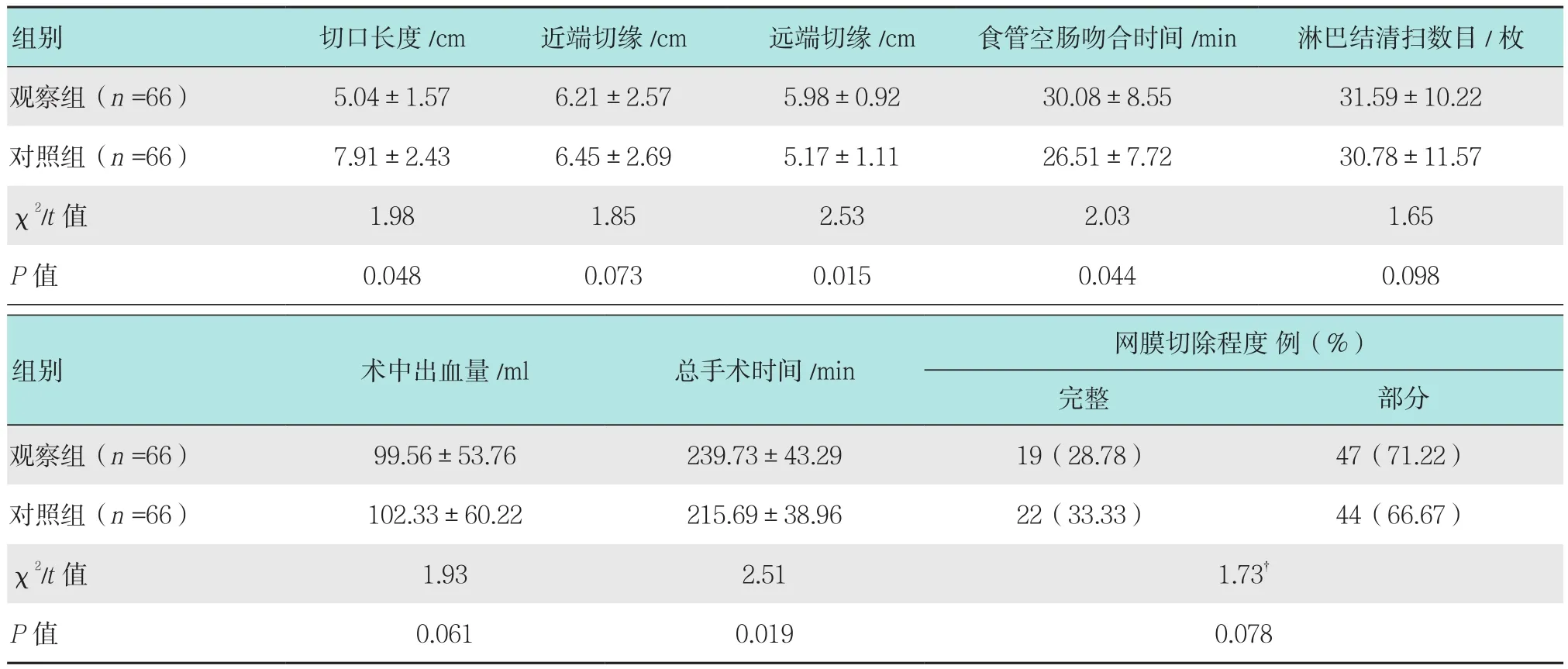
表1 两组术中情况比较Table 1 Comparison of intraoperative situation between the two groups
表2 两组术后情况比较 (d,±s)Table 2 Comparison of postoperative situation between the two groups (d,±s)
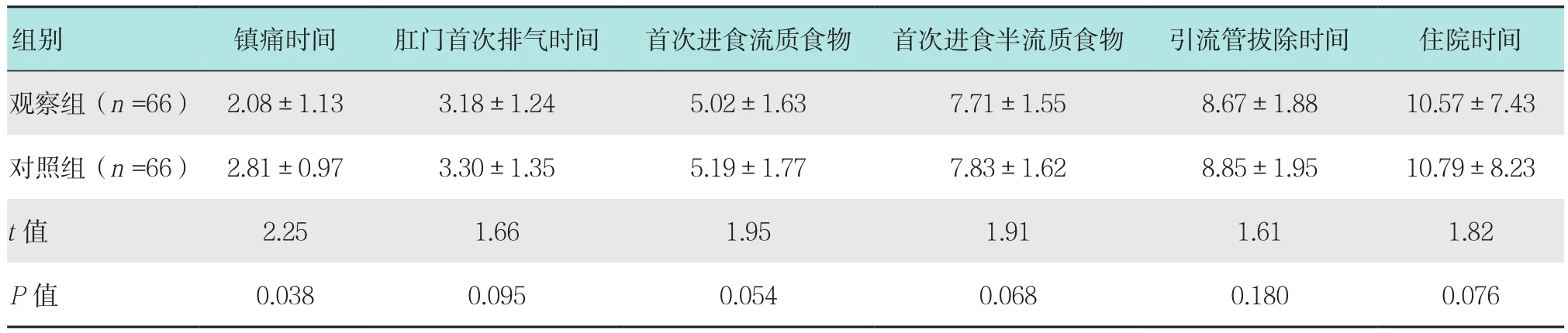
表2 两组术后情况比较 (d,±s)Table 2 Comparison of postoperative situation between the two groups (d,±s)
组别 镇痛时间 肛门首次排气时间 首次进食流质食物 首次进食半流质食物 引流管拔除时间 住院时间观察组(n =66) 2.08±1.13 3.18±1.24 5.02±1.63 7.71±1.55 8.67±1.88 10.57±7.43对照组(n =66) 2.81±0.97 3.30±1.35 5.19±1.77 7.83±1.62 8.85±1.95 10.79±8.23 t值 2.25 1.66 1.95 1.91 1.61 1.82 P值 0.038 0.095 0.054 0.068 0.180 0.076
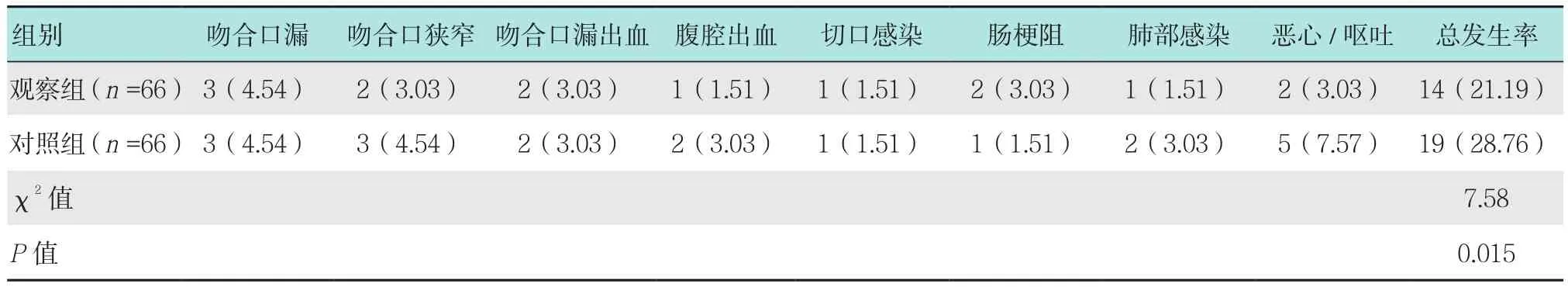
表3 两组并发症情况比较 例(%)Table 3 Comparison of complications between the two groups n(%)
3 讨论
腹腔镜根治性全胃切除术已逐渐成为临床中治疗胃癌的常规手术方式,传统的腹腔镜辅助根治性全胃切除术完成胃周血管离断后在剑突下取切口行直视下消化道重建,而近年来出现的完全腹腔镜根治性全胃切除术在腹腔镜下完成消化道重建,然后将切除的标本在脐部切口取出,操作简单,术中牵拉少,避免了术中过度牵拉残胃和食管等组织而带来的二次损伤时,更具备无瘤优势[6-7]。但完全腹腔镜根治性全胃切除术开展较晚,这要求手术医师需要具备娴熟的腹腔镜吻合技术。因此,为了提高手术安全性,降低风险,多数医疗中心还未将其作为治疗胃癌的首选方法[8]。本研究对两种微创全胃切除手术的手术效果进行了比较,以期能为后期临床治疗提供参考。
腹腔镜辅助食管空肠吻合术中消化道重建在腹上区正中切口直视下完成,被认为快速有效,而完全腹腔镜食管空肠吻合术是在全腹腔镜下完成,被认为耗时且困难[9]。本文研究结果显示,观察组患者的切口长度短于对照组患者,远端切缘、食管空肠吻合时间和总手术时间长于对照组患者,差异有统计学意义(P<0.05)。这是由于随着生活水平的提高,患者中多发肥胖患者,对于肥胖患者来说其切口皮下脂肪层较厚,胸廓前后径较大,行腹腔镜辅助食管空肠吻合术则难度较大,术野显露不清,操作视野相对较深,圆形吻合器钉砧座置入难度较大,进而延长了吻合时间[10]。而完全腹腔镜下食管空肠吻合术难度并未有显著影响,且完全腹腔镜下手术由扩大观察孔绕脐取出切除标本,切口美观隐蔽,符合微创理念,因而较对照组患者来说,观察组患者的手术情况更具优势[11]。同时完全腹腔镜下根治性全胃切除术中对患者所做辅助切口较小,由切口创伤而导致的疼痛较轻,缩短了患者术后镇痛时间[12]。其次,本文研究结果显示,观察组和对照组患者的并发症总发生率分别为21.19%和28.76%,差异有统计学意义(P<0.05)。这可能是由于观察组患者所做辅助切口较小,患者应激反应影响小,也能够有效减少切口感染的发生率。同时在全腹腔镜下完成食管空肠吻合,视野清晰,解剖暴露实现骨骼化,无需将胃提出切口外以完成食管空肠吻合,极大地降低了腹腔出血和腹腔感染的发生率。因此,观察组患者的术后并发症发生率较低,安全性较佳[13]。同时全腹腔镜下操作,避免了因手术视野暴露不佳和吻合口牵拉过度而造成的吻合口撕裂出血,手术视野更清晰,能够有效进行近端空肠定位和肠系膜方向判断等,手术效果较好[14]。
综上所述,完全腹腔镜根治性全胃切除术较腹腔镜辅助根治性全胃切除术治疗胃癌患者术后疼痛时间短,并发症发生率低,但食管空肠吻合时间略长,造成总手术时间延长。

