维持性血液透析中血压变异性的相关探讨
兰秀君,吴道全,2
(1.西南医科大学附属医院,四川 泸州 646000; 2.内江市第二人民医院肾内科,四川 内江 641100)
维持性血液透析(maintenance hemodialysis,MHD)治疗是延长终末期肾病(end stage renal disease,ESRD)患者生命的主要治疗方法之一,虽然血液净化技术快速发展,使ESRD患者的生存时间及质量逐年改善,但MHD患者的病死率仍较高,尤其是心血管病病死率较普通人群高10倍[1]。这种死亡风险增高与心血管危险因素密切相关,其中包括血压变化,如透前收缩压低下或者显著升高以及透析时发生低血压[2]。已有研究证明,在非透析人群中血压变异性(blood pressure variability,BPV)是心血管事件、卒中、左心室肥厚的危险因素[3]。而在MHD患者中,BPV亦是重要的心血管危险因素之一。BPV,以24h BPV为研究对象的最为常见。多项研究表明,长期BPV(多以透析前血压为主)都与心血管病发病率和病死率等不良预后有关[4,2-3],就透析过程中血压变异性研究较少。进一步的研究充实这些研究是必要的。本研究通过对143例MHD患者3年透析过程中BPV与各临床资料进行回顾性分析,进而研究血液透析中BPV及其影响因素,并探讨其与病死率的相关性。
1 资料与方法
1.1 临床资料 收集西南医科大学附属医院2014年1月至2016年12月进行维持性血液透析的患者,入选条件:(1)年龄≥18岁的慢性肾衰竭患者;(2)维持性血液透析时间≥3个月,每周2~3次,每次透析时间>3 h。(3)近期无心肌梗死、脑出血等严重疾病。排除条件:(1)双上肢无法测量肱动脉血压者,包括双侧均有内瘘者及严重肱动脉血管畸形者;(2)精神障碍等无法配合测量血压者;(3)行腹膜透析或肾移植者;(4)原发性高血压或肿瘤所致肾衰竭者;(5)研究中途转院或其他原因导致数据收集不全者。最终共143例患者纳入本研究。其中:男77例,女66例;平均年龄(56.71±14.5)岁;平均透析史(29.80±19.62)个月。糖尿病患者40例,其余为慢性肾小球肾炎、肾盂肾炎、多囊肾、肾结石等梗阻肾。
1.2 方法 (1)收集所有患者的一般资料和临床、生化及透析相关参数(每3个月随访1次),包括性别、年龄、透析龄、原发病、通路[动静脉瘘(AVF)/中心静脉置管(CVC)]、血红蛋白(Hb)、血清白蛋白(Alb)、血钙(Ca2+)、血磷(P3+)、透前和透后的尿素氮(BUN)及肌酐(Cr)、上一次透析后体质量、透析日透前体质量、干体质量、透析时间、超滤量,并计算平均透析间期体质量增长率(IDWG%)、尿素清除指数(Kt/V)。其中IDWG%=(透析日透前体质量-上次透析后体质量)/干体质量×100%。Kt/V=-Ln(R.0.008xt)+(4-3.5×R)×UF/W。其中Ln为自然对数;R为透析后BUN与透析前BUN的比值;t为透析时间,单位h;UF为超滤量,单位L;W为患者透析后的体质量,单位kg。(2)所有透析患者采用电子血压计于非自体动静脉瘘侧上肢肘横纹上两指处测量患者透析前、透析过程中每小时及结束后的血压值,计算透析前收缩压及舒张压平均值、整个透析过程中收缩压及舒张压平均值及标准差(SD),计算变异系数(CV,等于SD/平均值),以CV表示透析过程中收缩压和舒张压BPV。由于各个条件的限制,目前正常BPV的参考值范围并没有一个确切的共识[5],受限于样本的数量,故参照谷立杰等[6]的方法分组。本研究透析过程中收缩压BPV为(9.94±3.88),舒张压BPV为(10.50±3.50)。根据CV的均数将患者分为高收缩压BPV组(CV>9.94)64例和低收缩压BPV组(CV<9.94)79例,根据舒张压BPV(10.50±3.50)将患者分为高舒张压BPV组(CV>10.50)67例和低舒张压BPV组(CV<10.50)76例。
1.3 统计学处理 使用SPSS 22.0进行统计学分析,满足正态分布的计数资料组间比较,方差齐时采用独立样本t检验,方差不齐时采用秩和检验;计数资料组间比较采用χ2检验。BPV的影响因素采用多元线性回归分析,P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者各项指标的比较
2.1.1 高收缩压BPV组与低收缩压BPV组各项指标比较 各项指标中,除性别、原发病、通路3项计数资料采用χ2检验,其余项计量资料中,两组患者透前收缩压、超滤量、IDWG%、Kt/V、Ca2+、Hb、Alb不满足方差齐性采用秩和检验,余下采用独立样本t检验。结果显示,高收缩压BPV组年龄、糖尿病患病率、透前收缩压、超滤量、透析间期体质量增长率(IDWG%)均显著高于低SBPV组(P<0.05)。Alb及Kt/V均显著低于低SBPV组(P<0.05)。见表1。
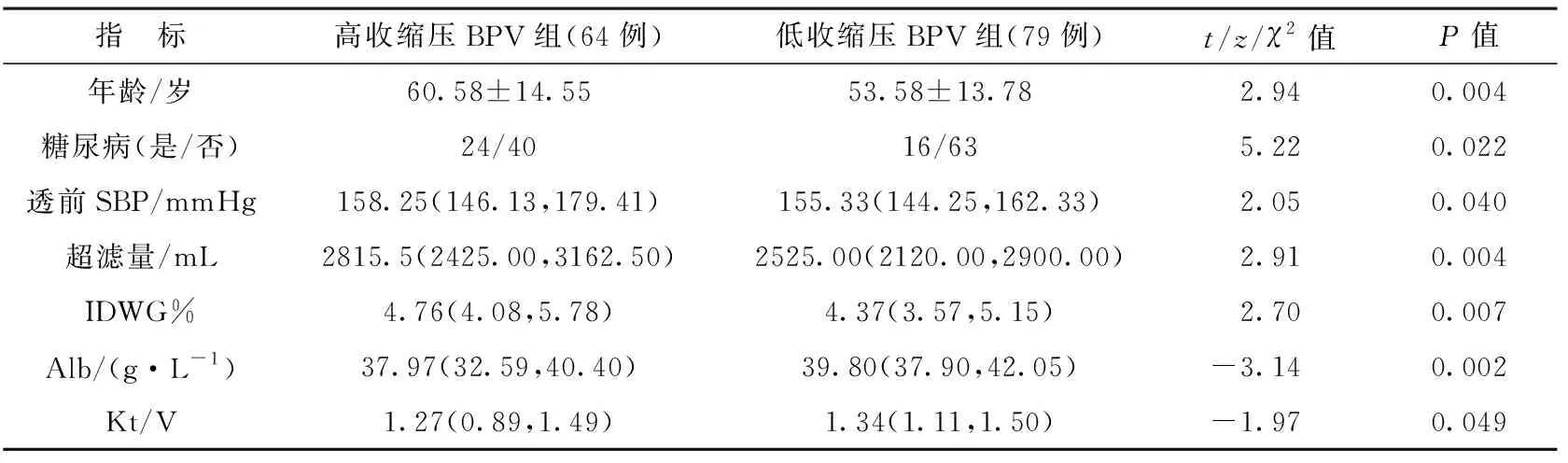
表1 高收缩压BPV组与低收缩压BPV组各项指标比较[M(P25,P75)]
2.1.2 高DBPV组与低DBPV组各项指标比较 除性别、原发病、通路三项计数资料采用χ2检验,其余项计量资料中,两组患者透前收缩压、Ca2+不满足方差齐性采用秩和检验,余下采用独立样本t检验。高舒张压BPV组内瘘(AVF)、超滤量、IDWG%均显著高于低舒张压BPV组。详见表2。

表2 高DBPV组与低DBPV组各项指标比较
2.2 BPV相关因素分析
2.2.1 SBPV相关因素分析 以SBPV为因变量,以年龄、透析龄、透前SBP、透前DBP、超滤量、IDWG%、Alb、Kt/V、Hb、Na+、Ca2+、P3+、BUN、Cr作为自变量进行多元线性回归分析。结果表明,SBPV的独立影响因素为年龄、透前SBP、超滤量、Hb、Alb、Ca2+。收缩压BPV与年龄、透前SBP、超滤量、Hb及Ca2+呈正相关,与Alb呈负相关。详见表3。

表3 收缩压BPV影响因素的多元线性回归分析(逐步回归法)
注:回归方程的线性假设检验R=0.545,F=9.581,P=0.000
2.2.2 DBPV相关因素分析 以DBPV为因变量,以其余因素作为自变量进行多元线性回归分析。结果表明,舒张压BPV的独立影响因素为IDWG%、Alb、Kt/V。DBPV与IDWG%呈正相关,与Alb、Kt/V呈负相关。详见表4。

表4 舒张压BPV影响因素的多元线性回归分析(逐步回归法)
注:回归方程的线性假设检验R=0.378,F=7.718,P=0.000
2.3 结局 回顾性分析显示,透析患者死亡原因多以心脑血管疾病为主,其次为感染、消化道出血等。采用χ2检验分析得出:无论SBPV组还是DBPV组,高BPV组病死率均高于低BPV组(P<0.05)。详见表5。

表5 各BPV组结局
3 讨 论
高血压是MHD患者的常见并发症之一,且难以控制,显著增加患者心血管疾病患病率和病死率。血压变异性(BPV)反映了自主神经系统对心血管的调节,已被作为有别于血压的一项独立的反映心血管活动的指标。目前就非透析人群BPV的研究已很成熟,就透析人群,越来越多的研究证实BPV与维持性血透患者的不良预后有关[7-8,1]。
谷立杰等[6]研究表明,高龄、透析前收缩压(透前SBP)高、IDWG%增加、Hb水平降低为MHD患者透析中SBPV升高的独立危险因素,透析中SBPV升高与MHD患者全因病死亡率增加有关。本研究得出相似结论。对影响透析过程中BPV的相关因素进行分析,结果显示,高SBPV组和低SBPV组的年龄、糖尿病患病率、透前SBP、超滤量、IDWG%、Alb、Kt/V有显著性差异(P<0.05)。但却发现两组Hb呈正相关。导致这一差异的原因可能是,高SBPV组透析间期IDWG%较低SBPV组高,透析清除大量液体导致浓缩及再分布影响大于低SBPV组。其次,本研究未排除促红素使用对Hb及BPV的干扰。
年龄、透前SBP、超滤量、Hb、Alb、Ca2+为SBPV的独立影响因素。透前SBP越高则SBPV越大,可能与在血液透析间期水盐摄入过多,容量负荷增加,电解质代谢紊乱,神经体液调节使心输出量增加及血管阻力增加,同时肾素-血管紧张素-醛固酮系统(RAAS)反射性激活有关。多元线性回归分析未得出IDWG%为收缩压BPV的独立影响因素,分析其原因可能因为IDWG%导致的血压变异性多影响透析间期BPV,透析过程中的BPV与透析超滤量相关性更大,随着透析血流加快,水分、毒素快速清除、渗透压改变使酸碱平衡骤变、交感神经异常活跃[9],导致血压波动大。但IDWG%增加仍会造成透析超滤增加,与本研究相符。
本研究显示,高SBPV组、低SBPV组的Alb、 Kt/V有显著性差异。究其原因,透析过程中,随着液体及血管活性介质快速清除、血浆渗透压及酸碱平衡剧变,使得BPV大幅度变化[10]。而且透析不充分,水分及代谢产物清除不良,容易造成营养摄入不良、Alb下降而引起血浆胶体渗透压下降,进而导致组织间液渗透压升高,增加透析间期体质量、炎症因子释放增加,构成营养不良-炎症-动脉粥样硬化综合征(MIA综合征)[11],进而加剧血压变异性。
本研究得出血Ca2+浓度是收缩压BPV的独立影响因素。众所周知,钙磷代谢紊乱及其后引起的继发性甲状旁腺功能亢进是MHD患者的常见并发症,故血钙升高可能是甲状旁腺激素(PTH)动员骨钙入血导致血管僵硬、弹性降低。MHD患者因继发性甲状旁腺功能亢进促进破骨细胞释放,同样会使得血磷升高,促进血管钙化,但本研究未得出此结论,可能系服用磷结合剂有关。Cheng等[12]研究表明SBPV越高,动静脉内瘘失功风险越高,系SBPV加重静脉壁炎导致动静脉功能障碍。而本研究未对此进行探讨。Chang等[4]研究长时BPV与MHD关系时表明使用中央静脉导管有更高的BPV。
本研究发现高、低DBPV组通路选择、超滤量、IDWG%有显著差异性(P<0.05)。多元线性回归分析,IDWG%、Alb、Kt/V是DBPV的独立影响因素,前者呈正相关,后两者呈负相关。原因在于,导管的使用可增加感染机会,而炎症会加剧血压波动,增加血液透析患者心血管风险和相关死亡率[11]。Kt/V降低,Alb下降,导致MIA综合征及IDWG%增加,导致容量负荷过重,加重心脏负担,而IDWG%与DBPV呈正相关,因此控制BPV有助于延迟器官、血管损伤的发展,进而减少心脑血管事件及全因死亡率。
Yoon等[13]研究表明,接受血液透析的患者的病死率在治疗的第1年是20%,而在5年后是70%。心血管疾病占死亡人数的50%。由于本研究3年研究时限并非严格从每位患者开始透析时起观察,故无法研究其病死率。但就这3年研究期间,本研究发现高BPV组病死率高于低BPV组,推测血压变异性大者发生全因病死率更大。
本研究具有一定的局限性。首先,本研究为回顾性研究,且未排除吸烟、体质量指数、血脂、继发性甲状旁腺功能亢进、降压药及促红素使用等因素对血压变异性的影响,有进一步研究的必要性。其次,本研究没有使用如生物阻抗等客观的方法来评估干体质量,因此,不能排除部分患者在透析结束时没有达到真正的干体质量。
4 结 论
高龄、透前SBP高、超滤量大、Alb低、高Ca2+是收缩压BPV的独立影响因素。IDWG%大、Alb低、Kt/V低是舒张压BPV的独立影响因素。临床中,控制透析前血压和透析间期体质量增长率,适当减少超滤量、纠正低蛋白,充分透析有助于降低透析中血压波动,进而改善透析患者预后,在老年人群尤应关注以上指标。

