电化学转化效率问题的解答策略
卢国锋
黑龙江
装置、过程和效率是电化学研究的三驾马车,作为电化学重要组成的效率问题,教材中出现了比能量和比功率的定义,但很少引起教师的关注,思则有备,有备无患,及时修复知识体系的漏洞,避免失分是非常重要的。
策略一:厘清法拉第常数与阿伏加德罗常数的关系
电化学中传递电子的数量是计算的核心,宏观测量的电流强度和时间,通过法拉第常数或阿伏加德罗常数都能获得电子的物质的量。
1 mol元电荷所具有的电量的绝对值称为法拉第常数(F),元电荷又称“基本电量”, 是1个电子或1个质子所带的电量,电子与质子电性相反,绝对值不考虑正负问题,只考虑数值。
1个电子电量是1.6×10-19C,1 mol电子数约为 6.02×1023,1 mol电子所带电量的绝对值即F=6.02×1023mol-1×1.6×10-19C=96 320 C/mol,试题中经常提供的数值为F=96 500 C/mol。


例1以石墨为电极,用电流强度为I(安培)的直流电电解足量RCly的水溶液,tmin后,精确测得电极上析出ng金属R,设金属R的摩尔质量为Mg/mol,则阿伏加德罗常数的计算式可表示为(每个电子电量:1.6×10-19C)
( )

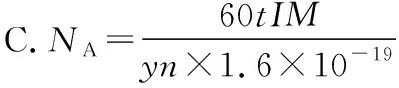
解析:阴极析出金属,电极反应式为

Mgymol
ngn(e-)


答案:C
策略二:利用题中新定义信息逆向求解
1.比能量:电池单位质量或单位体积所输出电能的多少[单位:(W·h)/kg或(W·h)/L]。
单位质量或体积指表达式中质量或体积处在分母位置,从单位看是kg或L。电池理论产生的电能处在表达式的分子位置,计算公式W=U×I×t=U×Q=P×t,其中W是电功,单位为焦耳(J);U是电压,单位为伏特(V);I是电流,单位为安培(A);t是时间,单位为秒(s);Q是电量,单位为库仑(C),P是功率,单位为瓦(W),1 kW·h=3.6×106J。
2.比功率:电池单位质量或单位体积所输出功率的大小[单位:(W)/kg或(W)/L],P=UI。

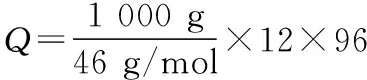
答案:8.39(kW·h)/kg
策略三:物质与能量两大角度题型归纳训练
化学变化过程同时存在着物质和能量变化,同时遵守质量守恒和能量守恒。原电池和电解池电极反应式直接计算属于理想状态,不考虑效率问题,若用实际析出物质数据计算,因存在其他副反应,要考虑电流效率问题。
类型一:理论物质消耗和析出的相关计算
例3酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是由碳粉、二氧化锰、氯化锌和氯化铵等组成的糊状填充物。该电池在放电过程产生MnOOH,维持电流强度为0.5 A,电池工作5 min,理论消耗Zn g。(已知F=96 500 C/mol)
解析:锌是活泼金属,为负极,电极反应式:

65 g 2 mol


答案:0.05

(1)正、负极的电极材料中, 极先消耗完。
(2)理论上该电池放电最长时间是多少小时?(已知F=96 500 C/mol)
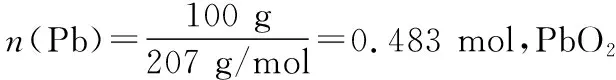
(2)Q=n(e-)·F=0.418 mol×2×96 500 C/mol

答案:(1)正 (2)22.41 h
类型二:能量转化效率的相关计算


答案:80.4%





