高效液相色谱法测定芪蓉润肠口服液中松果菊苷与毛蕊花糖苷的含量
闫 瑶, 孟新源, 许欢欢, 杨建华, 胡君萍
(新疆医科大学1第一附属医院药学部, 乌鲁木齐 830054; 2附属肿瘤医院药学部, 乌鲁木齐 830000; 3药学院, 乌鲁木齐 830011)
芪蓉润肠口服液是由黄芪(炙)、肉苁蓉、白术、太子参、地黄、玄参、麦冬、当归、黄精(制)等15味中药材加工而成,临床上多用于气阴两虚、脾肾不足、大肠失于濡润而致的虚症便秘[1]。芪蓉润肠口服液成分中的肉苁蓉具有提高结肠收缩幅度、加强肠道收缩力、纠正胃肠激素水平等作用,对脾肾阳虚型便秘效果显著[2]。肉苁蓉的主要活性成分是苯乙醇苷,松果菊苷和毛蕊花糖苷是苯乙醇苷中的指标性成分[3-4]。有研究表明[5-7],松果菊苷可能通过增加转化生长因子-β1来促进肠道上皮细胞MODE-K细胞的增殖和细胞存活率,从而修复肠道上皮细胞,促进小肠推进力,引起排便时间缩短;毛蕊花糖苷则具有增强免疫、抗自由基和防止脂质过氧化等作用。本研究采用HPLC法,同时考察芪蓉润肠口服液中松果菊苷和毛蕊花糖苷的含量,以期为该药品的质量控制提供参考,现报道如下。
1 仪器与试药
1.1仪器Waters Alliance 2695型高效液相色谱仪(Waters科技有限公司),Waters 2487型紫外检测器(Waters科技有限公司),Empower色谱工作站(Waters科技有限公司),Sartorius BP211D型电子天平(瑞士METTLER公司),UV2550型紫外分光光度计(日本岛津公司),KQ-200VDB型双频数控超声波清洗器(昆山市超声仪器有限公司),基因研究型超纯水机FJY1002-UVF(青岛富勒姆科技有限公司)。
1.2试药甲醇(美国Fisher 公司,批号145629,色谱纯),磷酸(天津市富宇精细化工材料有限公司,批号20141020),乙腈(天津市富宇精细化工有限公司,批号20121207,分析纯)。松果菊苷对照品与毛蕊花糖苷对照品为本课题组从盐生肉苁蓉Cistanchesalsa中分离制备,UV,IR,EI-MS,1H-NMR,13C-NMR数据与文献报道相符,含量经HPLC面积归一化法测定纯度大于95%。
1.3药品芪蓉润肠口服液(北京北卫药业有限责任公司,批号:120534、141042、141232、150538)。
2 方法与结果
2.1对照品溶液的制备称取毛蕊花糖苷对照品和松果菊苷对照品适量于10 mL容量瓶,用80%甲醇溶解并定容至刻度,制备成毛蕊花糖苷对照品浓度为224 μg/mL和松果菊苷对照品浓度为513 μg/mL的混合溶液,备用。
2.2供试品溶液的制备取芪蓉润肠口服液每个批号各3份,12 000 r/min离心20 min,去沉淀部分,取上清液0.5 mL于10mL容量瓶,用蒸馏水定容至刻度,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.3色谱条件采用HypersilODS-2色谱柱 (4.6 mm×250 mm,5 μm);流动相A为0.4%磷酸水溶液,B为乙睛,梯度条件为0~5 min 83% A-17% B;5~20 min 80% A-20% B;20~25 min 80% A-20% B;25~30 min 83% A-17% B,流速为1.00 mL/min;柱温为30℃;检测波长为333 nm,进样量为20 μL见图1、2。
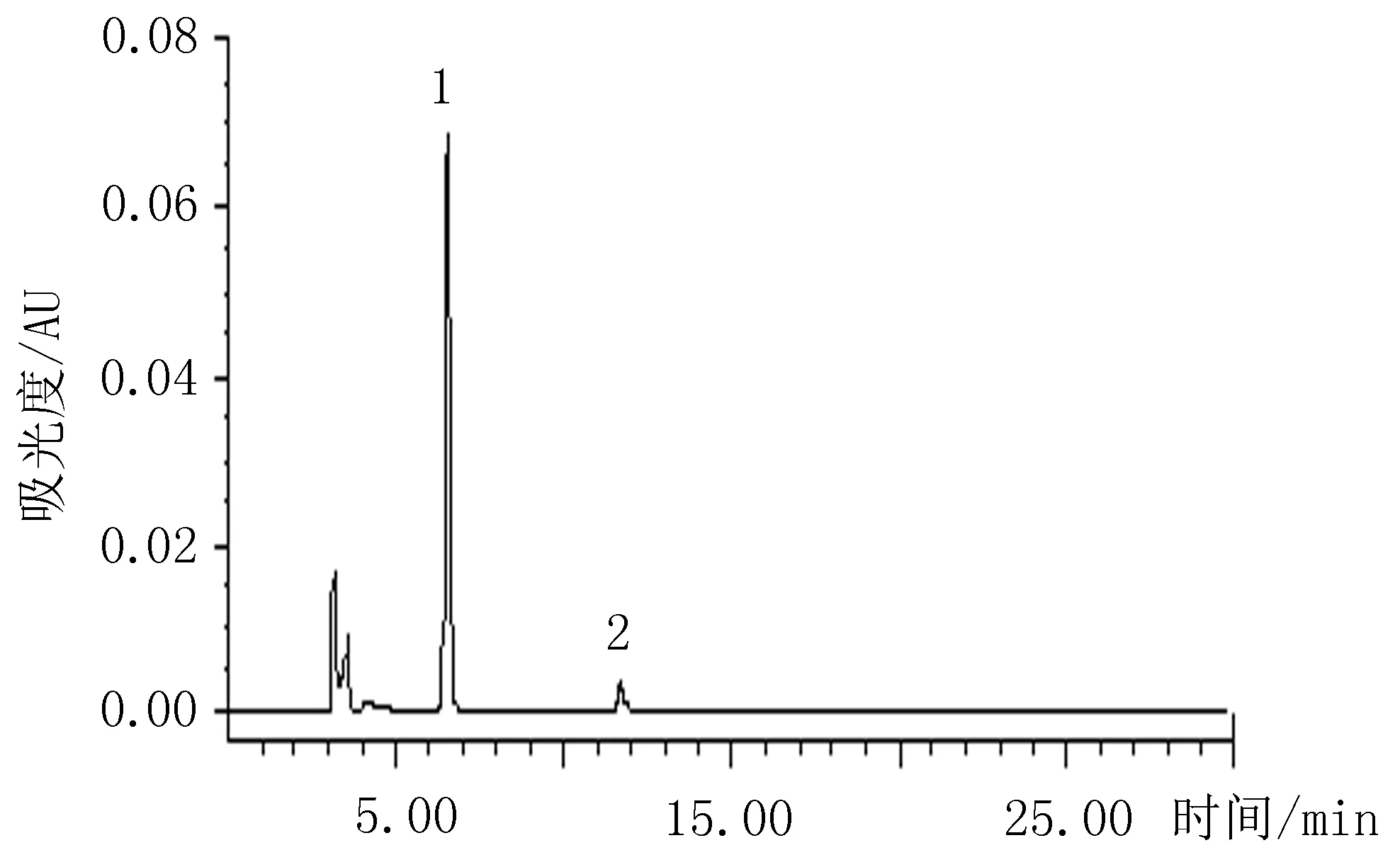
图1 混合对照品HPLC色谱图 (1 松果菊苷;2毛蕊花糖苷)
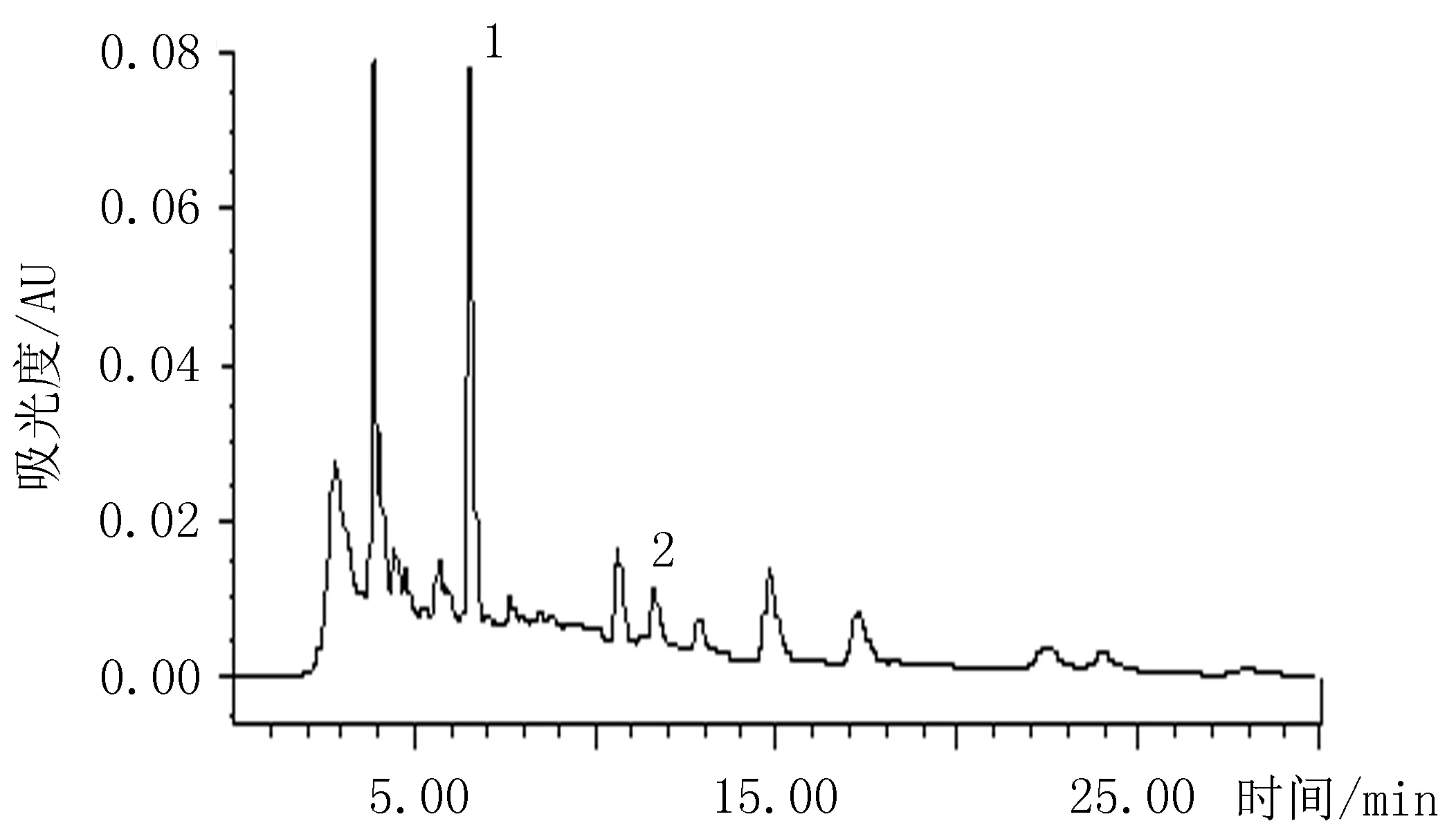
图2 供试品HPLC色谱图 (1 松果菊苷;2毛蕊花糖苷)
2.4标准曲线的建立
2.4.1 松果菊苷标准曲线的建立 分别吸取“2.1”项下对照品溶液0.125、0.250、0.500、1.000、2.000 mL,用80%甲醇定容至5 mL容量瓶,制成系列混合对照品溶液,按“2.3”项下方法测定,以峰面积为纵坐标,对照品溶液质量浓度为横坐标进行线性回归,得松果菊苷线性回归方程Y=13 600X+35 137,r=0.999 5,松果菊苷浓度在12.83~205.20 μg/mL范围内线性关系良好。
2.4.2 毛蕊花糖苷标准曲线的绘制 分别吸取“2.1”项下对照品溶液各12.5、25.0、50.0、100.0、200.0 μL,用80%甲醇定容至5 mL容量瓶,制成系列混合对照品溶液,按“2.3”项下方法测定,以峰面积为纵坐标,对照品溶液质量浓度为横坐标进行线性回归,得毛蕊花糖苷的线性回归方程Y=25 431X-12 768,r=0.999 3,毛蕊花糖苷浓度在0.56~8.96 μg/mL范围内线性关系良好。
2.5精密度试验吸取“2.1”项下对照品溶液20 μL,按“2.3”项下方法测定3次,测得松果菊苷峰面积的RSD为1.4%、毛蕊花糖苷峰面积的RSD为1.7%,表明方法精密度良好。
2.6重现性试验取同一批芪蓉润肠口服液(批号为150538)样品,按“2.2”项下方法制备供试品溶液,平行制备3份供试品溶液,按“2.3”项下方法测定,测得松果菊苷峰面积的RSD为1.3%,毛蕊花糖苷峰面积的RSD为1.4%,表明方法的重现性良好。
2.7稳定性试验取同一批号供试品溶液,按“2.2”项下方法制备供试品溶液,按“2.3”项下方法测定,分别于0、2、4、8、16、24 h测定,松果菊苷与毛蕊花糖苷峰面积值的RSD分别为1.6%和1.8%。
2.8加样回收率试验取9份含量已知的芪蓉润肠口服液,分别加入等量低浓度(松果菊苷41.04 μg,毛蕊花糖苷1.79 μg)、中浓度(松果菊苷51.30 μg,毛蕊花糖苷2.24 μg)、高浓度(松果菊苷61.65 μg,毛蕊花糖苷2.69 μg)的混合对照品溶液,按“2.3”项下方法测定,计算加样回收率。测得松果菊苷平均加样回收率为99.9%,RSD为1.2%,毛蕊花糖苷平均加样回收率为100.3%,RSD为1.3%。见表1。

表1 加样回收率试验结果(n=3)
2.9样品含量测定按“2.2”项下方法制备供试品溶液,按“2.3”项下色谱条件测定4个批号的芪蓉润肠口服液各3份。结果4个批次芪蓉润肠口服液中松果菊苷的质量浓度分别为1 157.46、343.86、905.54、1 527.40 μg/mL,平均质量浓度为983.57 μg/mL;毛蕊花糖苷的质量浓度分别为42.87、27.54、48.73、92.21 μg/mL,平均质量浓度为52.84 μg/mL。见表2。
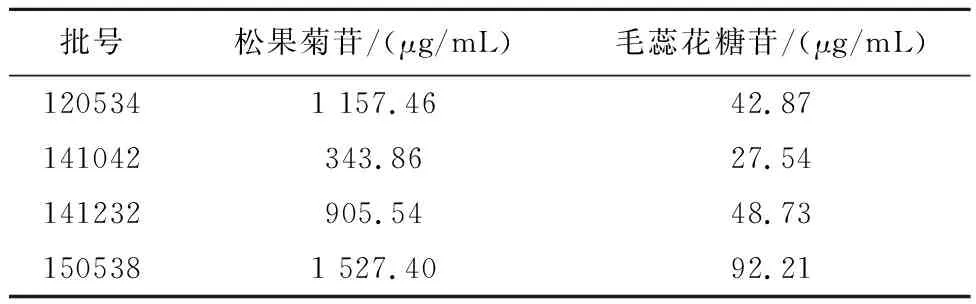
表2 芪蓉润肠口服液中松果菊苷与毛蕊花糖苷质量浓度测定结果(n=3)
3 讨论
近年来,对肉苁蓉生药、商品药材及部分复方制剂中松果菊苷和毛蕊花糖苷进行的HPLC法测定的报道较多[8-10],但对芪蓉润肠口服液中相关成分含量测定的报道尚不多见。本研究实验发现,不同批号之间毛蕊花糖苷含量与松果菊苷含量差异大,且同一批次中毛蕊花糖苷含量均较松果菊苷低,分析原因可能有以下几点:(1)肉苁蓉生长环境不同:目前肉苁蓉野生资源濒临枯竭,需依靠人工栽培的肉苁蓉来满足国内外与日俱增的市场需求。但人工栽培和野生肉苁蓉在生长环境、年限以及采收加工方式上均有一定的差异,其药材有效成分含量也存在着差异。据徐荣等[11]等研究,人工栽培肉苁蓉中松果菊苷含量高于毛蕊花糖苷含量,而野生肉苁蓉中2种苷类成分的含量是较为接近的。本研究结果显示,不同批次药品中毛蕊花糖苷含量均低于松果菊苷含量,推测芪蓉润肠口服液中使用的肉苁蓉可能为人工栽培。(2)肉苁蓉品系不同:正品肉苁蓉为列当科植物肉苁蓉CistanchedeserticolaY. D. Ma,而全国不少地区将同属植物盐生肉苁蓉C.salsa(C. A. Mey) C. Beck和管花肉苁蓉C.tubulosa(Schenk) R. Wight也作为肉苁蓉入药。王义明等[12]相关研究表明,苯乙醇苷类化合物含量在3种肉苁蓉中存在较大差异。因此本研究中各个批次间松果菊苷与毛蕊花糖苷的含量差异较大,可能由入药的肉苁蓉品系不同所导致。(3)光敏感性:松果菊苷与毛蕊花糖苷都是易分解的成分,对强光较敏感,不同批次供试品制备时可能因实验室光线强度不同或供试品保存时间不尽一致,使各批次含量测定结果差异较大。
综上所述,本研究使用HPLC法测定芪蓉润肠口服液中松果菊苷与毛蕊花糖苷,该法灵敏度高、重现性好、结果准确、方便易行,适用于芪蓉润肠口服液中松果菊苷与毛蕊花糖苷的测定。

