共轭微孔聚合物的羧基基团含量对体系吸附性能的影响
王文君,刘艳丽,王衍茜,巩家旺,许彦红,2,姚 婵*,2
(1.吉林师范大学 环境友好材料制备与应用教育部重点实验室,吉林 长春 130000;2.吉林师范大学 化学学院,吉林 四平 136000)
二氧化碳是导致全球变暖的主要温室气体之一。为了缓解二氧化碳带来的气候变化危机,大量具有选择性吸收二氧化碳性能的多孔材料被研究和开发。在众多新型多孔材料中,金属有机框架、分子筛和纯有机材料脱颖而出,因为它们具有分子骨架可设计、孔道可控制和孔径可调等优点。共轭微孔聚合物(Conjugated Polymer Microporous,CMPs)是一类有共价键连接,具有永久性纳米孔道的有机多孔聚合物[1]。最近,CMPs也逐渐成为气体吸附领域的一个研究热点,如CMPs对氢气、二氧化碳和甲烷等气体的吸附研究[2]。多孔材料的孔隙参数,如孔体积、孔径、孔径分布等,对测定材料的气体吸附性能至关重要[3]。已有的研究发现,多孔聚合物的孔结构上的极性基团可以显著增强聚合物与二氧化碳的结合能,从而提高体系对二氧化碳的吸附量和选择性吸附能力[4]。这主要是由于二氧化碳和多孔聚合物的富羧基框架之间发生氢键和四极偶极的相互作用[5]。因此,我们合成了四个富羧酸基团的共轭微孔聚合物CMPs(CMP@1,CMP@2,CMP-COOH@1和CMP-COOH@2),研究了它们的二氧化碳吸附性能,探讨了羧基基团的数量对体系孔隙、气体吸附和选择性的影响。
1 实验合成
1.1 四(4-((三甲基硅甲基)乙炔基)苯基)甲烷的合成
将四溴四苯甲烷(2.04 g,3.16 mmol),PdCl2(PPh3)2(0.135 g,0.18 mmol),CuI0.024 g,0.125 mmol),PPh3(0.1 g,0.38 mmol)置入250 mL的双颈烧瓶中,用氮气循环脱气3次。再向体系中加入iPr2NH(30 mL)和三甲基乙炔基硅(2.2 mL,30.37 mmol),升温至80 ℃,反应24 h。降至室温,旋蒸除去溶剂后,加入三氯甲烷溶解固体,通过一层硅藻土过滤。取滤液并用Na2EDTA稀溶液洗涤后,加入无水Na2SO4干燥,最后加入乙醇获得白色固体,为产品。
1.2 四(4-乙炔基苯基)甲烷的合成
将四(4-((三甲基硅甲基)乙炔基)苯基)甲烷(1.8 g,1.2 mmol)溶于CH2Cl2(20 mL),NaOH(0.98 g, 24.6 mmol)溶于CH3OH(10 mL),混合后室温搅拌6 h。反应后的溶液水洗,再用CH2Cl2萃取,最后用盐水洗有机相,再加入无水Na2SO4干燥,最后加入乙醇获得淡黄色固体,为产品。
1.3 CMP@1和CMP@2的合成
将2-溴对苯二甲酸(92.4 , 0.33 mmol)和1,3,5-三乙炔基苯(50 ,0.33 mmol)、(CMP@1)/四(4-乙炔基苯基)甲烷(104 ,0.25 mmol)(CMP@2)置入50 mL双颈烧瓶中,氮气脱气循环3次,如图1(a)所示。向反应体系中注入N, N'-二甲基甲酰胺(DMF,2 mL) 和三乙胺(Et3N,2 mL),用冷冻-解冻循环法再次循环脱气3次,最后氮气保护。体系升温至120 ℃,将四(三苯基膦)钯(0)(23.11 ,0.025 mmol) 分散在DMF(1 mL)中,CuI(4.8 ,0.025 mmol)分散在Et3N(1 mL)中,注入反应体系。保持反应温度120 ℃,反应48 h。抽滤,用四氢呋喃(THF)、甲醇、丙酮和水依次洗涤沉淀4次。采用索氏提取法依次使用甲醇和THF对产品进一步纯化,每次纯化时间为24 h。CMP@1为黄色固体,CMP@2为黄绿色固体。
1.4 CMP-COOH@1和CMP-COOH@2的合成
将2,5-二溴对苯二甲酸(107 , 0.33 mmol)和1,3,5-三乙炔基苯(50 , .33 mmol)、(CMP-COOH@1)/四(4-乙炔基苯基)甲烷(104 ,0.25 mmol)(CMP-COOH@2)置入50 mL双颈烧瓶中,氮气脱气循环3次,如图1(b)所示。向反应体系中注入N, N'-二甲基甲酰胺(DMF,2 mL)和三乙胺(Et3N,2 mL),用冷冻-解冻循环法再次循环脱气3次,最后氮气保护。体系升温至120 ℃,将四(三苯基膦)钯(0)(23.11 ,0.025 mmol)分散在DMF(1 mL)中,CuI(4.8 ,0.025 mmol)分散在Et3N(1 mL)中,注入反应体系。保持反应温度120 ℃,反应48 h。抽滤,用四氢呋喃(THF)、甲醇、丙酮和水依次洗涤沉淀4次。采用索氏提取法依次使用甲醇和THF对产品进一步纯化,每次纯化时间为24 h。CMP-COOH@1为棕黄色固体,CMP-COOH@2为黄绿色固体。
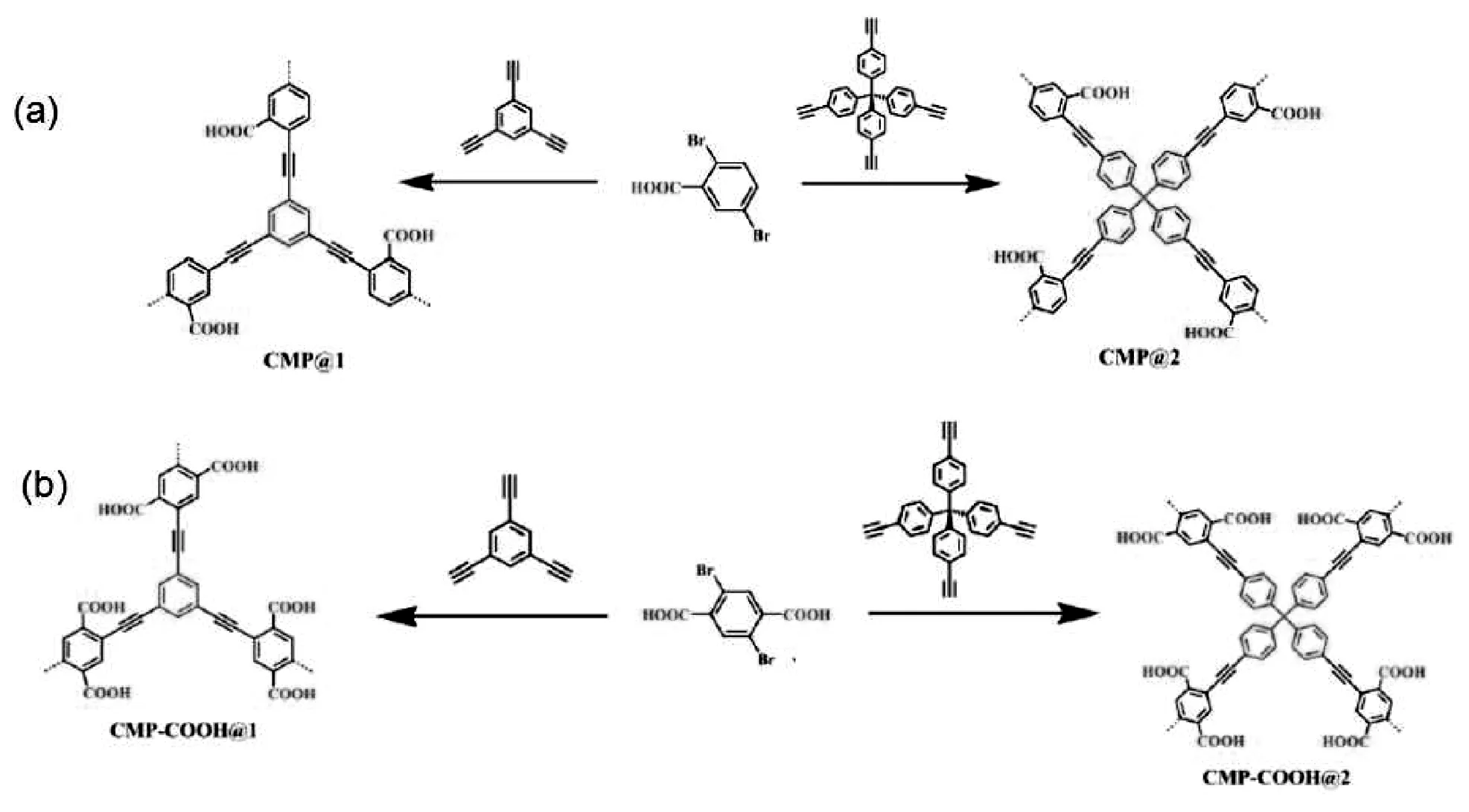
图1合成路线(a)CMP@1和CMP@2(b)CMP-COOH@1和CMP-COOH@2
Fig.1Schematic representation of synthesis of CMP@1,CMP@2,CMP-COOH@1 and CMP-COOH@2
2 结果与讨论
2.1 CMP@1,CMP@2,CMP-COOH@1和CMP-COOH@2的多孔性
77 K,我们采用氮气吸附来探测CMP@1,CMP@2,CMP-COOH@1和CMP-COOH@2的孔隙特征。实验结果表明,四种聚合物的吸附/脱附等温曲线主要表现为Ⅰ型等温曲线特征。四种聚合物样品在p/p0<0.1的相对压力范围表现出快速的吸附,说明它们具有微孔。在较高的相对压力(p/p0>0.8)范围,CMP@1和CMP-COOH@1的等温线急剧上升,这表明样品中存在介孔/大孔隙。孔径分布的计算采用非线性密度泛函理论(NLDFT),如图2所示,四个聚合物都具有较宽的孔径分布范围,在0~2 nm的尺寸范围内均显示出明显的峰。在2~12 nm范围内,CMP-COOH@1和CMP-COOH@2可以观察到孔径分布曲线有小的波动。这个结果与聚合物氮气吸附等温线获得的结论一致,说明聚合物中存在微孔和介孔。
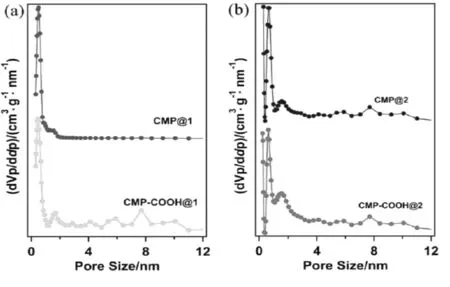
图2 CMP@1,CMP@2,CMP-COOH@1 和CMP-COOH@2的孔径分布曲线Fig.2 Pore size distribution of CMP@1,CMP@2, CMP-COOH@1 and CMP-COOH@2
2.2 CMP@1,CMP@2,CMP-COOH@1和CMP-COOH@2的二氧化碳吸附性能
基于已有的研究,聚合物良好的孔隙度和丰富的羧基位点均有利于多孔材料对二氧化碳的高吸附性能的提高。我们研究了1.05×105Pa条件下,298 K和273 K下的二氧化碳吸附性能。CMP-COOH@1和CMP-COOH@2在298 K和1.05×105Pa下分别显示出1.61 mmol·g-1和1.92 mmol·g-1的二氧化碳吸附容量。当温度降低为273 K时,聚合物CMP-COOH@1和CMP-COOH@2显示更高的二氧化碳捕获量分别为2.17。在5×106Pa和318 K条件下,CMP-COOH@1和CMP-COOH@2二氧化碳吸附值随压力的增加呈线性的增加,显示出了更高的二氧化碳捕获能力。这些结果表明,该类多孔聚合物对二氧化碳吸附不仅仅取决于骨架中的表面积、孔体积和极性基团,测量压力对其吸附性能也有很大影响。
2.3 羧基基团含量对吸附性能的影响
为了研究共轭微孔聚合物中羧基基团的含量对聚合物的二氧化碳吸附能力影响,我们比较了二羧基偶联的CMP@1和CMP@2和四羧基偶联的CMP-COOH@1和CMP-COOH@2的吸附性能。从BET表面积比较,CMP@1和CMP@2的BET表面积高于对应的CMP-COOH@1和CMP-COOH@2。从孔径比较,CMP@1和CMP@2的主要孔径分布范围大于CMP-COOH@1和CMP-COOH@2。这种现象可能是由于CMP-COOH@1和CMP-COOH@2中的2,5-二溴对苯二甲酸的体积明显比CMP@1和CMP@2中的2-溴苯甲酸大,因而占据更多的空腔空间。在273 K和1.05×105Pa下,CMP-COOH@1和CMP-COOH@2的二氧化碳吸附量分别是CMP@1和CMP@2的1.31和1.15倍。因此,羧基含量的增加可以明显提高体系二氧化碳的吸附量。另外,吸附热大小顺序为CMP-COOH@1>CMP-COOH@2>CMP@1>CMP@2。这正是因为CMP-COOH@1和CMP-COOH@2的羧基含量高于CMP@1和CMP@2。此外,318 K和5×106 Pa条件下,CMP-COOH@1和CMP-COOH@2的二氧化碳捕获能力也明显强于CMP@1和CMP@2。以上研究结果表明羧基的含量对聚合物气体吸附能力有很大的影响。
3 结论
综上所述,我们成功合成了四种羧基共轭微孔聚合物CMP@1、CMP@2、CMP-COOH@1和CMP-COOH@2,它们均具有相对较高表面积。CMP-COOH@1和CMP-COOH@2具有良好的二氧化碳吸附能力。就目前关于多孔有机聚合物二氧化碳吸附的报道,同等条件下,这个值位于前列。另外,我们的研究还表明,增加聚合物羧基基团的含量,可以有效提高在相同条件下材料的吸附能力和选择性。

