固相萃取—超高效液相色谱法测定水产品中6种氟喹诺酮类药物残留
贺 江 李晓月 仇玉洁 李博恩 杨品红
(1. 湖南文理学院生命与环境科学学院,湖南 常德 415000;2. 环洞庭湖水产健康养殖与加工湖南省重点实验室,湖南 常德 415000;3. 湖南省水产高效健康生产协同创新中心,湖南 常德 415000)
中国作为世界上著名的水产品养殖、生产和出口大国,水产品养殖产量约占世界2/3,而渔药残留问题一直都是各方关注的焦点。氟喹诺酮类药物(Fluoroquinolone,FQs)是一类十分重要的人工合成抗菌药物,因其具有抗菌谱广、抗菌活性强、组织穿透力强、价格低廉、与其它抗菌药物无交叉耐药性等特点[1],曾被广泛应用于水产养殖业中。但不合理的用药可导致氟喹诺酮类药物及其代谢产物在水产品中的残留,进而引起食用者肠道菌群失衡或产生远期毒性作用及潜在“三致”(致癌、致畸、致突变)作用[2-3]。近年来,随着社会对食品安全问题关注度逐渐增大,氟喹诺酮类药物在水产养殖等领域的应用开始受到限制,或制定了相应的最大残留限量(MRL)。欧盟和北美等国家早已在水产养殖业中禁用环丙沙星,中国也在NY 5070—2002《无公害食品水产品中渔药残留限量》和NY 5071—2002《无公害食品渔用药物使用准则》中将其列为禁用药物。中国农业部于2015年又发布了第2292号公告,禁止洛美沙星、培氟沙星、氧氟沙星、诺氟沙星4种氟喹诺酮类药物在食用动物中的使用。欧盟及中国规定水产品中恩诺沙星及其代谢产物环丙沙星的最高残留总限量为100 μg/kg。
建立方便有效的残留检测方法,是加强水产品中氟喹诺酮类药物残留监控的前提与基础。目前,文献报道中已有一系列的关于喹诺酮类药物的检测方法,如免疫分析法[4-5]、毛细管电泳法[6]、高效液相色谱法(HPLC)[7-8]、液相色谱-质谱联用法[9-10]等。其中HPLC方法相对来说最普遍,但其在灵敏度和检测效率上仍存在不足。超高效液相色谱技术(UPLC)是一种较传统HPLC方法更加灵敏和快速的分析方法,随着该技术的发展和普及,极有望替代HPLC成为新一代食品安全检测技术标准。此外,在氟喹诺酮类药物残留检测中,样品前处理的传统方法多为液液萃取法,不仅复杂耗时而且精确度不高;而固相萃取(SPE)技术已在食品安全检测中广泛应用。本研究旨在基于固相萃取(SPE)和超高效液相色谱(UPLC)技术,建立可同时测定水产品中诺氟沙星、氧氟沙星、环丙沙星、培氟沙星、洛美沙星、恩诺沙星6种氟喹诺酮类药物残留量的检测方法,为水产品的安全提供技术保障。
1 材料与方法
1.1 材料与试剂
草鱼、鳊鱼、鲫鱼、黄骨鱼:市售;
氧氟沙星、培氟沙星、诺氟沙星、恩诺沙星、环丙沙星、洛美沙星标准溶液:美国A ChemTek公司;
Cleanert PEP-2固相萃取柱:填料量200 mg,体积6 mL,博纳艾杰尔公司;
乙腈:色谱纯,美国TEDIA公司;
磷酸二氢钾、柠檬酸、乙酸铵、磷酸等:均为国产分析纯。
1.2 仪器与设备
超高效液相色谱仪(配有FLR荧光检测器): Acquity H-Class型,美国Waters公司;
液相色谱柱:Acquity UPLC®BEH C18(1.76 μm,2.1 mm×50.0 mm),美国Water公司;
高速冷冻离心机: Multifuge X1R型,赛默飞世尔科技中国有限公司;
固相萃取装置: DG-24型, 美国Supelco公司;
电子分析天平: TX223L型, 日本岛津公司;
氮吹仪: HAD-24B型,北京恒奥德仪器仪表有限公司。
1.3 方法与步骤
1.3.1 6种氟喹诺酮类药物UPLC分析条件的优化及标准曲线的建立
(1) UPLC分析条件的优化:配置浓度均为500 ng/mL的6种氟喹诺酮药物的混合标准溶液,设定进样体积为0.2 μL,柱温为50 ℃,检测波长为λex=278 nm,λem=465 nm。参考有关文献资料[11-14],重点对流动相的类型和流速进行优化,以获取最佳检测效果。
(2) 标准曲线的建立:按照表1用乙腈分别配制氟喹诺酮系列混合标准溶液,采用已确定的UPLC分析检测条件进行检测,并进一步建立标准曲线。

表1 6种氟喹诺酮类药物混合标准溶液的配制Table 1 Preparation of mixed standard solution of six fluoroquinolones
1.3.2 水产品中6种氟喹诺酮药物检测前处理方案的建立
(1) 固相萃取小柱的效果验证:将2 mL浓度为500 ng/mL的混合标准溶液用磷酸盐缓冲液稀释至10 mL作为模拟提取液过SPE小柱(用前分别用6 mL甲醇和6 mL水活化),再用3 mL 5%甲醇水淋洗,最后用6 mL甲醇洗脱。分别收集上样过柱液、淋洗液、洗脱液,各取1 mL过0.22 μm滤膜上机检测其中各种氟喹诺酮类药物的含量,以验证所用固相萃取柱的效果。
(2) 提取方案的选择:准确称取5 g经搅碎的鱼肉样品(并做加标处理),分别加入10 mL酸化乙腈(2%甲酸)、盐酸(1 mol/L)、四丁基溴化铵(3 mol/L)和磷酸盐缓冲溶液(0.1 mol/L,pH 4.5)4种不同溶剂,涡旋混匀1 min后超声波(40 kHz, 50 W)提取10 min,再于10 000 r/min离心10 min 取上清液,重复提取3次。合并提取液,按上述SPE操作进行净化,洗脱液经氮吹浓缩至干后,残渣用0.2%的甲酸水溶液溶解后过0.22 μm滤膜供UPLC分析。
1.3.3 方法评价
(1) 添加回收试验和重复性试验:按照表2所示A、B、C 3组不同的添加水平,在空白基质鱼肉中添加标准溶液,每个添加水平重复3次,同时做空白试验。按照所优化的方案进行前处理,再用所建立的UPLC方法检测氟喹诺酮药物的含量。用添加回收率评价方法的准确度,用多次检测的添加回收率相对标准偏差(RSD)评价方法的精密度。
(2) 最低检出限和最低定量限试验:参照美国EPA标准中规定的单浓度重复试验方法进行最低检出限和最低定量限的测定[15]。
1.3.4 市售水产样品中6种氟喹诺酮药物的检测 按照1.3.1 和1.3.2所优化的色谱方法和前处理方法,分别对某超市采购的草鱼、鳊鱼、鲫鱼、黄骨鱼进行氟喹诺酮类药物检测。
2 结果与分析
2.1 6种氟喹诺酮类药物UPLC分析条件的优化及标准曲线建立
氟喹诺酮类药物结构上有羧基和哌嗪基,具有酸碱两性,又由于分子结构相似,给液相色谱分离带来一定的难度。根据国内外相关文献[11-14]报道,为防止色谱峰拖尾,通常选用酸性溶液如柠檬酸、乙酸铵、乙腈、甲醇、三乙胺等多种配比作为流动相。在本试验条件下,尝试采用多种流动相配比和流速。最终结果表明:以体积比为93∶7的0.05 mol/L 柠檬酸+0.1 mol/L 乙酸铵缓冲液-乙腈为流动相,流速为0.42 mL/min 时,在Waters Acquity UPLC®BEH C18柱(1.7 μm, 2.1 mm×50.0 mm)上10 min内将6种氟喹诺酮类药物有效分开(图1),与传统的HPLC方法相比,检测效率明显提高。以此色谱条件,分析1.3.1中氟喹诺酮系列浓度的混合标准溶液,得到6种氟喹诺酮药物的标准曲线方程、决定系数R2和线性范围见表3。
2.2 水产品中6种氟喹诺酮药物检测前处理方案的建立
2.2.1 固相萃取小柱的效果验证 固相萃取柱应用效果的影响因素除填料类型外,也包括填料的粒径以及填料装填的紧密程度等,因此不同品牌的同一类型固相萃取柱也可能会产生不同的效果。本研究用标准溶液作为模拟样品,对所选用的Cleanert PEP-2固相萃取小柱进行了有效性验证。结果表明,上样过柱液、淋洗液中均未检出6种氟喹诺酮,而洗脱液中6种氟喹诺酮类药物的含量与预期基本相符,回收率为95.9%~100.7%(表4),说明选用的固相萃取柱有效。

表2 添加回收试验中6种氟奎诺酮类药物的 添加水平设置Table 2 Spiking levels of six fluoroquinolones in recovery test μg/kg

诺氟沙星、氧氟沙星、环丙沙星、洛美沙星浓度为160 ng/mL;培氟沙星浓度为40 ng/mL;恩诺沙星浓度为80 ng/mL

图1 6种氟喹诺酮类药物标准品的液相色谱图Figure 1 UPLC chromatogram of six kinds of fluoroquinolones standard表3 6种氟喹诺酮类药物的标准曲线方程和线性范围Table 3 Standard curve equation and linear range of six kinds of fluoroquinolones
表4固相萃取过程中各部分收集液中6种氟喹诺酮类药物的含量及回收率†
Table 4 Concentration and recovery of six kinds of fluoroquinolones in different part of solution during SPE process (n=3)

药物名称含量/(ng·mL-1)上样过柱液a淋洗液洗脱液b回收率/%诺氟沙星未检出未检出166.77100.1氧氟沙星未检出未检出159.9095.9环丙沙星未检出未检出164.5698.7培氟沙星未检出未检出162.2297.3洛美沙星未检出未检出167.88100.7恩诺沙星未检出未检出161.1496.7
† a. 将2 mL浓度均为500 ng/mL的混合标准溶液用磷酸盐缓冲液稀释至10 mL作为模拟样品进行上样; b. 洗脱液体积为6 mL。
2.2.2 提取方案的选择 样品前处理过程中不同的提取剂的提取能力有很大差异,目前常用的提取剂主要有酸性乙腈[16]、磷酸盐缓冲液[17]、盐酸[18]、二氯甲烷[19]等水溶液或有机溶剂。为了最大效率提取样品中6种氟喹诺酮类药物,本研究比较了酸化乙腈(2%甲酸)、盐酸(1 mol/L)、四丁基溴化铵(3 mol/L)和磷酸盐缓冲液(0.1 mol/L,pH=4.5) 4种提取溶剂的提取效果,结果见表5。使用酸化乙腈提取时,样品蛋白质极易快速沉淀,造成待测物包裹损失,提取效果不佳;使用1 mol/L的盐酸溶液提取时,提取液中脂肪和蛋白质等杂质含量较高,后续净化过程中易堵塞固相萃取柱;而四丁基溴化铵和磷酸盐缓冲液提取时效果较好。综合考虑,选用磷酸盐缓冲溶液(pH 4.5)作为最终的提取溶剂。
2.3 方法评价
在确定UPLC分析条件和水产品中6种氟喹诺酮药物提取、净化等前处理方案的基础上,本研究进一步对整套检测方法的准确度、精密度和灵敏度进行了评价,结果见表6。由表6可知,6种氟喹诺酮药物的添加回收率为63.69%~90.83%,最低检出限为0.5~1.8 μg/kg,相对标准偏差均低于10%,表明方法的准确度、精密度和灵敏度均符合GB/T 27404—2008《实验室质量管理规范食品理化检测》的相关要求。
2.4 市售鱼样品中6种氟喹诺酮药物的检测
按照1.3.1和1.3.2所优化的色谱方法和前处理方法,对常德市区某超市出售的草鱼、鳊鱼、鲫鱼、黄古鱼4种水产品进行了6种氟喹诺酮类药物残留的检测,相关色谱图见图2。结果表明:诺氟沙星、氧氟沙星、环丙沙星、培氟沙星、洛美沙星5种禁用药物在4种水产品中均未检出;恩诺沙星在草鱼、鳊鱼、鲫鱼中有检出,黄古鱼中未检出,其中草鱼中的残留量低于检测方法的最低定量限,鳊鱼和鲫鱼的残留量分别为5.158,7.083 μg/kg,也均低于恩诺沙星在水产品肌肉中的最大残留限量(100 μg/kg)。

表5 不同提取剂提取效果的比较Table 5 Comparison of extraction effects of different extractants

表6 水产品6种氟喹诺酮类药物检测分析方法准确度、精密度和灵敏度评价结果Table 6 The accuracy, precision, and sensitivity of the analysis methods for 6 kind of fluoroquinolones in aquatic products (n=3)
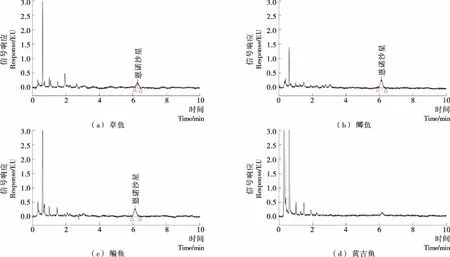
图2 4种鱼中氟喹诺酮类药物残留检测色谱图Figure 2 UPLC chromatogram of fluoroquinolones determination in grass carpa
3 结论
本研究基于固相萃取(SPE)和超高效液相色谱(UPLC)建立了水产品中的6种氟喹诺酮药物残留的检测方法,并利用该方法对4种常见的市售水产品进行了分析。结果表明,该方法的前处理过程简单有效,上机分析过程较传统的HPLC分析耗时明显缩短(10 min即可完成分析);灵敏度明显提高(最低检出限为0.5~1.8 μg/kg);准确度和稳定性符合检测要求,添加回收率为63.69%~90.83%,相对标准偏差均低于10%。综合说明,该方法有望为氟喹诺酮类药物标准分析方法的建立提供借鉴和参考。

