HRCT在间质性肺疾病诊断中的应用价值
余世勇 李新伟 彭燕
间质性肺疾病(interstitial lung disease, ILD)是由多种原因引起的以肺间质弥漫性渗出、浸润和纤维化为主要病理改变的一种临床综合征[1]。有学者统计间质性肺疾病的病因多达170多种疾病,因为ILD的发病原因、临床特征、治疗和预后都各不相同,进行准确的临床诊断较为困难[2]。而高分辨率CT(high resolution CT, HRCT)检查能够清楚显示肺的次级肺小叶水平,可以精确的显示病变的分布范围和某一些特征性表现,确定病变是否具有活动性,在HRCT的指导下可显著提高ILD的确诊率[3]。随着对ILD的HRCT表现和与之对应的病理生理学变化之间关系的进一步研究,人们逐渐认识到HRCT对于这类疾病的诊断具有重要作用。
资料和方法
一、一般资料
选择第三军医大学新桥医院2013年2月至2016年11月收治的ILD患者50例。其中男性28例,女性22例,年龄 38~80岁,平均年龄为(60.28±11.25)岁,病程30 d至18年。主要临床表现:咳嗽、咳痰、胸闷、气喘、进行性呼吸困难,发绀、杵状指、胸部可闻及湿啰音。常规检查:血沉、血常规、肝功能、肾功能、肺功能、肿瘤标志物、降钙素原、C-反应蛋白等。
二、检查方法
所有患者都先摄取X线片,然后采用GE 64排128层Light Speed螺旋CT(VCT) 机行HRCT检查,所有患者取头先进仰卧位,于吸气后屏气扫描,扫描范围从肺尖至肺底行HRCT扫描。扫描层厚2.5 mm,层距5 mm螺旋间隔扫描; 扫描参数: 管电压 120 KV,管电流280 mA,螺距1.375︰1,FOV 350 ~ 400 mm,高分辨重建算法,肺窗观察,窗宽 1 000 HU,窗位 -700 HU。
结 果
ILD在X线胸片上病变多位于中下肺野,早期呈磨玻璃样,周边肺野常见播散性结节影,多发环状影。晚期呈典型弥漫性线条状、结节状、云絮状、网状阴影、肺容积缩小,无肺门淋巴结肿大。ILD在HRCT的基本表现:根据ILD在行HRCT检查后所得的图像按照形态学大体可以分为两类: ①表现为密度增高影,包括异常线状影、网格状影、结节影、磨玻璃影以及实变影;②表现为密度减低影,包括囊状影、蜂窝影。
50例肺间质疾病患者的病变均呈弥漫性分布,以两肺中外带、胸膜下为主,病灶自肺尖向肺底逐渐加重,两肺基底病变更加明显,多为双侧病变。在HRCT的检查结果中显示50例患者的HRCT的阳性表现见表1。肺间质性病变HRCT图像特征,见图1。
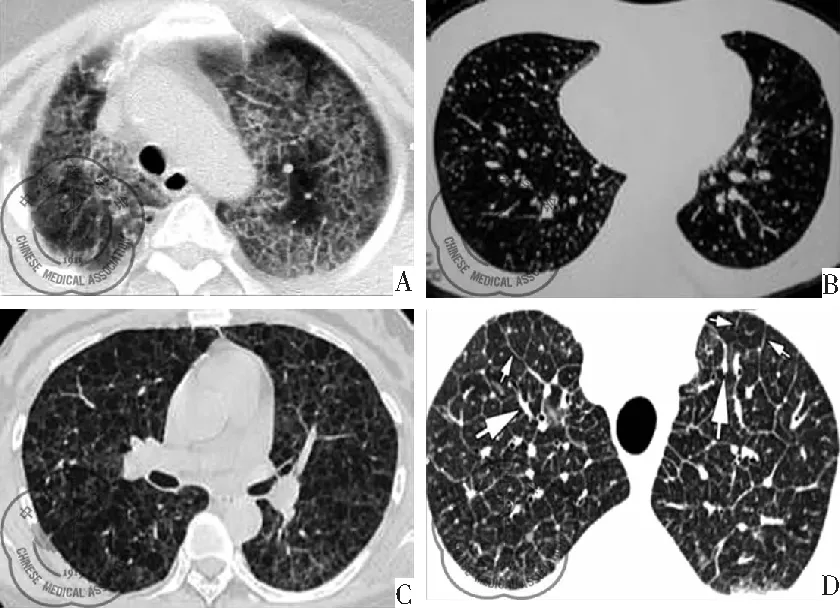
图1 肺间质性病变HRCT图像特征;注:A:HRCT显示双肺呈磨玻璃影改变;B:HRCT显示双肺多发小结节影;C:HRCT显示双肺呈弥漫性囊性阴影;D:HRCT显示双肺小叶间隔增厚
讨 论
ILD是一种主要累及肺间质、肺泡、和细支气管的肺部弥漫性疾病,临床主要表现为渐进性劳力性气促、限制性通气功能障碍伴弥散功能降低、低氧血症和影像学上的双肺弥漫性病变[3]。病程多发病隐匿,缓慢进展,预后不良。而早期诊断和尽早干预是改善预后的关键。随着影像学技术的不断发展,特别是HRCT运用到临床当中,对ILD的HRCT表现有更加深刻的认识,对ILD的确诊有很大的提高,能够使一部分ILD患者避免肺活检,因此了解HRCT下ILD的基本表现形式,对于ILD的判断和分析,临床诊断ILD起着非常重要的作用[4]。

表1 肺间质性病变HRCT图像特征及HRCT图像描述(n=50)
ILD呈慢性进展进性行加重,为肺部疾病中的疑难重症[6]。晚期出现肺动脉高压的原因和高血压不同。一般认为肺动脉高压的原因是肺小动脉痉挛,但从患者的临床表现推测应该是肺毛细血管通透性障碍所致[7]。正常人的肺泡区总面积约100平方米,大约相当于一个网球场大小,担负着全身的氧和二氧化碳的交换作用。它的通过能力和全身其它组织器官毛细血管的通过能力应该是平衡的。无论是肺泡炎还是纤维化,这种弥散性损害使肺泡的毛细血管的通透能力下降,从右心室泵出的血液不能顺利通过肺泡完成气体交换,打破了小循环和大循环血量的平衡,致使肺动脉压力增高,严重时可发展为右心室衰竭[8]。目前肺间质病变早期诊断的方法如下:
1. 高分辨率CT: 鉴于X线检查对ILD不敏感,约80%的ILD被胸部X线片漏诊,用更敏感和更特异的检查来提高ILD早期诊断非常必要。近年来最重要的进步是将HRCT列为诊断ILD的首选检查,其敏感性高达80%,并可根据HRCT的不同表现对ILD进行影像分型如蜂窝样变、磨玻璃样变、网格影及实变影等,由此推断其相应的病理分型,帮助临床选择治疗方案和评估预后[9]。
2. 肺功能检查: 用力肺活量(forced vital capacity, FVC)和一氧化碳弥散度(carbon monoxide diffusing capacity, DLCO)是检查ILD不可或缺的项目,它对早期病变的发现甚至较HRCT更敏感,缺陷是不够直观。对于病理类型相同的ILD而言,肺功能的差异反映着预后的不同,即肺功能越差预后越差,经治疗后肺功能好转,患者生存期也随之提高。所以监测肺功能不但可以有效地判断患者的预后,而且也能帮助评估治疗反应。
3. 肺组织活检: 病理是诊断ILD的金标准。虽然CT和肺功能检查可使大部分ILD患者确诊,但仍有一些患者缺少特异性的临床征象,仍需要肺活检方能正确诊断[10]。经典的开胸肺活检创伤较大,患者不易接受,临床很少开展;胸腔镜肺活检很少引起开胸肺活检常见的急性并发症,同时取材满意,是目前最推荐的方法;CT引导下经皮肺穿刺损伤更小,能预先确定和调整进针的角度及深度,具有较高的安全性[11],但取材不够多,其应用价值尚有争议。
4. 炎性因子的检测: 转化生长因子(transforming growth factor-β, TGF-β)、络氨酸激酶(tyrosine kinases, c-Abl)、血清肺表面活性蛋白(pulonary surface acfive protein-A, PSAP-A)、SP-D及小窝蛋白-1(caveolin-1)等众多的炎性因子参与了ILD发病,它们都是影响反映肺纤维化的重要生物标记物,这些炎性因子的测定可帮助ILD的诊断,特别是多个因子联合检查符合率明显优于单个指标的应用。
ILD的早期诊断还有赖于详细的职业接触史、发病经过、伴随症状、既往病史和治疗经过等重要线索。职业性的粉尘接触可以在10~20年后才出现ILD的症状。而在风湿病,可以先有ILD,然后出现关节或其他器官的病变;也可以先有风湿病的其它病变,再出现ILD的临床表现[12]。易出现ILD的风湿病有类风湿关节炎、干燥综合征、系统性硬化症、炎性肌病、混合性结缔组织病、系统性红斑狼疮、结节性多动脉炎、Wegener肉芽肿等,对于这类患者必要时行HRCT检查可尽早明确有无肺间质病变的发生。
目前作为肺间质疾病诊断的首选检查方法为HRCT。HRCT重建成像可显著提高空间分辨率,能更好地显示肺部微细病变和解剖结构获取更多的诊断信息。临床医师怀疑是ILD,对患者都应该进行HRCT检查[13]。肺活检对肺间质性病变的确诊率高,尤其是开胸肺活检的确诊率可高达 90%~100% ,所以肺组织活检的病理诊断被称为诊断的“金标准”,但是由于其具有一定风险,且可出现并发症,故不易为患者所接受[14]。影像学检查是目前诊断ILD的首要检查手段,HRCT 因其分辨率高,扫描层面影像不重叠,作为一种简便无创性手段,容易为患者所接受。HRCT 对肺组织的检查能够达到次级肺小叶水平,能够很好地显示肺组织的细微结构、肺内细小病变,为肺部间质性病变的诊断及鉴别提供了更多的影像信息,是分辨肺部组织微细结构最敏感的无创性方法[15-16]。HRCT为间质性肺部疾病的诊断提供了重要的工具,因此大多数具有典型临床症状及 HRCT 表现的间质性肺间质疾病患者几乎可以不需要进一步的病理学检查即可作出明确诊断。HRCT 薄层扫描和骨算法重建,能优化显示肺微细结构供应肺小叶的气道、血管及小叶间隔,能在小叶水平上认识肺解剖微细结构,而X线胸片很难诊断尘肺早期肺间质改变。HRCT 对肺内弥漫小结节的形态、大小、密集度、弥漫性肺气肿、肺间质纤维化的各种改变和淋巴结肿大与钙化及胸膜改变的显示能力明显优于 X线平片和常规CT[17]。由于HRCT 扫描技术是在常规 CT 的基础上利用了薄层扫描和高分辨率重建技术,具有良好的空间分辨率,使图像显示更清晰,更有利于准确判断病变的范围和性质,在肺间质性病变的诊断上具有很高的临床价值[18]。因此,对肺间质性病变的诊断,应大力推广HRCT 扫描技术的临床运用。
参 考 文 献
1 任成山, 钱桂生. 特发性间质性肺炎的现代概念及研究进展[J/CD]. 中华肺部疾病杂志(电子版), 2010, 3(4): 276-284.
2 Loring WE. Small airway disease in the pathogenesis of pulmonary emphyse ma[J]. J Maine Med Assoc, 1967, 58(5): 95-101.
3 Mc Donough JE, Yuan R, Suzuki M, et al. Small-airway obstruction and emphy semin chronic obstructive pulmonary sease[J]. N Engl J Med, 2011, 365(17): 1567-1575 .
4 Manoharan A, Anderson WJ, Lipworth J, et al. Small airway dysfunction is associated with poorer asthma control[J]. Eur Respir J, 2014, 44(5): 1353-1355.
5 刘建东, 廖强, 李建国, 等. 肺部磨玻璃密度影的CT诊断与鉴别诊断[J]. 中国当代医药, 2011, 18(13): 94-97.
6 刘巨涛, 于书奎. 高分辨CT在肺部检查中的应用价值[J]. 中国实用医药, 2010, 5(8): 66-67.
7 王建军, 吕群, 冯哲敏, 等. 以肺间质性改变为影像学表现的肺结核33例分析[J]. 现代实用医学, 2013, 25(1): 24-25.
8 马锦秀, 毛家仁, 李捷. 肺部磨玻璃影的胸部X线与CT分析[J]. 实用医学影像杂志, 2002, 3(4): 248-250.
9 张晓荣, 唐震. HRCT结合免疫组织化学对间质性肺疾病分期的初步研究[J]. 临床放射学杂志, 2007, 26(9): 872- 875.
10 陈炽贤. 高分辨率CT对间质性肺疾病的诊断价值[J]. 中华结核和呼吸杂志, 1999, 22(1): 25-26.
11 樊娜, 史红阳, 李维, 等. CT引导下经胸壁肺活检在肺癌精准治疗中的临床应用[J/CD]. 中华肺部疾病杂志(电子版), 2017, 10(5): 521-524.
12 Webb WR. Radiology of obstructive pulmonary disease[J]. Am J Roentgenol, 1997, 169(3): 637-647.
13 修建军, 李轶忻, 崔允峰. 间质性肺疾病的高分辨CT(HRCT)诊断[J]. 医学影像学杂志, 2004, 14(7): 585-588.
14 臧丽莉. 高分辨率CT检查技术在诊断小儿慢性肺间质病变中的应用价值研究[J]. 当代医药论丛, 2017, 15(9): 136-137.
15 吴晓华, 马大庆, 张淑红, 等. 特发性肺间质纤维化的早期HRCT表现及其病理基础探讨[J]. 医学影像学杂志, 2014, 24(10): 1734-1737.
16 吴东, 袁亚连, 陈敏, 等. 特发性肺纤维化患者诱导痰中SDF-1的表达与高分辨CT表现的相关性研究[J/CD]. 中华肺部疾病杂志(电子版), 2017, 10(3): 296-299.
17 李燕北, 李云秀, 王宝军, 等. 小剂量多层螺旋CT(MSCT)VHRCT在小儿慢性肺间质病变中的诊断价值[J]. 世界最新医学信息文摘, 2016, 16(47): 23-24.
18 马大庆, 李铁一, 关硕生, 等. 肺间质疾病的高分辨率CT表现及其病理基础和诊断意义[J]. 中华放射学杂志, 1999, 33(2): 101-105.

