决奈达隆的特性和应用进展
李洪仕 万征
决奈达隆(dronedarone)是新型Ⅲ类抗心律失常药,由法国赛诺菲 · 安万特公司开发,于2009年相继在美国和欧洲上市。其化学结构类似胺碘酮(乙胺碘呋酮胺碘酮)但不含碘,既有与胺碘酮相似的电生理作用,又摒除了碘相关不良反应,因而备受推崇。然而,随着临床试验结果的不断报告,曾为人们看好的决奈达隆治疗慢性心力衰竭(心衰)和急性心肌梗死的探索提前终止。其适应证仅限于心房颤动(房颤)转复之后窦性心律的维持。当下决奈达隆的路在何方仍然备受关注。
1 决奈达隆的化学结构和药理学特点
1.1 分子结构
决奈达隆的分子式为C31H44N2O5S,相对分子质量为593.22,其化学名为 N-[2-丁基 -3-[4-[3-(二丁氨基)丙氧基]苯基]-5-苯并呋喃基]-甲烷磺酰胺盐酸盐,有着与胺碘酮相似的化学结构,二者同属苯并呋喃衍生物;不同之处在于决奈达隆的苯环上不含碘,却增加了甲基磺胺基团(图1)。
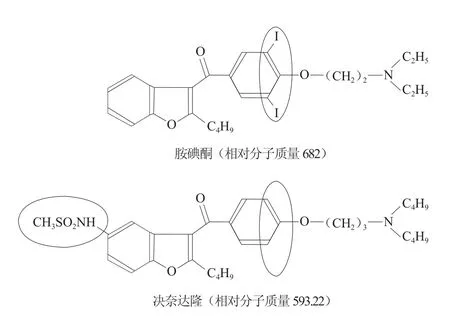
图1 决奈达隆与胺碘酮的分子结构[1]
1.2 药动学
决奈达隆的口服吸收率为70%~100%,存在肝首过效应,口服生物利用度为15%,膳食脂肪可增加其生物利用度(高脂增加3~4.5倍,低脂增加2~3倍)[2-3]。在体内,口服决奈达隆主要由肝细胞色素氧化酶(CYP)450 3A4代谢,其主要代谢产物为N-去叔丁基代谢产物(SR35021,活性代谢产物,但其活性比决奈达隆弱3~10倍,与血浆蛋白的结合率超过98%)和氧化N-去氨基代谢产物(SR90154,非活性代谢产物)[4]。决奈达隆的血浆蛋白结合率为99.7%,其稳态分布容积(volume of distribution at steady-state, Vss)为1200~1400 L,在 400 mg、每日2次的推荐剂量下,其达峰时间(Tmax)为3~6 h,达稳态血浆浓度(84~167 ng/mL)需 4~8 d(平均 7 d)[2,5],稳态终末半衰期(steady state terminal half-lifes, t1/2z)为 27~31 h[4]。决奈达隆主要经粪便排出(约84%),其次经肾排出(约6%),其清除半衰期为13~19 h[4],明显短于胺碘酮,同时由于亲脂性也较胺碘酮低,因而较少出现组织蓄积。
1.3 心电生理特性
与胺碘酮相似,决奈达隆亦为多通道的抑制剂,对钠、钾、钙离子通道和β受体等均有抑制作用,且同等效应下的剂量低于胺碘酮(表1)。动物实验表明,决奈达隆可延长心肌动作电位时程,减慢房室传导速率和窦性心律;有明显的负性肌力作用,实验中在心输出量不变的情况下可增加左心室舒张末期压力,但不会改变左心室射血分数(left ventricular ejection fractions, LVEF)或缩短分数[2,6]。
1.4 不良反应[7-8]
区别于胺碘酮,决奈达隆由于不含碘基且组织蓄积少,故无碘相关的肺毒性、眼毒性和甲状腺毒性,并能减少神经病变;其主要不良反应是引起心动过缓和QT间期延长,但尖端扭转型室性心动过速罕见。与胺碘酮相似,决奈达隆会抑制肾小管分泌肌酸酐,从而增加血肌酸酐水平,但却不会降低肾小球滤过率。由于早期有严重肝损伤的报道,因此,在临床上应用决奈达隆时要求定期检测肝酶,特别是起始治疗的6个月内。
1.5 药物间相互作用[1,8]
凡经CYP3A4、CYP2D6和P-糖蛋白代谢和转运的药物,均可与决奈达隆产生相互作用(表2),这是因为决奈达隆不仅是CYP3A4的底物,同时也是CYP2D6和P-糖蛋白的抑制剂。最新动物实验表明,与洋地黄联合应用时,决奈达隆和胺碘酮均可增加心室易损性,而前者更为明显[9]。此外,由于决奈达隆可延长QT间期,故当其与大环内酯类抗生素、吩噻嗪类药物、三环类抗抑郁药、美沙酮、西沙必利等合用时,可能会增加尖端扭转型室性心动过速风险,故应避免联合应用。
2 循证医学:决奈达隆临床证据之路
房颤是常见的心律失常,严重威胁人类健康,维持窦性心律、控制心率和抗凝仍是三项主流治疗原则。在药物中,胺碘酮疗效显著,但因心脏外不良反应,长期应用受限。作为胺碘酮结构类似药,人们期待决奈达隆能够保留良好的抗心律失常作用,同时进一步降低不良反应。

表1 决奈达隆和胺碘酮的电生理作用比较[2,6]

表2 与决奈达隆相互作用的药物
2.1 在安慰剂对照的疗效验证试验中初露锋芒
2003年,DAFNE研究[10]指出决奈达隆800 mg/d是房颤复律后维持窦性心律安全、有效的最佳剂量。该研究入选了199例电复律成功的持续性房颤患者,分为决奈达隆组(依剂量分3组,分别为800 mg/d、1200 mg/d与1600 mg/d,连续给药)和安慰剂组。结果显示,决奈达隆800 mg/d系维持窦性心律的最佳剂量,其房性心律失常复发的中位时间为60 d(安慰剂组仅为5.3 d),剂量增加并不提高疗效;随访6个月时,决奈达隆800 mg组35%患者维持窦性心律,优于安慰剂组(10%);因胃肠道不良反应提前停药的受试者在决奈达隆1600 mg组和800 mg组分别为22.6%和3.9%,而药物致QT间期延长者仅见于决奈达隆1600 mg组,未观察到甲状腺、眼或肺毒性事件。
2007年,EURIDIS研究和ANDONIS研究将上述结论进一步推广至除永久性房颤以外的其他类型房颤和心房扑动(房扑)患者。这是同期进行的两个独立的多中心、双盲、随机对照试验,依人群分布可分别简称欧洲试验和非欧洲试验,总共1237例患者,分为决奈达隆组(400 mg 、每日2次)和安慰剂组。结果显示,两组房颤或房扑复发中位时间,在欧洲试验中分别为96 d和41 d(P=0.01),在非欧洲试验中分别为158 d和59 d(P=0.002);复发患者的心室率,在欧洲试验中分别为(102.3±24.7)次/min和(117.5±29.1)次/min(P<0.001),在非欧洲试验中分别为(104.6±27.1)次 /min 和(116.6±31.9)次 /min(P< 0.001)[11]。因此,决奈达隆不仅能够有效维持窦性心律,而且可以降低房颤或房扑复发时的心室率。
2008年,ERATO试验[12]将研究范围锁定为永久性房颤,旨在评估决奈达隆在标准治疗基础上控制心室率的有效性。174例患者随机接受决奈达隆(400 mg、每日2次)或安慰剂治疗。结果显示,与安慰剂相比,在服药14 d时,决奈达隆组24 h平均心室率降低11.7 次/min(P<0.0001),并在6个月试验期间持续;同时,决奈达隆组最大运动心率平均降低24.5 次/min(P<0.0001),且不伴运动耐量下降。因此,在β阻滞药、钙拮抗剂和地高辛等治疗基础上,决奈达隆能进一步改善永久性房颤患者的室率控制。
2.2 在与胺碘酮的较量中忧喜参半
2010年,DIONYSOS试验[13]对比了胺碘酮和决奈达隆治疗持续性房颤患者的有效性和安全性。504例未曾应用胺碘酮的患者,随机分入决奈达隆组(400 mg 、每日2次,249例)或胺碘酮组(600 mg、每日1次,维持28 d,后200 mg、每日1次, 255例)。主要复合终点是房颤复发或研究早期中止,主要安全终点是出现各种不良事件,或不良事件致早期停药。随访12个月,决奈达隆组和胺碘酮组主要复合终点分别是75.1%和58.8%(P< 0.0001),其中房颤复发分别为63.5%和42.0%,早期停药在决奈达隆组更少(分别10.4%和13.3%);两组主要安全终点分别为39.3%和44.5%(P=0.129),其中决奈达隆组甲状腺、神经、皮肤和眼部事件更少。因此,决奈达隆在降低房颤复发方面稍逊于胺碘酮,但其安全性更好。
2.3 在改善预后研究登峰后铩羽而归
Ⅲ类抗心律失常药具有多通道阻断和β受体阻断作用,故在理论上可以减少心衰患者发生恶性室性心律失常的比率,并进一步降低心源性猝死发生率。早期的EMIAT研究[14]将胺碘酮用于心肌梗死后的心功能不全患者,结果全因死亡率并未降低,而心律失常死亡率却下降了35%。参照EMIAT研究,ANDROMEDA研究[15]将决奈达隆用于新发或未完全控制的不稳定心衰患者(NYHA心功能分级Ⅲ~Ⅳ级),预期随访2年。结果在首位患者入组7个月后,该研究便因决奈达隆组死亡率明显高于安慰剂组而提前终止。
在对重度和不稳定心衰患者的探索折戟之后,ATHENA研究[16]将决奈达隆的研究人群限定在NYHA分级Ⅳ级之外的阵发性或持续性房颤和房扑患者,其入选标准为年龄≥70岁且至少合并下列一项危险因素:≥2类降压药物控制的高血压病、糖尿病、既往卒中或短暂性脑缺血发作、体循环栓塞、左心房内径≥50 mm或LVEF≤40%(后因死亡人数小于预期而加入年龄≥75岁的人群)。该研究亦分为决奈达隆组(400 mg、每日2次)和安慰剂组,主要终点为首次因心血管病住院或全因死亡。共4628例患者入选,其中心衰患者979例(21.2%),NYHA分级Ⅱ级779例(17.1%),NYHA分级Ⅲ级者200例(4.4%);具备LVEF测量值 4544例(98.2%),LVEF<35% 179例 (3.9%),LVEF <45% 540例(11.9%)。在平均随访(21 ± 5)个月后,决奈达隆组和安慰剂组主要终点发生率分别为31.9%和39.4%(风险比为0.76,P<0.001);全因死亡率分别为5.0%和6.0%(风险比0.84,P=0.18);心血管病死亡率分别为2.7%和3.9%(风险比0.71,P=0.03),但主要原因是决奈达隆降低了心律失常死亡率。在安全性方面,与安慰剂相比,决奈达隆组心动过缓、QT间期延长、恶心、腹泻、皮疹和血清肌酸酐升高的发生率较高;而两组甲状腺和肺相关不良事件的发生率差异无统计学意义。至此,作为抗心律失常药物,决奈达隆第一次得出经临床研究证实能够改善心血管病终点事件的结果,但其适用范围是NYHA分级Ⅳ级之外的阵发性或持续性房颤和房扑患者。该研究并未在纳入的NYHA分级Ⅱ~Ⅲ级患者中针对决奈达隆是否安全有效作出确切说明,这可能是欧美指南未将其列入的原因之一。
在ATHENA研究的基础之上,PALLAS试验[17]进一步在高危永久性房颤患者中探索决奈达隆对终点事件的改善作用——即将入选标准限定为年龄≥65岁,且合并下列至少一项高危因素:冠心病、既往卒中或短暂性脑缺血发作、症状性心衰(NYHA分级Ⅱ~Ⅲ级症状,且早年曾因心衰入院)、LVEF≤40%、外周动脉疾病或年龄≥75岁并同时合并高血压病和糖尿病。同时将主要联合终点设定为卒中、心肌梗死、体循环栓塞或心血管病死亡。研究计划入选10 800例患者,但在入选3236例患者后,因安全原因于2011年被迫提前中止。结果显示,研究终止前入选患者中LVEF≤40%占20.7%,决奈达隆组和安慰剂组分别有43例和19例达到主要联合终点(风险比2.29,P=0.002);心血管病死亡患者分别为21例和10例(风险比 2.11,P=0.046),其中心律失常死亡分别为13例和4例(风险比3.26,P=0.03);卒中患者分别为23例和10例(风险比2.32,P=0.02);因心衰入院患者分别为43例和24例(风险比1.81,P=0.02)。因此,决奈达隆并不适用于伴有高危因素的永久性房颤患者。
3 精准医疗时代的新探索
3.1 房颤合并冠心病
房颤合并冠心病患者在选用抗心律失常药物时应警惕发生药物相关的致命性心律失常风险。为评估在阵发或持续性房颤合并冠心病患者中,决奈达隆应用的安全性和心血管病预后,研究人员对ATHENA研究进行了事后分析,将1405例合并冠心病的亚组患者随机分入决奈达隆组(400 mg 、每日2次, 668例)和安慰剂组(737例),继续随访2.5年,主要终点为首次因心血管病入院或全因死亡。结果,决奈达隆组和安慰剂组主要终点发生率分别为38%和47%(P=0.0002),两组急性冠状动脉综合征患者的例数分别为42例和 67例(P=0.04)[18]。由此可见,决奈达隆在合并冠心病的房颤患者中同样可以发挥其心血管保护作用,不过也同样受限于ATHENA研究的入选标准。
3.2 与雷诺嗪联合治疗阵发性房颤
房颤机制涉及心房多种离子通道和受体的变化,而让单一药物既阻滞多种通道,又兼顾安全性则难以实现,于是人们便开始探索多药物联合策略。HARMONY研究[19]正是在这样的背景下进行的,旨在探索雷诺嗪(具有晚钠电流抑制作用)联合决奈达隆治疗阵发性房颤的疗效。这两种药物在钠通道阻滞方面具有协同效应;而低剂量决奈达隆不会阻滞钙通道,进而降低了负性肌力效应。该研究共纳入134例阵发性房颤患者,且均有指征植入双腔起搏器,故能持续评估房颤负荷;分为安慰剂组、雷诺嗪组(750 mg、每日2次)、决奈达隆组(225 mg、每日2次)和2个联合治疗组,即应用雷诺嗪(750 mg、每日2次)联合决奈达隆(150 mg 、每日2次和225 mg 、每日2次)两种剂量,治疗12周。结果与安慰剂组相比,雷诺嗪组和决奈达隆组房颤负荷均未见下降;而2个联合治疗组的房颤负荷却分别下降了43%和59%(分别P=0.072和P=0.008,前者呈下降趋势),且患者均能较好耐受。由此可见,雷诺嗪联合低剂量决奈达隆可安全、有效地减少房颤负荷。
为了解释上述现象,Hartmann等[20]利用人类心房肌细胞进行膜片钳研究,发现联合用药(雷诺嗪5 μmol/L,决奈达隆0.3 μmol/L)能更有效地抑制各种膜电流,特别是Na+和K+电流;同时能有效延长心房动作电位时程,且能使房颤节律下已经缩短的动作电位时程得到最大限度恢复;更有趣的是,决奈达隆本身并不引起房颤心肌细胞静息电位超极化,但他却可协助雷诺嗪引起细胞膜进一步超极化。此外,共聚焦显微镜还发现联合用药可有效抑制舒张期肌浆网Ca2+外流,减少异常电活动。这就进一步证实了人们最初构想的联合用药策略,为决奈达隆治疗房颤又开辟出一条新的探索之路。
4 指南对决奈达隆的评价
随着临床试验的延伸,决奈达隆的适应证也在不断调整(表3)。前期安慰剂对照试验使决奈达隆相继于2009年7月和12月在美国和欧洲上市。ANDROMEDA研究[15]使决奈达隆禁用于NYHA分级Ⅳ级或不稳定的NYHA分级Ⅱ~Ⅲ级患者。ATHENA研究[16]显示决奈达隆具有改善房颤/房扑患者预后的作用,但适用人群限定于伴有血栓栓塞危险因素的阵发性或持续性房颤/房扑患者。而PALLAS试验[17]又将决奈达隆排除在永久性房颤治疗的大门之外,因为它可能增加卒中、心血管病死亡和住院率的联合终点。在2014年美国心脏协会/美国心脏学会/美国心律学会(AHA/ACC/HRS)房颤患者管理指南中,决奈达隆的适应证最终被限定于无心衰的非永久性房颤患者节律和室率控制[8]。由于临床试验在冠心病患者中取得成功结果,2016年欧洲心脏病学会/欧洲胸外科学会(ESC/EACTS)房颤管理指南还将决奈达隆推荐用于不伴心衰的稳定性冠心病患者[21](表 3)。
5 小结与展望
决奈达隆最初作为胺碘酮的替代药物出现,其疗效略逊色于胺碘酮,但是不良反应小于胺碘酮;然而,在严格筛选的临床试验中,虽然改善了房颤患者的预后,但增加重度心衰和永久性房颤患者死亡率而处于“山穷水复疑无路”的境地。尽管如此,2014年AHA/ACC/HRS房颤患者管理指南[8]和2016年 ESC/EACTS房颤管理指南[21]仍推荐决奈达隆可以用于阵发性和持续性房颤或房扑患者维持窦性心律(尤其是门诊患者),推荐使用剂量为400 mg、每日2次(表3),不能用于NYHA分级Ⅲ~Ⅳ级心衰,或此前4周内有失代偿性心衰的患者,或永久性房颤患者;应用决奈达隆期间应关注心率、QT间期和肝功能。作为一种临床新药,决奈达隆要经历的真实临床实践验证的路还很长,在现在循证医学和精准医疗时代,更多更新的基础和临床数据将会为其开辟更多更细化的用武之地,由此可见,“柳暗花明又一村”是决奈达隆所历经兴衰之路的今天。

表3 指南对决奈达隆的评价
[1] Rosa GM, Bianco D, Parodi A, et al. Pharmacokinetic and pharmacodynamic profile of dronedarone , a new antiarrhythmic agent for the treatment of atrial fibrillation. Expert Opin Drug Metab Toxicol, 2014, 10(12):1751-1764.
[2] Patel C, Yan GX, Kowey PR. Dronedarone.Circulation, 2009,120(7):636-644.
[3] Patel PD, Bhuriya R, Patel DD, et al. Dronedarone for atrial fibrillation: a new therapeutic agent.Vasc Health Risk Manag,2009,5:635-642.
[4] European Medicines Agency.Assessment report for Multaq.[2009-09-24].http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/001043/WC500044538.pdf.
[5] European Medicines Agency: Withdrawal public assessment report of the marketing authorisation application for multaq.[2006-10-18].http://www.ema.europa.eu/docs/en_GB/document_library/Application_withdrawal_assessment_report/2010/01/WC500069271.pdf.
[6] Heijman J, Heusch G, Dobrev D. Pleiotropic effects of antiarrhythmic agents: dronedarone in the treatment of atrial fibrillation. Clin Med Insights Cardiol, 2013,7:127-140.
[7] Kozlowski D, Budrejko S, Lip GY, et al. Dronedarone: an overview. Ann Med, 2012,44(1):60-72.
[8] January CT, Wann LS, Alpert JS, et al.2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation: a report of the American College of Cardiology/American Heart Association Task Force on practice guidelines and the Heart Rhythm Society. Circulation, 2014,130(23):e199-e267.
[9] Frommeyer G, Puckhaber D, Ellermann C, et al. Interactions of digitalis and class-III antiarrhythmic drugs: Amiodarone versus dronedarone. Int J Cardiol, 2017,228:74-79.
[10] Touboul P, Brugada J, Capucci A, et al. Dronedarone for prevention of atrial fibrillation: a dose-ranging study.Eur Heart J,2003,24(16):1481-1487.
[11] Singh BN, Connolly SJ, Crijns HJ, et al. Dronedarone for maintenance of sinus rhythm in atrial fibrillation or flutter. N Engl J Med, 2007,357(10):987-999.
[12] Davy JM, Herold M, Hoglund C, et al. Dronedarone for the control of ventricular rate in permanent atrial fibrillation:the Efficacy and safety of dronedarone for the control of ventricular rate during atrial fibrillation (ERATO) study. Am Heart J, 2008,156(3):e1-e9.
[13] Le Heuzey JY, De Ferrari GM, Radzik D, et al. A shortterm, randomized, double-blind, parallel-group study to evaluate the efficacy and safety of dronedarone versus amiodarone in patients with persistent atrial fibrillation: the DIONYSOS study.J Cardiovasc Electrophysiol, 2010,21(6):597-605.
[14] Julian DG, Camm AJ, Frangin G, et al. Randomised trial of effect of amiodarone on mortality in patients with leftventricular dysfunction after recent myocardial infarction:EMIAT. European myocardial infarct amiodarone trial investigators. Lancet, 1997,349(9053):667-674.
[15] Køber L, Torp-Pedersen C, McMurray JJ, et al. Increased mortality after dronedarone therapy for severe heart failure. N Engl J Med, 2008,358(25):2678-2687.
[16] Hohnloser SH, Crijns HJ, van Eickels M, et al. Effect of dronedarone on cardiovascular events in atrial fibrillation. N Engl J Med, 2009,360(7):668-678.
[17] Connolly SJ, Camm AJ, Halperin JL, et al. Dronedarone in high-risk permanent atrial fibrillation. N Engl J Med, 2011,365(24):2268-2276.
[18] Pisters R, Hohnloser SH, Connolly SJ, et al.Effect of dronedarone on clinical end points in patients with atrial fibrillation and coronary heart disease: insights from the ATHENA trial.Europace, 2014,16(2):174-181.
[19] Reiffel JA, Camm AJ, Belardinelli L, et al. The HARMONY trial: combined ranolazine and dronedarone in the management of paroxysmal atrial fibrillation: mechanistic and therapeutic synergism.Circ Arrhythm Electrophysiol, 2015,8(5):1048-1056.
[20] Hartmann N, Mason FE, Braun I, et al. The combined effects of ranolazine and dronedarone on human atrial and ventricular electrophysiology. J Mol Cell Cardiol, 2016,94:95-106.
[21] Kirchhof P, Benussi S, Kotecha D, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS.Europace, 2016,18(11):1609-1678.
[22] MULTAQ (dronedarone) tablets [prescribing information].[2009-06-09].https://www.accessdata.fda.gov/drugsatfda_docs/label/2009/022425lbl.pdf
[23] European Medicines Agency. European Medicines Agency recommends restricting use of Multaq.[2011-09-22].http://www.ema.europa.eu/docs/en_GB/document_library/Press_release/2011/09/WC500112800.pdf.
[24] Camm AJ, Kirchhof P, Lip GY, et al. Guidelines for the management of atrial fibrillation: the task force for the management of atrial fibrillation of the European Society of Cardiology (ESC).Europace, 2010,12(10):1360-1420.
[25] Wann LS, Curtis AB, January CT, et al. 2011 ACCF/AHA/HRS focused update on the management of patients with atrial fibrillation (updating the 2006 guideline): a report of the American College of Cardiology Foundation/American Heart Association task force on practice guidelines.Circulation, 2011,123(1):104-123.
[26] Camm AJ, Lip GY, De Caterina R, et al.2012 focused update of the ESC Guidelines for the management of atrial fibrillation:an update of the 2010 ESC guidelines for the management of atrial fibrillation--developed with the special contribution of the European Heart Rhythm Association. Europace, 2012,14(10):1385-1413.

