普洱茶安全性毒理学评价研究概述
马燕,陈立佼,吕才有,赵明
云南农业大学龙润普洱茶学院,云南 昆明 650201
食品安全性毒理学评价是保障食品安全和国民健康的重要手段,也是评价某种食品安全性的重要指标。我国已针对不同食品制定了安全性毒理学的评价标准和技术规范,发展了相应的新方法和新技术,使得我国食品安全性毒理学评价整体水平从检验设备、人员素质,到检验的技术水平等均有显著的提高,并逐渐与国际接轨,在保障食品安全方面发挥了重要作用[1]。
我国现行的食品安全性毒理学评价程序和方法标准是由国家卫生和计划生育委员会制定并于2015年5月1日起实施的,一共包括26项[2],如《食品安全性毒理学评价程序》(GB 15193.1—2014)、《食品毒理学实验室操作规范》(GB 15193.2—2014)、《急性经口毒性试验》(GB 15193.3—2014)、《细菌回复突变试验》(GB 15193.4—2014)、《90天经口毒性试验》(GB 15193.13—2015)。标准规定了食品安全性毒理学评价程序,适用于评价食品生产、加工、仓储(或贮藏)、运输和销售过程所涉及的可能对健康造成危害的化学、生物和物理因素的安全性,检验对象包括食品及其原料、食品添加剂、新食品原料、辐照食品、食品相关产品(用于食品的包装材料、容器、洗涤剂、消毒剂和用于食品生产经营的工具、设备)以及食品污染物[3]。食品毒理学安全性评价试验内容包括急性经口毒性试验、遗传毒性试验、28 d经口毒性试验、90 d经口毒性试验、致畸试验、生殖毒性试验和生殖发育毒性试验、毒物动力学试验、慢性毒性试验、致癌试验、慢性毒性与致癌合并试验等[3]。
普洱茶加工的关键工序是一个多种微生物作用的自然发酵过程,微生物的发酵丰富了产品的内含成分与风味[4],也增加了一定的安全风险[5]。因此对普洱茶进行有效的安全性毒理学评价十分必要。基于此,自2003年起,西南大学的刘勤晋教授已开始了普洱茶毒理学研究[6]。笔者查阅中国知网、Pubmed,ACS Publications,ScienceDirect-Elsevier,Wiley 和Springer Link等国内外科技文献数据库,发现9篇中文、6篇英文论文和硕士、博士论文各1篇,以普洱茶或含普洱茶的食品为材料,开展了毒理学评价研究。
1 急性经口毒性实验
急性经口毒性试验(GB 15193.3—2014)是指1次或24 h内多次经口给予实验动物受试物后,动物短期内(一般观察7 d或14 d)出现的毒性效应。根据急性毒性的半数致死剂量(LD50),即能够引起动物死亡率为50%的受试物剂量,毒物分成5级(表1)[7]。
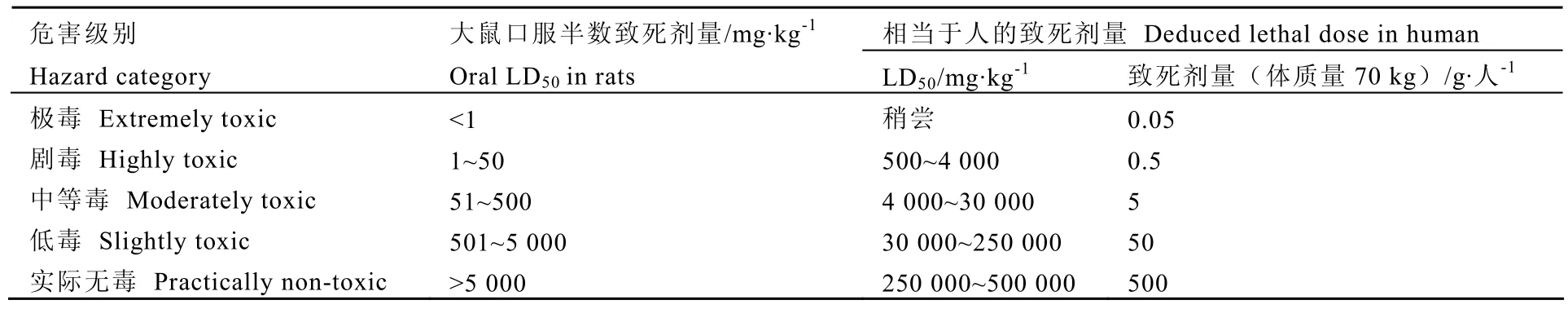
表1 急性毒性(LD50)剂量分级表Table 1 The classification of dose (LD50) in acute oral toxicity tests
刘勤晋等[6]、陈文品等[8-9]、龚加顺等[10]、陈娜等[11]、胡雪婷[12]、马伟光等[13]、Wang等[14]、梁名志等[15]和吴婧等[16]学者以大、小鼠为模型,研究市售普洱茶、普洱茶特征成分、配方普洱茶、人工接菌发酵普洱茶、抗氧化制剂(含普洱茶)的急性毒性,结果发现 LD50大于5 000 mg·kg-1,属于实际无毒级别。另外,Fujita等[17]研究显示,一次性摄入 2 000 mg·kg-1体质量的普洱茶提取物,小鼠无异常和死亡(表2)。
2 28 d或90 d经口毒性试验
28 d 经口毒性试验(GB 15193.22—2014),即通过实验动物连续 28 d经口接触受试物后引起的健康损害效应,用于评价受试物的短期毒性作用[18]。胡雪婷[12]开展28 d亚急性毒性试验,发现普洱生茶高剂量组和熟茶高剂量组肝脏组织切片出现轻微病理学改变,大鼠的进食量、体质量、临床症状、血液学指标、器官病理学观察、肾脏组织病理学检查无不良反应,初步认为普洱生茶与熟茶未观察到有害作用剂量分别为 2 500、5 000 mg·kg-1·d-1。Wang等[19]研究发现 2 500、5 000 mg·kg-1·d-1的普洱生茶提取物观测到了轻微毒性,而 5 000 mg·kg-1·d-1的普洱熟茶提取物未观察到任何不良反应,认为摄入 1 250 mg·kg-1·d-1剂量的普洱生茶和 5 000 mg·kg-1·d-1的普洱熟茶提取物是安全的。
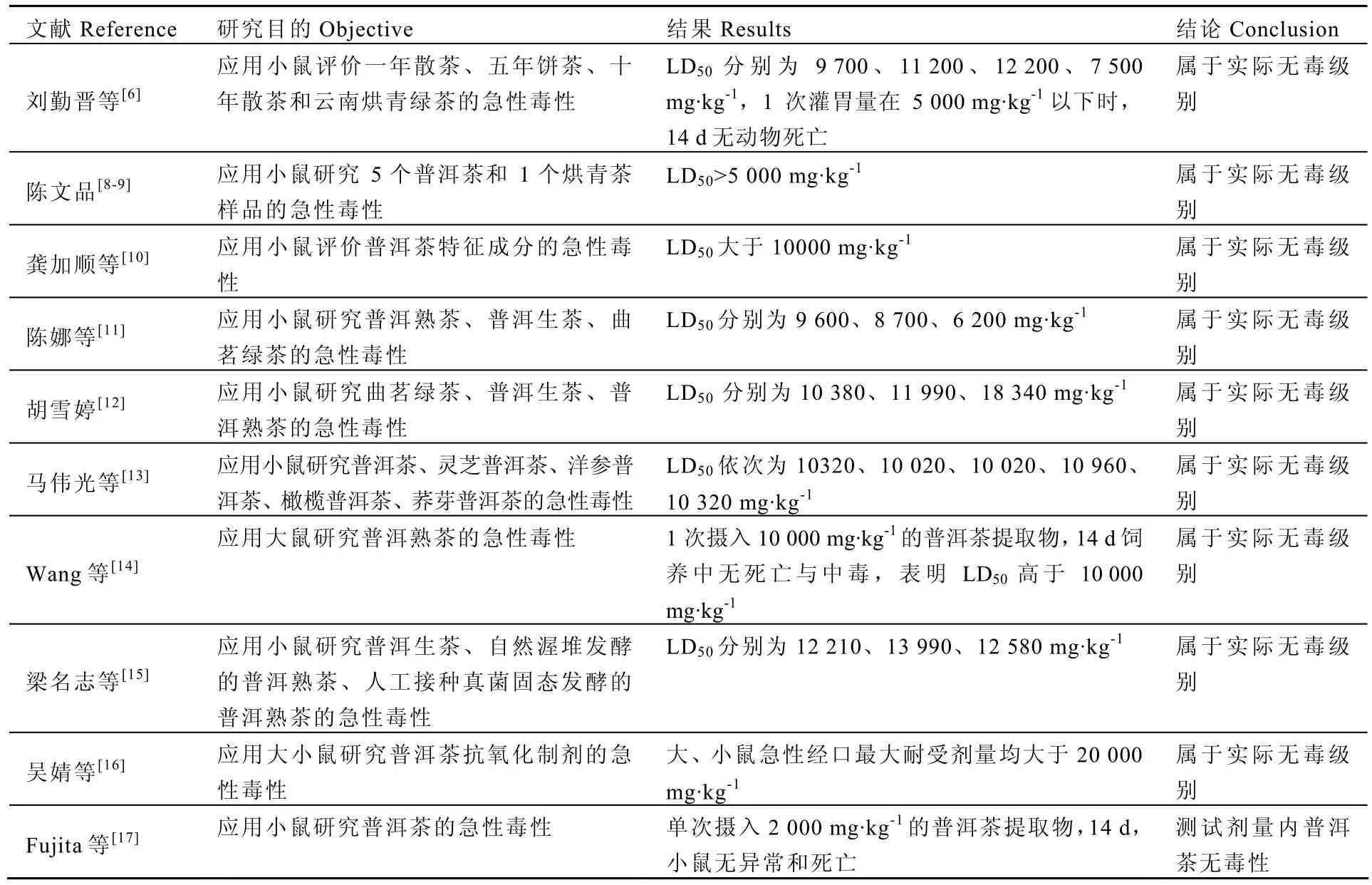
表2 普洱茶动物急性毒性实验研究概述Table 2 Summary of the acute animal oral toxicity tests of Pu-erh tea
90 d经口毒性试验(GB 15193.13—2015)通过实验动物在不超过其寿命期限10%的时间内(大鼠通常90 d),重复经口接触受试物后引起的健康损害效应,以评价受试物的亚慢性毒性[20]。Wang等[14]研究发现持续 90 d摄入不同剂量(1 250、2 500、5 000 mg·kg-1·d-1)的普洱茶提取物,大鼠无死亡,体质量、摄食率、器官重量无改变,无肉眼、临床和组织病理学的改变,表明每天5 000 mg·kg-1剂量的普洱熟茶提取物无明显不良效应。李艳艳等[21]以普洱熟茶(510、1 710 和 5 120 mg·kg-1·d-1)和普洱生茶(550、1 820、5 460 mg·kg-1·d-1)剂量灌胃90 d,各组各项血常规指标与对照组相比无显著差异(P>0.05),除甘油三酯值显著降低(P<0.05)外,其他各项生化指标均在正常值范围内,表明适宜浓度的普洱茶对 SD大鼠血液生理生化指标无不良影响(表3)。
3 遗传毒性研究
遗传毒性试验是指对化学物质改变细胞内遗传物质的能力进行测试,确定其致突变性及对生物的影响,对可遗传损伤、致癌性以及其他有关损伤进行评价的方法。陈文品等[8,22]、龚加顺等[10]和吴婧等[17]开展了鼠伤寒沙门氏菌回复突变实验(Ames试验)、小白鼠骨髓微核试验、中国仓鼠细胞(CHL)染色体畸变试验、畸形精子检测试验,研究发现对原核细胞、真核细胞和生殖细胞都没有致突变性。Wu等[23]发现普洱茶提取物不仅无细胞和遗传毒性,还具有抗突变作用(表4)。

表3 普洱茶28 d或90 d经口毒性试验研究概述Table 3 Summary of the 28 d or 90 d oral toxicity tests of Pu-erh tea

表4 普洱茶遗传毒性研究概述Table 4 Summary of the genetic toxicity evaluations of Pu-erh tea
4 其他毒性研究
Wang等[24]应用SD大鼠研究普洱茶的生殖毒性和发育毒性,发现 2 500 mg·kg-1·d-1的普洱茶提取物能减少F0亲本和F1后代的体质量增加,改变睾丸、前列腺和卵巢等器官的相对重量,引起胚胎-胎儿期的胚胎发育障碍,结果认为普洱茶的生殖毒性和发育毒性无效应剂量水平是 700 mg·kg-1·d-1。李红霞等[25]发现普洱熟茶对小鼠肝细胞的毒性极小或无。王迪[26]研究发现各剂量的普洱茶提取物,均能够降低喹烯酮所致的DNA损伤,而本身对肝细胞DNA没有损伤作用。
5 临床毒性或不良反应研究
Hwang等[27]研究发现,健康志愿者(16位男性)每天摄入1 000 mL普洱茶提取物(约20 g原茶),连续7 d,体质量无变化,无副作用,血液总胆固醇、甘油三酯、游离脂肪酸、LDL-胆固醇、HDL-胆固醇无显著变化。Fujita等[17]以志愿者为对象,开展了以下 3项试验研究普洱茶安全性:试验1,健康(n=10)和临界高胆固醇血症(n=10)的志愿者,每天摄入(0.75 g或1 g)普洱茶提取物,持续8周;试验2,健康志愿者(n=10)1次摄入10 g普洱茶提取物研究急性毒性;试验3,健康志愿者(n=11)每天摄入5 g普洱茶提取物,持续摄入5周;以上试验中志愿者无腹胀、腹痛、腹泻、恶心和胀气等副作用,8个血液指标(白血球、红血球、血红蛋白、红细胞压积、血细胞比容、红细胞平均容量、平均红细胞血红蛋白浓度、血小板)和14个生化指标(谷草转氨酶、谷丙转氨酶、碱性磷酸酶、三磷酸鸟苷、总蛋白、淀粉酶、血糖、总胆固醇、LDL胆固醇、甘油三酯、尿素、血尿素氮、肌酸酐、C型反应性蛋白)无显著变化。
另外 Kubota等[28]以超重的日本志愿者(n=36)研究普洱茶减肥活性,发现每天摄入1 g普洱茶提取物,持续12周,无腹胀、腹痛、腹泻、过敏等不良反应,测定的血液、生化指标无异常。Chu等[29]发现代谢综合征病人(n=45),每天摄入约5 g普洱茶,3个月,除一人腹泻外,未见其他不良反应,血液、尿液检查未见异常。Yang等[30]以代谢综合征患者(n=36),每天摄入1 g普洱茶提取物,持续3个月,试验中未观察到腹痛、腹泻或过敏症等不良反应。
在以上研究中,Fujita等[17]、Kubota等[28]和Yang等[30]制备普洱茶提取物的方法相同,流程为100 g茶叶加入900 mL水,100℃提取60 min,2 050×g离心 30 min,滤纸过滤,浓缩,热风干燥制得粉末。他们的研究均未明确得率,笔者根据普洱茶速溶粉和茶膏的加工经验推算,其得率可能为20%左右,也即1 g提取物相当于约5 g原茶。因此Fujita等[17]的研究中,每天摄入 5 g普洱茶提取物,推测相当于25 g普洱茶。根据 Fujita等[17]的研究(推测每天约25 g普洱茶,持续5周)以及Hwang等[27]的报道(每天摄入约20 g原茶的提取物,7 d),笔者认为成人一次性摄入 20 g左右普洱茶是安全的。但是由于大剂量的多酚、咖啡碱等化学物质对身体存在副作用,建议适量饮用。
6 结论
从已有细胞、动物和人体安全性毒理学试验结果来看,除孕妇、儿童外,普洱茶具有较高的饮用安全性。但是,茶业科研、加工人员应当科学认识和重视普洱茶的真菌毒素风险,通过接种安全菌种、实时监控发酵过程等措施改良工艺,控制普洱茶的安全性风险。
[1] 李宁. 国内食品安全性毒理学评价的现状和发展[J]. 毒理学杂志, 2007, 21(5): 368-370.
[2] 张婧, 张晓鹏, 贾旭东, 等. 我国食品毒理学评价程序和方法标准现况与管理对策[J]. 毒理学杂志, 2015, 29(2):109-113.
[3] 中华人民共和国国家卫生和计划生育委员会. 食品安全国家标准 食品安全性毒理学评价程序:GB 15193.1—2014[S]. 2014.
[4] 郑晓燕, 张倩茹. 普洱茶发酵过程中微生物研究现状[J].食品安全导刊, 2017, 23: 26-27.
[5] 马燕, 张冬莲, 苏小琴, 等. 茶叶中真菌毒素污染的国内外研究概况[J]. 中国食品卫生杂志, 2014, 26(6): 627-630.
[6] 刘勤晋, 陈文品, 白文祥, 等. 普洱茶急性毒性安全性评价研究报告[J]. 茶叶科学, 2003, 23(2): 141-145.
[7] 中华人民共和国国家卫生和计划生育委员会. 食品安全国家标准 急性经口毒性试验. GB 15193.3—2014 [S].2014.
[8] 陈文品, 刘勤晋, 白文祥, 等. 普洱茶毒理学安全性评价研究[Z]. 杭州: 2004, 09.
[9] 陈文品. 经典遗传毒理学试验表明普洱茶抗癌不致癌[J].普洱, 2012, 5: 80-85.
[10] 龚加顺, 陈文品, 周红杰, 等. 云南普洱茶特征成分的功能与毒理学评价[J]. 茶叶科学, 2007, 27(3): 201-210.
[11] 陈娜, 侯艳, 徐昆龙, 等. 云南普洱茶急性毒性研究[J].云南农业大学学报, 2008, 23(2): 233-237.
[12] 胡雪婷. 普洱茶毒理学的初步研究[D]. 武汉: 华中科技大学, 2009.
[13] 马伟光, 黄之镨, 游文龙, 等. 配方普洱茶的急性毒性研究[J]. 茶叶科学, 2010, 30(1): 9-12.
[14] Wang D, Xu K, Zhong Y, et al. Acute and subchronic oral toxicities of Pu-erh black tea extract in sprague-dawley rats[J]. Journal of Ethnopharmacology, 2011, 134(1): 156-164.
[15] 梁名志, 王丽, 王立波,等. 人工接种真菌固态发酵普洱茶的急性毒性安全性评价[J]. 西南农业学报, 2012, 25(05):1956-1958.
[16] 吴婧, 孙世利, 徐平, 等. 普洱茶抗氧化制剂毒理学研究与安全性评价[J]. 中国茶叶加工, 2014, 4: 18-24.
[17] Fujita H, Yamagami T. Efficacy and safety of Chinese black tea (Pu-ehr) extract in healthy and hypercholesterolemic subjects [J]. Annals of Nutrition and Metabolism, 2008,53(1): 33-42.
[18] 中华人民共和国国家卫生和计划生育委员会. GB 15193.22-2014 食品安全国家标准 28天经口毒性试验[S]. 2014.
[19] Wang D, Xiao R, Hu X, et al. Comparative safety evaluation of Chinese Pu-erh green tea extract and Pu-erh black tea extract in Wistar rats [J]. Journal of Agricultural and Food Chemistry, 2010, 58(2): 1350-1358.
[20] 中华人民共和国国家卫生和计划生育委员会. 食品安全国家标准 90天经口毒性试验:GB 15193.13—2015 [S].2015.
[21] 李艳艳, 肖蓉, 江波, 等. 普洱茶对SD大鼠血液生理生化指标影响的研究[J]. 云南农业大学学报(自然科学版),2011, 26(2): 254-259.
[22] 陈文品, 刘勤晋, 白文祥, 等. 普洱茶遗传毒性安全性评价研究[J]. 茶叶科学, 2005, 25(3): 208-212.
[23] Wu S, Yen G, Wang B, et al. Antimutagenic and antimicrobial activities of Pu-erh tea [J]. LWT - Food Science and Technology, 2007, 40(3): 506-512.
[24] Wang D, Meng J, Gao H, et al. Evaluation of reproductive and developmental toxicities of Pu-erh black tea (Camellia sinensisvar.assamica) extract in Sprague Dawley rats [J].Journal of Ethnopharmacology, 2013, 148(1): 190-198.
[25] 李红霞, 孙永科, 李艳艳, 等. 普洱茶对原代小鼠肝细胞的毒性初探[J]. 食品工业科技, 2010, 31(12): 322-325.
[26] 王迪. 氧化应激介导的喹烯酮遗传毒性及普洱茶水提取液保护作用研究[D]. 武汉: 华中科技大学, 2011.
[27] Hwang L S, Lin L, Chen N, et al. Hypolipidemic effect and antiatherogenic potential of Pu-Erh tea [M]. ACS Symposium Series, 2003, 859: 87-103.
[28] Kubota K, Sumi S, Tojo H, et al. Improvements of mean body mass index and body weight in preobese and overweight Japanese adults with black Chinese tea (Pu-Erh)water extract [J]. Nutrition Research, 2011, 31(6): 421-428.
[29] Chu S, Fu H, Yang J, et al. A randomized double-blind placebo-controlled study of Pu'er tea extract on the regulation of metabolic syndrome [J]. Chinese Journal of Integrative Medicine, 2011, 17(7): 492-498.
[30] Yang T, Chou J I, Ueng K, et al. Weight reduction effect of pu-erh tea in male patients with metabolic syndrome [J].Phytotherapy Research. 2014, 28(7): 1096-1101.

