废旧锂离子电池中锰的回收利用
卢东亮,朱显峰,蔡东方,赵瑞瑞
(1.广东环境保护工程职业学院,广东 佛山 528216; 2.华南师范大学化学与环境学院, 广东 广州 510006)
目前,正极材料主要采用酸浸出法进行溶解,通常分为有机酸浸出体系[2]和无机酸浸出体系[3],之后,采用化学或物理分离技术对所需有价金属进行分离和回收利用。采用苹果酸(C4H6O5)和还原剂过氧化氢(H2O2)作为浸出剂,在优化条件下,Mn、Ni、Co和Li等4种元素的浸出率都可达到95%以上[2],再通过分步沉淀,就可以获得对应的有价金属回收产物。由三元正极废料直接回收获得的MnO2难以满足电极材料的性能要求,直接煅烧制备的Mn2O3/Mn3O4材料的电化学性能也不理想。
针对上述问题,本文作者使用苹果酸-过氧化氢体系对正极材料进行浸出,以高锰酸钾溶液氧化沉锰法回收得到MnO2,作为锂离子电池负极材料,并以葡萄糖为碳源改性制备得到的材料,研究还原煅烧制备的超细纳米MnOx/C负极材料的电化学性能。
1 实验
1.1 MnO2材料的回收与改性
以苹果酸(天津产,AR)为浸出酸、H2O2(天津产,AR)为还原剂,配制100 ml苹果酸浓度为1.25 mol/L、H2O2体积分数为1%的浸出剂,加入烧瓶中,按固液比30 g∶1 L称取3 g LiNi0.5Co0.2Mn0.3O2三元正极材料(杉杉公司提供)样品,加入烧瓶中,在80 ℃下水浴加热,搅拌反应80 min,过滤,即得到LiNi0.5Co0.2Mn0.3O2三元材料的浸出液。用0.5 mol/L KMnO4(天津产,AR)溶液对Mn2+进行氧化沉淀,分离得到棕红色的MnO2。
将MnO2和葡萄糖(C6H12O6,天津产,AR)以不同质量比混合,在氮气气氛中、600 ℃下煅烧3 h。将得到的产物研磨、过300目筛,得到MnOx/C复合材料。实验选择m(MnO2)∶m(C6H12O6) = 1∶0(直接煅烧)、1∶1、1∶3和1∶5。
1.2 材料的分析
用D8 Advance型X射线衍射仪(德国产)对材料进行晶体结构分析,CuKα,波长0.154 nm,管压40 kV、管流30 mA,扫描速度为6 (°)/min,步长为0.02 °;用JEM-2100HR透射电子显微镜(TEM,日本产)分析材料的形貌和内部结构。
1.3 电池的组装
将电极活性材料、导电剂乙炔黑(广州产,电池级)、黏结剂聚偏氟乙烯(PVDF,Aladdin公司,电池级)按质量比8∶1∶1混合,以氮甲基吡咯烷酮(NMP,天津产,AR)为溶剂混合均匀,涂覆于10 μm厚的铜箔(深圳产,电池级)上,制成湿膜极片,然后在80 ℃下真空(-0.1 MPa)干燥12 h,切片(直径为14 mm),以10 MPa的压力辊压,制成极片(约含3 mg活性物质)。
虽然这些青年教师的背景不同、资历不同、经验不同,但他们的目标是一致的,他们聚集在一起交流上课经验,分享实用的例题,将学生多数会遇到的问题拿出来讨论,他们会互相帮助,一起做项目,从而全面提高个人素质。
在充满干燥氩气的手套箱中,按金属锂片(深圳产,电池级)、Celgard 2500隔膜(美国产)和待测电极极片的顺序组装CR2032型扣式电池,滴加电解液1 mol/L LiPF6/EC+DEC(体积比1∶1,广州产,电池级)。组装完成的电池先静置3~4 h,再进行相关电化学性能测试。
1.4 电化学性能测试
用BTS-5 V10mA型充放电仪(深圳产)电极材料的充放电性能及循环性能进行测试,电压为0.01~3.0 V,电流为0.1C(70 mA/g)。用CHI600E电化学工作站(上海产)进行循环伏安(CV)测试,电位为0~3 V,扫描速度为1 mV/s,对氧化还原峰的电位、电流及测试参数进行分析。
2 结果与讨论
2.1 还原煅烧对MnO2回收产物物相和形貌的影响
回收得到的MnO2的XRD图见图1。
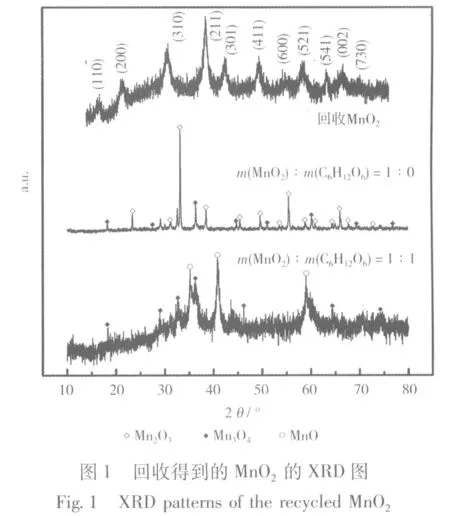
将图1与MnO2的标准卡(JCPDS:44-0141)对照可知,回收得到的MnO2为四方晶系的α-MnO2,说明通过本方法可回收得到较纯净的MnO2。与Mn2O3的标准卡(JCPDS:41-1442)和Mn3O4的标准卡(JCPDS:41-1442)对照可知,m(MnO2)∶m(C6H12O6) = 1∶0煅烧后的产物,主要由Mn2O3与Mn3O4组成;m(MnO2)∶m(C6H12O6) = 1∶1煅烧后的产物,主要由MnO(JSPDS:07-0233)与Mn3O4两种相组成。
图2为回收得到的MnO2煅烧前的TEM图及选区电子衍射(SAED)图。

按m(MnO2)∶m(C6H12O6) = 1∶0煅烧得到的Mn2O3/Mn3O4材料的TEM图见图3。
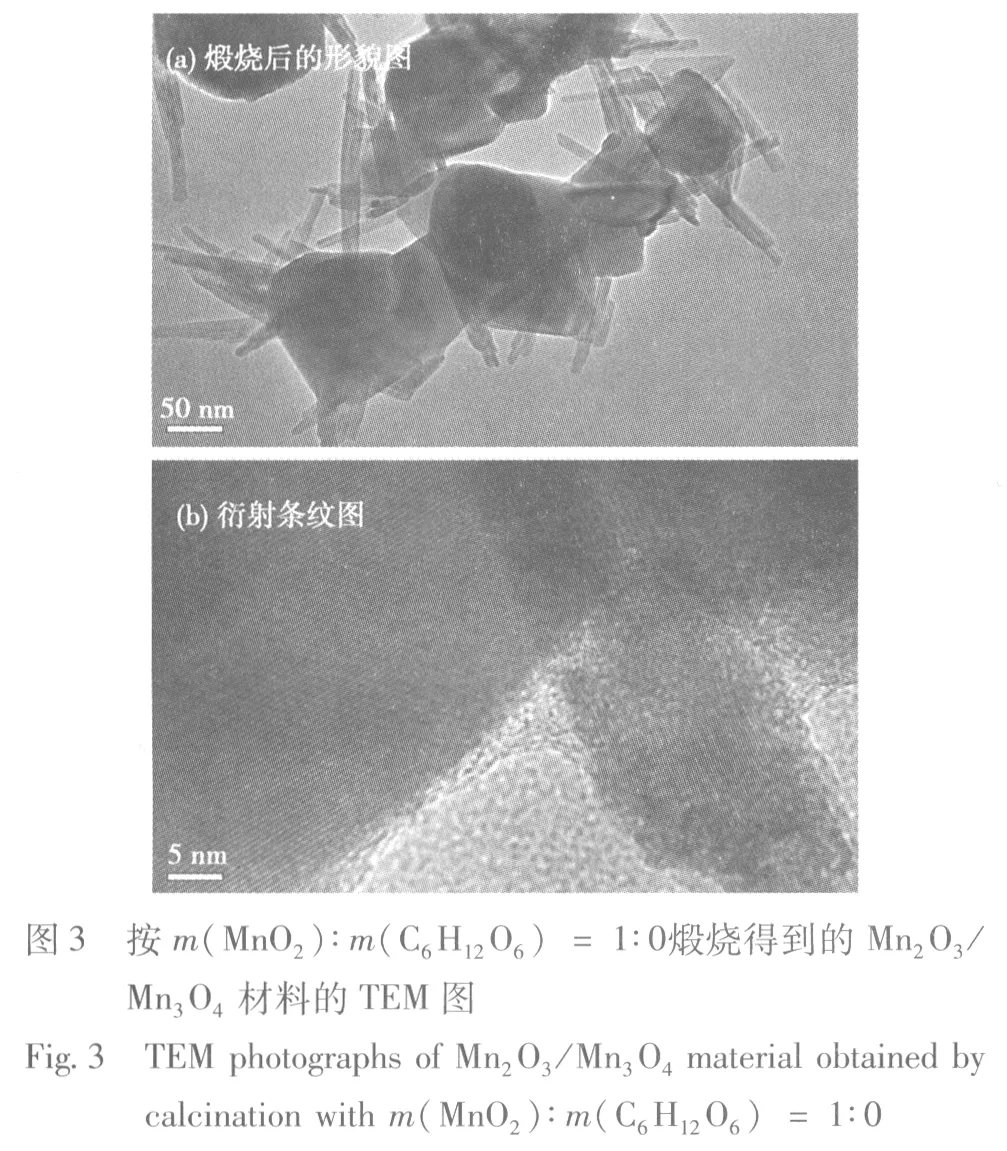
从图3可知,与煅烧前规则的棒状结构相比,煅烧后的产物呈不规则的球块状结构,粒径从几十纳米到几百纳米,说明煅烧后随着Mn2O3与Mn3O4新相的生成,材料的微观形貌和粒径都发生了变化。此外,生成的产物部分保留了原来的棒状结构,但物相组成发生了根本性的变化。从图3(b)可看出,该衍射条纹是由Mn3O4晶体的(112)晶面产生的[4]。
按m(MnO2)∶m(C6H12O6) = 1∶1煅烧得到的MnOx/C材料的TEM图及SAED图见图4。

从图4(a)、(b)可知,经还原煅烧,MnO2由之前的纳米棒状结构转变为碳包覆结构,粒径分布约为几十纳米;从图4(c)、(d)可观察到由Mn3O4晶体的(112)晶面和MnO的(111)晶面所产生的衍射晶格条纹[4]。
2.2 MnO2产物及还原煅烧产物的电化学性能
m(MnO2)∶m(C6H12O6) = 1∶0、1∶1煅烧制备材料的充放电曲线见图5。
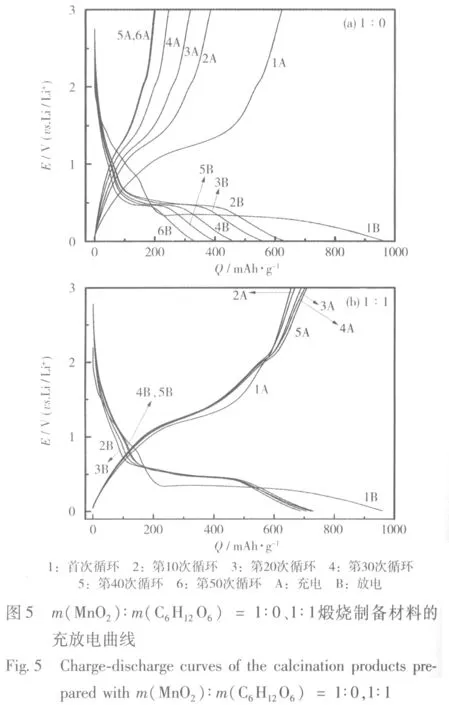
从图5可知,由m(MnO2)∶m(C6H12O6) = 1∶0煅烧制备的Mn2O3/Mn3O4材料以0.1C充放电,首次放电曲线在1.5~0.5 V的放电平台主要是由固体电解质相界面(SEI)膜的产生和Mn3+还原为Mn2+引起的;之后,电压很快降至约0.3 V的平台,然后缓慢减小到0.01 V,对应于Mn2+完全还原为金属Mn的过程;首次充电曲线在约1.0 V处的平台,对应于金属Mn被氧化成Mn2+的过程。充电比容量约为625 mAh/g,略低于Mn氧化为Mn2+的理论值679 mAh/g[5]。
由m(MnO2)∶m(C6H12O6) = 1∶1煅烧制备的MnOx/C材料(MnO/Mn3O4/C),首次放电曲线在2.0~0.5 V的放电平台也是由SEI膜的形成和Mn3+还原成Mn2+所引起的;之后,电压快速下降到Mn2+还原为金属Mn过程的约0.3 V处的电压平台,然后缓慢减小到0.01 V;首次充电曲线在1.0~1.5 V的一个平台,对应于金属Mn被氧化成Mn2+的过程,平台电压的理论值出现在1.032 V处[6]。平台位置的不同,一般认为是由阳极过电位引起的。首次充电比容量约为653 mAh/g,随着循环进行,充电比容量有所提升。
整体而言,回收得到的MnO2材料直接煅烧所制备的Mn2O3/Mn3O4材料,循环性能不理想,比容量衰减快;而改性后的MnOx/C材料表现出较好的循环性能。
m(MnO2)∶m(C6H12O6) = 1∶0、1∶1煅烧制备材料的CV曲线见图6。
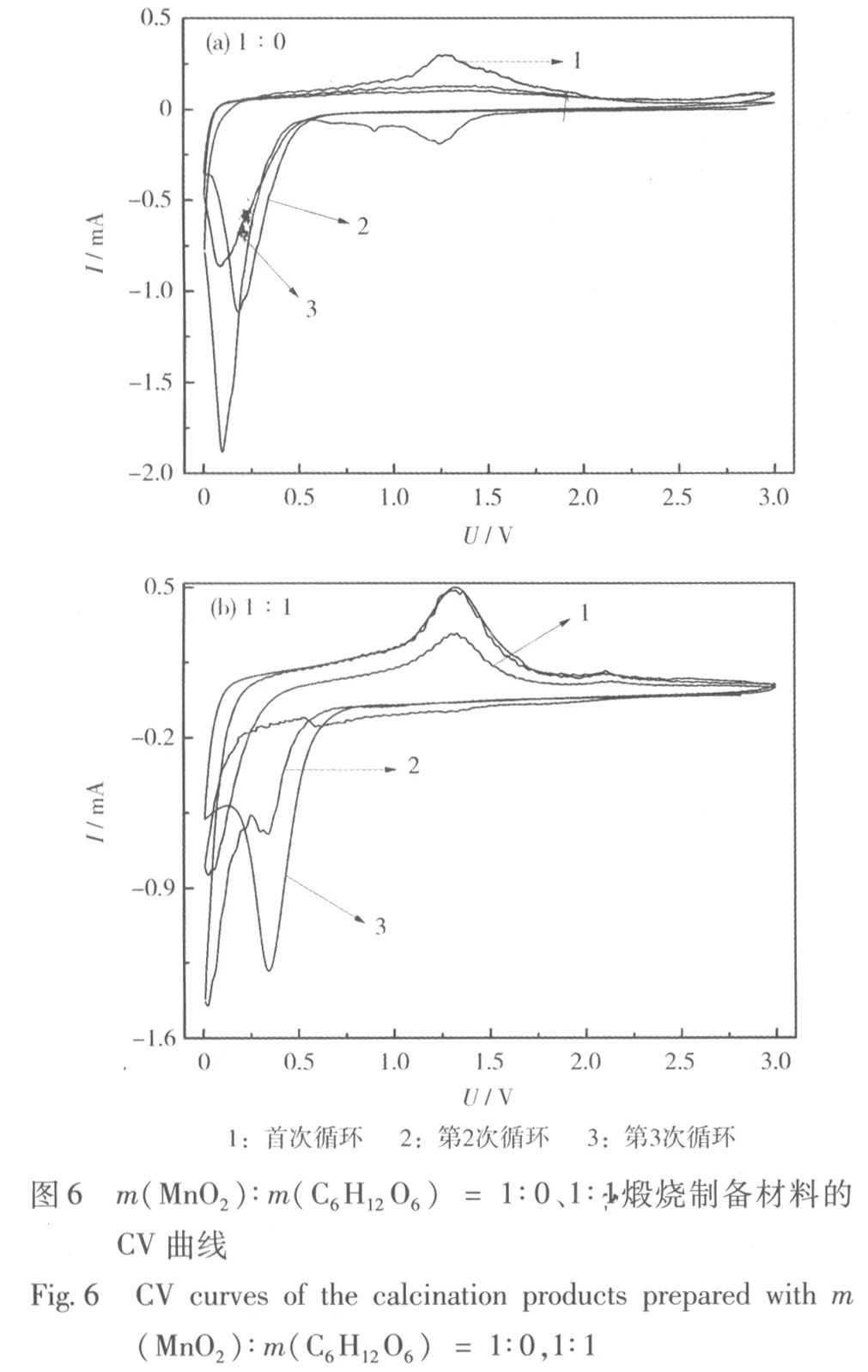
从图6可知,由m(MnO2)∶m(C6H12O6) = 1∶0煅烧制备的Mn2O3/Mn3O4材料,首次放电过程在1.25 V和0.60 V两处可以分别观察到一强一弱两个还原峰;由m(MnO2)∶m(C6H12O6) = 1∶1煅烧制备的MnOx/C材料,在首次放电过程中仅在0.60 V处观察到一个还原峰,而且这个还原峰在之后的扫描中消失。根据CV测试的结果和文献[7]报道,1.25 V处出现的还原峰对应于SEI膜的生成过程;0.60 V处出现的小还原峰对应于Mn3+还原为Mn2+的过程;在电压靠近0.01 V处有一个尖锐的峰,是Mn2+被还原成金属Mn引起的。由于样品中Mn2+的含量多,相应还原峰的电流很大。
在首次充电过程中,两种材料在电压为1.25 V处左右都出现了一个明显的氧化峰,对应于金属Mn氧化为Mn2+的过程;而对于m(MnO2)∶m(C6H12O6) = 1∶1煅烧制备的MnOx/C材料而言,在电压约2.1 V处还出现了一个小的氧化峰,对应于Mn2+氧化为Mn3+的行为[5]。总的来说,两种材料恒流充放电与CV测试的结果基本保持一致。
m(MnO2)∶m(C6H12O6) = 1∶0、1∶1、1∶3和1∶5煅烧制备材料的倍率性能见图7。
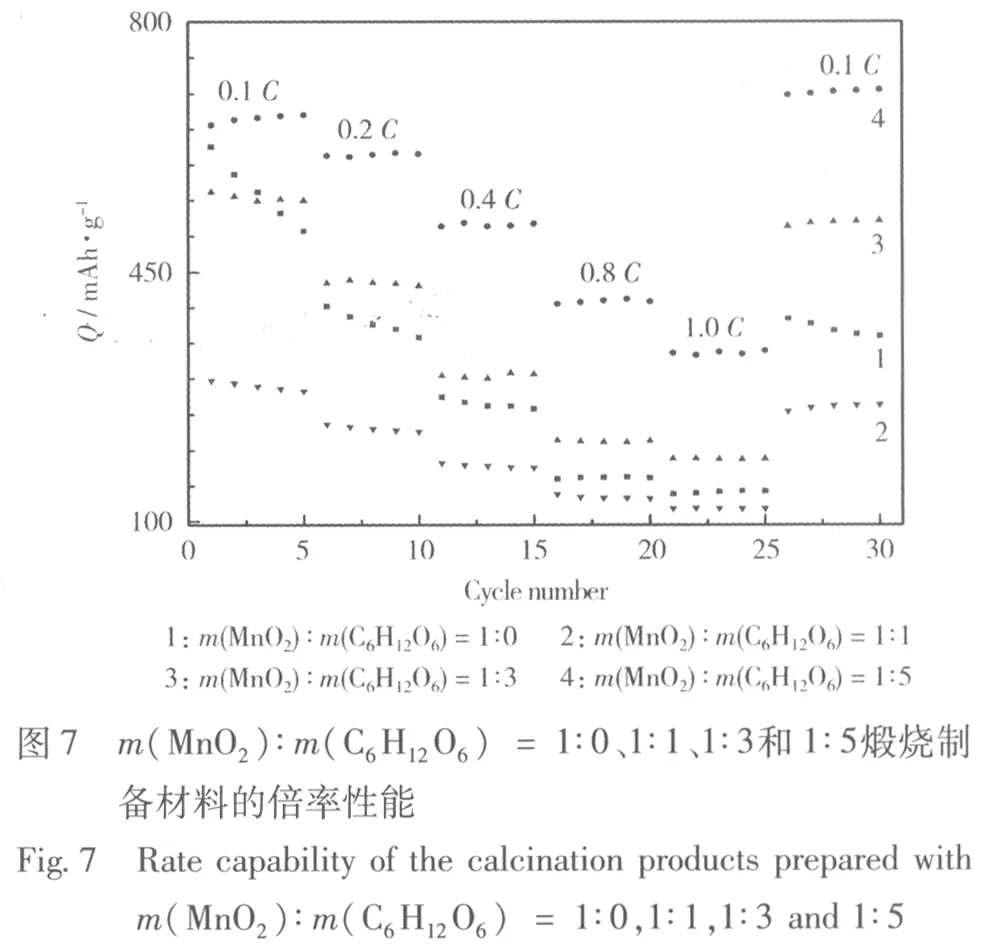
从图7可知,由m(MnO2)∶m(C6H12O6) = 1∶1煅烧制备的材料,在0.1C、0.2C、0.4C、0.8C和1.0C倍率下的可逆比容量分别为652 mAh/g、603 mAh/g、491 mAh/g、372 mAh/g和319 mAh/g,在同一倍率下高于以其他样品。完成倍率测试后,将充放电倍率恢复到0.1C,除由m(MnO2)∶m(C6H12O6) =1∶0煅烧制备的材料比容量有明显衰减外,大都接近或高于初期在0.1C倍率时的充电比容量。比容量的增加可归因于锰氧化物的活化作用和电解液分解形成的SEI膜的保护作用,抑制了电解液的进一步分解[8]。
回收的MnO2材料、m(MnO2)∶m(C6H12O6) = 1∶0、1∶1、1∶3和1∶5煅烧制备材料的循环性能见图8。
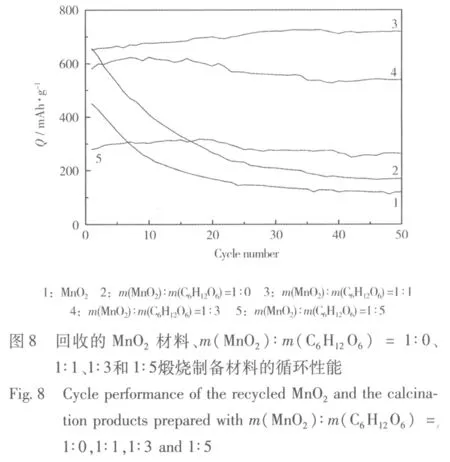
从图8可知,回收的MnO2材料和由m(MnO2)∶m(C6H12O6) = 1∶0煅烧制备的材料,循环性能都比较差;由m(MnO2)∶m(C6H12O6) = 1∶1、1∶3和1∶5煅烧制备的材料,循环性能较好。相比之下,由m(MnO2)∶m(C6H12O6) = 1∶3和1∶1煅烧制备的材料,电化学性能更理想,前者经过50次循环,充电比容量随着循环的深入虽有所衰减,但仍能保持在约540 mAh/g;后者经过50次循环,随着电解液对材料润湿程度的增加和材料上反应活性位点的增多,比容量从首次循环时的653 mAh/g逐渐增加,并稳定在约708 mAh/g。
3 结论
采用苹果酸-过氧化氢体系对动力锂离子电池正极废料LiNi0.5Co0.2Mn0.3O2正极材料进行浸出,以高锰酸钾溶液氧化沉锰法可回收得到纯度较高的棒状结构的二氧化锰(MnO2)。将回收产物煅烧后,生成具有不规则的球块状结构的Mn2O3/Mn3O4。将m(MnO2)∶m(C6H12O6) = 1∶1的材料经过煅烧后,生成具有碳包覆结构的MnOx/C材料,粒径分布在几十纳米左右。
对不同m(MnO2)∶m(C6H12O6)煅烧制备材料的电化学测试表明,回收得到的MnO2和由m(MnO2)∶m(C6H12O6) = 1∶0煅烧制备的Mn2O3/Mn3O4材料,循环性能都很差,容量衰减快;而由m(MnO2)∶m(C6H12O6) = 1∶1煅烧制备的材料,在0.1C倍率下的首次充电比容量达到了653 mAh/g,经过50次循环也没有衰减,表现出较理想的循环性能。

