前列欣浓缩丸中芍药苷高效液相色谱测定方法的建立
孙冰雪,牟凤辉,王睿,王艳
(吉林大学药学院,长春 130021)
前列欣胶囊是一种对前列腺增生具有良好治疗作用的颗粒剂,对前列腺增生引起的排尿不畅等病症具有明确的疗效[1,2]。本研究首次将前列欣胶囊进行剂型的改革创新,将胶囊剂转剂型为浓缩丸剂。浓缩丸剂具有很多其他剂型无法取代的优势,包括比表面积小、容易被吸收、经浓缩后单丸药物浓度高、口服给药病人顺应性高等[3]。
本研究中用到的前列欣浓缩丸是将国家中成药标准汇编收载的前列欣胶囊〔WS3-048(Z-013)-98(Z)〕经剂型改革制成的新药[4]。经过剂型改变后明显改善了药物稳定性差、吸收利用度低等缺点。前列欣浓缩丸中的主治成分为芍药苷。目前,未见有关前列欣浓缩丸含量测定的研究报道。本试验通过HPLC法对前列欣浓缩丸中芍药苷的含量进行检测,并对检测结果进行分析讨论,为前列欣浓缩丸的生产研发提供参考。
1 仪器与试药
1.1 仪器
LC-20AT高效液相色谱仪、SPD-10Avp紫外可见检测器(日本岛津公司);日立U-3400型分光光度计(日立新技术公司);XS105分析天平(1/100 000,梅特勒托利多仪器有限公司);XSP-2CA双目光学显微镜(上海光学仪器厂);HWS24型电热恒温水浴锅(上海一恒科技有限公司)
1.2 试药
前列欣浓缩丸:0.2g/丸,包含桃仁(炒)、没药(炒)、丹参、赤芍、红花、泽兰、王不留行(炒)、皂角刺、败酱草、蒲公英、川楝子、白芷、石苇、枸杞子,吉林大学药学实验中心自制。
芍药苷对照品(批号:0736-200014,中国药品生物制品检定所);乙腈(色谱纯,批号:013110532,美国J.T.Baker公司);其他试剂均为分析纯。
2 方法与结果
2.1 溶液的配制
2.1.1 对照品溶液 称量芍药苷对照品(2.00±0.03)mg,将称取的芍药苷粉末用甲醇-水(v∶v=50∶50)作为溶剂于25mL容量瓶中将其稀释定容。
2.1.2 供试品溶液 称量约0.4g浓缩丸研细粉,倾倒于 50mL容量瓶中,加入水-盐酸(v∶v=40∶1),超声30min,冷却,定容,放置10min后,移取上层液体10mL,CHCl3萃取2次,将2次得到的萃取液合并,定容于10mL容量瓶,备用。
2.1.3 阴性对照溶液 依照芍药苷浓缩丸的制法,制备仅不含芍药苷的浓缩丸,并按“2.1.2”项下处理方法制备阴性对照溶液。
2.2 色谱条件
色谱柱:GL-WondasilC1(84.6 150mm,5m);流动相:乙腈-0.2%磷酸溶液(v∶v=14∶86);检测波长:230nm;柱温箱温度:40℃;进样量:10L;流速:1mL/min[5]。
2.3 专属性试验
将对照品溶液、供试品溶液、阴性样品溶液按照“2.2”项下方法进行分析,对处理后的色谱图进行整理。通过色谱图可知,前列欣浓缩丸中其他成分对芍药苷的检测没有干扰,分析方法专属性好,芍药苷特征的出峰时间是10.367min。结果见图1。
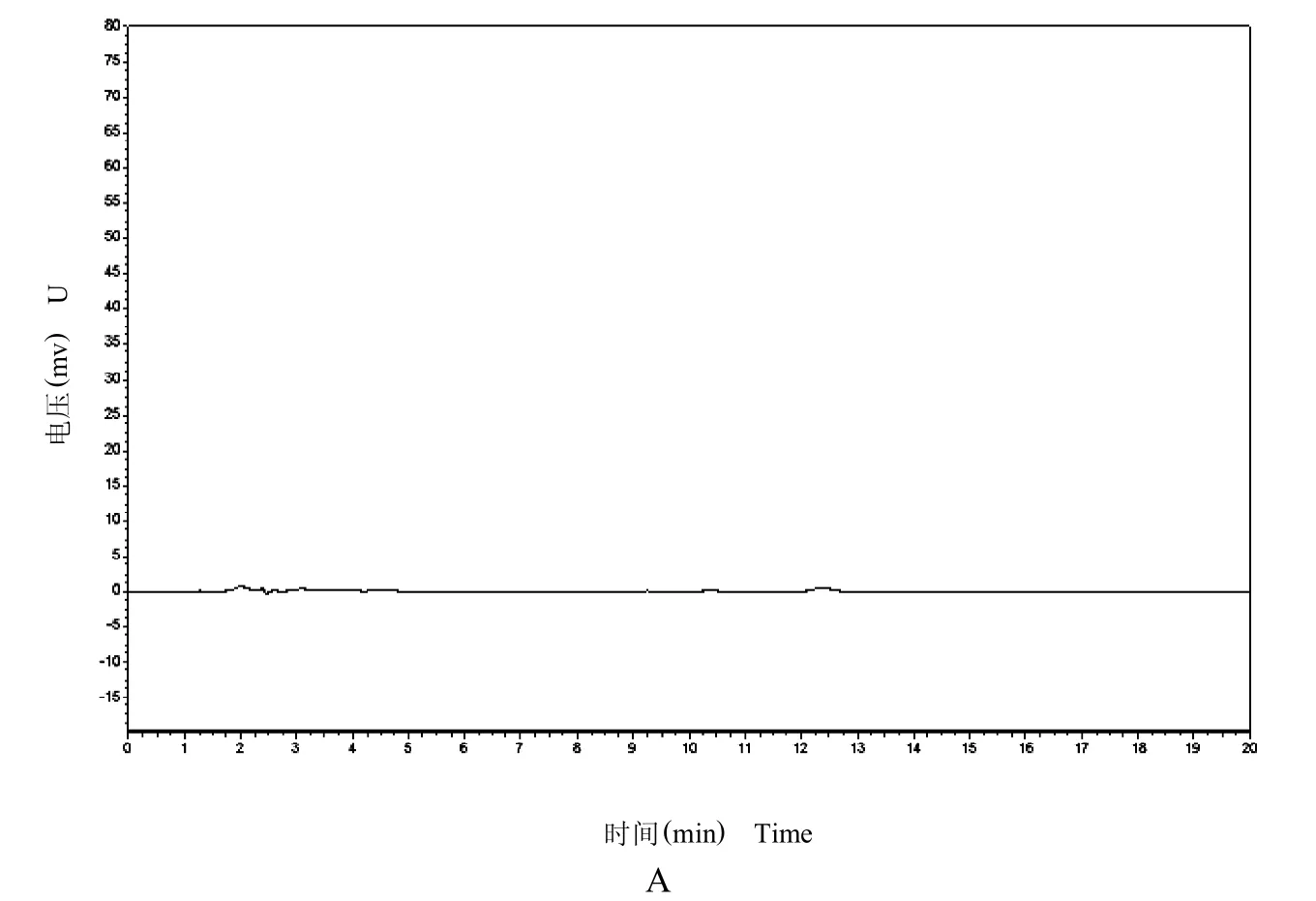

图1 高效液相色谱图Fig.1 HPLC chromatogram
2.4 线性关系考察
吸取“2.1.1”项下配置好的对照品溶液0.1mL~1.3mL(每间隔0.2mL为1组,共7组),分别置2mL容量瓶中,加甲醇-水(v∶v,50∶50)溶液分别进行定容。分别吸取上述溶液各10L(浓度由低到高),按“2.2”项下设定的条件进行检测,以进样量为横坐标、峰面积为纵坐标绘制标准曲线,得线性回归方程为Y=24 558+1 585 535X,r=0.999 7,芍药苷在0.054g~0.702g范围内线性关系良好。
2.5 精密度实验
吸取任意一个浓度的对照品溶液,进样10L,进行HPLC分析,连续进样分析5次,记录色谱图,对芍药苷的特征色谱峰进行积分,记录峰面积的积分值[5]。5次进样分析得到的RSD值为0.037%(n=5),表明方法精密度较好。
2.6 稳定性实验
取供试品和对照品溶液各取10L进行稳定性检测,按照“2.2”项下色谱条件,对上述溶液在配制后0h、1h、2h、4h、6h 含量进行检测,结果 RSD 为 1.85%(n=5),表明6h内待测样品稳定性良好。
2.7 重复性实验
同一批次的自制前列欣浓缩丸6份,制备待检测液,按照“2.2”项下色谱条件进行检测,RSD为2.44%,<3%(n=6),说明测定方法重复性好。
2.8 回收率实验
称取已知明确含量的自制前列欣浓缩丸研细粉6份,将1.48mg/mL芍药苷对照品溶液1mL分别加入到上述研细粉中,将6份样品按“2.1.2”项下方法进行同一处理,依照“2.2”项下色谱条件进行分析测定,利用得到的特征峰面积计算回收率,回收率平均为99.8%、RSD值为2.56%(n=6),表明该方法回收率良好。
2.9 3批次样品含量测定
分别取3批次的样品(批号:170611、170612、170613),按“2.1.2”项下方法配制成待测样品溶液。按照“2.2”项下色谱条件分析测定。结果见表1。
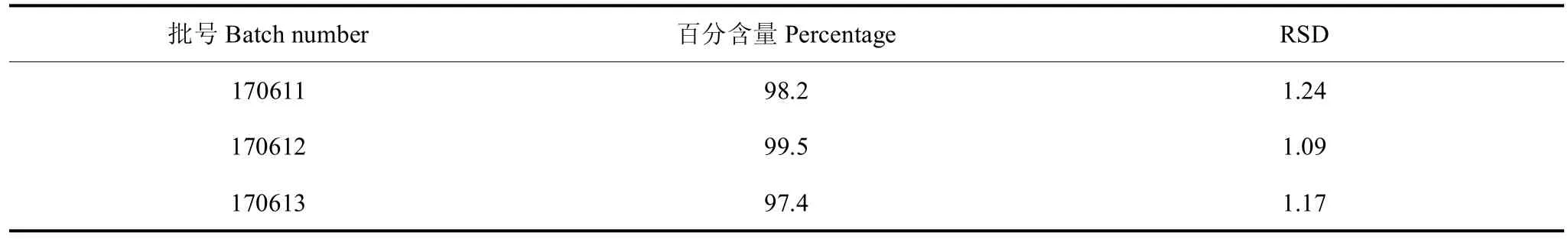
表1 样品含量测定结果Table 1 Sample contentdetermination results (%,n=3)
3 讨论
3.1 波长的选择
称取芍药苷对照品,分别用乙腈-水(v∶v=50∶50)和甲醇-水(v∶v=50∶50)作为溶剂,制成0.02mg/mL的溶液,待测。分别取供试品溶液置石英比色皿中,以甲醇为参比,扫描并记录芍药苷在190nm~400nm范围内的吸光度值,绘制吸收曲线,结果表明,芍药苷在2种溶液中都是在230nm处吸光度值最大,于是将230nm作为本研究中芍药苷的紫外检测波长。
3.2 样品处理方法的选择
方法 1:称取研细粉,加水-浓盐酸(v∶v=40∶1)40mL,超声处理,放冷,定容,摇匀,静置,取上清,用CHCl3萃取2次,量取10mL,取水层2次,合并于10mL容量瓶中,定容。
方法2:称取研细粉,加入40mL纯甲醇,超声处理,放冷,加甲醇定容,摇匀,静置,取上清液,蒸干,残渣加水8mL溶解,用CHCl3萃取2次,每次10mL,取水层2次,合并于10mL容量瓶中,定容。
方法3:称取研细粉,加水饱和正丁醇40mL,超声处理,冷却,加水饱和正丁醇定容,摇匀,静置,挥发干上清液,剩余底层加入8mL水将其溶解,用CHCl3萃取2次,每次10mL,取水层2次,合并于10mL量瓶中,定容。
分别量取上述3种方法处理得到的待测样品溶液10L,进行HPLC测定,得到色谱图,分析色谱图发现,方法1处理得到的待测样品的分离分析效果较其他2种方法好,且积分得到的峰面积积分值最高,故选定该法为前列欣浓缩丸的样品处理方法。
3.3 流动相的选择
前列欣浓缩丸为复方制剂,干扰成分众多,流动相的选择很重要。结合中国药典2015年版(一部)和相关文献报道[6~9],选用甲醇-水和乙腈-水2种流动相体系进行分析时,样品中芍药苷均能与其他杂质峰完全分离,但是,经实验对比发现,以乙腈-0.2%磷酸溶液(v∶v,14∶86)流动相时,能够达到基线分离,峰型好,确定该流动相作为芍药苷HPLC含量测定的流动相。
[1]范海东.前列欣胶囊治疗良性前列腺增生症疗效观察[J].山西医药杂志,2016,45(15):1806-1807.
[2]刘一凡,李海松,韩亮,等.前列欣胶囊治疗气滞血瘀兼湿热型良性前列腺增生症疗效分析[J].北京中医药,2012,31(12):892-894.
[3]王东青,唐月荣,刘卫红.浓缩丸的制备与包衣方法[J].职业与健康,2001,17(2):133.
[4]国家药典委员会.中华人民共和国药典:一部[K].北京:中国医药科技出版社,2010:147-148.
[5]孟勤,赵俊艳,李慧颖,等.桃红清血胶囊中 2,3,5,4′-四羟基二苯乙烯-2-O--D葡萄糖苷HPLC测定方法的建立及评价[J].吉林大学学报:医学版,2010,36(4):803-806.
[6]钟桂香,严佳,周欣,等.HPLC法测定硝酸甘油软膏的含量[J].中国药师,2017,20(1):182-184.
[7]李伟,张建军,卫茜,等.高效液相色谱法测定白芍药材中芍药苷和芍药内酯的含量[J].中药与临床,2011,2(6):8-11.
[8]吴君剑,付克,闫广利,等.高效液相色谱法同时测定柴芩清肝胶囊中黄芩苷和芍药苷含量[J].中医药信息,2008,25(6):71-73.
[9]伦立军,李强荣.HPLC法测定前列欣胶囊中芍药苷的含量[J].齐鲁药事,2012,31(6):343-344.

