基于影像的病脑检测方法综述
贾文娟,王水花,张煜东
JIA Wenjuan1,WANG Shuihua1,ZHANG Yudong2
1.南京师范大学 计算机科学与技术学院,南京 210023
2.莱斯特大学 信息系,英国 莱斯特 LE1 7RH
1.School of Computer Science and Technology,Nanjing Normal University,Nanjing 210023,China
2.Department of Informatics,University of Leicester,Leicester LE1 7RH,United Kingdom
1 引言
由于人类的脑部容易受到病毒感染、物理撞击、化学中毒等伤害,并且随着人类社会的老龄化,大脑内部疾病的发病率正在提高,已经成为威胁人类健康的重大疾病之一。普通医学的研究可以借助动物及其器官,但在脑部的研究中,人脑和动物脑又有本质的不同,人脑部结构错综复杂、精细程度高,主要表现为人脑对思维和记忆的计算,这就削弱了动物脑研究的可靠性,而直接进行人脑研究又受到社会伦理的制约,所以现代医学对脑部的研究几乎只能通过计算机辅助的方法。
脑血管疾病作为脑部疾病的一种,是神经科最常见的疾病,其中脑中风是导致成年人残疾的主要原因。这里以脑血管疾病的危害为例,根据资料不难发现在发达国家中,脑中风是导致死亡最常见的疾病之一。同样,据不完全统计,在我国中风患者约有500~700万,年发病率150/100 000,病死率为120/100 000,每一年都有195万左右的人饱受这种疾病的折磨,大约有156万人死于中风。据统计,脑血管疾病突发病死率约为20%,第一年复发率为30%,第五年复发率高达59%,第二次复发死亡率更高。阿尔茨海默氏症即俗称的老年痴呆症,它属于一种神经系统退行性疾病,是痴呆最常见的一种类型。该疾病的起因不易发现,患病过程呈慢性进行性,是老年期痴呆最常见的一种类型,患病率随着年龄的增长而提高。主要表现为记忆功能的渐渐退化、认知功能逐步降低、人格发生变化和语言出现障碍等症状,严重影响了患者的正常社交、工作与生活能力。但是由于该疾病的病因及发病机制尚不明确,而且病情多样,这给诊断治疗和预防带来了极大的困难[1-2]。脑出血疾病是脑中风中最严重的一种类型,身患该类疾病的患者在30天内死亡的几率可达35%~52%,其中,一半以上的患者会在发病后2天之内死亡,而在6个月后仅有20%左右患者的生活能够自理。之前,专家认为该疾病的危险性会随着年龄的增长而提高,但最近研究又发现该类疾病的发病年龄有年轻化的趋势。在我国,该类疾病的发病情况没有整体的统计资料,仅有部分地区的统计资料,资料显示,1996—1998年上海累计40~44岁年龄段脑出血疾病发病率为53/100 000[3]。
脑部疾病由于其肉眼无法检测,所以给医生及病人带来了很多困扰,但是计算机技术的发展给该类型疾病的诊断与治疗带来了福音,人体某些疾病的诊断变得具有可预测性及准确性。研究者们通过核磁共振成像(MRI)等技术获取人脑部图像,并根据脑部图像,使用计算机辅助检测(CAD)的方法来诊断是否患有脑部疾病,从而达到及时发现、及时治疗的目的。此外,本文将重点分析与讨论通过当前较为火热的深度学习来诊断脑部疾病的方法。
2 成像技术
2.1 早期成像技术
计算机可视化技术的快速发展也促进了医学成像技术的进步,成像方式不断涌现并不断得以完善,自局部到整体、从静态到动态、由二维到三维的变化已然成为医学成像技术的一个发展趋势。
X射线的发现被评为19世纪医学诊断学上最伟大的发现,它作为最早的医学影像技术直至今天仍然具有广泛的应用。X射线成像技术所获得的图像能够较为清楚地显示患者组织、器官和病变部位的形状[4]。而XCT的发明被公认为是Roentgen发现X射线以来的重大进步,CT扫描仪的密度分辨率较高,解剖结构显示较为清楚,并且对病变部位的定位和定性能力较强,可以对人体几乎任何部位组织器官的扫描进行成像,因此,CT扫描仪已经成为临床影像检查的常用工具[5]。但是该技术得到的影像只能显示二维的器官大小与形状,且成像平面只能是横向,成像范围只能是有限的断面方向。
超声回波是超声成像[6]系统的检测信号,这种技术所形成的图像能够反映人体组织声学特性的不同,并且能够显示人体中被检测的不同器官的大小和形状。这种设备通过将给定频率的超声波导入病人体内,利用超声波遇到不同组织或者器官界面时得到的不同物理信息这一物理特性进行处理,经过处理后显示为不同的波形、曲线或者图像,从而根据临床表现和得到的超声监测结果对疾病做出诊断。但是,这种成像技术只能显示器官大小与形状的二维图像,并不能显示人体组织中形态、生理生化状态的变化过程,而且成像范围只是自由的断面方向。芦钺等[7]利用36例窒息新生儿作为研究对象,分析超声在窒息新生儿颅脑疾病诊断中的性能。实验结果表明该方法的准确率较高,但准确率依赖于MRI检查的结果,这也说明了MRI成像比超声成像的方法具有较好的应用价值。
由于上述成像技术的限制以及计算机技术的飞速进步,核磁共振成像技术在成像技术中的价值越来越大。核磁共振成像技术通过图像能够显示出体层内的组织形态和生理生化信息,并且通过调整梯度磁场的方向和方式,可以直接获得不同断面、不同体位的体层图像。
2.2 核磁共振成像技术
由于人体大脑的灰、白质的密度相近,使用计算机层析成像(CT)技术页很难分辨,而核磁共振成像[8](MRI)技术所获得的图像中可采用白、灰、黑三级来表示[9]。因此,在脑部疾病检测的过程中,MRI技术的应用更为广泛。由于计算机技术、电子技术、超导技术等技术的迅猛发展,核磁共振已然成为一种更加适用于临床医学的生物磁学核自旋成像技术。该技术利用核磁共振原理,通过检测外加梯度磁场,得到其发射出的电磁波来绘制物体内部的结构图像。该技术在科学研究、临床诊断中的应用极大地推动了医学、神经生理学和认知神经科学的发展和进步。
核磁共振成像技术是一种对人体没有任何伤害的技术,并且安全性高、准确度高、速度快,适合于疾病的临床诊断。核磁共振图像对人体内的软组织具有极高的分辨率,各种参数都可以用来成像,大量的成像参数能够给临床医学提供丰富的诊断信息,因此,这种技术也使得医疗诊断、对人体内代谢和功能的研究更加方便、更加有效。除此之外,通过对磁场进行调节,可自由选择临床中所需要的剖面,能够得到其他成像技术所不能达到或很难达到部位的图像。尤其在颅脑疾病研究中,基于MRI技术的诊断具有更高的预测性及确定性,并且在诊断过程中可以直接显示脑血管及颅神经,能够在早期发现神经上的病变[10]。因为氢元素在人体内普遍存在,并且信号是最强的,所以在对人体内部利用该技术进行成像时,用于显像的装置基本都是对氢原子成像。人体中不同组织的氢含量不同,所以一旦在同一组织中检测出氢原子核的密度和弛豫时间存在着明显差异,就说明该部位存在着病变的情况。因此,核磁共振技术就是把人体中质子密度和弛豫时间的空间分布进行分析处理,然后展现成便于医生观察的医学图像。
张雪林等[11]针对颅脑疾病对MRI与X-CT诊断价值进行了比较,实验分析了530例颅脑MRI检查结果,并与同时进行的X-CT检查的345例的结果进行比较。从显示病变部位、病变种类来看,两者相似,但是显示脑干、基底节、中线结构、颅底及脑池、枕骨大孔区肿瘤、腔隙脑梗塞、脑池囊性占位病变、慢性硬膜下血肿等方面时,MRI要优于X-CT。
为了便于清晰地认识核磁共振图像,本文从哈佛医学院官方网址(http://www.med.harvard.edu/AANLIB/)中下载了部分脑部疾病的核磁共振图像,如图1所示。
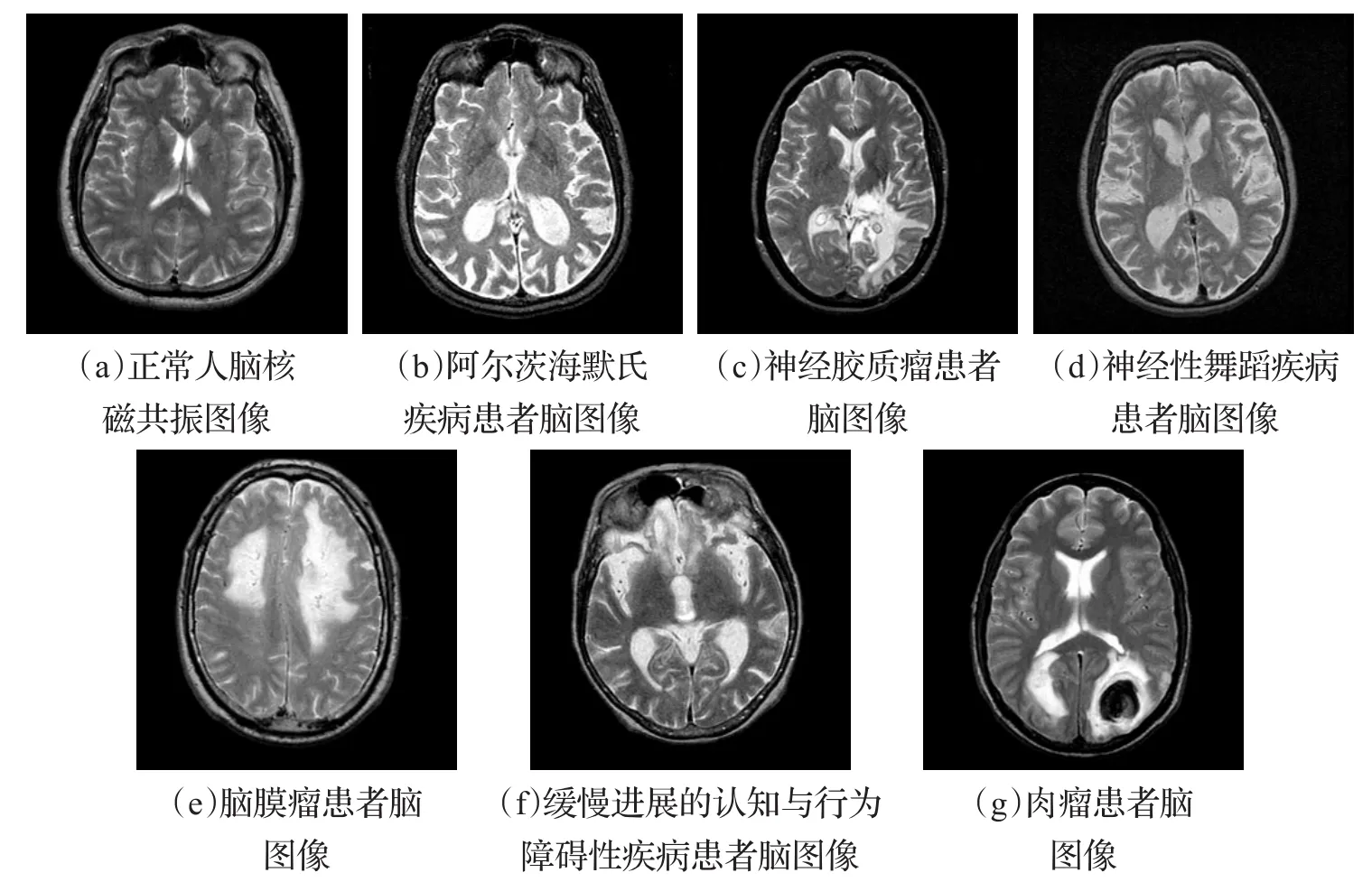
图1 不同种类脑部疾病的核磁共振图像
然而,由于射频场的不均匀特性,脑部核磁共振图像的灰度均匀性会变差,在实际应用中,这将会直接导致传统的基于灰度值的分割模型分割失败。除此以外,在成像过程中,由于受到设备等物理原因影响,所获得的图像中常含有噪声,检测结果受到较大的干扰。上述的因素都使得基于核磁共振图像的脑部疾病检测方法难度提升。因此,王利[12]在文章中提出了采用连续的方法,基于图像局部均值的分割模型来克服上述内容中所存在的灰度不均匀性,并通过多相位水平集方式来拟合局部灰度,从而在图像中同时得到白质、灰质和脑脊液。
吴海远[13]在实验中选择了核磁共振成像技术对患者进行诊断,实验包括脑血管病患者与健康体检者各45例,其中脑血管类疾病患者包括脑出血患者5例、脑梗死患者36例、颅内动脉瘤患者4例。在实验完成很顺利情况下,45例正常测试者的脑部血管显示均很清晰,45例该类疾病的患者可以看到明显的影像图征象。实验总诊断率为92%(83/90),定位诊断率为100%(100/100)。该实验表明,针对该类疾病患者使用核磁共振成像技术进行脑部检查,有利于尽快明确病情,给医生制定实施方案提供有效的依据,能够在临床医学中推广并得到有效的应用。董会卿等[14]在实验中发现MRI线性测量局部脑萎缩程度的方法能够鉴别轻度痴呆的阿尔茨海默氏症与多发脑梗塞性痴呆以及正常患者,实验中使用的核磁共振成像仪是由德国西门子公司生产,在MRI诊断台上进行两点间线性测量,精确度为1 mm。实验敏感度为93%,特异性为95%。
3 基于图像的病脑检测方法
在利用不同成像方法获得的脑部图像之后,传统方法是利用医生的工作经验对患者的疾病进行诊断,但这种情况下医生的判断会受到各种主观及客观因素的影响。例如,年长医生的视力较弱,或者由于各种原因造成的图像噪声等都会造成医生对病人病情的诊断误差,轻度地会影响病人的早期预防和治疗,严重地则可能影响病人的生命安全。因此,大量的研究者通过将计算机辅助诊断的方法对病人的病情进行诊断,并且从研究实验来看,计算机辅助诊断的方法具有较高的准确性、敏感性和特异性。
3.1 传统人工智能方法
周珂等[15]利用MRI技术以及VBM-DATEL(基于体素的形态学测量-基于指数分布的微分解剖解析)方法对阿尔茨海默氏症患者、轻度认知障碍(MCI)患者以及正常人对照组进行实验,其中AD患者14例、MCI患者21例、健康对照者23名,实验在MATLAB软件下进行。实验结果表明该结果与临床研究的报道基本一致,进一步证明了DARTEL方法的有效性。
刘佳超[16]基于脑部核磁共振成像数据,提出了利用相关分析法和贝叶斯网络模型法研究阿尔茨海默氏症病人和正常人的脑结构网络。实验首先将两组数据进行预处理,将脑区的体素平均值作为统计分析的输入变量;然后分别对两组数据进行组内相关性分析和组间的相关性分析;最后对两组数据分别构造贝叶斯网络模型,并做了组间差异的检验和对比分析。实验结果表明所提出的方法与核磁共振图像分析中得出的结果有一定的共通之处,并且符合病理学的解释,这也证明了文中提出方法的合理性和可靠性。
李逸尘[17]提出了基于多模态神经影像的CAD方法,来对阿尔茨海默氏症患者进行诊断检测,实验首先对原始图像进行预处理,解决分辨率、图像尺寸、相对位置等不一致的问题;然后根据基于ROI特征提取的方法对原始特征使用耦合特征表达和稀疏特征选择的方法,计算特征之间Pearson相关系数,表达ROI间的互联信息;其次使用耦合的Boosting算法对这种疾病进行分类。该方法在多模态数据的AD和正常对照组(NC)分类准确率高达98.1%,与单模态数据和其他传统方法相比具有明显的优势。但是研究中MCI(轻度认知功能障碍)与AD或NC的分类效果不太好。
Canisius[18]通过随机森林算法对MRI图像数据进行分析,以达到对AD疾病的诊断。随机森林算法能够从MRI的高维数据中学到低维特征和表达。实验使用AD、MCI以及NC图像数据各64、103、71例。实验中,AD/NC组准确率为93.25%,MCI/AD组准确率为88.73%,MCI/NC组准确率为81.45%。实验结果与文中列出的其他方法相比具有一定的优势。
王磊等[19]提出了一种基于统计学纹理特征的阿尔茨海默氏症的诊断方法,实验通过使用基于统计学理论的纹理分析的方法,利用灰度共生矩阵和游程长矩阵来提取AD患者MR图像上重要区域的纹理特征参数,首先从实验数据集中所有图像的ROI共提取了64个统计纹理特征参数,之后根据Fisher系数选择了12个纹理特征参数作为实验中所使用的有效参数,然后对AD患者和HC对照组进行分类识别。研究结果表明,使用该方法和Fisher判别分析法得到的识别率最高达到90.12%,但是在参数选择的过程中,有可能被丢失部分重要的特征信息从而影响疾病诊断的准确性。
朱旭艳[20]提出了一种基于图像信息融合的AD疾病计算机辅助诊断算法,实验中AD和HC数据共87个,针对实验数据,作者首先利用像素级融合中的加权平均法对MRI和PET 3D图像进行融合,然后利用图像间配准的形变场提取MRI图像特征,最后使用支持向量机的方法对提取的样本特征进行分类,并使用交叉验证的方法对分类结果进行评估。实验对脑部34个大脑皮层分区分类,结果显示对内嗅区皮质区域分类准确率最高为94.25%。虽然实验取得了较好的准确率,但是时间耗费比较大,特征维度的降低仍值得深入的研究。
Nayak等[21]提出了一种有效的病脑检测方法,克服了类似小波熵的特征提取方法,类似前馈神经网络和支持向量机的分类器等存在的限制与不足。该方法使用二维离散小波变换的方法提取特征,然后结合改进的粒子群优化和极限学习机(MPSO-ELM),对病脑图像进行检测。改进的粒子群优化用来优化单隐层前馈神经网络的隐层结点参数(输入权值和隐层的偏置项),实验中的输出权值由分析后得到。实验结果表明相比于传统的ELM-BPNN分类方法,MPSO-ELM算法能够得到更高的分类精度。
杨宁等[22]在MRI的前提下,提出了一种基于张量法的AD脑图像分类方法。实验采集了70例AD患者、112例MCI患者和70例NC脑部图像,通过提取脑灰质个体素的灰度,得到三阶灰度张量;然后通过张量的独立成分分析得到三阶灰度张量的独立成分。通过将张量特征转化为向量特征来降低数据维数,然后利用递归特征取消法得到有效的主要特征,该分类系统采用7折交叉验证的方法进行训练测试。从实验结果可以得到,AD/NC的分类正确率为99.29%,敏感度为98.57%,特异性为100.00%;AD/MCI的分类正确率为91.39%,敏感度为80.95%,特异性为97.92%;MCI/NC的分类正确率为89.38%,敏感度为95.24%,特异性为80.00%。
庞宇等[23]在对颅内图像进行处理分析时,根据Ahmed等人[24]提出的FCM_S(FCM_Spatial)算法,在此基础上加入了空间距离因素进行实验,这种方法有效抑制了噪声并降低了该方法的时间复杂度。实验中对颅内图像分别加入10%的高斯噪声和椒盐噪声,文中分别针对标准FCM、FCM_S和作者提出的FCM_SPW算法进行了实验,结果表明文中提出的方法对两种噪声都有着很好的抑制作用,并且该方法的时间复杂度较低,适合于大量数据的运算,但是这种方法所进行的实验较为简单,泛化能力较弱。
栾信海[25]实现了多种不同的算法并对结果进行了分析,首先使用Level Set对肿瘤进行分割的改进方法找到初始轮廓,并在加入了形态学的修正之后得到最终结果;然后使用模糊C均值(FCM)聚类方法将同一簇相似度最大、不同簇相似度最小的类别进行划分,从而得到肿瘤的分割结果;最后基于差值变换的阈值分析利用MRI成像特点对T1和T2加权像进行一定的变换,使得不同组织之间的信号对比度更强;FCM与水平集结合的算法可以提高寻找的准确度和稳定度,减少实验的时间消耗。但是实验过程中的手工操作难免会浪费人力资源。
Nayak等[26]采用一种简化脉冲耦合神经网络(SPCNN)进行ROI分割,并使用快速离散曲波变换(FDCT)方法进行特征提取,然后利用PCA+LDA方法进行特征降维,最后引入概率神经网络(PNN)对病脑图像进行病理和健康的二分类。使用该方法进行病脑分类时,在不同阶段需要调整的参数数量明显减少,实验精度更高,学习速度优于文中的其他算法。
Jha等[27]利用维纳滤波降噪的新模型,使用二维离散小波(2D-DWT)进行特征提取,概率主成分分析(PPCA)进行降维,然后采用基于K近邻(KNN)算法的随机子空间集成分类器(RSE)对病脑图像进行病理和正常的二分类。实验基于5×5交叉验证,分类准确度、灵敏度、特异性均优于文中的其他算法。
Yang[28]首先在二元树复小波变换(DTCWT)的基础上进行s级分解,进而从每个子带获得12个方差和熵的特征,然后,作者使用支持向量机(SVM)及其变体:广义特征值近似支持向量机(GEPSVM)和双支持向量机(TSVM)。实验结果表明使用双支持向量机的方法取得的平均准确率高达99.57%,优于文中提出的其他方法。
从表1中可见病理脑检测的传统方法仍有很多的不足,主要体现在:(1)需要手动提取特征,这可能造成部分重要信息的丢失,并且对人工的要求较高,在临床诊断中的适用性不强;(2)只能对病理脑图像进行二分类,而不能同时检测出不同类型的疾病,对于当前仍未发现的疾病来说没有任何价值和意义;(3)实验采用的数据量相对较少,实验的泛化能力不强。
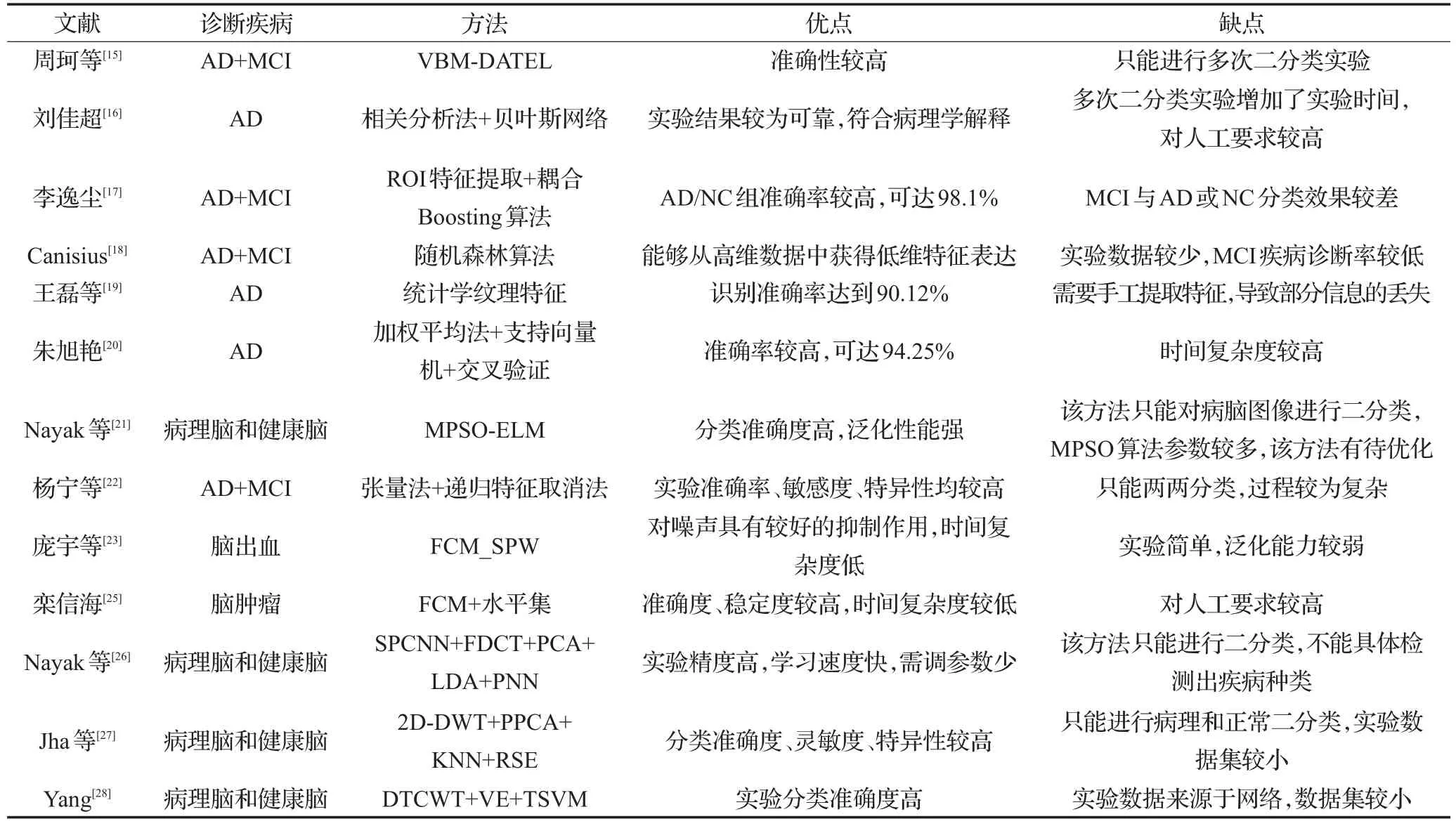
表1 基于传统方法的脑部疾病诊断方法比较
3.2 深度学习方法
针对传统病理脑检测方法上存在的不足,研究者们深入研究深度学习方法,并发现它不仅能够自动提取出有利于图像识别的图像数据的特征,对数据集中的病脑数据同时进行多分类,而且对于大量的图像数据也能够同时进行处理,通过大量的训练数据来学习更加抽象的深层特征,并由此提升分类或者预测的准确性,得到的实验准确率较高[29-30]。
Jia等[31]采用堆叠式稀疏自编码器(SSAE)的方法,对具有听力损失的患者脑图像进行分类,将其分为左耳听力损失、右耳听力损失以及正常听力三类。在训练数据集之前,作者采用数据增强(DA)的方法扩大数据集,使得不同类别脑图像的分布更加均匀。文中使用的方法能够自动学习特征,并使用softmax分类器对其进行较高准确度的分类,实验结果表明该方法高于文中列出的其他算法。
惠瑞等[32]利用深度学习中卷积神经网络的方法,对脑影像进行分类,从而达到提高脑影像智能化分类性能的目的,为临床上检查阿尔茨海默症疾病提供便利。该实验的数据集包括AD、器质性病变(如脑肿瘤、脑出血等)和正常老年化人群的数据,实验结果显示,该方法对AD疾病的检测准确率高达84.2%,该实验也为检测AD疾病提供了新的方法。但是该方法对实验中脑器质性病变类疾病的检测准确率不高。
Poole等[33]提出一种三维卷积神经网络(3D-CNNs)的方法来检测大脑中微妙的中风迹象,实验将122个CT图像平均分成训练集和测试集来验证该方法的有效性,实验结果表明该方法的ROC曲线精确度为99.6%,召回率为56.3%。虽然该方法还没有达到常规临床应用的水平,但实验结果仍令人鼓舞。
马宗帅[34]基于受限玻尔兹曼机网络和BP神经网络,提出了一种脑血管疾病的预测方法,实验中使用的数据集中各个属性的平均值和整个数据集的标准差是通过使用Z-score标准化方法计算得到,从而实现对脑血管疾病数据的归一化处理,达到消除指标之间的互相影响的目的;然后,构建基于DBN的脑血管疾病模型,使用逐层贪婪学习算法进行训练,设置输入结点、隐层层数及各隐层结点的个数,经过多次实验,得到最优参数,并根据这些参数得到一个最终的DBN预测模型;实验结果与BP模型进行比较得到,文中使用的模型平均准确率高于BP模型得到的准确率。但是实验所使用的数据量仍然较少,不能达到更加具有普遍性的预测效果。
程俊龙等[35]在对脑部核磁图像进行小波去噪和直方图均衡化预处理之后,分别采用栈式自编码(SAE)神经网络和卷积神经网络(CNN)两种深度学习方法提取图像的特征,从而构建了特征模型;使用模糊C均值聚类算法(FCM)对其进行粗分割,然后将粗分割结果中的灰质和白质部分区域作为训练集,使用支持向量机进行分类器训练,最后对整个脑部区域进行分类,最终得到了精确的脑部灰质和白质区域。实验结果表明,虽然这两种方法在特征提取中都可以取得较为理想的分割结果,但是与SAE相比,CNN方法在分割效果和分割效率上都更具有优越性。
Arezou等[36]实现了特征融合(FF)与稀疏降噪自编码器(SDAE)相结合的方法来揭示阿尔茨海默氏症的不同阶段。通过堆叠自编码器进行高层特征提取,实验数据包括晚期轻度认知障碍、早期轻度认知障碍和正常对照组,正常对照组,采用高层和低层特征融合的多项式logistic回归对实验数据进行分类,结果表明基于特征融合的SDAE具有较高的准确度和召回率。
杨星[37]提出了一种基于RBM和反向传播(BP)算法的脑血管疾病的诊断方法,实验通过RBM的构建与堆叠深度置信网络的建立,在最后一层使用BP算法实现整个网络的微调,最终生成DBN模型。实验数据来自于脑血管病医联体云平台,对数据集中所有2 970例入组人群采用随机抽取数据样本的方式,将其中2/3进行模型训练,剩余1/3用来对模型的性能进行评价,训练数据包含1 980个患者的31维输入特征和5维目标特征,测试数据包含990个患者的31维输入特征和5维目标特征。实验的最优预测准确率为82.1%,而对比算法的最优准确率仅为74.17%。但是,对非结构化数据的相关处理仍值得研究。
Sui[38]提出了一种基于漏纠正线性单元(L-ReLU)和最大池化的八层卷积神经网络的AD疾病分类方法,实验表明该方法的性能优于其他方法,该方法实验灵敏度为97.96%,特异性为97.35%,准确度为97.65%,与实验中对比的其他算法相比,该方法提高了约5%的精确度。但是该算法中的超参数是通过实验获得的,整体时间复杂度较高。
秦臻等[39]发明的一种基于深度学习的脑肿瘤分类方法利用Gabor小波变换的方法来提取脑肿瘤图像的纹理特征,然后采用堆叠降噪自编码(SDAE)来构建深度网络,利用深度学习来提取更高层的特征,与纹理特征与形状特征结合形成最后的特征向量,然后将提取出的特征向量输入支持向量机中进行训练得到分类器。这一发明克服了现有脑肿瘤分类方法中的不足,降低了分类错误率,有利于医生在临床中更加准确直观地判断肿瘤的类型,并制定合适的手术方案。
林伟铭等[40]针对阿尔茨海默氏症会导致海马体区域萎缩的现象,提出了一种基于卷积神经网络(CNN)的识别方法。实验数据来自ADNI数据库中的188位患者和229位正常人的MR脑图像,在对图像进行预处理之后,使用CNN对图像数据进行训练和检测,在训练网络时,使用随机梯度下降法(SCG)调整参数,然后通过多次十折交叉验证方式的实验,得到该方法的平均准确率为88.02%。文中提出的算法相比其他算法,其准确率均提高了5个百分点以上。文章虽然得到了与该类疾病相关的海马体形态特征,但却没有分析这些海马体形态特征,并利用可视化技术为病理学研究提供参考价值。
Yota等[41]提出了使用BING对象估计的方法来分割单元区域,利用基于深度残余学习的深度卷积神经网络(CNNs)来对脑肿瘤图像进行分类。BING是一种目标快速检测方法,通过预训练BING模型来检测脑细胞,在此基础上采用一系列后处理方法,如二值化、分水岭变换等进行精细分割。实验证明,采用该方法的准确率较高。
吕鸿蒙等[42]基于增强AlexNet的深度学习提出了阿尔茨海默氏症的诊断方法,实验数据集为从ADNI得到的超过7万幅MR脑图像,其中包括AD患者43例、MCI患者113例、HC 148例。然后在改进现有AlexNet网络模型的基础上,得到实验所使用的深度学习模型,实验在大量数据集的情况下,耗时不超过30 min,在测试集准确率上,AD/HC组为96.14%,AD/MCI组为90.52%,MCI/HC为84.80%,AD/MCI/HC组为86.05%,实验过程实现了全自动化,可以避免人工筛选造成的误差。
黄若菡[43]在对MR图像进行去噪、亮度变换和直方图处理后,利用堆叠降噪自动编码器对图像进行分类。实验数据来自四川华西医院10个真实脑肿瘤患者的MRI图像,由于图像数据较大,所以采用Mini-batch方法对数据进行批处理,从而降低训练时间,设置不同的隐层数目得到的准确率最大为98.04%。但是实验采用的只是灰度特征,没有考虑组织纹理等作为网络的输入提取潜在特征,同时,实验基于二维的图像,今后可利用三维图像,更加直观地观察病变位置及形状。
连伟烯[44]采用了稀疏自编码器(SAE)的模型来构建图像检测系统,实现特征的自动提取,并将多个稀疏自动编码器进行堆叠,并连接形成深度学习网络,在完成无监督的自动特征提取之后,分类器基于BP算法,最后实现对图像的分类。实验数据来自十组真实病人的大脑MRI图像,在设置隐含层层数分别为3、4、5时,结果准确率分别为91.59%、93.16%、93.33%。但是实验采集的数据相对较少,实验次数也较少,所以利用该方法进行的实验有待于进一步研究。
从表2中,可见深度学习在多种疾病的MRI图像诊断方面具有较高正确率,并且在处理大量数据时,相较于传统方法有很大的进步,除此以外,深度学习在医学图像处理中的泛化能力较强。

表2 基于深度学习的疾病诊断分析与比较
3.3 不同方法的性能比较
在对疾病进行诊断及治疗时,计算机辅助的方法解决了人工诊断的缺点,对于传统的CAD方法以及最近热点的DL方法,作如表3所示的分析与比较。

表3 传统CAD方法和深度学习方法的比较
传统CAD方法的基本流程如图2所示,基于DL的CAD方法基本流程如图3所示,从传统和深度学习两种CAD方法的基本流程来看,可得传统CAD方法虽然步骤简单,但是需要人工操作的加入,而DL方法只需要对网络进行微调,该方法对于不同的输入数据不需要再次进行特征提取和选择。
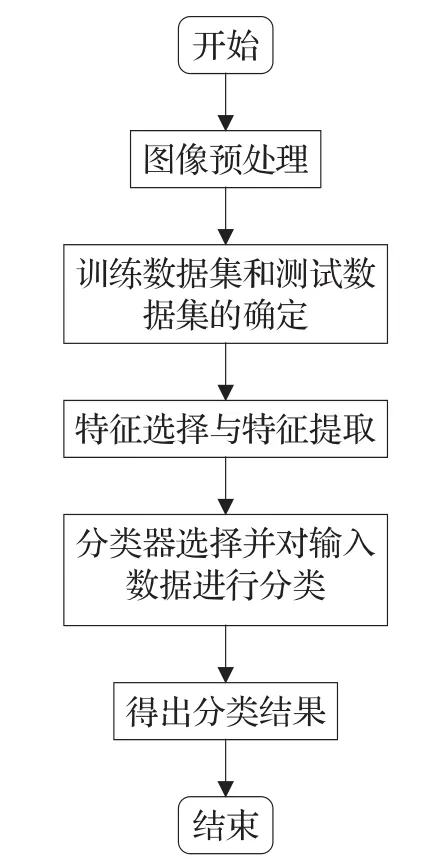
图2 基于CAD的传统人工智能方法的基本流程

图3 基于CAD的深度学习方法基本流程
4 总结及今后研究重点
医学影像是在当前阶段医疗疾病诊断过程中的重要方法和参考依据,随着计算机技术在医学上的应用越来越广泛,传统的人工诊断方法渐渐被淘汰,而MRI图像在计算机辅助诊断方法中的地位也越来越重要,因此,本文主要针对MRI医学成像技术和基于CAD方法的病脑图像分类性能进行比较与分析。本文的主要工作包括:(1)简单介绍了医学影像诊断的发展过程,并对存在的问题进行了分析;(2)介绍了MRI技术在医学诊断中的重要作用以及应用性能;(3)对传统CAD方法在病理脑疾病诊断方面的实验进行了分析;(4)基于当前较为火热的深度学习,研究者对疾病的诊断所提出的方法进行分析;(5)对传统及深度学习的方法进行了比较。更多关于病脑检测的方法,可参见2017年、2018年的两篇专著[45-46]。
在文献分析中,深度学习在病理脑疾病诊断方面的性能更为优越,但是也存在着一些问题,比如:(1)对计算机配置要求较高;(2)对数据量的要求也较高,只有数据较多的情况下实验性能才好;(3)实验所消耗的时间较多,这些问题也是值得日后深入研究与探讨的内容。
因此,日后研究重点应该放在基于深度学习的病脑检测当中,应努力查找方法来提高算法的时间复杂度。由于当前基于深度学习的病脑检测方法泛化能力较弱,今后也需要深入算法的研究,使得算法能够对不同疾病都能进行诊断,同时提高病脑检测方法的临床应用水平。
参考文献:
[1]张于,程伟.中西医治疗阿尔兹海默病的研究现状[J].中医临床研究,2012,4(13):115-117.
[2]李润辉.阿尔兹海默病的研究现状[J].沈阳医学院学报,2013,15(3):129-133.
[3]夏淳,张宜友,翁宇清.脑出血的流行病学研究进展[J].中国预防医学杂志,2010,11(10):1075-1077.
[4]Panchbhai A.Wilhelm Conrad Röntgen and the discovery of X-rays:Revisited after centennial[J].Journal of Indian Academy of Oral Medicine and Radiology,2015,27(1):90.
[5]王骏,周桔.多排探测器CT成像技术[J].医疗卫生装备,2006,27(2):52-54.
[6]Menikou G,Yiannakou M,Yiallouras C,et al.MRI-compatible breast/rib phantom for evaluating ultrasonic thermal exposures[J].Int J Med Robot,2018,14(1):1-12.
[7]芦钺,郑义.颅脑超声成像在窒息新生儿颅脑疾病的应用分析[J].世界最新医学信息文摘,2017,17(87):23-24.
[8]Qin Y,Li G L,Xu X H,et al.Brain structure alterations and cognitive impairment following repetitive mild head impact:An in vivo MRI and behavioral study in rat[J].Behav Brain Res,2018,340:41-48.
[9]裴晴.核磁共振成像技术在颅脑疾病诊断中的应用[J].基层医学论坛,2015,19(11):1499-1500.
[10]潘鹤松.核磁共振成像技术在颅脑疾病诊断中的应用[J].医学影像,2015,15(42):99.
[11]张雪林,黄其流.颅脑疾病MRI与X-CT诊断价值的比较[J].中风与神经疾病,1989,6(3):131-133.
[12]王利.脑核磁共振图像分割技术研究[D].南京:南京理工大学,2010.
[13]吴海远.核磁共振血管成像对脑血管疾病的临床诊断及应用价值[J].医学影像,2015,15(16):128.
[14]董会卿,颜振瀛,李坤成,等.MRI线性测量局部脑萎缩对早期阿尔兹海默病的诊断意义[J].中华神经科杂志,1998,31(2):92-94.
[15]周珂,蔡洁,熊刚强.VBM-DARTEL方法在阿尔茨海默症MRI图像分析中的应用[J].计算机应用与软件,2014,31(3):187-190.
[16]刘佳超.基于贝叶斯网络的脑结构网络研究及其在阿尔茨海默氏症的应用[D].北京:北京师范大学,2011.
[17]李逸尘.基于多模态神经影像的阿尔兹海默症计算机诊断方法研究[D].福建厦门:厦门大学,2016.
[18]Canisius G.基于随机森林的阿尔兹海默症计算机辅助诊断算法研究[D].福建厦门:厦门大学,2016.
[19]王磊,童隆正,周晓霞,等.基于统计学纹理特征的阿尔兹海默病MR图像研究[J].北京生物医学工程,2009,28(1):14-16.
[20]朱旭艳.基于图像信息融合的阿尔茨海默氏症计算机辅助诊断算法研究[D].长沙:湖南大学,2013.
[21]Nayak D R,Dash R,Majhi B.Discrete ripplet-II transform and modified PSO based improved evolutionary extreme learning machine for pathological brain detec-tion[J].Neurocomputing,2017,282:232-247.
[22]杨宁,徐盼盼,刘佩嘉,等.基于张量法的阿尔兹海默症脑图像分类[J].中山大学学报,2017,56(2):40-47.
[23]庞宇,霍修坤,潘丽丽,等.一种改进的FCM算法在脑出血图像中的应用[J].电子技术,2011,38(6):45-47.
[24]Ahmed M N,Yamany S M,Mohamed N.A modified fuzzy C-means algorithm for bias field estimation and segmentationofMRIdata[J].IEEE Transactionson Medical Imaging,2002,21(3):193-199.
[25]栾信海.MRI脑部疾病计算机辅助诊断系统设计与实现[D].沈阳:东北大学,2009.
[26]Nayak D R,Dash R,Majhi B,et al.Automated pathological brain detection system:A fast discrete curvelet transform and probabilistic neural network based approach[J].Expert Systems with Applications,2017,88:152-164.
[27]Jha D,Kim J I,Choi M R,et al.Pathological brain detection using weiner filtering,2D-discrete wavelet transform,probabilistic PCA,and random subspace ensemble classifier[J].Comput Intell Neurosci,2017,8:1-11.
[28]Yang M.Dual-tree complex wavelet transform and twin support vector machine for pathological brain detection[J].Applied Sciences,2016,6(6).
[29]侯宇昆.深度学习在图像处理领域的研究[J].信息系统工程,2017(7):163.
[30]陆家发,张国明,陈安琪.基于深度学习的疾病诊断[J].医学信息学杂志,2017,38(4):39-43.
[31]Jia W,Yang M,Wang S H.Three-category classification of magnetic resonance hearing loss images based on deep autoencoder[J].J Med Syst,2017,41(10):165.
[32]惠瑞,高小红,田增民.基于深度学习的CT脑影像分类方法用于阿尔茨海默病的初步筛查[J].中国医疗设备,2017(12):15-19.
[33]Poole I,Muir K,Beveridge E,et al.Thrombus detection in CT brain scans using a convolutional neural network[C]//Int Conf on Bioimaging,2017:24-33.
[34]马宗帅.基于深度学习的心脑血管疾病预测方法研究[D].西安:西安建筑科技大学,2015.
[35]程俊龙,赵越.基于深度学习的脑部核磁图像分割算法[J].轻工科技,2017(8):93-97.
[36]Arezou M K,Mo J,Subhashie W.Feature fusion for denoising and sparse autoencoders:Application to neuroimaging data[C]//IEEE International Conference on Machine Learning and Applications,2017:605-610.
[37]杨星.基于深度置信网络的脑血管病风险预警研究[D].北京:北京交通大学,2016.
[38]Sui Y.Classification of Alzheimer’s disease based on eightlayer convolutional neural network with leaky rectified linear unit and max pooling[J].Journal of Medical Systems,2018,42(5).
[39]秦臻,杨晓明,蓝天,等.一种基于深度学习的脑肿瘤分类方法:中国,CN104834943A[P].2015-08-12.
[40]林伟铭,高钦泉,杜民.卷积神经网络诊断阿尔兹海默症的方法[J].计算机应用,2017,37(12):1-5.
[41]Yota I,Kiyotada W,Kota A,et al.Brain tumor classification of microscopy images using deep residual learning[C]//SPIE BioPhotonics Australasia Conference,2016.
[42]吕鸿蒙,赵地,池学斌.基于增强AlexNet的深度学习的阿尔茨海默病的早期诊断[J].计算机科学,2017,44(6A):50-60.
[43]黄若菡.脑肿瘤的计算机辅助检测[D].成都:电子科技大学,2016.
[44]连伟烯.基于SAE的MRI图像检索系统[J].电子世界,2016(5):160-161.
[45]Lu S.Pathological brain detection by advanced extreme learning machines[M].Germany:Lambert Academic Publishing,2017.
[46]Wang S H.Pathological brain detection[M].Germany:Springer,2018.

