硝苯地平缓释片的质量标准研究
赵 静,宗春燕
(泰州职业技术学院, 江苏 泰州 225300)
缓释片是更具安全、有效、方便的新剂型,在口服药物中极具竞争力。而骨架控缓释技术更易推广,便于实现工业化生产。按中国药典2015版规定,缓释片系指在水中或规定的释放介质中缓慢的非恒速释放药物的片剂,与其相应的普通制剂比较,给药频率减少一半或有所减少,且能显著增加患者顺应性的制剂[1]。
硝苯地平的半衰期很短,仅仅为2~3 h,因此在患者服下药物后,血药浓度在短时间内很快就会上升到最高值,短暂而又强烈的扩张血管的作用,会造成反射性兴奋交感,从而会增加患者得冠心病的几率。另一方面,由于药效时间太短,患者不得不在单位时间内增加服药次数,血药浓度时高时低,波动很大,从而导致心律加快、面部潮红等不良反应,严重的还会引发心律失常,心衰甚至猝死等后果。因此,研制长效的硝苯地平缓释片,以减少患者的服药次数和避免诸多不良反应,是一个急需解决的问题[2-4]。
1 仪器
AL104型分析天平(梅特勒-托利多仪器(上海)有限公司生产);ZRS-8L型智能释放试验仪(天津市天大天发科技有限公司);UV-754型紫外检测仪(上海精密科学仪器有限公司);78X-3A型片剂四用测定仪 (上海黄海药检仪器有限公司)。
2 方法与结果
2.1 最大吸收波长的选择
用分析天平精密称取硝苯地平原料药,称得24.6 mg,置于100 mL容量瓶中。加入适量无水乙醇,置于超声仪中,进行超声,以保证完全溶解。至其完全溶解,定容至刻度,做为储备液。然后移取储备液容量瓶中的溶液0.4 mL至10 mL容量瓶中,加入无水乙醇定容至刻度线,配得9.84 μg/mL的溶液。另外精密称取HPMC K4M 58.6 mg,MCC 57.3 mg,乳糖 60.0 mg,加到 50 mL的容量瓶中,加无水乙醇定容,以考察辅料的干扰情况,最后进行紫外扫谱。
紫外扫谱:以在200~400 nm范围内进行紫外光谱扫描,测得硝苯地平在237 nm和333 nm处有较强的吸收峰,且辅料无干扰,含量测定选择333 nm作为含量测定的吸收波长。扫谱结果见图1和2。
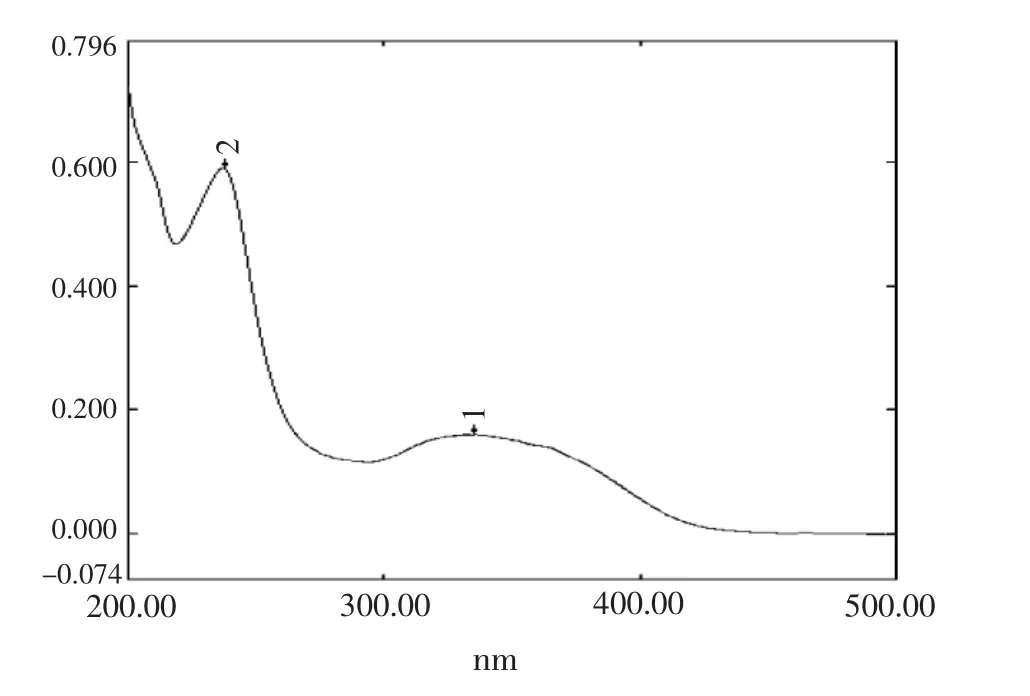
图1 硝苯地平的无水乙醇溶液的紫外扫谱图
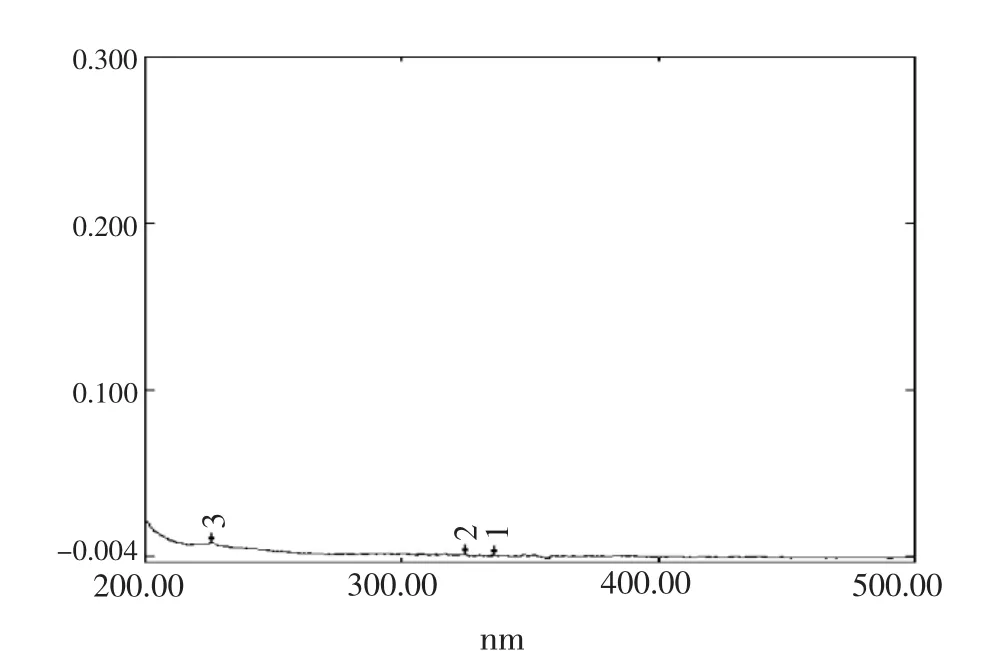
图2 辅料的无水乙醇溶液的紫外扫谱图
2.2 标准曲线的建
分别移取储备液 0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.2 mL、1.6 mL 至 6个 10 mL 容量瓶,加入无水乙醇定容至刻度线,配成相应浓度的供试品溶液,将其编号1~6号。平行做三组,以减少实验中仪器造成的误差。此时,稀释后的标准溶液的浓度分别为 4.92 μg/mL、9.84 μg/mL、14.76 μg/mL、19.68 μg/mL、29.52 μg/mL、39.36 μg/mL。
测量紫外:打开紫外分光光度仪,预热30 min。以介质无水乙醇作空白试剂,用紫外-分光光度法,在333 nm下测定各供试品溶液的吸光度,记录测得的吸光度值。以浓度(μg/mL)对吸光度进行线性回归,结果如表2,回归曲线见图3。

表2 无水乙醇为介质时的溶液吸光度记录

图3 含量测定的标准曲线图
2.3 含量测定的方法
取自制的硝苯地平缓释片
20片,用分析天平精密称定,记录总质量。放入研钵,研细,精密称取适量(约相当于硝苯地平15 mg),置研钵中,加三氯甲烷2 mL,研磨,并把称量纸上残留的粉末用少量无水乙醇冲入研钵,以减小误差。用无水乙醇把研钵中的药物分次定量转移至50 mL容量瓶中,超声振荡使硝苯地平溶解,再用无水乙醇稀释至刻度,摇匀,过滤。精密吸取续滤液5 mL置50 mL容量瓶中,加无水乙醇定容,用紫外分光光度仪测吸光度,计算含量,并判断含量是否符合标准。含量应为标示量的90.0%~110.0%。
含量=[(A-0.002)/0.013]×500/取样量×平均片重。
标示量%=(含量/标示量)×100%。
2.4 回收率试验
回收率试验用来考察实验方法是否可行,如果回收率太低,说明含量测定时的测得量也会很小,方法就不可行。回收率试验的方法为:用分析天平精密称取干燥至恒重的硝苯地平原料药,约为理论含药量的80%,100%,120%,至50 mL容量瓶,按照处方中最大辅料量加入辅料,加入无水乙醇适量,并使用超声溶解,然后用无水乙醇稀释至刻度线。过滤,取续滤液5 mL,加到50 mL容量瓶中,加无水乙醇至刻度,测吸光度。每个平行做三组。根据测得的吸光度,代入标准曲线算得含量,称取的主药量为m1,测得的主药量为m2,计算回收率。回收率结果见表3。
回收率=m2/m1×100%,RSD%=STDEV/AVERAGE×100%。
结果显示该实验条件下,硝苯地平的回收率良好。

表3 回收率实验结果
2.5 释放度测定
2.5.1 释放介质的选择
经查阅相关文献,发现已经报道的释放介质有不少,比如0.1 mol/L HCl溶液[5],磷酸盐缓冲溶液[6],蒸馏水[7],5%乙醇溶液[8],0.02%SDS 水溶液[9],0.4% 吐温-80磷酸盐缓冲液[10]。2015版药典中,硝苯地平片剂的溶出度检查使用的溶出介质为0.25%的十二烷基硫酸钠溶液,故本文也将采用0.25%的十二烷基硫酸钠溶液900 mL作为释放介质。其配制方法为:称取十二烷基硫酸钠2.5 g,倒入1000 mL容量瓶中,加蒸馏水溶解稀释至刻度,经过超声脱气,然后用1000 mL的量筒量取900 mL倒入溶出杯。
2.5.2 标准曲线的建立
用分析天平精密称取105℃干燥至恒重的硝苯地平原料药25.4 mg,置于50 mL容量瓶中,加无水乙醇溶解并稀释至刻度,摇匀,再量取5 mL,置于50 mL容量瓶中,加无水乙醇定容。精密量取储备液 0.2 mL、0.4 mL、0.8 mL、1.2 mL、1.6 mL、2.0 mL、2.4 mL分别加0.25%十二烷基硫酸钠溶液稀释至刻度得浓度为 1.016 μg/mL、2.032 μg/mL、4.064 μg/mL、 6.096 μg/mL、 8.128 μg/mL、10.160 μg/mL、12.192 μg/mL 的系列浓度溶液, 照紫外分光光度法,记录测得的吸光度值,并算得标准曲线。结果如表4,回归曲线见图4。
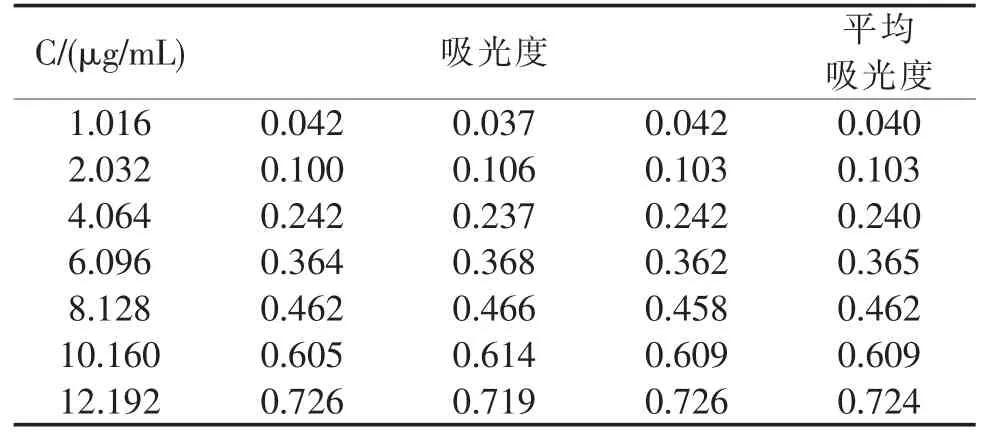
表4 吸光度记录
得到标准曲线方程为 A=0.061C-0.017,R=0.9990。
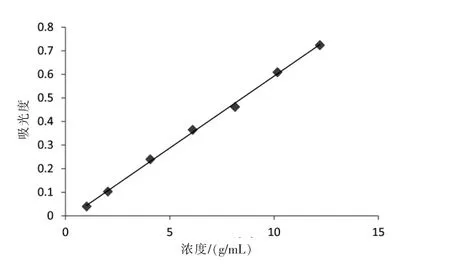
图4 释放度测定的标准曲线
2.5.3 释放度的测定方法
以0.25%十二烷基硫酸钠溶液900 mL(已超声脱气处理)作为释放介质,配好倒入6个溶出杯,另外配制一份供补充以及测吸光度时的对照液用。再将装置搭好,设置温度恒定为37℃,取样点为十个,方法为浆法,转速为50 r/min。设置完成后,开始加热,用温度计测量溶出杯中的温度37℃的时候,启动搅拌,取制得的硝苯地平缓释片6片分放入,并按下计时开关。依法操作,分别于 0.5 h,1 h,2 h,3 h,4 h,5 h,6 h,8 h,10 h,12 h时取出溶液10 mL,所取各溶液经0.45 μm微孔膜过滤后,弃去2 mL初滤液,取续滤液放入试管供测量。及时补充10 mL的释放介质。用紫外分光光度法测吸光度,代入标准曲线计算硝苯地平的释放量,再计算硝苯地平的释放度,并做出释放曲线图。
3 结论
本文采用紫外分光光度计法测量硝苯地平的含量,测定波长为333 nm,建立了含量测定的标准曲线,其方程为A=0.013C+0.002,R=0.9995,在4.92~39.36 μg/ml浓度范围内线性良好,通过回收率试验证明实验方法可行,制备的缓释片含量合格。以0.25%的十二烷基硫酸钠溶液作为释放介质,在37℃下采用浆法测定硝苯地平缓释片的释放度,建立标准曲线,得到标准曲线方程的回归方程为为 A=0.061C-0.017,R=0.9990, 在 1.016~12.192 μg/mL的浓度范围内线性良好,进而计算硝苯地平的释放度。
[1] 潘卫三.工业药剂学[M].第1版.北京:高等教育出版社,2006:305.
[2] 李晖.硝苯地平的不良反应[J].食品与药品,2006,8(09):61~63.
[3] 肖亚宝,崔生法,周中根,等.国产硝苯地平缓释制剂的研究进展[J].中国药业,2001,1(5):44-45.
[4] 易以木,杨唐玉.硝苯地平长效缓释片的研究[J].中国医院药学杂志,1999,19(5):267.
[5] 陈旭,李哗,赵志刚,等.两厂硝苯地平缓释片溶出度比较[J].华西药学杂志,2000,15(1)7l-72.
[6] 叶俊鹏,昊爱琴,黄培良,等.硝苯地平缓释片及控释片的体外释放度试验[J].广东药学,2003,13(5):25-26.
[7] 文君,崔生法,肖亚宝,等.高效液相色谱法测定24h型硝苯地平缓释片释放度[J].中国现代应用药学杂志,2003,20(1):36-37.
[8] 易以木,杨唐玉.硝苯地平长效缓释片释放度的试验研究[J].中国药学杂志, 1999, 34(5):327-328.
[9] 肖亚宝,文君.硝苯地平缓释片释放度测定方法的改进[J].药物分析杂志, 2000, 20(6):425-426.
[10]马萍,孙淑英,辛艳茹.硝苯地平缓释微丸的体外释药机制[J].解放军药学学报, 2003, 19(6):424-425.
——一个解释欧姆表刻度不均匀的好方法

