苯乳酸微生物代谢研究进展
孙大庆 ,李 芬 ,李洪飞
(1.黑龙江八一农垦大学牡丹江食品与生物技术创新研究院,黑龙江牡丹江 157000;2.黑龙江八一农垦大学国家杂粮工程技术研究中心,黑龙江大庆 163319)
苯乳酸是近年发现的一种天然生物防腐剂,抑菌谱宽、溶解性高、稳定性强、安全无毒,在食品工业中具有良好的应用前景。随着生活水平的提高,人们对健康问题日益关注。虽然化学防腐剂可以显著延长食品的保质期,但目前使用的多种化学防腐剂对人类健康具有一定的风险,因此天然、安全、高效的食品防腐剂的开发和应用研究越来越受到人们关注。
1 苯乳酸结构和来源
苯乳酸化学名2-羟基-3-苯基丙酸,又称β-苯乳酸或3-苯基乳酸,是一种天然的小分子有机酸,它的第2个碳原子为手性碳原子,因此存在2种对映异构体(图1)。Dieuleveux V S等人[1]研究表明D-苯乳酸抑菌效果稍优于L-苯乳酸,因此苯乳酸2种异构体的抑菌效果存在一定的差异。
苯乳酸异构体的结构式见图1。
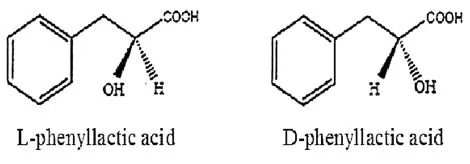
图1 苯乳酸异构体的结构式
目前已有研究证实,苯乳酸存在于多种蜂蜜、干酪和发酵蔬菜等食品中,对这些食品的防腐和保鲜具有十分重要的作用,如苯乳酸已成为蓟花蜂蜜品质的标志性检测物。
2 苯乳酸抑菌活性和机制
以往研究表明,苯乳酸是一种广谱抑菌化合物,它对革兰氏阳性细菌、革兰氏阴性细菌和真菌均有抑菌作用(表1)。这与细菌素Nisin不同,大部分细菌素只对近缘微生物产生抑菌作用,虽然Nisin可以抑制多种革兰氏阳性细菌,但对大多数革兰氏阴性细菌和真菌没有抑菌作用。苯乳酸抑菌谱见表1。

表1 苯乳酸抑菌谱
近年来,通过观察苯乳酸作用前后微生物细胞的结构变化,发现微生物的细胞膜没有显著变化,而细胞壁有明显破损现象[1]。这表明,苯乳酸抑菌机制的作用靶点很可能在细胞壁上,这与多数细菌素破坏细胞膜机制不同,而与溶菌酶的抑菌机理相似,但至今苯乳酸更详细的抑菌机制仍不清楚,需要更多、更深入的研究。
3 苯乳酸微生物合成和分解代谢
3.1 苯乳酸合成途径
目前苯乳酸微生物合成研究中利用的底物有2种,苯丙氨酸和苯丙酮酸。
苯乳酸微生物合成途径见图2。
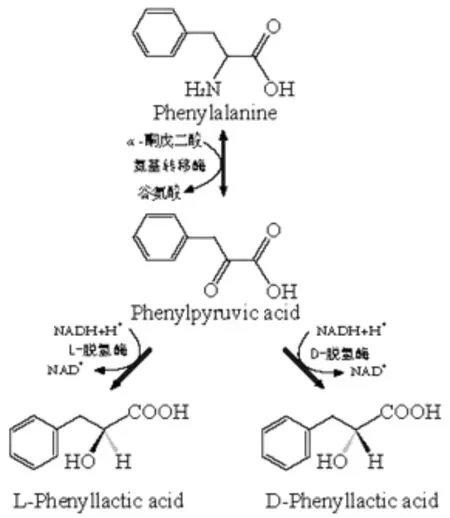
图2 苯乳酸微生物合成途径
由图2可知,苯丙酮酸是苯乳酸的最直接前体,而苯丙氨酸主要被氨基转移酶转化为苯丙酮酸后,再被氧化还原酶(主要是乳酸脱氢酶) 还原为D-苯乳酸或L-苯乳酸。
氨基转移酶是苯乳酸合成的重要限速酶,它广泛存在于动物、植物和微生物细胞中,催化转氨反应,参与氨基酸的合成与分解。其主要催化氨基酸中氨基转移到氨基接受体上,微生物代谢中的氨基接受体主要是α-酮戊二酸,而α-酮戊二酸是三羧酸循环中的重要物质之一,因此多个研究推测α-酮戊二酸、三羧酸循环途径对苯丙氨酸的转化、苯乳酸的合成具有很重要的作用[2]。Dallagnol A M C C等人[3]和Vermeulen G M等人[4]均报道,在植物乳杆菌发酵过程中添加α-酮戊二酸可使苯乳酸的产量增加5%~30%。
乳酸脱氢酶是苯乳酸合成最后一个反应的催化酶,它同样广泛分布于动物、植物和微生物细胞中,但其性质存在较大差异,在生物体内的氧化产能、解毒等生理活动中起重要作用。乳酸脱氢酶又称为NAD+氧化酶,是糖酵解最后一步反应的催化酶,即能逆催化氧化乳酸生成丙酮酸[5]。Meistei A等人[6]首次研究证明,牛瘤胃中微生物在代谢过程中,乳酸脱氢酶在NADH作用下,可将苯丙酮酸脱氢后转化为苯乳酸。
3.2 苯乳酸分解途径
苯乳酸产量不仅与合成途径密切相关,同时与苯乳酸分解代谢途径也是息息相关。然而,目前关于苯乳酸分解代谢途径的研究比较匮乏,只有个别报道对苯乳酸分解代谢终产物进行了初步研究。
李远颂[7]研究发现,苯乳酸不仅可以代谢为非蛋白氨基酸,也还可以直接转化为1-溴-2,3苯甲烷,再转化为2-苯基双氢苯并吡喃,最后转化为四氢噻唑二酮衍生物。除此之外,Wegst W等人[8]利用物理化学和色谱分析方法,在添加苯丙氨酸的无机盐培养基中分离并鉴定了一种新的代谢产物-二氢化二醇。这一结果表明,乳酸菌可以将苯乳酸转化为二氢化二醇。2009年,Zhang Z Y等人[9]利用KEGG数据库分析发现,苯乳酸可以先转化为苯乳酸辅酶A,而苯乳酸辅酶A还可以进一步降解为苯基甘氨酸和苯基谷氨酸。
4 展望
近年来,抑菌化合物已经成为微生物研究领域的一个热点,目前微生物产生的抑菌化合物主要有有机酸、细菌素、环二肽等,通过综合比较这些抑菌化合物的优缺点,人们普遍认为苯乳酸是一种非常具有开发前景的新型天然防腐剂。近年研究表明,众多微生物可以合成苯乳酸,但苯乳酸产量存在菌株特异性,因此深入了解苯乳酸结构和抑菌功能,深入细致地解释微生物苯乳酸合成与分解代谢途径,将为今后苯乳酸微生物合成和工业化应用提供十分重要的理论基础和依据。
参考文献:
[1]Dieuleveux V S,Lemarinier M.Gueguen.Antimicrobial spectrum and target site of D-3-phenyllactic acid[J].International Journal of Food Microbiology,1998,40 (3):177-183.
[2]Rijnen L C P, Gripon J C, Yvon M.Expression of a heterologous glutamate dehydrogenase gene in Lactococcus lactis highly improves the conversion of amino acids to aroma compounds[J].Applied Environment Microbiology,2000,66(4):1 354-1 359.
[3]Dallagnol A M C C,Mercado M I,de Valdez G F,et al.Effectofbiosynthetic intermediatesandcitrate on the phenyllactic and hydroxyphenyllactic acids production by Lactobacillus plantarum CRL 778[J].Journal of Applied Microbiology,2011(6):1 447-1 455.
[4]Vermeulen N G M,Vogel RF.Influence of peptide supply and cosubstrates on phenylalanine metabolism of Lactobacillus sanfranciscensis DSM20451 (T) and Lactobacillus plantarum TMW1.468[J].Journal of Agriculture Food Chemistry,2006,54 (11):3 832-3 839.
[5]Ai-Jassabi S.Purification and kinetic properties of skeletal muscle lactate dehydrogenase from the Lizard agam-stellio stellio[J].Biochemistry (Moscow), 2002, 67 (7):786-789.
[6]Meister A.Reduction of α, γ -Dike to anda-keto acids catalyzed by muscle preparation and by crystalline lactic dehydrogenase[J].Journal of Biological Chemistry,1990(3):117-129.
[7]李远颂.生物合成R-3苯基乳酸的研究 [D].儋州:华南热带农业大学,2006.
[8]Wegst W,Tittmann U,Eberspacher J,et al.Bacterial conversion of phenylalanine and aromatic carboxylic acids into dihydrodiols[J].Biochem J,1981 (3):679-684.
[9]Zhang Z Y,Liu C,Zhu Y Z,et al.Complete genome sequence of Lactobacillus plautarum JDM1[J].Journal of Bacteriology,2009 (15):5 020-5 021.◇

