药物性肝损伤与自身免疫性肝炎临床和肝组织病理学特征比较研究
刘靓懿,宿冬远
药物性肝损伤(drug induced liver injury,DILI)是由应用药物导致的肝脏损伤,通常是药物本身或代谢产物对肝细胞直接造成的损伤,患者往往出现恶心、乏力、腹痛或黄疸等症状[1]。自身免疫性肝炎(autoimmune hepatitis,AIH)是自身免疫反应引发的慢性进行性肝炎,临床表征与DILI相似[2],临床诊断往往依赖于血清学检测。本研究分析了本院收治的41例DILI和50例AIH患者的临床和病理学资料,以比较它们之间可能存在的差异。
1 资料与方法
1.1 一般资料 2014年2月~2016年4月在本院接受治疗的DILI患者41例,男性24例,女性17例,平均年龄36.6±12.7岁;AIH患者50例,男性12例,女性38例,平均年龄33.4±9.1岁。DILI诊断符合2007年中华医学会制订的《急性药物性肝损伤诊治建议(草案)》[3],即(1)出现恶心、呕吐、尿黄、发热、食欲不振、乏力、腹胀;(2)初次用药后5~90 d出现肝损伤症状;(3)停止使用药物后异常的肝功能指标恢复正常;(4)肝组织病理学检查显示汇管区有中性粒细胞浸润,伴胆汁淤积;(5)无HBV或HCV感染证据。AIH诊断符合1998年国际自身免疫性肝炎小组修订的《自身免疫性肝炎描述性诊断标准及评分诊断标准》[4],即(1)AIH诊断评分大于或等于12分;(2)血清Ig G、Ig M、Ig A水平异常升高;(3)肝组织学检查出现淋巴细胞、浆细胞浸润和玫瑰花样样结构增多;(4)无HBV 或HCV感染证据。所有患者签署知情同意书,本研究经本院医学伦理委员会批准。
1.2 检测方法 常规检测肝功能指标和血清抗核抗体(ANA)、抗肝肾微粒体抗体(anti-LKM)、抗平滑肌抗体(ASMA)、抗可溶性肝抗原抗体(anti-SLA)。
1.3 肝活检 常规进行肝穿刺。
1.4 统计学处理 应用SPSS 19.0统计软件进行数据分析,计量资料以±s表示,两组间比较采用t检验,计数资料采用x2检验,P<0.05表示差异有统计学意义。
2 结果
2.1 两组肝功能指标比较 两组血清CHE1、ALP和GGT水平无显著性差异(P>0.05);DILI组血清 ALT、AST、ALB 和TBIL水平均显著高于AIH 组(P<0.05,表1)。
2.2 两组免疫学指标比较 AIH患者血清自身抗体阳性率显著高于 DILI组(P<0.05),血清 Ig G、Ig M、Ig A 水平也显著高于 DILI组,差异有统计学意义(P<0.05,表2)。
表1 两组肝功能指标(±s)比较

表1 两组肝功能指标(±s)比较
与DILI组比,①P<0.05
?
表2 两组血清抗体阳性率(%)和免疫球蛋白水平(±s)比较
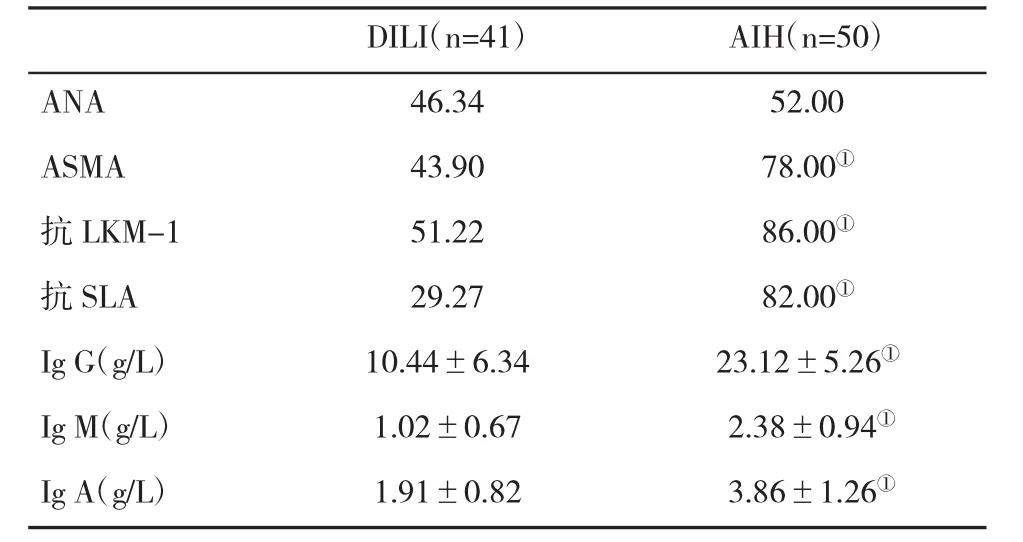
表2 两组血清抗体阳性率(%)和免疫球蛋白水平(±s)比较
与DILI组比,①P<0.05
?
2.3 肝组织病理学表现情况 AIH患者肝组织淋巴细胞、浆细胞浸润、肝细胞玫瑰花样结构出现率显著多于DILI组(P<0.05),DILI患者汇管区中性粒细胞浸润和肝内胆汁淤积发生率比AIH组多(P<0.05),差异有统计学意义(表3)。
表3 两组肝组织病理学表现(%,±s)比较

表3 两组肝组织病理学表现(%,±s)比较
与DILI组比,①P<0.05
?
3 讨论
根据自身抗体阳性类型分为3型,即Ⅰ型AIH表现为ANA或抗SMA阳性,Ⅱ型为抗LKM-1阳性,Ⅲ型为抗SLA或抗LP阳性[5]。对AIH的治疗主要以免疫抑制剂的应用为主。研究显示,皮质类固醇或其他免疫抑制剂,如强的松、硫唑嘌呤[6]、FK506、环孢素A等,可使65%患者血生化指标恢复,肝组织细胞损伤得到缓解[7]。AIH患者以女性为主,男女比例约1:4,发病高峰期以18~29岁和40~60岁为主[8]。
药物肝毒性、代谢产物肝毒性或过敏反应等引发DILI。研究表明[9],大量中药或化学药物均可引发DILI,特别是针对慢性疾病的中药所致DILI较多,且最终造成的肝损伤程度也高于化学药物,如心血管内科、精神类或免疫调节药物等的应用。在停药后一段时间内,患者肝功能逐渐恢复是DILI的特征之一,恢复的快慢与基础疾病、肝细胞损伤类型、年龄呈负相关,但少数患者由于肝损伤严重,停药后仍会出现肝衰竭而死亡。DILI患者临床表现与其他肝病相似,同样出现乏力、发热、腹胀、黄疸等症状,肝组织可见中性粒细胞和嗜酸性粒细胞浸润、胆汁淤积,血清 ALT、AST、ALP、TBIL、Ig G等指标升高。
DILI与AIH都具有肝炎的临床特征。在本研究中,我们对两种疾病患者肝功能、免疫学检测和病理学检查结果进行了对比分析。血生化检测中两组患者ALT、AST、ALB和TBIL升高达5~10倍,但DILI组显著高于AIH组。总的来说,AIH组患者自身抗体如ASMA、抗LKM-1、抗SLA阳性率较DILI组明显升高。肝组织病理学检查结果能较好地区分DILI与AIH,前者肝组织汇管区中性粒细胞浸润和肝内胆汁淤积发生率显著高于后者,而淋巴细胞、浆细胞浸润及玫瑰花样结构发生率则低于后者。同时,在对患者药物使用史详细了解的基础上,根据血生化检测、免疫学检测和病理学检查结果进行对比分析,可进一步准确地分清DILI与AIH。
【参考文献】
[1]D′Ambrosio R,Aghemo A.Treatment of patients with HCV related cirhosis:many rewards with very fewrisks.Hepat Mon,2012,12:361-368.
[2]蒋音.肝穿刺对鉴别自身免疫性肝炎与DILI的价值.肝脏,2012,17(1):47.
[3]中华医学会消化病学分会肝胆疾病协作组.药物性肝损伤诊治建议(草案).中华消化杂志,2007,27(11):765-767.
[4]Schiff E,Sorrell M,Maddrew W.Schiffs disease of the liver.8ed,Philadelphia:Lippincott Raven,1999:919-926.
[5]Zhang Y,Wang B,Wang T.De novo autoimmune hepatitis with centrilobular necrosis following liver transplantion for primary biliarycirrhosis:a case report.TransplantProc,2010,42(9):3854-3857.
[6]Maillette de Buy WL,Beuers U.Bile salts and cholestasis.Dig Liver Dis,2010,42(6):409-418.
[7]何艳.药物诱导的自身免疫性肝炎研究进展.实用肝脏病杂志,2013,16(2):178-180.
[8]Appleyard S,SaraswatiR,Gorard DA.Autoimmune hepatitis triggered by nitrofurantoin:a case series.J Med Case Rep,2010,4:311.
[9]姚云洁,刘鸿凌,朱冰,等.441例DILI患者临床何肝组织病理学分析. 实用肝脏病杂志,2015,18(3):286-289.

