乌梁素海水体重金属元素赋存形态模拟分析
赵胜男,史小红*,张汉蒙,贾辛慧,孙驰,杜蕾
1.内蒙古农业大学水利与土木建筑工程学院,内蒙古 呼和浩特 010018;2.内蒙古水利与水电勘测设计院,内蒙古 呼和浩特 010020;3.内蒙古农业大学职业技术学院,内蒙古 包头 014109
镉(Cd)是一种具有较强生物毒性的重金属,易在机体内蓄积,对人体骨骼及各项器官造成危害。在联合国规划署提出的 12种具有全球性危害的危险化学物质中,Cd被列为首位(丁鸿等,2007;钟格梅,2012)。铬(Cr)是一种毒性很大的重金属,Cr6+已被美国环境保护局确定为17种高度危险的毒性物质之一。由于 Cd、Cr的可溶性化合物均有剧毒,已被美国环保署(EPA)与国际癌症研究机构(IARC)归类为致癌物(Straif et al.,2009)。铜(Cu)是生物体不可缺少的微量元素,但是过量的 Cu会对生物体造成危害(陈怀满,1996;邱锦泉等,2015)。由于自然地质和人为因素的双重作用,环境中重金属污染日益严重,据国家环保部的调查显示,我国江河湖库底质重金属污染率高达 80.1%(Cheng et al.,2015),加之重金属的生物毒性、易富集性等特点,环境中重金属污染已成为全球关注的重大环境与健康问题。
重金属的不同存在形态具有不同生物有效性与毒性,对环境质量与人体健康也有不同程度的影响(刘清等,1996)。重金属对水体中生物的毒性不仅与总浓度有关,还取决于重金属的赋存形态(刘勇等,2001)。游离态的 Cd离子、Cu离子毒性均较大,而其稳定配合物及其与胶体颗粒结合的形态的毒性均较小(Howarth et al.,1978;Wagemann et al.,1979;刘清等,1998;张季惠等,2013)。水体中Cr2+是无毒性的,而 Cr6+的毒性则是 Cr3+的 100倍(黄坚等,2007;贡晓飞等,2015)。此外,水体氧化还原条件、温度、酸碱度、有机质等均会对重金属形态产生影响,进而影响重金属在水环境系统中的迁移、转化及富集过程(Senn et al.,2002;Couture et al.,2013;Audry et al.,2011),外界环境的变化必然会影响水体中重金属Cu、Cr及Cd的存在形态及毒性。因此,对湖泊水体中重金属的存在形态的模拟与分析不仅对摸清重金属元素在水体中的地球化学行为具有指导作用,同时对探讨其对人类健康的影响有重大意义。
水体中重金属的形态分析方法主要包括计算机数值模拟与实验室实验测定,由于与痕量和超痕量元素总浓度分析相比,形态分析的要求更高,特别是对于盐度较高的湖水或者海水,目前的分析技术难以得到可靠的分析结果(夏彧等,2016)。此外,如果对于水体中元素的存在形态未经预先判识,将无法通过实验室进行全面的形态确定分析。因此,目前水体中元素的形态分析方法多应用水文地球化学模拟软件进行,该方法较为成熟。较多学者采用PHREEQC(地球化学模拟软件)程序模拟分析了铀和超铀元素Np、Pu、Am在地下水和盐湖水中的存在形态及影响因素(Nitzsche et al.,1999;朱义年等,2005;李广玉等,2006;黄支刚等,2012;王妍力等,2015;王妍力等,2017;司高华等,2017;常阳等,2016)。夏彧等(2016)对天然海水中痕量重金属元素进行了形态分布的数值模拟研究。
乌梁素海流域内矿产资源丰富,每年大约有2×108m3(马冬梅等,2012;何连生,2013)工业废水被排入乌梁素海造成水环境重金属Cu、Cr及Cd的富集与污染。乌梁素海沉积物中 Cu的含量为18.90~39.62 mg·kg-1,远大于背景值 9.68 mg·kg-1(Zhao et al.,2014),按照生态危害临界值(TEL)标准,超标率为23%;沉积物中Cr的含量30.52~69.65 mg·kg-1,基于生态危害临界值(TEL)标准,超标率高达85%(Zhao et al.,2014);沉积物中Cd的含量为 0.18~0.74 mg·kg-1,基于生态危害临界值(TEL)标准,Cd污染较小,仅有1个采样点超标。值得注意的是,重金属Cd的主要存在形态为酸可提取态,均值达 36.21%,Cd的生物活性值 MF、迁移系数MJ分别高达36.21%、40.42%,使得Cd的生物活性与潜在迁移能力为其他元素的4~50倍(赵胜男等,2014)。基于对乌梁素海Cu、Cr及Cd的研究可知,乌梁素海面临Cu、Cr及Cd的潜在污染风险。此外,乌梁素海地处中国北方的寒旱区,其冰封期具有冰层较厚(约0.3~1.2 m)、冰封期较长(约6~7个月)、占湖泊水体比例大(1/3~1/2)的特点,湖泊表面有冰层的覆盖,使自然曝气形成的复氧过程几乎完全停止,溶解氧浓度处于最低值,湖水还原性增强;过低的水温直接影响到微生物对污染物的降解作用。湖泊水环境中水体的物理化学性质发生改变则会引起水环境重金属赋存形态的改变。
本文分析了乌梁素海湖水中重金属 Cu、Cr及Cd含量,利用PHREEQC计算出湖泊水体中重金属赋存形态含量,并分析了不同 pH值、温度及不同pe值下水体中重金属的赋存形态变化,以期为寒区湖泊重金属迁移转化机制研究、污染治理与控制提供理论依据。
1 材料与方法
1.1 取样与分析
乌梁素海(40°36'~41°03'N,108°43'~108°57'E)位于内蒙古自治区巴彦淖市乌拉特前旗境内,目前水域面积293 km2,湖面平均高程为1018.5 m,水深为1.1~2.77 m,平均水深1.78 m。根据中国水环境及湖泊湿地调查规范,考虑乌梁素海排污入湖口的分布及水动力学特征,在空间上对乌梁素海进行2 km×2 km正方形网格化,在正方形网格的交汇点,设置样品采集点。本次实验共设置9个水体采样点,具体布点见图1。
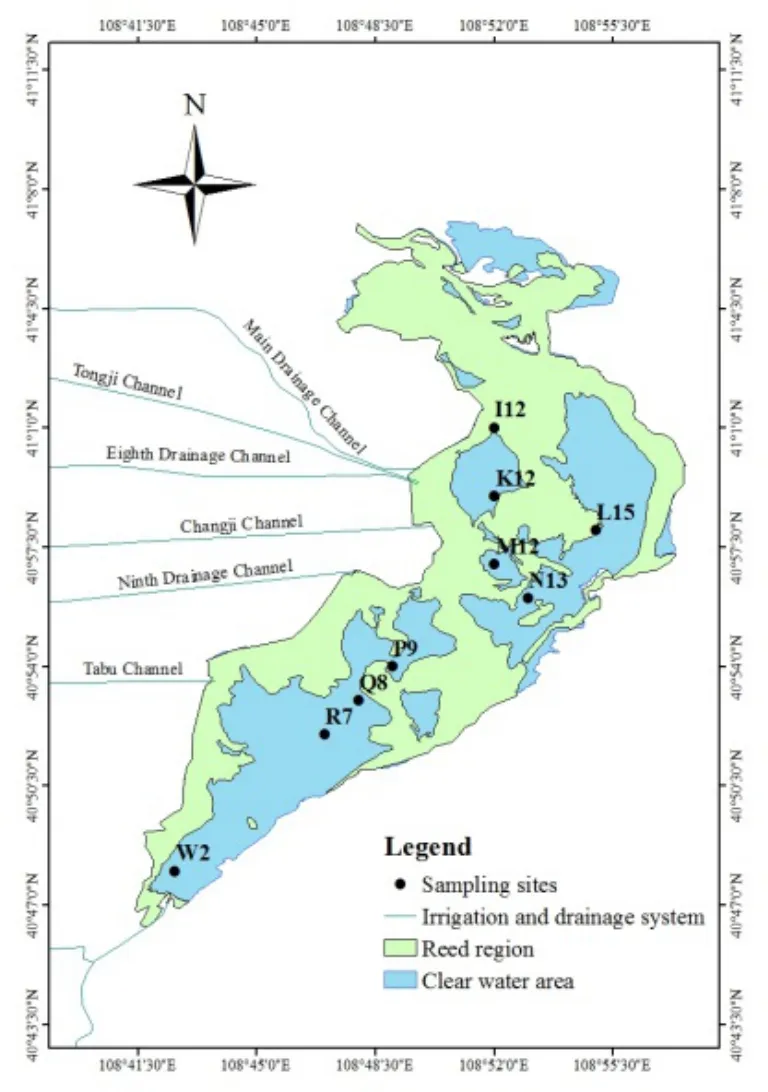
图1 采样点分布Fig.1 Sampling sites of water
开展水体取样前,清洗水样采集器及取样瓶,再用10%硝酸浸泡24 h后,取出用超纯水冲洗干净,备用。利用自制采水器(专利号:ZL201020680966.1)采集水样,并将样品置于低温冷藏箱中,使温度保持在-4~4 ℃,样品运回实验室后,立即进行元素Cu、Cd、Cr的分析测定。实验所用玻璃器皿均用1∶3(体积比)硝酸浸泡24 h以上,并用超纯水反复清洗,备用。相对标准偏差(RSD)小于3.0%。水体中Cu、Cd、Cr元素总量测定参照《水和废水监测分析方法》(水和废水监测分析方法编委会,2002),采用石墨炉–原子吸收分光光度计进行测定(中国林业科学研究院分析中心,1993)。水体温度、pH值、氧化还原电位采用便携式pH计进行测定。水体阴阳离子含量利用IS-90离子色谱仪进行测定。
1.2 研究方法
PHREEQC软件是以热力学平衡常数方法为基础的水文地球化学模拟软件程序,主要由数据库、输入文件、标准输出文件和选择性输出文件4部分组成。其中,数据库文件给出了主要离子、矿物质、吸附交换、动态和平衡化学反应等的表达式和常数。输入文件需要用户编写的文本文件。标准输出文件是模拟运算过程中的输出结果。选择性输出文件是根据用户需要选择性地输出计算结果(史小红等,2015)。模型所需参数:温度t、pH值、pe值,Ca2+、Mg2+、K+、Na+、Cl-、SO42-、CO32-及 Cu、Cr、Cd总量。
HSC Chemistry是集成热力学数据库软件,其拥有超过20000种无机物详细热力学性质的数据库以及针对不同应用而设计的 22个计算模块(王艳坤,2013;史小红等,2015)。本文主要利用HSC Chemistry v5.0计算不同反应方程式的平衡常数logK、反应焓delta_h,从而建立Cu、Cr、Cd的存在形态模拟数据库(表1)。计算方法为:首先通过HSC Chemistry v5.0的数据库(DATABASE)查找所研究重金属元素的所有存在形态,再从 Reaction Equations中计算不同温度下的各个物质的反应焓delta_h,再利用平衡常数K与反应焓之间的关系计算平衡常数Kh。
2 结果与讨论
2.1 乌梁素海水体中Cu、Cr、Cd总量评估
研究区湖泊水体中 Cu质量浓度为 2.21~15.37 μg·L-1,平均值为 7.91 μg·L-1。水体中 Cr质量浓度为 3.05~8.22 μg·L ,平均值为 4.91 μg·L 。水体中Cd 质量浓度为 0.006~0.049 μg·L-1,平均值为 0.0159 μg·L-1。以渔业用水标准作为评价标准,利用单因子指数对 Cu、Cr、Cd含量进行评价,Cu的值在0.22~1.54之间,说明部分监测点受到 Cu污染。Cr的值在 0.03~0.08之间,均值为 0.049;Cd的值在0.001~0.009之间,均值为0.003,均小于1,说明水体未受到Cr、Cd污染。国际上将Cr列为化学致癌物,其致癌强度系数较高,为 41 mg·kg-1·d-1(孙超等,2009)。乌梁素海湖水中Cr通过饮用水途径引起的致癌风险平均值为1.42×10-5a-1(赵胜男等,2013),高于瑞典环保局与荷兰建设和环境部所推荐的最大可接受值1.0×10-6a-1(钱家忠等,2004),因此重金属Cr在水体中的含量虽未超过各类用水标准,但由于其存在一定的健康风险,也应予以重视。
2.2 乌梁素海水体中重金属元素存在形态模拟
在重金属组分形态确定过程中,pH、pe和水温t这3个参数是必不可少的输入指标。本次采样水体pH范围7.86~8.57,pe值范围为-2.7~3.2,温度t范围为0.1~0.5℃(表2)。基于HSC Chemistry v 5.0软件以及物理化学理论,新建了Cu、Cr、Cd的存在形态模拟数据库,再利用PHREEQC模型进行存在形态模拟,模拟结果见图2。

表1 Cu、Cd、Cr的反应方程式及参数Table1 Chemical reaction equations and parameters of Cu, Cr, Cd

表2 乌梁素海水体中Cu、Cr、Cd含量及理化性质Table2 The Cu, Cr, Cd concentrations and physical-chemical of water in Ulansuhai Lake
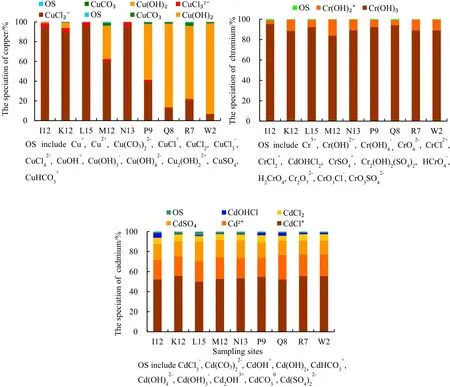
图2 乌梁素海水体中Cu、Cr、Cd的主要存在形态及质量分数比例Fig.2 The copper, and cadmium speciation and content percentage in lake water
乌梁素海水体中的Cu主要以低价态的CuCl2-、CuCl32-和高价态的CuCO3和Cu(OH)2存在。其中,I12、K12、L15、M12、N13采样点的主要组成形态为 CuCl2-,占比为 60.05%~95.75%;Cu(OH)2占比为0.038%~33.79%。采样点P9、Q8、R7、W2的主要组成形态为 Cu(OH)2,占比为 33.79%~91.78%;CuCl2-占比为 6.52%~ 39.56%,CuCO3占比为1.2%~3.19%。除 CuCl2-、CuCl32-、CuCO3、Cu(OH)2外,所有采样点其他形态 Cu的含量均较低,仅占0.21%~1.01%。
乌梁素海水体中的 Cr的主要形式为三价态的Cr(OH)3与 Cr(OH)2+;从图 2可知,所有水样均以Cr(OH)3占绝对优势,占比为 84.03%~95.33%,Cr(OH)2+含量相对较低,占比为3.47%~15.68%;除Cr(OH)3与Cr(OH)2+外,其他形态Cr的含量极低,总和仅占0.2%~1.20%。
乌梁素海水体中的 Cd的主要形式为二价态的CdCl+、Cd2+、CdSO4和CdCl2;从图2可知,所有水样均以 CdCl+占绝对优势,占比为50.03%~59.95%,Cd2+含量相对较低,占比为19.12%~24.27%;CdSO4占比为 14.02%~19.82%;CdCl2占比为 4.88%~6.96%;CdOHCl占比为0.61%~4.49%;除CdCl+、Cd2+、CdSO4和CdCl2外,其他形态的含量极低,总和仅占1.45%~3.44%。
2.3 乌梁素海水体中Cu、Cr、Cd存在形态影响因素分析
2.3.1 环境温度对Cu、Cr、Cd存在形态的影响
保持pH=8、pe=1.6不变,设置t分别为0、10、20、30 ℃,对不同温度下水体中Cu、Cr、Cd的存在形态进行模拟。
任何化学反应过程中都伴随着热量的转化,故水温对水中物质的存在形态及含量也有一定的影响。从图 3可知,随着温度的改变,重金属 Cu、Cr、Cd的各种存在形态均发生了微小的改变,但变化不是十分明显。
2.3.2 环境酸碱性对Cu、Cr、Cd存在形态的影响
保持t=0.1 ℃、pe=1.60不变,设置pH分别为6、7、8、9、10、11,对不同pH值下水体中Cu、Cr、Cd的存在形态进行模拟。
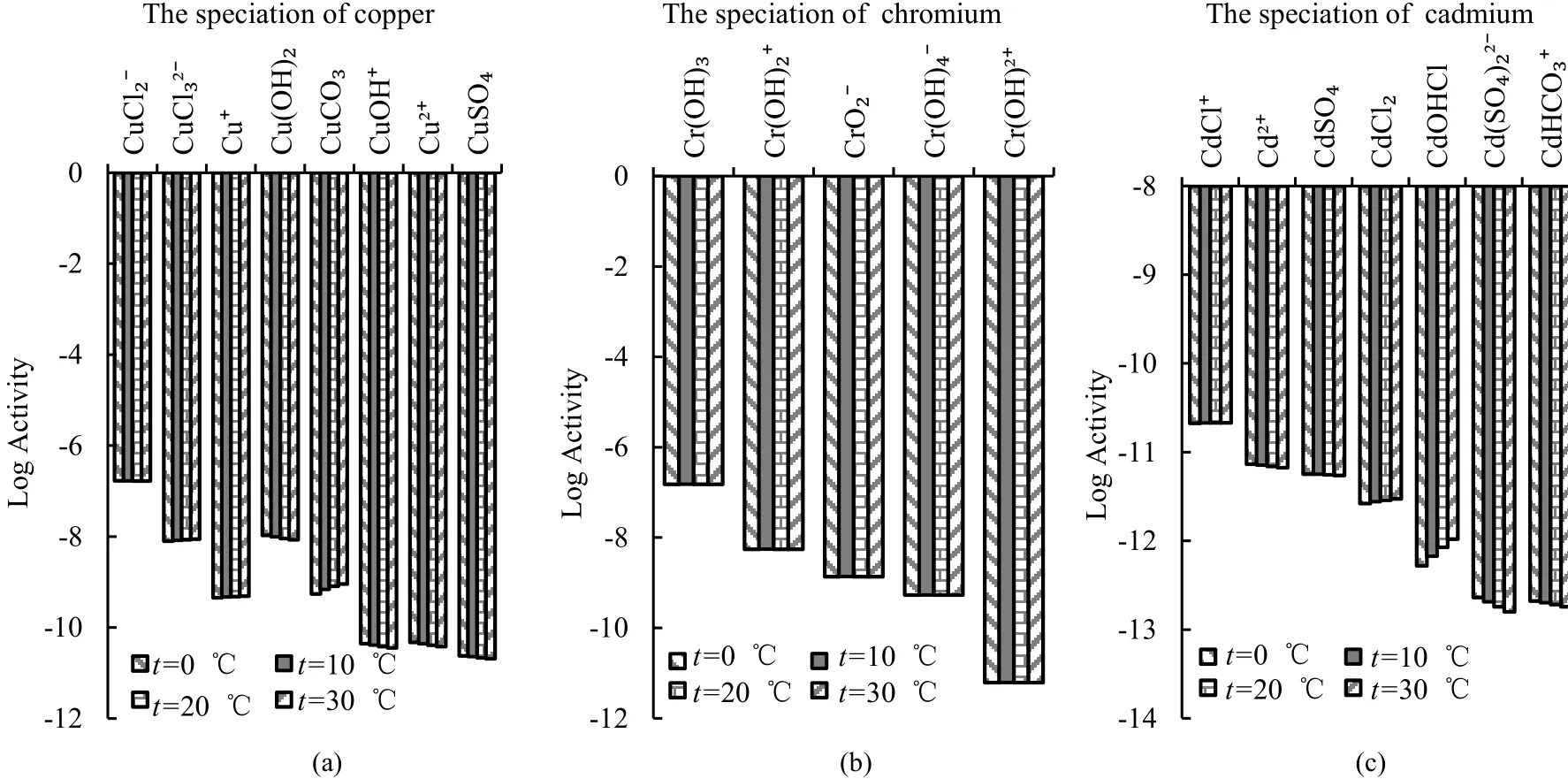
图3 水体中重金属Cu、Cr、Cd的主要存在形态含量随温度的变化Fig.3 The changes of different heavy metals in different temperature
水体中重金属Cu的存在形态受pH影响较大,从图4可知,水体pH=6时,处于酸性环境,加之此次水样采取时间在冬季,水体与氧气接触相对少,最主要的是由于乌梁素海水体盐化污染较为严重,水体中 Cl-含量较高,而 Cu+与 Cl-有较强的配合能力,Cu+在含Cl-的水溶液中,能够比较稳定地存在,CuCl2-含量最大,达到95.12%。由于水体处于酸性环境,H+含量较高,OH-含量较低,因此Cu2+与OH-结合能力较弱,Cu(OH)2配合物含量极低,仅为0.00052%;随着 pH增大,H+含量逐渐减少,OH-含量逐渐增加,溶液中的离子的配位反应倾向于OH-与 Cu2+的配合,且 Cu(OH)2的平衡常数较其他离子与Cu2+的配合物大,争夺离子能力更强,使得多数离子以二价态的形式存在,所以Cu(OH)2含量逐渐增大;当pH=11时,Cu(OH)2含量逐渐达到最大值,约为99.5%。从图4(b)可知,其他形态Cu含量发生了轻微变化,CuCl32-含量变化相对较为明显,由于Cu+含量逐渐降低,使得CuCl32-含量也随之降低。在pH增大初期,CuCO3含量有上升趋势,随着 pH的继续增大,OH-含量也增加,此时 Cu2+与 OH-的配合反应趋势增强,使得较多的 Cu2+与OH-相结合,CuCO3含量又开始出现下降趋势,从图4(b)可知,其含量本身较低且变化不显著。
水体中重金属Cr属于典型的两性元素,当乌梁素海水体呈弱酸性时(图 5),Cr主要以 Cr(OH)2+形式存在,约占65%;其次是Cr(OH)2+,约占30%;随着pH升高,Cr(OH)2+与Cr(OH)2+含量逐渐减少,Cr(OH)3含量逐渐增加,水体处于中性-弱碱性环境时,Cr(OH)3含量达到最大值,约占99.5%,并趋于稳定状态;随着pH继续升高,Cr(OH)3含量出现下降趋势,六价铬形式的CrO2-含量开始增加;当pH处于碱性状态(pH=11),CrO2-含量约占 70%,Cr(OH)3含量约占25%。
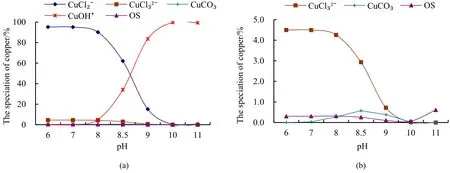
图4 水体中Cu的主要存在形态含量随pH的变化Fig.4 The copper speciation change with pH change
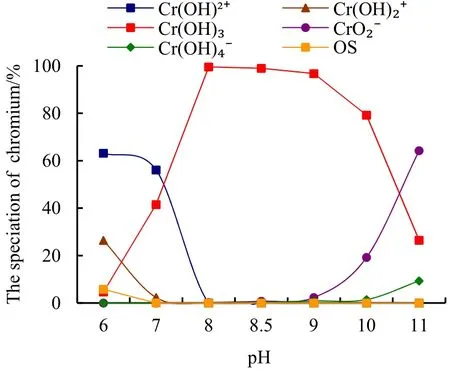
图5 水体中Cr的主要存在形态含量随pH的变化Fig.5 The chromium speciation change with pH change
水体中重金属Cd的存在形态变化受pH的影响相对显著(图 6)。乌梁素海水体处于弱酸-弱碱环境,水体中镉的主要存在形式为 CdCl+、CdCl2、CdSO4以及游离Cd2+;水体处于碱性环境,主要存在形式为 CdOHCl和Cd(OH)2。Cd2+在水环境中容易形成各种络合物,一般在没有任何阴离子配位体的情况下,水体 Cd全部以二价离子态存在。乌梁素海水体中存在Cl-、SO42-等阴离子配位体,Cd及其化合物的化学性质近似于Zn而异于Hg,与邻近的过渡金属元素相比,Cd2+属于较软的酸,Cl-具有较低的电负性,根据软硬酸碱理论,水体有利于Cl-等与Cd2+生成络合离子CdCl+;乌梁素海水体中盐度较高,因此也存在着一定含量的CdCl2;。当水体处于弱酸性、中性及弱碱性时,CdCl+、、CdCl2含量较高,CdCl+约占 55%,CdCl2约占 7%,含量也较为稳定;随着pH增高,水体处于碱性状态,OH-含量逐渐增加,Cd发生强水解反应,由于有 Cl的存在,逐渐生成CdOHCl,;当pH达到11时,水体中CdOHCl占比达到55%;同时随着OH-含量增加,Cd2+发生水解反应也会生成Cd(OH)2,约占38%。
2.3.3 环境氧化还原性对Cu、Cr、Cd存在形态的影响
保持pH=8、t=0.1 ℃不变,设置pe分别为-6、-5、-4、-3、-2、-1、1、、3、4、5、6,对不同 pe值下水体中Cu、Cr、Cd的存在形态进行模拟。
水体中重金属 Cu的存在形态受 pe值影响较大,从图7可知,当水体表现出还原性时,Cu离子主要以低价态形式存在,Cu+属于“软”酸,Cl-具有较低的电负性,它与 Cl-络合时导致较高的极化率,有利于电子强烈地转移到Cu+,因此Cu+与Cl-的络合物具有高稳定性。因此,当pe值较低,处于-6~0时,水体中 Cu以 CuCl2-含量最大,占93.73%~95.24%;其次为 CuCl32-,占比为4.4%~4.5%;Cu(OH)2配合物含量极低,几乎可以忽略。随着pe值增大,氧化性逐渐增强,部分Cu+逐渐被氧化为Cu2+,此时,水体中金属离子的水解作用占主导地位,重金属离子的水解作用即为金属离子和质子争取OH-的过程,随Cu2+含量的逐渐增多,其争夺OH-的能力也逐渐增强,故Cu(OH)2的含量逐渐增加。pe值处于1~6时,Cu(OH)2占比从1.48%增至 93.94%。从图 7(b)可知,CuCO3的含量随着pe值升高而逐渐增大,变幅较大,但是含量较少,最高值仅为4.85%,主要是由于此反应模拟的pH值在8左右,Cu2+与 OH-的配合反应趋势增强,使得较多的Cu2+与OH-结合,CuCO3含量相对较低。因此,随着pe值增大,水体中重金属Cu的反应主要是水解反应,而配合反应的能力逐渐降低。水体中重金属Cr形态变化受pe值的影响则不显著。水体的pe值是指平衡状态下的电子活度,衡量的是溶液接受或提供电子的相对趋势,可作为电子有效性的一种量度。pe值越大,电子浓度越低,体系接受电子的倾向越大,反之,pe值越小,体系供给电子的倾向越大。从上述含义分析,当水体pe值发生改变,实质上是重金属元素得失电子的过程,重金属元素得失电子,必定会影响元素的化合价态,由于Cd价态属于稳定,属于单一价态元素,因此Cd存在形态未受pe值影响。
3 讨论
3.1 乌梁素海水体中不同重金属的存在形态分析
水体中 Cu存在形态受多种因素共同控制,一般水体中 Cu+不能稳定存在,因为其自身会发生歧化反应,或者很容易被氧化为Cu2+;本研究水样采集时间为冬季,水体与氧气接触相对少,最主要的是由于乌梁素海水体盐化污染较为严重,水体中Cl-含量较高,由于 Cu+与 Cl-有较强配合能力,Cu+在含Cl-的水溶液中,能够比较稳定地存在(薛娟琴,2008)。采样点I12、K12、L15、M12、N13采样点的pe值较小,Cl-含量较高,对于Cu-Cl-H2O溶液体系来说,Cu+属于“软”酸,Cl-具有较低的电负性,它与Cl-络合时导具有较高的极化率,有利于电子强烈地转移到Cu+,因此Cu+-Cl-的络合物具有高稳定性。随着溶液中 Cl-浓度的增加,有利于生成CuCl2-、CuCl32-、CuCl3-、CuCl42-。Cu2+属于中性酸,根据软硬酸碱理论,它与Cl-形成的配合物稳定性较差。CuCl2和 CuCl3-的平衡常数比 CuCl2-和 CuCl32-小(薛娟琴,2008)。因此,I12、K12、L15、M12、N13的 Cu的主要价态为一价态 Cu的 Cl-络合物CuCl2-,仅有少量的CuCl32-和CuCl42-。采样点P9、Q8、R7、W2的pH与pe值都较高(pH:7.92~8.55;pe:2.4~3.1),随着氧化性的增强,部分Cu+逐渐被氧化为Cu2+,水溶液中OH-含量逐渐增大,溶液中的离子的配位反应倾向于 Cu2+与 OH-的配合,Cu(OH)2的平衡常数较其他Cu2+与OH-的配合物大,因此,P9、Q8、R7、W2的主要存在形态为二价态Cu的OH-配合物Cu(OH)2;水溶液的pe值不属于强氧化性范围,因此溶液中存在一定的 Cu+,Cu2+属于中性酸,根据软硬酸碱理论,它与Cl-形成的配合物稳定性较差。Cu+属于“软”酸,与Cl-形成的配合物稳定性较高。因此,溶液中还存在着一定的CuCl2-。
Cu是人体生命活动与动植物生长所必须的微量元素,但摄取量超过一定的限度则会造成中毒。Cu的毒性以 CuSO4较大,乌梁素海水体中具有较大毒性的 CuSO4活度水平在 2.83×10-16~1.43×10-10之间,占Cu总浓度的0.005%~0.069%,含量极低,因此不会对乌梁素海的水体造成较大的危害。游离Cu2+的毒性比络合态 Cu2+的毒性大得多,因此 Cu对鱼类的毒性大小主要取决于游离的Cu2+及其氢氧化物(王春秀,2010)含量高低。游离态Cu2+含量越高,毒性越强,相反,Cu的氢氧化物含量越高,毒性则越小。从图2可知,游离态Cu2+含量较低,Cu(OH)2含量较高,因此,水体中铜的毒性较小。
重金属 Cr对不同的生物具有不同的毒性,Cr的不同形态的化合物毒性大小也不同。一般情况,无机铬的形态有Cr2+、Cr3+、Cr6+,Cr2+一般情况下是无毒的,Cr3+毒性相对较小,Cr6+的毒性较大,是Cr3+的100倍。乌梁素海冬季水体中Cr的形态主要以三价态的Cr(OH)3与Cr(OH)2+存在,毒性较小,六价态含量极低,几乎可以被忽略,因此,乌梁素海水体中Cr的危害性较低。
重金属Cd是生物体生长非必要元素,其化合物毒性较大,具有致癌、致畸作用,骨痛病即是由Cd所造成的。水中CdCl2对生物特别是鱼类的富集的影响很大,当水中CdC12质量浓度达0.01 mg·L-1时,能使鲤鱼在8~18 h内死亡(孟晓红,1997)。乌梁素海冬季水体中CdCl2含量占比为4.88%~ 6.96%,但由于水体中Cd的总浓度极低,故毒性较大的氯离子络合态浓度也相对较低,但仍应予以重视。
3.2 乌梁素海水体外界环境变化对重金属存在形态的影响
湖泊水环境的温度、酸碱性、氧化还原性会对重金属元素的存在形态产生不同程度的影响,可根据PHREEQC软件对各种环境指标控制下不同形态重金属元素比例的模拟,选择合适的方法降低重金属元素的污染风险。
从模拟结果分析,当水体处于中性-弱碱性环境时,Cu主要以CuCl2-和Cu(OH)2为主要形态,且其含量占比各为50%左右。铜的氢氧化物含量越高,毒性则越小。Cr的主要形态为CrO2-和Cr(OH)3,其中 CrO2-含量约占70%,Cr3+毒性相对较小。Cd的主要形态为CdOHCl和Cd(OH)2,镉的氢氧化物含量高,则毒性较小。如果水体处于弱酸性环境,Cu、Cr、Cd 主要存在形态为 CuCl2-、Cr(OH)2+、CdCl+、CdCl2,则毒性则有增强趋势。水体处于碱性环境时,主要形态为 Cu(OH)2、Cr(OH)3、CdCl+,氢氧化物增多,则毒性会降低。乌梁素海湖泊水体 pH值年际变化在7.5~9.25之间,呈中性-碱性。为防止重金属赋存形态向毒性增大的方向发展,应尽量控制水体pH值处于中性-弱碱性。
当水体处于还原状态时,水体中以CuCl2-含量最大;处于氧化性状态时,Cu(OH)2占比从1.48%增至93.94%。随着pe值增大,水中重金属Cu的反应主要是水解反应,而配合反应的能力逐渐降低。若水体处于氧化条件下,Cu的氢氧化物含量越高,毒性则越小。当水体处于中性条件,水体Cr的存在形态主要为Cr(OH)3,当水体氧化还原性发生变化时,Cr3+可以转化为Cr6+,其反应式为:2Cr(OH)2++3/2O2+H2O=2CrO42-+6H+,但反应速率及其缓慢,而且必须加入其他物质才能使反应顺利进行。随着pe值的改变,其Cr3+得电子的能力也会受到限制,反应速率也比较慢,故pe值的变化对重金属Cr的形态变化不会有较大的影响。因此,在水体处于弱碱性-中性状态下,氧化还原电位发生变化并不会对水体中重金属Cr的形态产生较大影响。乌梁素海水体氧化还原电位值季节波动较大,冬季氧化还原电位值最低,平均值为70 mV,最低值-367 mV,春季平均值为102 mV,夏季氧化还原电位值最高,平均值为194 mV,秋季氧化还原电位平均值为177 mV,大部分时间都处于氧化状态,因此,重金属Cu、Cr、Cd以毒性较小的氢氧化物为主;而当乌梁素海处于冰封期时,水体氧化还原电位相对较低,盐度较高,水体易处于还原状态,铜的氢氧化物含量降低,氯化物含量增强,毒性则增强。
4 结论
(1)乌梁素海冰封期表层水体中 Cr、Cd在所有监测点中的含量均未超出地表水标准和国家渔业用水标准,且Cr、Cd主要以毒性较小的价态存在。部分监测点Cu含量超标,水体中Cu主要是以低价态的CuCl2-、CuCl32-和高价态的CuCO3和Cu(OH)2存在。
(2)水温对3种元素的存在形态分布影响较小,而水体酸碱性及氧化还原性对 Cu存在形态具有较大影响。水体处于弱酸性环境时,Cu主要存在形态为CuCl2-、CuCl32-,水体处于中性-弱碱性环境时,Cu主要以CuCl2-和Cu(OH)2形态存在,且含量各占50%左右。当水体处于还原状态时,水体中 Cu以CuCl2-含量最大,处于氧化性状态时,Cu(OH)2的占比从 1.48%增至 93.94%。由于乌梁素海水体中 Cu部分监测点超标,且其存在形态受到pH及pe值的影响较大,故在今后的监测中应予以重视。
(3)由于寒区湖泊冰封期较长,受到冰层覆盖的影响,湖泊水体常处于还原状态,冰下水体盐度较高,此时应控制湖泊水体处于中性-弱碱性环境以抑制重金属赋存形态向毒性增大的方向转化。
参考文献:
AUDRY S, POKROVSKY O S, SHIROKOVA L S. 2011. Organic matter mineralization and trace element post-depositional redistribution in western Siberia themokarst lake sediments [J]. Biogeosciences, 8(11):3341-3358.
COUTURE R M, WALLSCHLAGER D, ROSE J. 2013. Arsenic binding to organic and inorganic sulfur species during microbial sulfate reduction:a sediment flow-through reactor experiment [J]. Environmental Chemistry, 10(4): 285-294.
CHENG K, WANG Y, TIAN H Z, et al. 2015. Atmospheric Emission Characteristics and Control Policies of Five Precedent-Controlled Toxic Heavy Metals from Anthropogenic Sources in China [J]. Environmental Science and Technology, 49(2): 1206-1214.
HOWARTH R S, SPRAGUE J B. 1978. Copper Lethality to rainbow trout in waters of various hardness and pH [J]. Water Research, 12(7):455-462.
NITZSCHE O, MERKRL B. 1999. Reactive transport modeling of uranium 238 and radium 226 in groundwater of the Koenig stein uranium mine,Germany [J]. Hydrogeology journal, 7(5): 42-430.
SENN D B, HEMOND H F. 2002. Nitrate controls on iron and arsenic in an urban lake [J]. Science, 296(5577): 2373-2376.
STRAIF K, BENBRAHIM T L, BAAN R. 2009. A review of human carcinogens part C: metals, arsenic, dusts, and fibres [J]. The Lancet Oncology, 10(5): 453-454.
WAGEMANN R, BARICAL J. 1979. Speciation and rate of loss of copper from lake water with implications to toxicity [J]. Water Research,13(6): 515-523.
ZHAO S N, SHI X H, LI C Y, et al. 2014. Seasonal variation of heavy metals in Sediment of Ulansuhai Lake, China [J]. Chemistry and Ecology, 30(1): 1-14.
常阳, 崔建勇, 谭靖, 等. 2016. 尕斯库勒盐湖水中铀形态分布及影响因素研究[J]. 世界核地质科学, 332(2): 106-110.
陈怀满. 1996. 土壤-植物系统中的重金属污染[M]. 北京: 科学出版社:110-150.
丁鸿, 杨杏芬. 2007. 环境镉危害早期健康效应风险评估的研究进展[J].国外医学卫生学分册, 34(5): 279-282.
付新峰, 谷晓伟, 刘晓岩, 等. 2008. 乌梁素海生态功能定位初步分析[J].人民黄河, 30(10): 61-61.
何连生, 席北斗, 雷宏军, 等. 2013. 乌梁素海综合治理规划研究[M]. 北京: 中国环境出版社: 1-105.
李广玉, 叶思源, 鲁静, 等. 2006. 胶州湾底层水痕量元素组分存在形态及其生物有效性[J]. 世界地质, 25(1): 71-76.
刘清, 王子健, 汤鸿霄. 1996. 重金属形态与生物毒性及生物有效性关系的研究进展[J]. 环境科学, 17(1): 89-92.
刘勇, 夏之宁, 袁佩. 2001. 水体中重金属形态的毒性研究方法[J]. 理化检验-化学分册, 37(6): 286-289.
刘清, 王子健, 汤鸿霄. 1998. 铜的形态分布与Daphnia magna急性毒性关系[J]. 环境化学, 17(1): 14-18.
马冬梅, 马军, 李兴, 等. 2012. 内蒙古乌梁素海引排水量动态分析[J].内蒙古水利, 15(1): 14-16.
孟晓红. 1997. 金属镉在鱼体中的生物富集作用[J]. 广东微量元素科学,3(1): 8-11.
贡晓飞, 鄂尔丁夫, 王琪, 等. 2015. 不同价态铬在不同水分条件下的生物有效性及其对水稻的毒性[J]. 生态毒理学报, 10(4): 170-176.
国家环境保护总局《水和废水监测分析方法》编委会. 2002. 水和废水监测分析方法[M]. 第4版. 北京: 国家环境科学出版社: 50-75.
黄坚, 李建文, 陈胜福, 等. 2007. 湘江(长沙段)水中铬的形态分布及其迁移[J]. 分析测试学报, 26(3): 335-339.
黄支刚, 王永利, 陆春海, 等. 2012. 地下水中Am的形态分布及影响因素[J]. 环境化学, 31(2): 168-174.
邱锦泉, 付善明, 宿文姬. 等. 2015. 粤北矿区横石河流域铜的生态地球化学特征及意义[J]. 生态环境学报, 24(10): 1695-1704.
钱家忠, 李如忠, 汪家权, 等. 2004. 城市供水水源地水质健康风险评价[J]. 水利学报, 16(8): 90-91.
史小红, 赵胜男, 李畅游, 等. 2015. 乌梁素海水体砷存在形态模拟及影响因素分析[J]. 生态环境学报, 24(3): 444-451.
司高华, 李哲, 富宝峰. 2017. 超铀核素在某处置工程地下水中化学形态分析研究[J]. 地下水, 39(1): 24-26.
孙超, 陈振楼, 张翠, 等. 2009. 上海市主要饮用水源地地水重金属健康风险评价[J]. 环境科学研究, 22(1): 60-65.
唐秋香, 缪新. 2013. 土壤镉污染的现状及修复研究进展[J]. 环境工程,31(增刊): 747-750.
王春秀. 2010. 水体铜对黄河鲤毒性作用的研究[D]. 郑州: 河南农业大学: 2-58.
王新伟, 何江. 2002. 水体中重金属的形态分析方法[J]. 内蒙古大学学报, 33(5): 587-591.
王妍力, 罗明标, 牛建国, 等. 2015. 某盐湖水中铀的形态分布研究[J].环境监测管理与技术, 27(4): 22-25.
王妍力, 罗明标, 杨智翔. 2017. 海水中铀的形态分布模拟研究——以上海近海洋山海水为例[J]. 世界核地质科学, 34(2): 92-95.
王艳坤. 2013. HSC Chemistry软件在高校化学科研中的应用[J]. 河南教育学院学报: 自然科学版, 22(2): 28-30.
夏彧, 徐真, 马英杰. 2016. 天然海水中痕量重金属元素种态分布的数值模拟[J]. 桂林理工大学学报, 36(2): 597-602.
薛娟琴. 2008. 萃取及离子交换法处理氯化亚铜废水的研究[D]. 西安:西安建筑科技大学: 1-63.
张季惠, 王黎虹, 张建奎. 2013. 土壤中镉的形态转化、影响因素及生物有效性研究进展[J]. 广东农业科学, (6): 169-171.
赵胜男, 李畅游, 史小红, 等. 2013. 乌梁素海沉积物重金属生物活性及环境污染评估[J]. 生态环境学报, 22(3): 481-489.
赵胜男, 史小红, 李畅游, 等. 2014. 乌梁素海水体汞的分布特征及污染风险评估[J]. 湖泊科学, 26(2): 221-227.
钟格梅. 2012. 环境镉污染及其对人群健康影响研究进展[J]. 应用预防医学, 18(5): 317-320.
中国林业科学研究院分析中心. 1993. 现代实用仪器分析方法[M]. 北京:中国林业出版社: 15-150.
朱义年, 王焰新. 2005. 地下水地球化学模拟的原理及应用[M]. 武汉:中国地质大学出版社: 1-140.

