血行播散性结核病并发骨髓增生异常综合征一例
——文献复习及临床诊治过程分析
宋艳华 齐荣艳 马丽萍 吕范永 刘荣梅 高孟秋
结核病目前仍然是一种威胁人类健康的重大传染性疾病,据2017年WHO结核病年报报道,2016年全球估计有1040万例新发患者,有167万例死于结核病[1]。血行播散性结核病是结核分枝杆菌一次或反复多次进入血液循环、可累及全身多脏器系统病变的一种重症结核病,以肺部血行播散性结核病最常见,但由于该病临床特征缺乏特异性,导致疾病早期容易误诊[2-4]。而血液系统疾病因为血液细胞,尤其是白细胞计数减少,和免疫紊乱等原因易并发各种感染,包括结核感染。当结核病并发血液系统疾病时,常导致病情互相掩盖,或疑为治疗过程中的药物不良反应,极易漏诊、误诊。笔者通过报道1例并发全血细胞严重减少的血行播散性结核病患者,分析该患者早期的骨髓增生异常综合征(myelodysplastic syndromes,MDS)特征并不典型、直至结核病治疗有效后持续出现血液系统异常、多次骨髓穿刺-病理检查才确诊并发MDS的临床诊治过程,以提高临床医生对两病并存的诊断认识,分享治疗经验。
临床资料
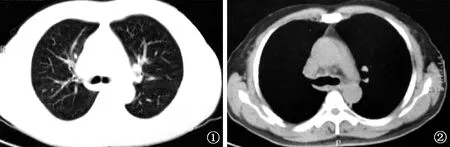
图1,2 患者,男,60岁,血行播散性结核病并发MDS。胸部CT检查(2017-03-09):可见右肺小的肺大疱,右侧胸膜粘连,纵隔多发肿大淋巴结,余肺部未见明显异常
患者,男,62岁,汉族。因“头晕、乏力3个月,发热2个月”,于2017年4月24日收治入住首都医科大学附属北京胸科医院。患者既往无结核病病史,否认结核病患者密切接触史;患者有高血压病史7年,否认其他病史;吸烟30年,每日20支,偶有少量饮酒,无其他不良嗜好。既往从事办公室工作,否认毒物、放射物接触史。
一、患者在襄阳市解放军某医院的诊治情况
患者于2017年1月末出现头晕、乏力,活动后心慌,无发热,无咳嗽、咳痰,持续15 d余未见缓解。2月14日就诊于襄阳市解放军某医院门诊。血常规检查:白细胞(WBC) 2.3×109/L[参考值(3.5~9.5)×109/L ],血红蛋白(Hb)77 g/L(参考值130~175 g/L),血小板(PLT) 133×109/L [参考值(125~350)×109/L],未进一步检查。结合患者高血压病史,该院初诊为心脑血管疾病,予以活血化瘀及降血脂等治疗1周(具体不详),症状缓解。
2017年2月27日,患者再次因“乏力、活动后心慌气短”收治入住该院。2017年2月28日实验室检查:WBC 2.1×109/L,Hb 65 g/L,平均红细胞体积(MCV)108.9 fL(参考值80~100 fL),平均红细胞血红蛋白量(MCH)34.1 pg(参考值27~34 pg),红细胞平均血红蛋白浓度(MCHC)313 g/L(参考值316~354 g/L),PLT 135×109/L,网织红细胞(Ret)1%(参考值0.5%~1.5%),叶酸 13.73 nmol/L(参考值>8.83 nmol/L)),维生素B12 202.49 pmol/L(参考值141~298 pmol/L),血红细胞沉降率(ESR)55 mm/1 h(男性参考值0~15 mm/1 h);尿常规阴性;便常规潜血“+”。心电图检查:窦性心律,频发房性早搏(部分呈二联律);尿本周蛋白阴性(2017-03-04)。
2017年3月1日骨髓穿刺细胞学检查:骨髓增生活跃(G/E=2.56∶1,参考值2∶1~4∶1),粒细胞系比例66%(参考值40%~60%),粒细胞系中幼粒细胞百分比13.5%[参考值(6.49±2.04)%],红细胞系增生25.75%[参考值(19.66±4.98)%],巨幼红细胞(RBC)3%(参考值0%),可见幼红细胞分裂象,成熟红细胞大小不一,大细胞多见;PLT、巨核细胞易见;骨髓铁染色细胞内铁5%(参考值19%~44%),细胞外铁阳性。
骨髓穿刺后第2天患者出现午后发热(37.5~38.4 ℃),予以抗感染对症等治疗(具体不详),患者仍有发热,PLT及Hb持续下降,血常规检查(2017-03-05):WBC 3.2×109/L,Hb 58 g/L,PLT 93×109/L。诊断为“全血细胞减少原因待查,冠心病,心绞痛,高血压病3级 极高危”。建议转诊襄阳市中心医院诊治。
二、患者在襄阳市中心医院血液科的诊治情况
2017年3月7日患者入住湖北襄阳市中心医院血液科。当日血常规检查:WBC 3.43×109/L,N 1.96×109/L[参考值(1.8~6.3)×109/L],Hb 41 g/L,MCV 108.8 fl,MCH 36.0 pg,MCHC 331 g/L,PLT 100×109/L,Ret 1.2%。血维生素B12 260.2 pmol/L,叶酸>45.4 nmol/L,血清铁 10.46 μmol/L(10.6~36.7 μmol/L),总铁结合力 31.7 μmol/l(20~62 μmol/L),转铁蛋白 1.6 g/L(2.0~3.6 g/L),C反应蛋白(CRP)64.2 mg/L(参考值<10 mg/L)。红细胞溶透脆性试验阴性。胸部CT检查(2017-03-09):右肺小的肺大疱,同时发现右侧胸膜粘连,纵隔多发肿大淋巴结,余肺部未见明显异常(图1,2)。
第一次骨髓穿刺细胞学检查(2017-03-15):骨髓增生活跃,G/E=11.64∶11,粒系增生旺盛,分类相对增高(82%),以中性粒细胞的中幼、晚幼及杆状、分叶为主,原始粒细胞及早幼粒细胞比例不高,细胞形态未见明显异常;红系增生低下(7%)(正常值2%左右),巨核细胞及血小板易见;血细胞涂片:成熟红细胞大小不一,白细胞分类未见明显异常,血小板易见;参考意见:单纯红细胞再生障碍性贫血趋势。骨髓活检病理:骨髓增生程度大致正常,巨核细胞增生,未见明显原始细胞增多,骨髓间质可见2个体积较小的肉芽肿结节;参考意见:组织学改变考虑MDS,但需除外感染、免疫、肿瘤疾病的反应性改变。骨髓染色体核型分析:46XY,正常男性核型,T细胞抗原受体(TCR)基因重排未检测到异常。血培养及血人类疱疹病毒4型(EB病毒)DNA检测阴性。
第二次骨髓穿刺细胞学检查(2017-03-29):淋巴细胞占有核细胞7%,比例降低;CD3+CD8+T淋巴细胞比例增高;原始区域细胞占有核细胞2%,髓系细胞占有核细胞比例增高(86%),部分细胞存在发育异常。
在逐步完善各项检查期间,积极给予患者对症治疗。予抗感染、输血、保肝及预防出血和升白细胞(具体用药不详),但仍有发热(体温最高达41 ℃),考虑患者染色体检查未见异常,骨髓病变也需要和MDS、感染、免疫肿瘤反应改变等相鉴别,认为血液系统疾病缺乏确诊依据,建议上级医院治疗。
三、河北燕达陆道培医院血液科诊治情况

图3,4 胸部CT扫描(2017-04-11),示双肺弥漫粟粒样结节影,大小均匀;纵隔、肺门可见大小不等的肿大淋巴结;心包见少许积液
2017年4月10日患者就诊于河北燕达陆道培医院血液科。当日血常规检查:WBC 2.32×109/L (参考值[(4~10)×109/L],N 1.89×109/L[参考值(2~7)×109/L],Hb 69 g/L(110~170 g/L),PLT 24×109/L[参考值(100~300)×109/L];肝功能检查:丙氨酸氨基转移酶(ALT)43 U/L(参考值0~40 U/L),天冬氨酸氨基转移酶(AST)47 U/L(参考值0~40 U/L)。结核病相关检查:结核菌素试验(PPD试验)弱阳性,ESR 35 mm/1 h。血细菌培养及常见病毒DNA及血清抗体检测均阴性。3次诱导痰抗酸杆菌染色镜检均阴性。胸部CT扫描(2017-04-11):肺部弥漫小结节影,直径均约2.0 mm,大小均匀;纵隔、肺门可见大小不等淋巴结,大者直径可达11.9 mm;心包少许积液影(图3,4)。超声检查:双侧颈部、锁骨上、腋窝、腹股沟未见肿大淋巴结;肝脏稍大,肝脏囊肿,左肾集合系统分离。
骨髓细胞相关检查:(1)骨髓穿刺细胞学检查。G/E=36.91∶1,粒细胞占有核细胞81%(正常值40%~60%),各阶段可见,原始2.4%(参考值0.0%~1.3%)、早幼粒细胞(3.60%,参考值0.37%~2.79%)比例偏高,中幼粒细胞比例为6.49%(参考值2.41%~10.57%),杆状核细胞比例偏低(0.20%,参考值0.00%~2.47%),分裂相可见,部分细胞可见轻度类巨变或者类巨变,浆中颗粒增多、增粗,嗜酸细胞可见;红系占有核细胞2.20%(参考值9.72%~29.61%),早幼红细胞及以下阶段可见,中幼(0.80%,参考值3.59%~11.23%)、晚幼(1.20%,参考值:6.03%~15.47%)红细胞比例减低,成熟红细胞大小略不等;巨核细胞(2 cm×1.5 cm)64个,其中颗粒型62个,裸核2个,大部分巨核细胞为多圆核,血小板少见。外周血血涂片:WBC计数减少,分叶核细胞比例增高,部分粒细胞胞质中颗粒增多、增粗,可见空泡。中性粒细胞碱性磷酸酶染色(NAP):“-”29%、“+”13%、“++”10%、“+++”25%、“++++”23%,阳性率 71% (参考值10%~40%),NAP积分200分(参考值 40~80分)。参考意见:粒系增生明显,红系增生不良,巨核细胞数量不少,发育异常,NAP积分增高。(2)骨髓组织病理学检查:髓腔内细胞成分明显增多,全血细胞可见,细胞成分混杂,小梁旁及髓质内可见较多量的幼稚细胞,免疫组化CD117(散在+)、CD33(多量+)、CD3(少量+)、MPO(多量+)、Ki67(+),CD34、CD68、CD20、CD123均阴性,抗酸染色阴性。病理诊断:髓系异常增生,建议结合临床检查除外急性髓细胞性白血病(AML)。(3)骨髓免疫分型(流式报告):成熟淋巴细胞比例不高(8.57%),未见明显异常细胞;异常表型髓系原始细胞占有核细胞0.2%,粒细胞比例升高(80.47%),颗粒性减低,粒细胞和单核细胞CD64表达增强,可能与感染和嗜血综合征有关。染色体:XY型,正常男性核型,未见异常克隆。染色体断裂实验阴性。MDS 5基因突变位点探针组合检查(FISH)未见异常。
患者发热及血液系统异常诊断未能明确,继续积极对症治疗,予间断输血(血小板、红细胞、血浆)、重组粒细胞刺激因子(rhG-CSF)升白细胞和重组人促红素注射液(CHO细胞)(rhEPO)升红细胞、美罗培南和左氧氟沙星抗感染,但患者仍间断高热,全血细胞减低未见改善(以上具体用药情况不详)。
四、首都医科大学附属北京胸科医院诊治经过
为进一步排除结核病诊断,患者2017年4月18日和4月 19日于我院门诊2次查痰结核分枝杆菌聚合酶链式反应RNA(RNA-PCR)阳性,诊断为血行播散性肺结核、继发性全血细胞减少。2017年4月21日在我院门诊予以H-E-PZA-Mfx方案抗结核口服治疗(其中H:异烟肼300 mg/次,1次/d;Mfx:莫西沙星0.4 g/次,1次/d;E:乙胺丁醇0.75 g/次,1次/d;PZA:吡嗪酰胺 0.5 g/次,3次/d),并予以强的松(30 mg/次,1次/d)口服,治疗3 d发热缓解。患者于2017年4月24日从河北燕达陆道培医院办理出院,入住我院。
患者入院体格检查:体温37.1 ℃,脉搏 90 次/min,呼吸频率20 次/min,血压140/90 mm Hg (1 mm Hg=0.133 kPa);平车推入病房,神志清楚,贫血貌,双下肢皮肤可见散在陈旧出血点,全身浅表淋巴结未触及肿大,颈软,双肺呼吸音清,心脏、腹部检查未见明显异常,神经系统检查阴性。血常规检查:WBC 5.35×109/L[参考值(3.5~10)×109/L],Hb 85 g/L(参考值120~160 g/L),PLT 45×109/L[参考值(100~300)×109/L](河北燕达陆道培医院当日输1 U血小板)。继续予以门诊抗结核药物治疗方案,辅以口服醋酸泼尼松(30 mg/次,1次/d)改善重症结核中毒症状,水飞蓟宾葡甲胺片(200 mg/次,3次/d)保肝治疗。
2017年4月27日血常规检查:WBC 0.7×109/L,Hb 58 g/L,PLT 23×109/L;ALT 51 U/L,AST 59 U/L,谷氨酰转肽酶(GGT)202.3 U/L(参考值0~50 U/L),总胆红素(TBIL)26.2 μmol/L(参考值3.4~20.5 μmol/L);肌酐(CREA)108 μmol/L(45~104 μmol/L),尿酸(UA)500.6 μmol/L(参考值45~104 μmol/L)。血结核感染T细胞斑点试验(T-SPOT.TB)特异性A抗原[早期分泌靶抗原6(ESAT-6)]:152 SFCs/106外周血单个核细胞(PBMC),特异性B抗原[培养分泌蛋白(CFP-10)]:28 SFCs/106PBMC (参考值<24个SFCs/106PBMC)。结合既往检查结果,初步诊断为血行播散性结核病、全血细胞减少原因待查。继续原方案抗结核及保肝等治疗,并每1~2天检测血常规1次,根据检测结果予以输血支持治疗(当日输入悬浮红细胞2 U)。

图5,6 胸部CT扫描(2017-05-04),可见双肺粟粒样结节影,同时见纵隔淋巴结肿大、双侧胸腔积液,心包积液 图7,8 胸部CT扫描(2017-06-01),可见双肺粟粒样结节影,双侧胸腔积液吸收,心包积液减少,纵隔淋巴结缩小
2017年4月28日请河北燕达陆道培医院血液科会诊,会诊意见为血行播散性结核病,继发性全血细胞减少。治疗建议为积极抗结核药物治疗,予以重组人粒细胞集落刺激因子(300 μg/次)、促红细胞生成素(1×104U/d)促进血细胞生成,继续泼尼松(30 mg/d)、丙种球蛋白[0.4 g·kg-1·d-1],抑制血细胞破坏,新鲜冰冻血浆(400~600 ml/d)、低分子肝素(5000 U/次)、凝血因子改善凝血功能,均为1次/d,治疗3~5 d;必要时输注悬浮红细胞及血小板,定期复查血常规、肝肾功能、凝血功能。当日患者病情危重,出现双下肢皮下出血点,血常规检查:WBC 3.14×109/L,Hb 72 g/L,PLT 26×109/L。分别于4月29日和30日、5月9日输血小板1 U,5月5日和13日输入悬浮红细胞2 U,据凝血功能持续间断输入血浆。
2017年5月2日根据肝肾功能检查结果(ALT 86 U/L,AST 113 U/L,TBIL 22.5 μmol/L,GGT 311.5 U/L,BUN 10.24 μmol/L,CREA 97.7 μmol/L),停用对肝功能影响最大的PZA,采用H-E-Mfx方案(剂量用法同前)抗结核及保肝等治疗。4日患者无明显发热,生命体征平稳,未发现新的皮下出血点。胸部CT扫描:可见双肺粟粒结节影,双侧胸腔积液,心包积液及纵隔淋巴结肿大(图5,6);痰抗酸杆菌染色阴性。继续原方案抗结核及对症治疗。患者家属5月 15、16日携带资料到北京大学第一医院血液科和北京大学人民医院血液科会诊,意见为全血细胞减少原因待明确,不能除外感染所致,建议积极抗结核药物治疗及对症支持治疗,并进一步骨髓穿刺检查。患者未同意进行骨髓穿刺检查,需密切观察病情。
根据患者病情及血液科会诊建议,5月15、16日分别输入PLT 1 U,25日再次输红细胞2 U,5月19—27日予以rhG-CSF 400 μg/d 1次/d;5月18日、23—27日予以rhEPO 1万U/d 皮下注射,间断应用,患者病情逐渐稳定。27日血常规检查:WBC 4.72×109/L,Hb 68 g/L,PLT 46×109/L。31日腰椎穿刺结果为:颅压18 cm H2O(1 cm H2O=0.098 kPa),脑脊液检查:蛋白0.569 g/L(参考值0.15~0.45 g/L),其他常规生化指标均阴性,脑脊液Gene Xpert MTB/RIF检测结核分枝杆菌DNA阳性,rpoB基因无突变。肝功能正常。遂在化疗方案中再次增加吡嗪酰胺(0.5 g/次,2次/d;6月8日调整为0.5 g/次,3次/d)进行抗结核药物治疗。6月1日胸部CT扫描:可见双肺粟粒结节影,双侧胸腔积液吸收,心包积液减少,纵隔淋巴结缩小(图7,8);头颅MRI检查:可见双侧大脑多个点状强化灶(图9)。6月1日血常规 WBC 1.54×109/L,Hb 70 g/L,PLT 56×109/L,继续应用 rhG-CSF 400 μg/d 1次/d皮下注射,6月10日血常规检查:WBC 3.66×109/L,Hb 60 g/L,PLT 84×109/L。 6月 20日血常规为WBC 3.84×109/L,Hb 87 g/L,PLT 119×109/L;7月5日胸部CT检查:显示肺部结节影减少,双侧胸腔积液消失(图10,11)。7月7日血常规检查:WBC 1.86×109/L,Hb 94 g/L,PLT 122×109/L,予以rhG-CSF 200 μg/d 1次/d皮下注射3 d;7月11日血常规为WBC 5.25×109/L,Hb 104 g/L,PLT 125×109/L,患者出院。
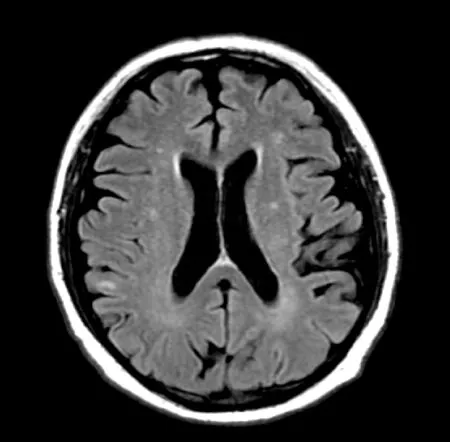
图9 头颅增强MRI(2017-06-01)检查: 可见双侧大脑多个点状强化灶
五、患者出院后情况
患者出院后我院通过电话、微信与患者沟通病情及进行进一步检查治疗的建议。患者继续原方案(H-E-PZA-Mfx)治疗,口服强的松25 mg/次,1次/d,建议每10天减量5 mg,观察病情变化;建议继续血液科就诊。患者未行血液科系统诊治。2017年8月4日患者于黑龙江某医院血常规检查:WBC 2.03×109/L,Hb 113 g/L,PLT 48×109/L;胸部CT检查(2017-08-09):可见双肺未见明显病变,纵隔淋巴结减小(图12,13)。于8月9开始应用粒细胞集落刺激因子50 μg(1次/d)皮下注射3 d。 8月11日血常规检查:WBC 5.73×109/L,Hb 106 g/L,PLT 61×109/L。患者一直采用原方案行抗结核药物治疗,并口服强的松逐渐减量及采用升白细胞等对症治疗(具体不详),建议患者血液科系统诊治及进行骨髓穿刺检查,患者未检查。8月21日在哈尔滨某医院行血常规检查:WBC 3.3×109/L,Hb 104 g/L,PLT 73×109/L。未行进一步治疗。

图10,11 胸部CT扫描(2017-07-05),可见双侧胸腔积液消失,肺部结节影减少。 图12,13 胸部CT扫描(2017-08-09),可见双肺未见明显病变,纵隔淋巴结缩小
2017年9月25日患者再次于襄阳市中心医院行骨髓穿刺检查:可见骨髓增生明显活跃,粒细胞系86%,幼粒细胞发育异常、幼核老浆样变及巨样变;红细胞系占6.5%(以中晚幼红细胞为主,可见双核、多核幼红细胞,成熟红细胞大小不等;巨核细胞成熟障碍,可见双核、多核巨核细胞,血小板散在、少见;血涂片可见大小不等成熟红细胞,血小板散在少见,考虑MDS,患者在湖北当地治疗,具体治疗不详。10月27日血常规检查:WBC 2.17×109/L, Hb 48 g/L,PLT 32×109/L。
2017年11月8日家属携带9月25日骨髓检查报告来我院,同时请河北燕达陆道培医院血液科会诊,考虑早期MDS特征不典型,结核感染系列表现可能掩盖了MDS的诊断,倾向血液系统疾病MDS的诊断,建议继续来北京进一步检查及考虑骨髓移植等治疗,但患者于当月在当地去世,死因未明确。
病例讨论及临床诊治
一、马丽萍(主任医师,北京胸科医院结核科)
患者临床特点:(1)老年男性,既往无结核病病史及结核病患者密切接触史;高血压病史7年,有房性早搏病史。(2)主要症状为乏力、头晕,活动后心慌3个月,伴有发热2个月,早期为午后低热,后期为高热。(3)血常规早期出现贫血及白细胞减少,后期红细胞、白细胞、血小板(简称“三系”)均减少,先后4次骨髓穿刺及其他血液疾病检查,无血液疾病典型特征。细胞化学染色:NAP阳性,支持感染性疾病。胸部CT检查可见典型的大小均匀及双肺弥漫粟粒结节影,头颅MRI检查可见颅内点状强化灶,血T-SPOT.TB阳性,痰结核分枝杆菌PCR检测阳性,脑脊液结核分枝杆菌基因检查阳性。(4)抗结核药物治疗后患者结核病及感染症状明显好转,血液系统实验室检测一度好转,后再次加重。再次骨髓检查考虑MDS骨髓像改变。考虑诊断:血行播散性结核病,全血细胞减少原因待查;MDS可能。
感染性疾病可对骨髓造血祖细胞产生不同程度的抑制作用,当这种抑制作用主要针对红细胞系时即产生贫血,当累及骨髓白细胞系或巨核细胞系时可导致白细胞及血小板减少;宿主结核感染后可能产生结核抗体,与血细胞表面的蛋白结合导致免疫破坏,另外结核感染可能引起营养不良,导致造血原料缺乏或者结核感染侵及骨髓,从而造成血液系统异常。血行播散性结核病患者早期可能表现不典型,多为发热、乏力,最容易出现病变的部位为肺部,肺部影像改变常常在有症状2周到1个月时出现,且多并发贫血、白细胞减少或血小板减少等情况。该患者早期以头晕、乏力为主要表现,体温先低热再高热,肺部影像学从无到典型的弥漫粟粒结节影,2次痰结核分枝杆菌基因检测阳性,抗结核药物治疗早期患者症状有缓解,血行播散性结核病诊断明确。患者并发全血细胞减少,已经在3家医院血液科进行了多项检查,从营养、免疫、感染、染色体突变等多方面寻找病因,并在多家三级医院血液科会诊,均考虑不除外与结核感染相关,均建议积极进行抗结核药物治疗;患者为重症结核病,积极抗结核药物治疗为首要选择,在我院行抗结核药物治疗后疗效明显,结核病情稳定后积极至血液科就诊可能会改善患者的预后。MDS在有些患者表现为症状或者辅助检查表现不典型,难以确诊,对此类患者应进行定期随访,定期完善相关检查,以协助疾病的确诊和观察转归。
二、高孟秋(主任医师,北京胸科医院结核科)
该患者为老年男性,早期因乏力伴发热就诊,血液系统可见全血细胞计数减低,骨髓穿刺曾发现肉芽肿改变,其胸部CT出现粟粒结节影,痰结核分枝杆基因检测阳性,血行播散性结核病诊断明确,为结核病中的重症结核感染形式,如果不及时治疗具有较高的致死性。该患者早期骨髓穿刺检查及其他血液病相关检查均无其他血液疾病的明确指向性结果,考虑结核感染继发血液系统异常。对这类患者建议进行以下治疗:(1)积极进行抗结核药物治疗。本例患者结核病诊断明确,无论继发性还是原发性结核病,都要积极抗结核治疗。但因患者血液系统异常、全血细胞计数明显减低,故不建议应用利福类抗结核药物;另外,患者为初治结核病,无耐药依据,建议应用异烟肼、乙胺丁醇、吡嗪酰胺、莫西沙星组成抗结核治疗方案;因糖皮质激素具有抗炎、抗过敏及免疫抑制等作用,继续强的松(30 mg/d)口服治疗,在有效抗结核药物保护下应用糖皮质激素治疗可取得良好的预后。但需密切观察药物不良反应。(2)加强支持治疗。患者全血细胞减低,有感染、出血等风险,和血液科及时会诊沟通,根据患者血细胞计数水平建议予以rhG-CSF和rhEPO治疗;如血小板明显减低或者有出血倾向时可采取积极输血小板,如血红蛋白水平持续降低可输血细胞改善贫血。治疗过程中还应注意对患者进行隔离保护,避免并发其他感染。(3)注意密切监测。患者为重症结核病,抗结核药物应用易引起血液系统、神经系统异常,以及肝肾功能损伤,应注意抗结核药物的不良反应,避免出现各系统的严重损伤;同时抗结核药物也可能引起骨髓抑制等情况发生,从而加重血液系统异常,故在抗结核药物治疗过程中应密切监测血常规各指标的变化及治疗后及时进行骨髓检测复查。(4)病情稳定后要进一步完善检查。血行播散性结核病患者有10%~37%并发结核性脑膜炎或者颅内结核病变,结核性脑膜炎患者的治疗及监测方式不同于血行播散性肺结核患者,患者病情平稳后建议完善腰椎穿刺、头颅MRI等检查,以协助诊断。患者为重症结核病病变,且并发严重的血液系统异常,在积极抗结核药物治疗的同时需要及时和血液科沟通,多学科合作以保证对患者的治疗安全可行。
三、燕达道培医院血液科会诊
MDS的诊断需要满足2个必要条件和4项确定标准[5]。2个必要条件为:(1)持续一系或者多系血细胞减少;(2)排除其他可以导致血细胞减少和发育异常的造血系统及非造血系统疾病。4项确定标准为:(1)发育异常:骨髓突变中红细胞系、粒细胞系、巨核细胞系中发育异常细胞比例≥10%;(2)环状铁幼粒红细胞占有核细胞比例≥15%;(3)原始细胞:骨髓涂片中达5%~19%;(4)MDS常见染色体异常。另外,有3项辅助标准:(1)流式细胞术检查显示骨髓细胞表型异常,提示髓系或者红系存在单克隆细胞群;(2)遗传学分析提示存在明确的单克隆细胞群;(3)骨髓或者外周血的CFU(集簇)形成显著并持续减少。
此患者血液系统表现为全血细胞减少,不能排除结核感染所致,并且确定标准及辅助标准均无MDS证据[未见明显病态造血、染色体、MDS相关的荧光原位杂交技术(fluorescence in situ hybridization,FISH)检测未见异常],仅仅骨髓免疫组化分型见异常表型髓系原始细胞,占有核细胞0.2%,不足以支持MDS诊断,需动态观察。因为结核病处于活动性感染状态,首先考虑结核分枝杆菌及其产物可能干扰血细胞生成或者导致血细胞消耗过多,如果此种情况存在,则随着结核病的好转,患者造血功能将得以改善,血细胞数量应该逐渐恢复;但该患者在结核病病情稳定后,其血细胞的数量未见明显上升,则考虑血液系统疾病所致,建议再次行骨髓穿刺,复查骨髓细胞形态、染色体、免疫分型、MDS相关的FISH检测、基因突变,但患者仅复查了骨髓细胞形态,显示血细胞均有明显病态造血,提示MDS。部分MDS患者早期骨髓形态学、免疫、FISH、遗传性学等检查可能不典型,随着病程进展可能会出现异常;如果一次检查未见异常,但病程及骨髓形态学支持,则需要再次进行染色体、免疫分型、FISH、基因突变筛查等,以协助诊断;另外,如果没有染色体及基因检测的证据,如果除血细胞减少外,还伴有病态造血的形态学变化,这类患者考虑诊断为难治性血细胞减少伴多系发育异常(RCMD),也属于MDS一种亚型[5]。患者抗结核治疗后结核病变好转,血液系统无改善,后期骨髓形态学改变和早期表现进展,形态学报告符合MDS,目前考虑MDS可能,但是很遗憾患者未继续完善其他检查,在诊断证据上的确MDS不够充分。如果能完善检查进一步检查,将有助于确诊及分型
讨 论
一、血行播散性结核病和MDS的概念及流行病学特征
血行播散性结核病是结核分枝杆菌进入血液循环导致的疾病,可侵及全身多个脏器(肺部、颅内、腹部脏器、淋巴结、骨骼、骨髓等)[2,4,6],其发病率在美国约占结核病的1%[7];在非洲及东南亚等结核病和艾滋病高流行地区发病率可能更高[8],而我国目前尚无确切的流行病学数据。血行播散性结核病多见于儿童及青少年,随着人口的老龄化及结核病疫情的回升,老年血行播散性肺结核有增多趋势;另外,由于艾滋病的流行、免疫抑制剂及糖皮质激素的应用,特殊人群中的播散性结核病也日益增多[2]。血行播散性结核病的临床特征和所侵及的不同脏器相关,可有乏力、发热、咳嗽、消瘦、盗汗、胸痛气短、头痛等症状。血行播散性结核病病程中结核分枝杆菌侵及造血骨髓,引起骨髓结核;或者营养不良、炎症及感染继发的病态造血、血细胞破坏,从而产生各种血液系统异常,如贫血,白细胞和淋巴细胞减少,血小板减少或全血细胞减少[9-11]。MDS是一组异质性克隆性造血干细胞疾病,骨髓内细胞增生,常同时或者先后出现红细胞、粒细胞和巨核细胞发育异常的病态造血,具有转化成急性白血病的风险[12]。MDS患者以50岁以上居多[12],多数患者起病隐匿,典型特征是外周全血细胞减少,从而出现头晕乏力、活动后心悸、出血、感染等相应症状。
在MDS引起白细胞减少的治疗中,免疫抑制剂的应用易伴发结核感染,据报道MDS并发结核病占恶性血液病并发结核感染患者的10.5%~15.7%[13-14];在我国的一项报道中显示,在17例MDS并发结核病患者中,血行播散性肺结核占13.3%(2/15)[15],发病的差异可能和各地区结核病流行情况不同有关,在我国结核感染高负担地区,要警惕MDS并发结核病尤其是血行播散性结核病的风险。
罹患MDS的病因不明确,考虑和理化因素引起基因突变或者基因表达异常有关。Lv等[16]在一项罹患MDS风险因素的病例-对照研究中指出,抗结核药物是罹患MDS的独立风险因素[OR=3.15,95%CI=1.22~8.12]。抗结核药物异烟肼、利福平、乙胺丁醇、吡嗪酰胺可能引起粒细胞减低、血小板减少、嗜酸细胞增多等多种血液系统异常;据报道,暴露于抗结核药物会导致染色体畸变、姐妹染色单体交换等异常[17],抗结核药物的基因毒性(染色体畸变)可能有助于MDS的发展[16]。作为慢性细菌感染,结核病可能通过产生细胞因子和活性代谢物或者外/内毒素诱导染色体损伤[16],但到目前为止,没有证据表明结核感染本身可能造成染色体畸形,结核感染导致MDS的证据尚未发现。
二、本例患者特征及诊治过程总结分析
血行播散性结核病的临床症状不典型,常并发血液系统的异常,而作为其诊断重要依据的肺部影像学病变,也往往在几周后才可出现;MDS早期症状或血液系统表现可能不具有特异性,两种疾病的早期诊断都比较困难。本例为老年患者,早期症状或者辅助检查均不典型,以乏力、贫血等全身症状为主要表现,骨髓穿刺等结果为非特异性,无MDS确诊证据。随着病变进展,早期的低热到后期的高热等症状出现,中性粒细胞碱性磷酸酶(NAP) 积分增高等感染病变特征显现,同时肺部、颅内影像学及痰结核分枝杆菌DNA等检查证实为并发全身结核感染,诊断考虑血行播散性结核病并发继发性三系减少,骨髓结核不除外。抗结核药物治疗后,临床症状、肺部病变及血液系统表现同时好转,可能与同时使用了糖皮质激素(强的松)有关。随着病情好转,强的松逐渐减量后,肺部病变进一步好转,而血液系统异常再次加重,骨髓穿刺复查考虑MDS诊断,但患者未进行进一步检查。该例患者在诊断血行播散性结核病之前已经发现骨髓异常,随着病情的进展表现更为典型,考虑是在MDS的基础上并发血行播散性结核病,两种疾病交叉重叠,原发病MDS被重症结核病的症状及辅助检查覆盖,同时重症结核病糖皮质激素的治疗方案也缓解了MDS的病情进展,造成MDS诊断延误;故在患者既往无原发血液疾病时,我们要综合判断血液系统异常是结核感染或药物导致的不良反应,还是并发原发性血液疾病,一定要引起重视,以免影响对原发疾病的治疗。但是在疑似或者确诊结核病时,抗结核药物的治疗是首要和必须的。
三、血行播散性结核病的诊断
血行播散性结核病最常见的是肺部病变,临床症状的出现一般早于肺部可见病灶的出现,几周后才出现肺部粟粒样结节等影像学改变,高分辨CT扫描可以较胸部X线摄影更早发现病变。血行播散性结核病标本涂片的细菌学检查阳性率较低,据报道为41%,痰标本AFB阳性率为32%,培养阳性率为67%[6]。但不是每例患者都能有效排痰,可以采用支气管肺泡灌洗液细菌学及肺部、肺外组织的活检病理组织学检查,可提高诊断阳性率;近些年分子诊断学技术在体液或者组织标本的应用,也可进一步提高诊断的敏感度[6];结核菌素皮肤试验在血行播散性结核病中的阳性率较低,据报道只有29%[6]。血行播散性结核病是一种重症结核病,早期发现及治疗可减少致残率及死亡率,各种可获得标本的细菌学、分子生物学及病理学检查都可有益于结核病的诊断。
四、血行播散性结核病并发MDS的治疗
血行播散性结核病早期发现及治疗对预后有重要影响,对一些没有确诊依据的患者,结合临床症状、影像学特征、血清结核免疫学(如T-SPOT.TB)检查结果,建议早期予以诊断性抗结核药物治疗。对于初治无耐药依据的血行播散性结核病一般使用初治方案(H-R-E-Z),疗程12~18个月;另外,给予MDS患者输血等对症支持治疗极其重要。血行播散性结核病往往伴发高热等结核中毒症状及多系统病变,在抗结核药物治疗基础上适量应用糖皮质激素,可改善症状及预后,但这可能导致包括MDS在内的许多血液系统疾病病情暂时缓解,在早期MDS没有确诊的情况下,可能延误诊断。1篇MDS的临床病例报道提示,对于MDS并发结核病的患者,在注意药物不良反应、同时积极输血对症治疗的情况下,免疫抑制剂及抗结核药物联合应用一般不会影响MDS的疗效及预后[15];但也提醒临床医生,在结核病患者并发血液系统异常时,利福平要慎用,以免加重骨髓抑制。
对于既往无明确MDS病史的结核病患者,很难早期就明确诊断两种疾病。有人建议,如果血行播散性结核病患者出现全血细胞减少症状,有可能同时并发潜在的血液病(通常是白血病或白血病前期)[18],故建议应密切观察血液系统疾病进展。另外,多种疾病可能以不明原因发热、乏力等为首发症状,当同时并发血液系统异常时,要警惕血行播散性结核病及药物不良反应的可能,并完善血液系统异常检查及动态观察,以与营养缺乏、化学药物不良反应、炎症及感染、血液系统等原发疾病进行鉴别,提高诊断率。
[1] World Health Organization. Global tuberculosis report 2017. Geneva: World Health Organization,2017.
[2] 马玙, 朱莉贞,潘毓萱.结核病学. 北京:人民卫生出版社, 2000.
[3] Sharma SK,Mohan A,Sharma A, et al. Miliary tuberculosis: new insights into an old disease. Lancet Infect Dis, 2005, 5(7): 415-430.
[4] 韩喜琴,高微微,黄学锐,等. 成人血行播散性肺结核202例临床及影像分析. 中国防痨杂志, 2009, 31(7): 425-429.
[5] 中华医学会血液学分会.骨髓增生异常综合征诊断与治疗中国专家共识(2014年版).中华血液学杂志,2014,35(11):1042-1048
[6] Mert A,Arslan F,Kuyucu T,et al. Miliary tuberculosis: Epidemiologicaland clinical analysis of large-case series from moderate to low tuberculosis endemic Country. Medicine (Baltimore), 2017,96(5): e5875.
[7] Rieder HL, Snider DE Jr, Cauthen GM. Extrapulmonary tuberculosis in the United States. Am Rev Respir Dis, 1990,141(2):347-351.
[8] Zumla A, Raviglione M, Hafner R, et al. Tuberculosis. N Engl J Med, 2013,368(8): 745-755.
[9] Brastianos PK,Swanson JW,Torbenson M, et al. Tuberculosis-associated haemophagocytic syndrome. Lancet Infect Dis, 2006,6(7): 447-454.
[10] 赵雪瑶, 韩利军,秦桂香,等. 一例血行播散性结核病患者的临床诊治过程分析. 中国防痨杂志, 2017,39(6): 648-653.
[11] Asaji M,Tobino K,Murakami K,et al. Miliary Tuberculosis in a Young Woman with Hemophagocytic Syndrome: A Case Report and Literature Review. Intern Med, 2017,56(12): 1591-1596.
[12] 陈灏珠.实用内科学.12版. 北京:人民卫生出版社, 2006: 2333-2338.
[13] 朱卫民,田陪军,陈士军,等.恶性血液病合并肺结核19例. 白血病·淋巴瘤,2008,17(4):303-304.
[14] De La Rosa GR,Jacobson KL,Rolston KV, et al.Mycobacteriumtuberculosisat a comprehensive cancer centre: active disease in patients with underlying malignancy during 1990—2000. Clin Microbiol Infect, 2004,10(8): 749-752.
[15] 黄世华,陈丹.15例骨髓增生异常综合征并发结核的临床分析. 华西医学, 2008,23(6):1329.
[16] Lv L, Lin G, Gao X, et al. Case-control study of risk factors of myelodysplastic syndromes according to World Health Organization classification in a Chinese population. Am J Hematol, 2011,86(2): 163-169.
[17] Attia SM. Chromosomal composition of micronuclei in mouse bone marrow treated with rifampicin and nicotine, analyzed by multicolor fluorescence in situhybridization with pancentromeric DNA probe. Toxicology, 2007,235(1/2): 112-118.
[18] Maartens G,Willcox PA,Benatar SR. Miliary tuberculosis: rapid diagnosis, hematologic abnormalities, and outcome in 109 treated adults. Am J Med, 1990,89(3): 291-296.

