咽舒康口服液薄层鉴别及含量测定研究
汪宏雷,吴成志,李易阳
(1.皖南医学院第二附属医院 药剂科,安徽 芜湖 241000;2.芜湖市中医医院 中药房,安徽 芜湖 241000;3.澳门科技大学 中医药学院,中国 澳门 519020)
抗生素是治疗咽炎的主要临床药物,但疗效并不明确,且在临床使用中常存在耐药性。皖南医学院第二附属医院根据治疗咽炎的经验方开发了咽舒康口服液,该处方由玄参、黄芩、青果、麦冬等七味中药组成。为了更好地控制该制剂的质量,我们对处方中的各味药按君臣佐使的顺序进行薄层及含量测定,提出青果、玄参、黄芩的薄层鉴别方法及黄芩中黄芩苷的质量控制方法,制定咽舒康口服液的质量标准。
1 仪器与试药
1.1 仪器 所用仪器包括U3000型高效液相色谱仪[赛默飞世尔科技(中国)有限公司]、KQ-500VDV型超声波清洗机(昆山市超声仪器有限公司)、DZKW-D-4型电热恒温水浴锅(北京市永光明医疗仪器厂)、WFH-3型三用紫外仪(上海米青科实业有限公司)、1011A型数显恒温干燥箱(常州市万丰仪器制造有限公司)。
1.2 试药 黄芩苷对照品(批号:110715-201317,规格:40 mg) 、玄参对照药材(批号:121008-201609,规格:1 g)和青果对照药材(批号:121643-201302,规格:1 g)均购自中国食品药品检定研究院;咽舒康口服液(批号:20160912、20160914、20160916);色谱甲醇;其余试剂均为分析纯。
2 薄层鉴别
2.1 黄芩的鉴别[1-3]取本品(批号:20160912、20160914、20160916)20 mL,依据文献[1-3]步骤制备黄芩供试品溶液、1 g/L的黄芩苷对照品和缺黄芩的阴性口服液样品。参照薄层色谱法[2](2015版《中华人民共和国药典》四部通则)试验,制备黄芩苷对照品-阴性样品-样品薄层板。结果:不同批号供试品溶液在硅胶G薄层板上显色板点与黄芩苷对照品显色Rf相同,且阴性溶液色谱无干扰。见图1。
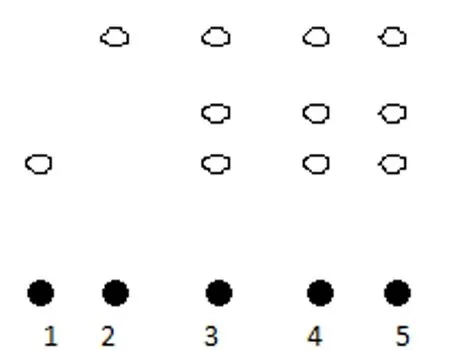
1.黄芩苷对照品;2.阴性样品;3.样品批号20160912;4.样品批号20160914;5.样品批号20160916 。
图1 黄芩TLC图
2.2 玄参的鉴别[1,4-6]取本品(批号:20160912、20160914、20160916)10 mL,依据文献[1,4-6]步骤制备玄参样品溶液、玄参对照溶液和缺玄参的阴性口服液样品。参照薄层色谱法(2015版《中华人民共和国药典》四部通则)试验,制备玄参对照品-阴性样品-样品薄层板。结果:不同批号供试品溶液在硅胶G薄层板上显色板点与玄参对照品显色Rf相同,且阴性样品色谱无干扰。见图2。

1.阴性样品;2.玄参对照药材;3.样品批号20160912;4.样品批号20160914;5.样品批号20160916。
图2 玄参TLC图
2.3 青果的薄层鉴别[1,7-8]取本品(批号:20160912、20160914、20160916)10 mL,依据文献[1,7-8]步骤制备青果样品溶液、青果对照溶液和缺青果的阴性口服液样品。参照薄层色谱法(2015版《中华人民共和国药典》四部通则)试验,制备青果对照品-阴性样品-样品薄层板。结果:不同批号供试品溶液在硅胶G薄层板上显色板点与对照药材显色Rf相同,且阴性样品色谱无干扰。见图3。

1.青果对照药材;2.样品批号20160912;3.样品批号20160914;4.样品批号20160916;5.阴性样品。
图3 青果TLC图
3 含量测定
通过对咽舒康口服液进行处方分析并结合药典中各个药材的质量标准,最终将处方中的黄芩作为考察成分,以其所含的黄芩苷作为质量控制的指标进行含量的测定[1,9-10]。
3.1 色谱条件 选用依利特Hypersil ODS2(4.6 mm×250 mm,5 μm) 色谱柱;以0.1%磷酸水溶液∶甲醇=53∶47为流动相;流速为1.0 mL/min,柱温30℃;检测波长280 nm;按黄芩苷计其理论塔板数应不少于2500。
3.2 溶液的制备
3.2.1 黄芩苷对照品溶液的制备 精密称取黄芩苷对照品,用甲醇配制成22.44 mg/L的溶液。
3.2.2 供试品溶液的制备 精密移取本品1 mL加甲醇定容至25 mL容量瓶中,从中精密量取1 mL置20 mL容量瓶中用甲醇定容,取续滤液即得。
3.2.3 阴性样品溶液的制备 取缺黄芩阴性制剂,同供试品溶液制备方法制备。
3.2.4 专属性试验 取黄芩苷对照品溶液、供试品溶液及咽舒康阴性溶液各5 μL,按“3.1”色谱条件注入高效液相色谱仪进行测定。结果显示:在与对照品色谱相应位置上供试品溶液有色谱峰,而阴性样品未出现色谱峰,表明在该HPLC测定条件下,黄芩苷的测定无阴性干扰,见图 4。
3.3 标准曲线的制备 按“3.1”色谱条件,分别精密吸取 2、4、6、8、10 μL“3.2.1”项下已制备的黄芩苷对照品溶液,以黄芩苷的量(ng)为横坐标,测得色谱峰面积为纵坐标,进行线性回归,得其方程:A=0.0576C+0.0816;R2=0.999 97。结果表明,黄芩苷在浓度为67.32~157.08 ng的范围内呈良好线性关系。
3.4 精密度试验 连续将对照品为22.44 mg/L的溶液进样6次,测得其平均峰面积为6.539,RSD为0.26%(n=6),表明仪器的精密度良好。

A:黄芩苷对照品;B:咽舒康口服液样品;C阴性对照样品。
图4 HPLC专属性
3.5 重复性试验 取咽舒康口服液(批号:20160912)6份,按照供试品制备方法制样,分别测定。测得其平均含量为9.8998 g/L,RSD为1.8%,表明该方法具有良好的重复性。
3.6 样品稳定性试验 取供试品(批号:20160912)溶液,按照“3.1”色谱条件,在配制后0、2、4、6、8、10、12、24 h分别进样测定峰面积,测得其平均值为5.981,RSD为0.5%(n=8),显示出该咽舒康样品溶液稳定。
3.7 加样回收试验 精密移取批号为20160912的咽舒康口服液(含量9.8998 g/L)6份(每份1 mL)置于50 mL的量瓶中,加入储备液4 mL(浓度2.8047 g/L),用甲醇定容,摇匀。于20 mL容量瓶中加入上述液1 mL,甲醇定容,摇匀,过滤,取续滤液,按“3.1”色谱条件,分别进样测定,记录峰面积,计算回收率,平均回收率为102.12%,RSD=1.06%,(n=6),可见此方法测定黄芩苷回收率较高,准确度较高。结果见表1。
表1 加样回收试验结果

取样量/mL样品量/mg加入量/mg测得量/mg回收率/%平均回收率/%RSD/%19.899811.218821.2722101.3719.899811.218821.2861101.4919.899811.218821.4771103.20102.121.0619.899811.218821.2006100.7319.899811.218821.4007102.5119.899811.218821.5014103.41
3.8 样品含量测定 将三个批次(批号:20160912、20160914、20160916)的咽舒康口服液进行含量测定,结果分别为9.74、10.18、8.59 g/L。
4 讨论
4.1 薄层色谱条件的选择优化
4.1.1 本文对处方中全部药味均进行了薄层鉴别的试验,但只能将黄芩、青果及玄参进行有效的分离鉴定,其余药味存在主斑点分离不开、阴性干扰等,所以仅将黄芩、青果和玄参的薄层鉴别暂时纳入本质量控制标准之中。依据2015版《中华人民共和国药典》及相关文献的查阅,最终确定本方中所做的薄层色谱法中目标成分分别为:黄芩鉴别的是黄芩苷,玄参鉴别的是哈巴俄苷,青果鉴别的是香豆素。
4.1.2 对黄芩的鉴别中,最初采用冰醋酸-水-正丁醇(1∶2∶7)为展开剂,但存在展开速度慢、拖尾及背景干扰等缺点。经摸索,以水-乙酸乙酯-丁酮(1∶5∶3)作为展开剂时,分离度等指标较好,但仍存在拖尾,因此在展开剂中加入少许甲酸,拖尾现象得到改善,最终展开剂为水-乙酸乙酯-甲酸-丁酮(1∶5∶1∶3),该色谱条件分离黄芩主斑点的效果较好。
4.1.3 对于处方中玄参的鉴别,按照药典及其他文献的方法发现存在较大干扰,将其方法进行梳理整合后采用酸解,乙酸乙酯提取,样品杂质较少,操作简单。
4.2 液相色谱条件的选择优化
4.2.1 考虑到样品中黄芩苷能否得到充分的提取,本试验对同一批次的样品进行如下两种不同处理方法的比较:超声(0、10、20、30 min)、提取溶剂(甲醇、乙醇)。测定结果表明超声提取对其含量无明显影响,而不同的提取溶剂对其有影响,且甲醇高于乙醇。故此次对黄芩苷的提取条件是甲醇溶解,混匀即可,该提取方法方便简单,利于实验的操作。
4.2.2 流动相的选择 本次分别考察了甲醇-水、甲醇-磷酸溶液(浓度分别为0.1%、0.2%、0.3%、0.4%)、乙腈-水系统为流动相时含量测定,以峰高、分离度、重复性、拖尾因子、不对称度等作为考察指标,结果发现流动相不管是甲醇-水还是乙腈-水,在色谱图中均有拖尾显现。结合以往经验,我们在水相中加入一定量磷酸,结果显示色谱的峰形和拖尾均得到改善。但考虑到乙腈的成本较甲醇高,所以此次用甲醇-磷酸溶液作为流动相,同时此次对不同浓度的磷酸溶液进行考察,结果发现在一定浓度范围内,随着磷酸浓度的增加,对峰形无明显影响,但是随着浓度的增加酸度增强,对色谱柱的损伤性也在增大且该损伤是不可逆的,最终本次实验采用了甲醇-0.1%的磷酸溶液作为流动相,效果较好。
【参考文献】
[1] 国家药典委员会.中华人民共和国药典[M].北京:化学工业出版社,2015.
[2] 段秀君.薄层色谱鉴别法鉴别清利合剂中的当归、金银花、黄芩[J].内蒙古中医药,2010,29(11):148-149.
[3] 赵琦,张军武,安国军.清热解毒口服液薄层鉴别方法的改进研究[J].长春中医药大学学报,2010,26(6):957-958.
[4] 段国玲,王丽,赵春香.清咽利喉颗粒主要成分的薄层色谱鉴别[J].药物鉴定,2011,20(24):45.
[5] 许春燕,刘希望,杨亚军,等.银翘蓝芩口服液薄层色谱鉴别方法研究[J].动物医学进展,2015,36(11):40-43.
[6] 余卫兵.消糖益肾饮中地黄、黄芪、丹参的TLC法鉴别[J].中国药师,2008,11(5):595-596.
[7] 李兵.桔梗清咽合剂的薄层鉴别研究[J].临床合理用药杂志,2011,4(22):124-124.
[8] 李煜,陈延翊.利咽清嗓口服液质量标准的研究[J].中国医院用药评价与分析,2013,13(6):537-540.
[9] 陈伟平,曾玉兰,黄晓丹.克感利咽口服液质量标准的提高研究[J].中药材,2015,38(5):1078-1080.
[10] 罗燕.越鞠口服液制备工艺及质量标准研究[D].成都:成都中医药大学,2009.
——徐州市青果小作家基地简介

