吻合口部位残胃癌患者的临床病理特点与生存状况分析
熊柏超,章晓景,丁渊明
残胃癌是指接受过手术切除部分或大部分胃部造成残胃发生远侧或近侧发生癌性病变的疾病[1-2]。残胃癌多发于吻合口部,由于该类疾病无特异诊断标准,患者确诊时多处于进展期,严重影响患者治疗效果,预后较差[3-4]。本文探讨吻合口部残胃癌的临床病理特点及生存状况,现报道如下。
1 资料与方法
1.1 一般资料 选取浙江省湖州市南浔区练市人民医院2007年1月至2017年1月收治的胃癌患者146例。纳入标准:(1)经临床病理学及实验室指标确诊患者为原发性胃癌;(2)年龄18~75岁;(3)接受过姑息性手术和根治性手术;(4)患者及其家属对本次研究知情并签署知情同意书。排除标准:(1)患者合并其他恶性肿瘤;(2)有精神障碍、意识障碍;(3)为妊娠期、分娩期妇女;(4)有严重肝脏、肾脏功能性损伤。根据肿瘤部位分为吻合口组(72例)和非吻合口组(74例)。吻合口组男43例,女29例;年龄25~52岁,平均(43.29±10.07)岁;病程1~3年,平均(2.07±0.35)年。非吻合口组男39例,女 35例;年龄 24~ 55岁,平均(44.16±11.21)岁;病程1~3年,平均(2.15±0.30)年。两组一般资料差异无统计学意义(>0.05)。本次研究经医院伦理委员会审核通过,符合相关伦理标准。
1.2 方法 根据国际抗癌联盟(UICC)第七版TNM分期标准对患者进行分期,分别是Ⅰ、Ⅱ、Ⅲ、Ⅳ期;根据日本第13版《胃癌处理规则》将患者分为分化良好型和分化不良型,分化良好型包括中分化型腺癌、高分化型腺癌;分化不良型包括低分化型腺癌、印戒细胞癌、黏液腺癌;对患者的体质量指数(BMI)、胃原发病(良性病变、恶性病变)、肿瘤浸润深度(T1、T2、T3、T4)、肿瘤大小、肿瘤 TNM分期(Ⅰ、Ⅱ、Ⅲ、Ⅳ期)、肿瘤组织分型(分化良好、分化不良)等病理特点进行统计;对患者手术时间、淋巴结切除数、术中出血量、淋巴结转移率、联合器官切除率、术后并发症发生率等手术情况进行统计;对两组患者手术治疗后3个月、手术治疗后6个月、手术治疗后1年内生存率进行统计。
1.3 统计方法 采用SPSS23.0软件对数据进行统计学分析。计量资料以均数±标准差表示,采用 检验;计数资料采用2检验。<0.05为差异有统计学意义。
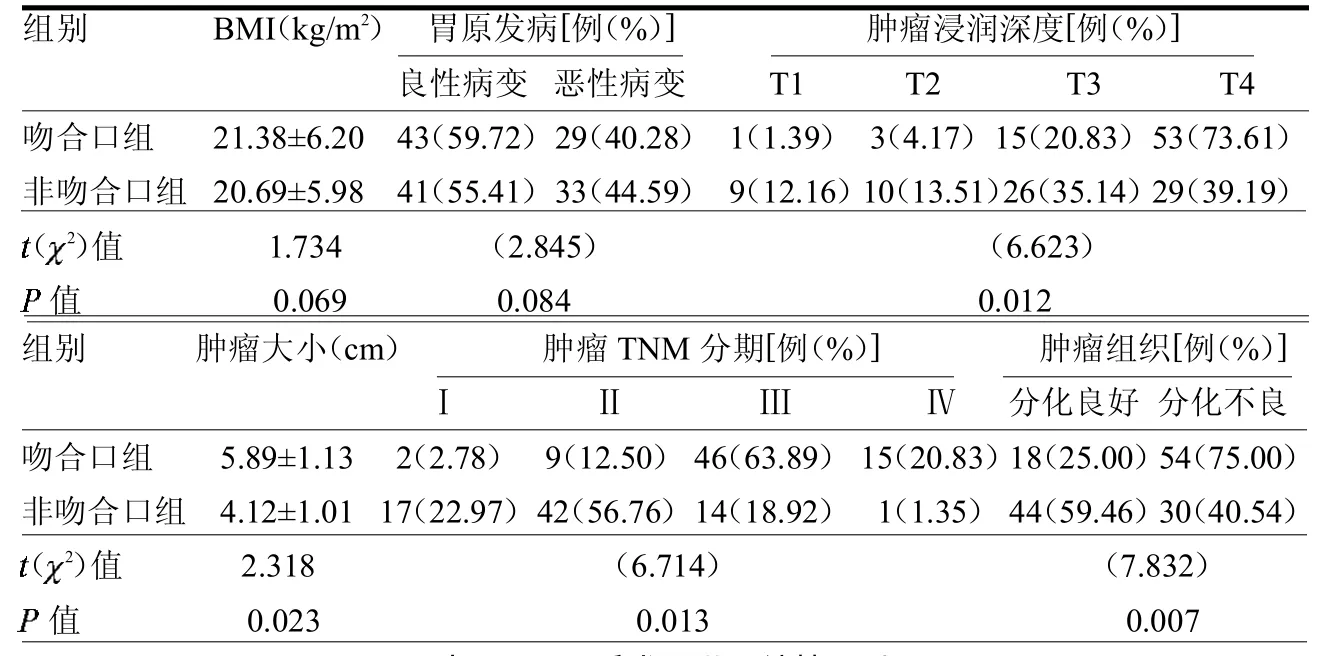
表1 两组临床病理特点对比

表2 两组手术及淋巴结情况对比

表3 两组手术治疗预后对比 例(%)
2 结果
2.1 两组临床病理特点 两组BMI、胃原发病差异均无统计学意义(均>0.05);而肿瘤浸润深度、肿瘤大小、肿瘤TNM 分期及肿瘤组织分化差异均有统计学意义(均< 0.05),见表 1。
2.2 两组手术及淋巴结情况 两组术中出血量、手术时间及淋巴结切除数差异均无统计学意义(均> 0.05);两组术后并发症发生率、联合器官切除率及淋巴结转移率差异均有统计学意义(均< 0.05),见表 2。
2.3 两组预后比较 吻合口组患者术后3个月、术后6个月生存率差异均无统计学意义(均>0.05);两组术后1年生存率差异有统计学意义(<0.05),见表 3。
3 讨论
残胃癌由于无显著病理特点,确诊时多为进展期,容易错过最佳的治疗时机,对患者身体造成极大的伤害[5-6]。研究报道表示,进展期残胃癌患者术后5年内生存率仅为5%,死亡率极高[7]。但近年来残胃癌诊断水平的提升和外科手术技术的不断提高使进展期残胃癌患者术后5年内生存率提高至50%左右,极大提高了患者治疗后的预后质量。国内外大量数据显示残胃癌患者好发于吻合口部,且吻合口部患者术后预后质量较差。同时目前我国对残胃癌的诊断方式尚未有完全一致的标准,且诊断水平尚需进一步提高,因此对残胃癌患者病理特点进行分析,总结得出吻合口部残胃癌患者与非吻合口部残胃癌患者之间的差异具有重要意义,能够为临床上治疗吻合口部残胃癌患者提供有效信息。
参考文献:
[1] 余稳稳,陶瑞雨,闫开旭,等.胃肠反流与残胃癌发生的研究进展[J].中华普通外科学文献:电子版,2016,10(6):455-458.
[2] 郭诚,王瑞智.残胃癌的诊断及治疗17例分析[J].中国药物与临床,2017,17(10):1511-1512.
[3] Nozaki I,Hato S,Kobatake T.et al.Incidenceof metachronousgastric cancer inthe remnant stomach after synchronous multiplecancer surgery[J].Gastric cancer,2014,17(1):61-66.
[4] Tokunaga M,Sano T,Ohyama S.et al.Clinicopathological characteristicsand survival differencebetweengastric stump carcinomaand primary upper third gastric cancer[J].Journal of gastrointestinal surgery,2013,17(2):313-318.
[5] 王晔,丁士刚.残胃癌发病机制及治疗[J].癌症进展,2016,14(1):4-6.
[6] 刘媛,周纯武,田艳涛,等.残胃癌的多层螺旋CT表现与术后病理对照分析[J].癌症进展,2016,14(1):10-13.
[7] MiyashitaT,MiwaK,InokuchiM.etal.Spontaneousclearanceof Helicobacter pyloriafter pylorus-preserving gastrectomy for gastric cancer[J].Oncology reports,2013,30(1):299-303.
[8] 侯剑波.残胃癌临床特点及诊治分析[J].中国医药导刊,2013,21(10):1576-1577.
[9] HikiN,Nunobe S,Kubota T.etal.Functionpreserving gastrectomy for early gastric cancer[J].Annalsof surgical oncology,2013,20(8):2683-2692.
[10]Choi YY,Kwon IG.,Lee SK.etal.Canwe apply thesameindicationof endoscopic submucosal dissection for primary gastric cancer to remnant gastric cancer[J]?Gastric cancer,2014,17(2):310-315.

