HPLC-ELSD法测定三草鼻咽清煎膏剂中黄芪甲苷的含量
朱日明 罗瑜
三草鼻咽清煎膏剂全方由黄芪、鱼腥草、 夏枯草、龙胆等十一味中药组成, 具有清热解毒、散结消炎的功效, 主要用于鼻咽部鼻咽部慢性炎症疾病。为了有效地控制制剂的内在质量, 本研究选择方中黄芪的活性成分黄芪甲苷作为质控指标[1], 采用HPLC-ELSD法对其含量进行方法学分析研究,现将实验结果报告如下。
1 材料与方法
1.1 仪器与试剂 Agilent1200高效液相色谱仪(配有G1312A二元泵、蒸发光散射检测器和安捷伦色谱工作站);色谱柱Eclipse XDB-C18柱 (200 mm×4.6 mm, 5 μm);YP202N 型电子天平(上海精密仪器有限公司)。
黄芪甲苷对照品(购自中国食品药品检定研究院, 供含量测定用);三草鼻咽清煎膏剂 (韶关市中医院制剂室自制 , 批号 :20170228, 20170414, 20170605, 20170810, 规格 :100 g/瓶);阴性样品(按处方比例, 除去被检药材同法制备而成);乙腈(色谱纯);水为重蒸馏水;其他试剂均为分析纯。
1.2 溶液制备 精密称取黄芪甲苷对照品适量, 加甲醇配制成约0.1 g/L的溶液, 作为对照品溶液;精密量取三草鼻咽清煎膏剂50 ml, 转移至分液漏斗中, 用水饱和的正丁醇提取4 次 (30 、30 、25 、25 ml), 合并正丁醇液 , 用氨试液洗涤 2 次 ,40 ml/次, 正丁醇液回收溶剂至干, 残渣加甲醇溶解, 并移至5 ml量瓶中, 用甲醇稀释至刻度, 摇匀, 用0.45 μm微孔滤膜滤过, 取续滤液作为供试品溶液;取按处方比例及制备工艺制备不含黄芪的阴性样品, 按照供试品溶液的制备方法制成阴性对照品溶液。
1.3 方法
1.3.1 色谱条件 色谱柱:Eclipse XDB-C18柱(200 mm×4.6 mm, 5 μm);柱温 :25 ℃ ;流动相 :乙腈 -水 32∶68);流速:1.0 ml/min;ELSD参数:漂移管温度:60 ℃;载气流速:1.6 ml/min。
1.3.2 色谱系统适用性试验 按“1.3.1”项下色谱条件,将对照品溶液、供试品溶液、阴性对照液各10 μl注入高效液相色谱仪, 测定, 并记录色谱图。
2 结果
供试品溶液中黄芪甲苷能与其他成分有较好的分离度,阴性对照液无干扰峰出现。色谱图见图1~3。

图1 供试品HPLC图

图2 黄芪甲苷对照品HPLC图

图3 阴性样品HPLC图
2.1 线性关系考察 分别精密吸取上述对照品溶液1、5、10、15、20 μL, 按拟定的色谱条件, 分别注入液相色谱仪, 记录色谱图、峰面积值。以峰面积的自然对数值为纵坐标(Y), 以浓度的自然对数值为横坐标(X), 得回归方程:Y=1.7733X+1.8092(R2=0.9990), 结果表明黄芪甲苷在0.5781~11.5614 g/L范围内峰面积与浓度之间呈良好的线性关系。
2.2 精密度试验 取同一份对照品溶液, 连续进样6次,15 μl/次, 记录黄芪甲苷峰面积, 结果RSD=0.55%。
2.3 稳定性试验 取同一份供试液, 分别于0、2、4、6、8、24 h进样, 记录黄芪甲苷色谱图的峰面积的RSD为0.19%。结果表明供试品溶液在24 h内具有良好的稳定性。
2.4 重复性试验 取同一批样品(批号为20170228)按“1.2”项下的方法制备6份供试液, 分别进样测定, 以黄芪甲苷的峰面积计算RSD为0.54%, 表明本品含量测定方法重复性良好。
2.5 加样回收率试验 精密量取已知含量的批号为20170228的样品(黄芪甲苷含量为0.0362 mg/ml)30 ml, 平行取样9份, 分别在1~3号样品中精密加入黄芪甲苷对照品溶液1.8 ml, 在4~6号样品中精密加入黄芪甲苷对照品溶液2.1 ml, 在7~9号样品中精密加入黄芪甲苷对照品溶液2.6 ml,按“1.2”项下的方法制备供试液, 按上述色谱条件测定, 计算回收率, 结果平均回收率为99.37%, RSD=0.44%。表明该方法符合定量分析的要求。见表1。

表1 加样回收率试验结果
2.6 样品的含量测定 取3批样品(批号分别为20170414、20170605、20170810), 按“1.2”项下的方法制备成供试品溶液, 依方法进样10 μl测定含量。见表2。
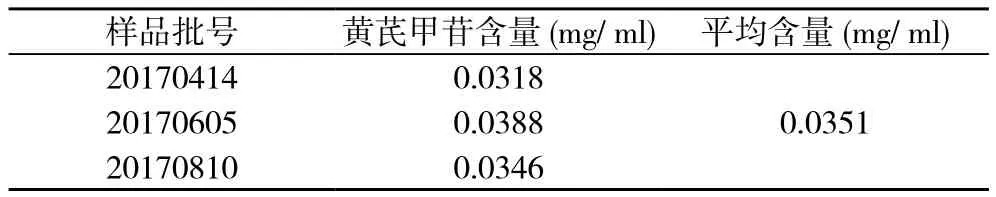
表2 样品含量测定结果
3 讨论
3.1 本文在制备三草鼻咽清煎膏剂中黄芪甲苷的供试液时,主要参考了参照2015年版《中国药典(一部)》及相关文献[2-4], 同时进行了黄芪甲苷不同的提取实验, 而从本院制剂室实际检验条件, 考虑成本, 操作方法, 因此本实验制备供试液采用水饱和的正丁醇提取、氨试液洗涤的方法, 确保次数及每次试剂用量, 经反复验证, 黄芪甲苷提取率较高,既缩短了样品前处理的时间, 而且样液的稳定性较好。
3.2 本文在参考关于黄芪甲苷含量测定相关文献报道的基础上[5-7], 进行了色谱系统的优化实验。考察了流动相乙腈-水的比例、色谱分离效果, 实验结果以乙腈-水(32∶68)为流动相时, 黄芪甲苷色谱峰与其他峰能达到较好的基线分离,且出峰时间合适[8-14]。
3.3 本文以方中主药黄芪中的主要活性成分黄芪甲苷为指标, 采用HPLC-ELSD法测定其含量, 通过方法学考察表明,本方法灵敏度高, 准确可靠, 可用于三草鼻咽清煎膏剂内在质量的控制。
[1] 孙政华, 邵晶, 郭玫.黄芪化学成分及药理作用研究进展.中医临床研究, 2015, 7(25):22-25.
[2] 国家药典委员会.中华人民共和国药典(一部).北京:中国医药科技出版社, 2015:55.
[3] 李长根.HPLC-ELSD法测定十味芪术通窍合剂中黄芪甲苷含量.安徽医药, 2013, 17(3):402-404.
[4] 王欣, 郭宏伟, 张悫, 等.HPLC-ELSD法测定阿胶黄芪口服液中黄芪甲苷的含量.现代中西医结合杂志, 2011, 20(13):1641-1642.
[5] 谢紫薇, 谭天林 , 王瑗萍, 等.高效液相色谱-蒸发光散射检测器法测定健儿宝颗粒中黄芪甲苷含量.中国药业, 2016,25(13):77-79.
[6] 王红, 杨慈海, 宋军, 等.高效液相色谱-蒸发光散射检测法测定抗栓通络丸中黄芪甲苷含量.中国药业, 2016, 25(4):75-77.
[7] 庄妍, 朱红, 范其坤, 等.HPLC-ELSD法测定九味肾清颗粒中黄芪甲苷的含量.南昌大学学报(医学版), 2015, 55(4):18-21.
[8] Zhao L, Zhu D, Yan Y.Determ ination of Astragaloside in Radix Astragali by HPLC-ELSD.Chinese Journal of Pharmaceutical Analysis, 1999, 19(3):403-405.
[9] Cao X, Liang J, He X, et al.D etermination of astragaloside in Yiganning Granules by HPLC-ELSD.Chinese Tra ditional Patent Medicine, 2005,27(2):165-167.
[10] 刘正磊, 冯素香, 李娟,等.高效液相-蒸发光散射检测法测定黄芪药材中黄芪甲苷含量.中医学报, 2012, 27(3):334-335.
[11] 王宗权, 贾继明 , 裴彩云.高效液相色谱 -蒸发光散射检测器法测定不同产地黄芪中黄芪甲苷含量.中国药业, 2013,22(19):10-12.
[12] 孙立华, 吴爱英, 张春辉.高效液相色谱-蒸发光散射检测器法测定虫草精口服液中黄芪甲苷的含量.中国现代应用药学,2004, 21(6):485-487.
[13] 庞兴寿, 牟晓崟.高效液相色谱-蒸发光散射检测器法测定仙芪眩宁颗粒中黄芪甲苷含量.中国药业, 2011, 20(17):32-33.
[14] 马宏达, 胡北, 史国兵,等.高效液相色谱法-蒸发光散射检测器测定参芪养心滴丸中黄芪甲苷的含量.山西医药杂志,2012, 41(22):1188-1189.

