克唑替尼对晚期非小细胞肺癌患者外周血清基质金属蛋白酶9的影响
于永涛,佟 倜
(吉林大学第二医院,吉林 长春 130041)
非小细胞肺癌(NSCLC)[1]具有肿瘤细胞生长分裂较慢、扩散转移相对较晚的临床特征,但恶性程度高,多数患者发现时已处于中晚期,手术治疗已不适宜[2-3]。对于Ⅲb/Ⅳ期患者,传统化学治疗(简称化疗)方案主要为含铂的两药联合方案,可在一定程度上改善患者的生存期,但不良反应较大,患者生存质量差[4]。随着分子遗传学研究的不断深入,NSCLC的治疗取得了突破性进展。2003年第一个被发现可选择性作用于表皮生长因子受体的酪氨酸激酶抑制剂(epidermal growth factor receptor tyrosinekinase inhibitors,EGFRTKIs)类靶向药物吉非替尼批准上市,标志着肿瘤治疗进入新纪元。克唑替尼(crizotinib)是口服型三磷酸腺苷(ATP)竞争性抑制剂,为小分子ATP模拟化合物,通过抑制间变性淋巴瘤激酶(ALK)信号通路活化发挥抗肿瘤活性[5]。本研究中回顾性分析了医院收治的晚期NSCLC患者应用克唑替尼对肿瘤的抑制作用,以及对外周血清基质金属蛋白酶9(MMP-9)的影响。现报道如下。
1 资料与方法
1.1 一般资料
诊断标准:组织病理学或细胞学结果证实为Ⅲ期或Ⅳ期NSCLC;经Ventana免疫组织化学或荧光原位杂交技术或实时荧光聚合酶链反应(RT-PCR)或二代测序法基因检测ALK重排融合基因阳性,或ROS1基因重排检测阳性。
纳入标准:诊断明确;体力状况(ECOG)评分0~2分,预计生存期大于6个月;根据实体瘤客观疗效评价标准(RECIST 1.1)至少有1个可测量病灶。患者自愿接受治疗并签署知情同意书;本研究方案经医院医学伦理委员会批准实施。
排除标准:骨髓造血功能异常;重要脏器功能受损;妊娠或哺乳期女性。
病例选择与分组:选择医院2015年至2016年收治的晚期NSCLC患者124例,根据患者诊断结果及个人意愿采用不同化疗方案治疗,并分为观察组(70例)和对照组(54例)。两组患者一般资料比较,差异无统计学意义(P >0.05),具有可比性。详见表 1。
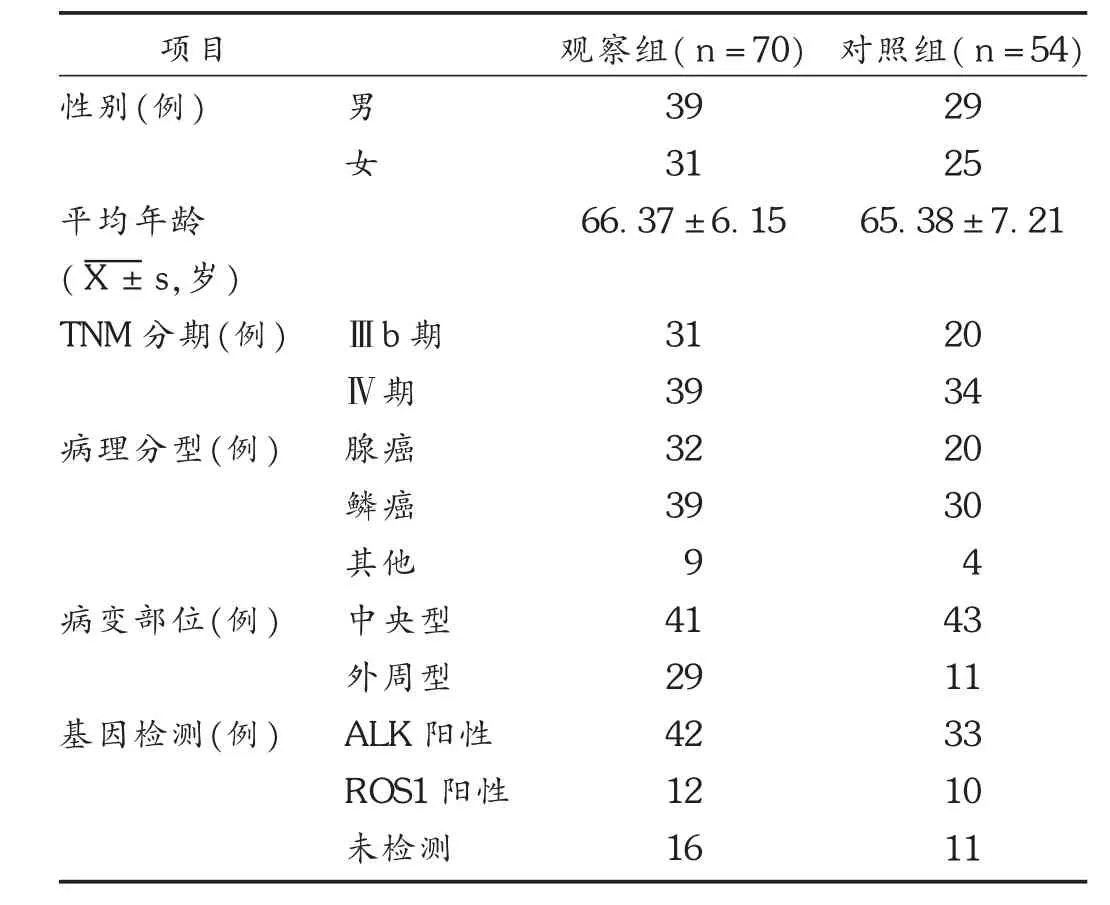
表1 两组患者一般资料比较
1.2 方法
观察组患者口服克唑替尼胶囊(商品名赛可瑞,德国 Pfizer Manvfacturing Devtschland GmbH,进口药品注册证号 H20130078,规格为每粒250 mg),每次250 mg,每日2次,早晚定时服用。对照组患者静脉滴注多西他赛注射液(商品名艾素,江苏恒瑞医药股份有限公司,国药准字 H20020543,规格为每支 0.5 mL ∶20 mg)化疗,75 mg/m2,化疗前1天口服地塞米松片每次8 mg,每日2次。两组均以21 d为1个化疗周期,化疗2个周期。
1.3 观察指标及疗效评价标准
观察指标:采用酶联免疫吸附(ELISA)法测定患者治疗前后血清MMP-9表达情况;采用生活质量评估量表(QOL)评价患者治疗后生活质量改善情况。
2个疗程后,参照世界卫生组织(WHO)制订的RECIST 1.1 评价临床疗效[6]:完全缓解(CR),肿瘤实体完全消失,临床症状及体征好转,无新病灶发生;部分缓解(PR),肿瘤实体最大直径与最大垂直直径乘积较治疗前缩小超过50%,转移淋巴结无变化;稳定(SD),肿瘤实体最大直径与最大垂直直径乘积较治疗前缩小不超过50%,增大不超过25%;进展(PD),治疗后肿瘤实体最大直径与最大垂直直径乘积较治疗前增大超过25%。总缓解(RR)=CR +PR。
1.4 统计学处理
2 结果
结果见表2至表4。

表2 两组患者临床疗效比较[例(%)]
表3 两组患者血清MMP-9表达情况及QOL量表评分比较()

表3 两组患者血清MMP-9表达情况及QOL量表评分比较()
注:与本组治疗前比较,*P <0.05;与对照组治疗后比较,#P <0.05。
组别MMP -9(pg/mL) QOL 量表评分(分)观察组(n=70)对照组(n=54)治疗前315.14 ± 31.63 318.70 ± 30.17治疗后231.23 ± 20.45*#294.31 ± 19.14*治疗前4.41 ± 1.14 4.40 ± 1.12治疗后3.38 ± 0.87*#2.27 ± 1.01*

表4 两组患者不良反应发生情况比较[例(%)]
3 讨论
NSCLC一线治疗药物主要为铂类药物联合其他类化疗药物,存在不良反应较多、易产生耐药性等问题[7]。40%的NSCLC患者一线化疗过程中出现病情进展及恶化,超过50%的患者在一线治疗4个周期后出现病情进展[8]。靶向药物为NSCLC患者开辟了新的治疗方向。有调查显示,我国接近1/3的肺癌患者具有明确的肿瘤驱动基因,相当一大部分的驱动基因具有明显的排他性,对此类患者采用个体化的靶向药物治疗效果确切[6]。表皮生长因子受体(EGFR)基因突变型NSCLC在亚洲人群中的比例最高,吉非替尼治疗NSCLC,具有特异性高、安全性好等优势[9]。首次接受吉非替尼治疗疗效较佳的绝大多数肺癌患者后期仍会复发,并对吉非替尼产生耐药性,发生获得性耐药反应。获得性耐药的机制目前尚不十分明确,但可能与EGFR基因存在T790M突变相关[10]。目前,吉非替尼耐药的处理策略主要为应用EGFR抑制剂和联合或单用多靶点药物,阻断信号通路[11]。
ALK基因是继EGFR基因后肺癌治疗的又一驱动基因,克唑替尼是第一个ALK酪氨酸激酶抑制剂,通过抑制c-Met激酶,破坏c-Met的信号转导通路,抑制ALK融合基因,干预蛋白合成,抑制肿瘤细胞生长[12-13]。ALK融合基因发生于3% ~7%的NSCLC患者,常见于年轻、不吸烟的NSCLC患者,EGFR基因与ALK融合基因突变的发生一般互相排斥,但临床也可见双基因突变腺癌患者,联合用药对症状改善有一定效果[14]。克唑替尼的出现为ALK融合基因突变型患者带来了曙光。临床研究证实,对于该类亚型NSCLC患者的预后,克唑替尼治疗客观缓解率达60%,无进展生存期达8~10个月,总生存期延长[15-17]。此外,ALK融合基因突变患者脑转移的发生概率大于基因未突变患者,PROFILE 1007临床研究发现,ALK阳性NSCLC患者在入组治疗时35%出现了脑转移[18],有部分研究探索了克唑替尼对NSCLC脑转移患者的获益。
本研究结果显示,观察组患者的总缓解率高于对照组,且治疗期间的生活质量评分高于对照组(P<0.05)。可见,从治疗短期疗效角度评定,克唑替尼对肿瘤细胞的增殖扩散无明显抑制或逆转作用,与传统的化疗药物比较,对患者的生存质量影响较小。此外,本研究中观察了两组患者治疗前后血清MMP-9的表达情况,试图分析克唑替尼能否影响肿瘤细胞的浸润及转移过程。MMPs是人体内降解细胞外基质的主要酶,在各亚型中MMP-9相对分子质量最大,作用最强,能够降解细胞外基质,使肿瘤细胞向远处播散,可作为判断临床肿瘤细胞转移的监测指标。MMP-9阳性率随肿瘤细胞分化程度的降低而升高,其表达水平可作为NSCLC独立的预后因素[19]。尽管ALK阳性NSCLC患者的获益明显,但有研究指出,接受克唑替尼治疗的患者1~2年内会出现对克唑替尼耐药,且中枢神经系统的复发进展较常见[20]。因此,后续研究应增加随访时间,观察克唑替尼治疗后患者中位生存期及耐药性等指标的变化。
综上所述,克唑替尼治疗NSCLC短期疗效良好,对患者的生存质量影响较小,可改善血清MMP-9的表达,利于延缓肿瘤细胞的侵袭、转移,值得进一步研究。
参考文献:
[1]丁万宝,张培先,石 岚,等.克唑替尼与化疗治疗ALK阳性晚期非小细胞肺癌的临床疗效对比分析[J].中国社区医师,2017,33(31):22.
[2]李国栋.克唑替尼辅助治疗ALK阳性非小细胞肺癌系统评价[J].医药导报,2016,35(z1):134 -136.
[3]朱礼阳,于忠和,许春伟.克唑替尼对比化疗在中晚期非小细胞肺癌患者中的疗效分析[J].临床肺科杂志,2016,21(12):2139 - 2141.
[4]刘自力,许 静,刘继柱,等.克唑替尼对比化疗治疗ALK阳性非小细胞肺癌的 Meta分析[J].国际呼吸杂志,2016,36(11):818 - 822.
[5]朱礼阳,于忠和.克唑替尼治疗肺癌的疗效及其耐药后的治疗[J].国际肿瘤学杂志,2016,43(7):532 - 534.
[6]崔海忠,曹德东,戈 伟.克唑替尼治疗ALK重排阳性非小细胞肺癌效果及安全性的Meta分析[J].中国医药导报,2016,13(17):77 - 81.
[7]朱礼阳,许春伟,于忠和.克唑替尼对ALK阳性非小细胞肺癌脑转移的疗效分析[J].临床与病理杂志,2016,36(9):1293-1296.
[8]毕国放,梁宇光,曲恒燕.克唑替尼在非小细胞肺癌治疗中耐药问题的研究状况[J].中国临床药理学杂志,2016,32(10):952 - 955.
[9]黄 伟,王 琳,秦叔逵,等.克唑替尼治疗ALK阳性非小细胞肺癌脑转移的疗效观察[J].中国癌症杂志,2015,25(6):467-471.
[10]陈少波,张厚德.克唑替尼抗肿瘤的研究进展[J].中国现代医生,2015,53(14):156 - 160.
[11]张 瑜,彭 枫.克唑替尼治疗晚期非小细胞肺癌研究进展[J].肿瘤防治研究,2017,44(11):774 -778.
[12]赵 静,张 坤,张力予,等.克唑替尼治疗ALK阳性晚期非小细胞肺癌患者的疗效观察[J].中国肺癌杂志,2015,18(10):616 - 620.
[13]姜媛利.克唑替尼治疗ALK阳性非小细胞肺癌脑转移的效果分析[J].河南医学研究,2017,25(10):1881 -1882.
[14]高峨嵋,赵 军,卓明磊,等.克唑替尼治疗晚期NSCLC患者单中心回顾性分析 [J].中国肺癌杂志,2016,19(3):161-168.
[15]Kwak EL,Bang YJ,Camidge DR,et al.Anaplastic lymphoma kinase inhibition in non-small-cell lung cancer[J].N Engl J Med,2010,363(18):1693 - 1703.
[16]Camidge DR, Bang YJ,Kwak EL,et al.Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer:updated results from a phase 1 study[J].Lancet Oncol,2012,13(10):1011 - 1019.
[17]Shaw AT,Kim DW,Nakagawa K,et al.Crizotinibversus chemotherapy in advanced ALK - positive lung cancer[J].N Engl J Med,2013,368(25):2385 - 2394.
[18]Blackhall F,Kim DW,Besse B,et al.Patient- reported outcomes and quality of life in PROFILE 1007:a randomized trial of crizotinib compared with chemotherapy in previously treated patients with ALK -positive advanced non-small-cell lung cancer[J].J Thorac Oncol,2014,9(11):1625 - 1633.
[19]吴 璇,李建雄.克唑替尼治疗EML4-ALK重排阳性患者的临床疗效[J].南方医科大学学报,2015,35(5):753 -757.
[20]韦亚娜.克唑替尼治疗非小细胞肺癌的研究进展[J].基层医学论坛,2017,21(7):873 - 874.

