我国中孕期产前筛查不同检测系统室内质量控制现状与行业标准的比较*
何法霖,王 薇,钟 堃,袁 帅,杜雨轩,王治国
(北京医院 国家老年医学中心 卫生部临床检验中心/北京市临床检验工程技术研究中心,北京 100730)
母血清产前筛查通过定量测定孕妇血清标记物,结合年龄、孕周、体重等信息,对胎儿21- 三体、18- 三体、开放性神经管缺陷等目标疾病进行风险评估。我国从20世纪末开始对胎儿唐氏综合征进行母血清学筛查,筛查指标主要为甲胎蛋白(α- fetoprotein,AFP)、游离人绒毛膜促性腺激素亚基(free β- human chorionic gonadotrophin,free β- hCG)、人绒毛膜促性腺激素亚基(β- human chorionic gonadotrophin,β- hCG)、人绒毛膜促性腺激素(human chorionic gonadotrophin,hCG)及去结合雌三醇(unconjugated oestriol,uE3)[1]。由于各地区、各实验室条件的差异,技术力量发展不均衡,以及所采用试剂、仪器、分析软件各不相同,筛查质量控制显得尤为重要。每个厂家对本厂家试剂性能都有相应要求,而卫生部颁布的行业标准《胎儿常见染色体异常与开放性神经管缺陷的产前筛查与诊断技术标准第1部分:中孕期母血清学产前筛查》(以下简称行业标准)对室内质量控制有具体的要求,批间不精密度小于5%[2]。本研究通过分析不同试剂厂家中孕期室内质量控制现状与行业标准的比较,希望能对产前筛查质量控制提供建议。
1 材料与方法
1.1研究对象卫生部临床检验中心收集2016年全国468家产前筛查实验室9月份的室内质量控制数据和各试剂厂家不精密度要求。室内质量控制数据包括:当月在控变异系数、累积在控变异系数。当月在控变异系数为9月所有在控测量值计算得到的变异系数,累积在控变异系数是指从检测同一批号质量控制样本开始至回报结果为止,计算得到的变异系数。
1.2研究方法
1.2.1统计所有9月份在控变异系数和累积在控变异系数满足行业标准(批间不精密度小于5%)结果。
1.2.2按实验室使用的试剂厂家分组,统计满足各试剂厂家不精密度要求(见表1)及行业标准结果。
2 结果

表1 各厂家说明书不精密度要求(%)
2.1AFP项目不精密度分析所有9月份在控变异系数和累积变异系数满足不同厂家标准和行业标准结果见图1,其中63.7%(298/468)实验室9月份在控变异系数满足行业标准要求,50.8%(238/468)实验室累积在控变异系数满足行业标准。按照不同检测系统分组,各检测系统9月份在控变异系数及累积变异系数满足相应厂家要求及行业标准的比例见表2。从表2可以看出,各检测系统满足厂家要求的比例分布在34.9%~100%,满足行业标准要求的比例分布在25.0%~78.0%。

图1 AFP项目9月份在控变异系数及累积在控变异系数满足不同厂家要求及行业标准结果
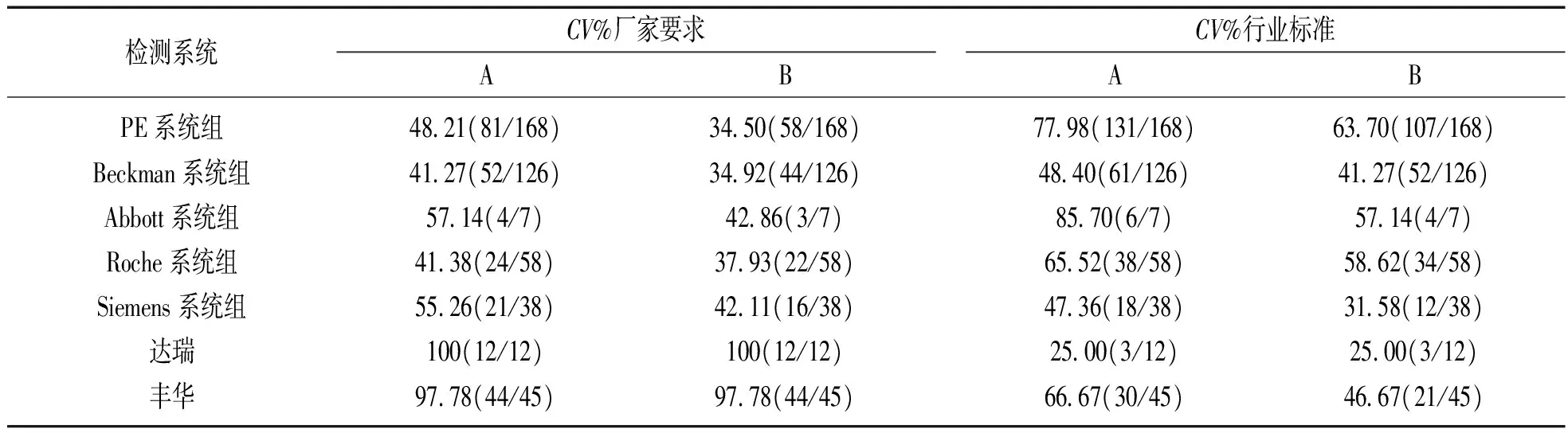
表2 AFP项目不同系统组满足厂家及行业标准的比例
注:A是9月份在控变异系数,B是累积在控变异系数。
2.2总HCG项目不精密度分析9月份在控室内质控数据按照厂家标准和行业标准统计室内质控的结果见图2。30.6%(15/49)实验室9月份在控变异系数满足行业标准的要求,24.5%(12/49)实验室累积在控变异系数满足行业标准的要求。81.6%(40/49)实验室9月份在控变异系数实验室满足Siemens要求,59.2%(29/49)实验室9月份在控变异系数实验室满足Siemens要求。
2.3freeβ- hCG项目不精密度分析9月份在控室内质控数据按照不同厂家标准和行业标准统计的室内质控结果见图3,其中59.4%(158/266)9月份在控变异系数满足行业标准要求,46.2%(123/266)累积在控变异系数满足行业标准要求。按照不同检测系统分组,各检测系统9月份在控变异系数及累积变异系数满足相应厂家要求及行业标准的比例见表3。从表3可以看出,各检测系统满足厂家要求的比例分布在38.9%~100%,满足行业标准要求的比例分布在27.3%~63.0%。

图2 总HCG项目9月份在控变异系数及累积在控变异系数满足不同厂家要求及行业标准结果
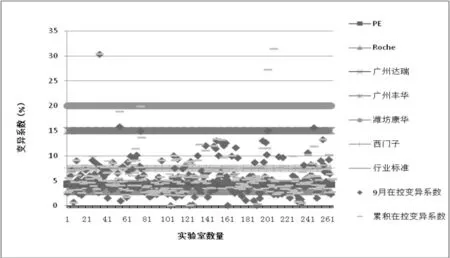
图3 freeβ- hCG项目9月份在控变异系数及累积在控变异系数满足不同厂家要求及行业标准结果
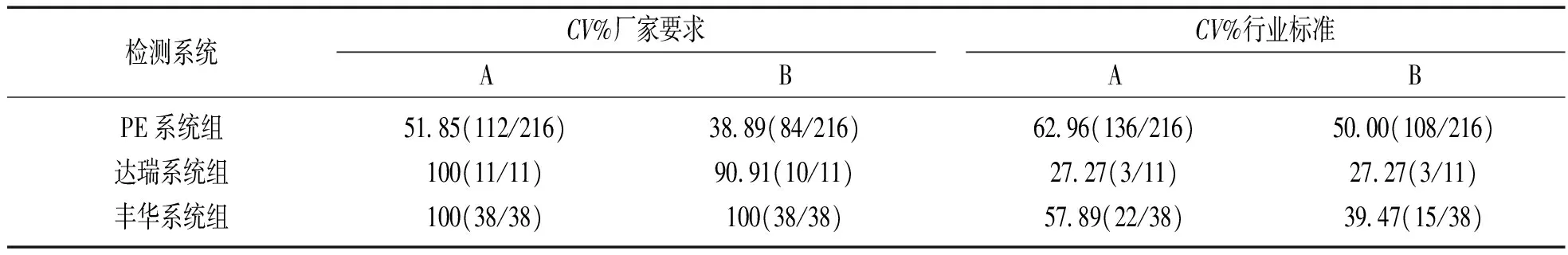
表3 freeβ- hCG项目不同系统组满足厂家及行业标准的比例
注:A是9月份在控变异系数,B是累积在控变异系数。
2.4β- hCG项目不精密度分析9月份在控室内质控数据按照不同厂家标准和行业标准统计室内质控的结果见图4,其中43.9%(69/157)9月份在控变异系数满足行业标准要求,31.8%(50/157)累积在控变异系数满足行业标准要求。按照不同检测系统分组,各检测系统9月份在控变异系数及累积变异系数满足相应厂家要求及行业标准的比例见表4。从表4可以看出,各检测系统满足厂家要求的比例分布在14.3%~68.8%,满足行业标准要求的比例分布在14.3%~61.3%。

图4 β- hCG项目9月份在控变异系数及累积在控变异系数满足不同厂家要求及行业标准结果
注:A是9月份在控变异系数,B是累积在控变异系数。
2.5UE3项目不精密度分析9月份在控室内质控数据按照不同厂家标准和行业标准统计室内质控的结果见图5,其中39.0%(128/328)9月份在控变异系数满足行业标准要求,27.7%(91/328)累积在控变异系数满足行业标准要求。按照不同检测系统分组,各检测系统9月份在控变异系数及累积变异系数满足相应厂家要求及行业标准的比例见表5。从表5可以看出,各检测系统满足厂家要求的比例分布在19.7%~100%,满足行业标准要求的比例分布在11.1%~54.8%。

表5 UE3项目不同系统组满足厂家及行业标准的比例
注:A是9月份在控变异系数,B是累积在控变异系数。
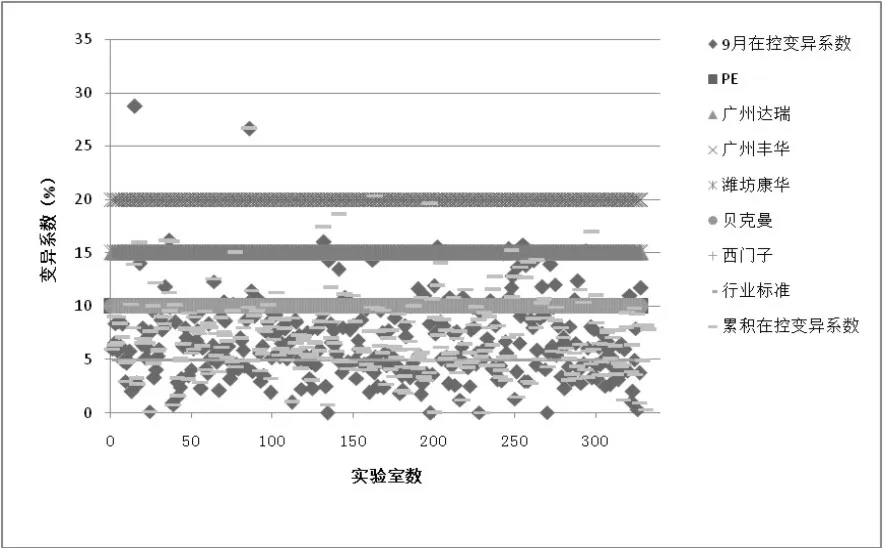
图5 UE3项目9月份在控变异系数及累积在控变异系数满足不同厂家要求及行业标准结果
3 讨论
参与本次研究的468家实验室涉及全国31个省,包含三级医院、二级综合及专科医院,覆盖目前实验室使用的主流筛查厂家,能反映我国目前实验室不同厂家检测系统室内质量控制现状及存在的问题:①产前筛查检测系统多样,且不同厂家检测系统性能要求不一。罗氏系统、雅培系统厂家不精密度要求比行业标准严格,珀金埃尔默系统UE3不精密度要求较行业标准宽松,贝克曼系统β- hCG项目不精密度要求较行业标准宽松,而西门子系统、广州丰华系统和广州达瑞系统厂家不精密度要求都低于行业标准。②不是所有实验室9月份在控变异系数及累积在控变异系数都能满足本检测系统性能要求,尤其是厂家性能要求高于行业标准的检测系统,比如PE检测系统,AFP项目累积在控变异系数满足厂家要求仅34.5%。③不同检测项目满足行业标准的比例不一样,且各厂家检测系统都存在不能满足行业标准的实验室。AFP项目较好,63.7%(298/468)实验室9月份在控变异系数满足行业标准要求,50.8%(238/468)实验室累积在控变异系数满足行业标准,而各检测系统满足行业标准要求比例分布在25.0%~78.0%,其中所占比例最高的为PE系统。UE3项目最差,39.0%(128/328)9月份在控变异系数满足行业标准要求,27.7%(91/328)累积在控变异系数满足行业标准要求,而各检测系统满足行业标准要求的比例分布在11.1%~54.8%,其中所占比例最高的为PE系统。
血清学筛查不以标志物测定值为最终结果,而是以风险的方式出具检验报告,而室内质量控制的好坏直接影响到患者风险值[3,4]。有研究表明,血清标志物浓度的检测误差达到7%,则风险计算结果误差将达到17%,因此对检测试剂性能提出了更高的要求,实验室在购买产前筛查检测试剂时,不仅需要选择购买具有国家药监局批准的试剂,需要验证试剂供应商提供的变异系数,并且能满足行业标准的要求,此外更换新批次试剂时,也应采用一定样本量(20~50份)对新旧试剂进行评估和验证[4,5]。关于如何验证厂家性能声明的方法可参考王治国教授的相关专著,书中描述了3种方案:第一种是精密度基于5天,每天分析3份重复质控样本;第二种是真实度基于分析20份患者标本;第三种是真实度基于分析至少2份具有指定值的参考物质[6]。本研究结果表明不论厂家声明的不精密度是高于行业标准还是低于行业标准,室内质量控制结果存在不满足行业标准的实验室,因此产前筛查实验室不仅需要评估和验证检测系统还需要重视室内质量控制,对于室内质控不能满足行业标准要求的实验室需要分析原因、撰写报告并进行整改。
参考文献:
[1]吕时铭.选择适合我国现状的唐氏综合征产前筛查和诊断模式[J].诊断学理论与实践,2010,9(5):413- 417.
[2]WS322.1- 2010.胎儿常见染色体异常与开发性神经管缺陷的产前筛查与诊断技术标准第1部分:中孕期母血清学产前筛查[S].北京:中国标准出版社,2010.
Ministry of Health People’s Republic of China.W S322.1- 2010.Technical standards of prenatal screening and diagnosis for fetal common chromosomal abnormalities and open neural tube defects Part1.Maternal serum prenatal screening in second trimester[S].Beijing:Standards Press of China,2010.
[3]边旭明,蒋宇林.重视唐氏综合征产前筛查的质量控制和评估[J].实用妇产科杂志,2014,30(2):81- 83.
Bian XM,Jiang YL.Quality control and evaluation of the prenatal screening of Down’s syndrome[J].Journal of Practical Obstetric and Gynecology,2014,30(2):81- 83.
[4]姜萍,张风琴,苍金荣.唐氏综合征和神经管畸形筛查实验的临床应用[J].现代检验医学杂志,2007,22(5):106- 108.
Jiang P,Zhang FQ,Cang JR.The clinical application of Down’s syndrome and neural tube defects screening experiment[J].J Mod Lab Med,2007,22(5):106- 108.
[5]朱宝生,朱姝.唐氏综合征血清学产前筛查室内质控的目标与方法[J].实用妇产科杂志,2014,30(2):89- 93.
Zhu BS,Zhu S.The goal and method of screening indoor quality control of the blood qingxue prenatal screening of down syndrome[J].Journal of Practical Obstetrics and Gynecology,2014,30(2):89- 93.
[6]刘珊玲,王和.唐氏综合征产前筛查实验室质量控制[J].中华检验医学杂志,2011,34(7):665- 668.
Liu SL,Wang H.Laboratory quality control for Do- wn’s syndrome[J].Clin J Lab Med,2011,34(7):665- 668.
[7]王治国.临床检验方法确认与性能验证[M].北京:人民卫生出版社,2014.
Wang ZG.Clinical test method validation and performance verification[M].Beijing:People’s Health Press,2014.

