二尖瓣及主动脉瓣置换术后患者超声心动图变化特征
洪云 吴庆 胡璇 周静
二尖瓣和主动脉瓣是心脏瓣膜病最常累及的瓣膜,炎症、缺血性坏死、退行性改变等原因导致的心脏瓣膜及其附属结构增厚、粘连、纤维化、缩短等病理改变,是导致单个或多个瓣膜狭窄和(或)关闭不全的主要原因[1]。人工心脏瓣膜置换术在改善患者血流动力学紊乱、缓解临床症状、提高生活质量方面发挥的积极作用已得到广泛认可[2]。然而,过往临床对于二尖瓣及主动脉瓣置换术的观察指标多集中于术后死亡率、远期存活率等,鲜有学者对患者近远期随访时超声心动图改变进行报道[3-4]。本研究总结术后远期超声心动图变化特征。
1 资料与方法
1.1 患者资料
对2011年1月至2013年5月行二尖瓣及主动脉瓣双瓣膜置换,随访期间超声心动图检查资料保存完整的患者进行回顾性分析,患者术后随访≥3年且已排除合并其他心脏畸形及再手术者。共103例患者符合,男30例,女73例,年龄16~72岁,平均(48.19±12.08)岁,患者均接受双瓣膜置换术,选择合适尺寸的机械瓣膜[5],植入二尖瓣及主动脉瓣[6]。
1.2 观察指标
分别于术前、术后6个月、术后3年,使用Philips iE33超声心动图仪(探头频率1~5 MHz)采集患者左房内径(LA)、左室内径(LV)、右房内径(RA)、右室内径(RV)、左室射血分数(LVEF),以及二尖瓣有效瓣口面积(EOA)、主动脉瓣EOA。此外,按照患者人工心脏瓣膜-患者不匹配(PPM)程度,将其分别纳入无或轻度组、中度组、重度组,比较各亚组患者术前、术后6个月、术后3年LVEF、平均主动脉瓣跨瓣压差(MPG)及主动脉瓣前向血流速度(Vjet)的差异,总结PPM对患者预后的影响。PPM判断标准[7]:二尖瓣:无或轻度:EOA/BSA>1.2 cm2/m2;中度:0.9 cm2/m2<EOA/BSA≤1.2 cm2/m2;重度:EOA/BSA≤0.9 cm2/m2;主动脉瓣:无或轻度:EOA/BSA>0.85 cm2/m2;中度:0.65 cm2/m2<EOA/BSA≤0.85 cm2/m2;重度:EOA/BSA≤0.65 cm2/m2。以二尖瓣及主动脉瓣PPM程度较重者进行分组,即若患者二尖瓣为轻度PPM、主动脉瓣为中度PPM,则将其纳入中度组。
2 结果
2.1 患者手术前后超声心动图指标变化
与术前比较,患者术后6个月LA、LV、LVEF、二尖瓣EOA及主动脉瓣EOA均升高,差异有统计学意义(P<0.05);与术前及术后6个月相比,患者术后3年LA、LV均降低,RV、LVEF均升高,差异有统计学意义(P<0.05);与术后6个月相比,患者术后3年二尖瓣EOA、主动脉瓣EOA有所降低,差异有统计学意义(P<0.05)。见表1。
表1 103例患者手术前后超声心动图各指标变化比较(±s)
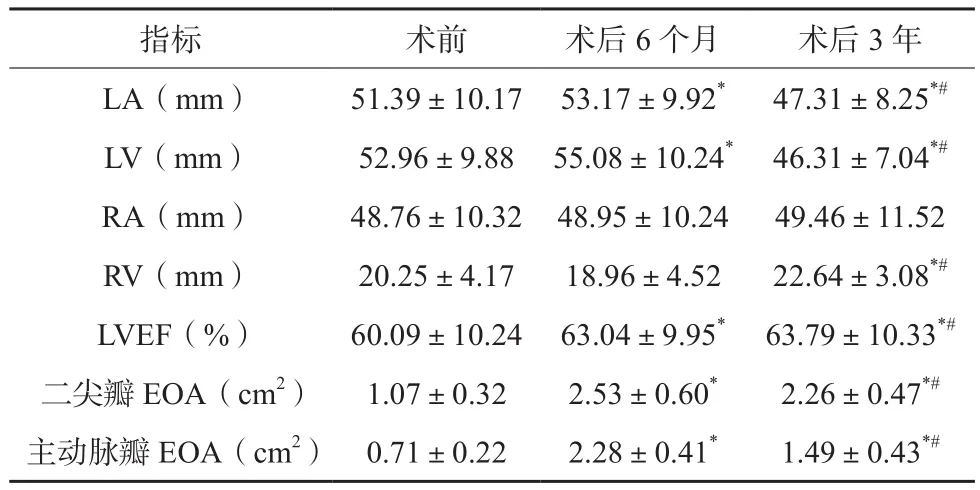
表1 103例患者手术前后超声心动图各指标变化比较(±s)
注:与术前比较,*P<0.05;与术后6个月比较,#P<0.05
指标 术前 术后6个月 术后3年LA(mm) 51.39±10.17 53.17±9.92* 47.31±8.25*#LV(mm) 52.96±9.88 55.08±10.24* 46.31±7.04*#RA(mm) 48.76±10.32 48.95±10.24 49.46±11.52 RV(mm) 20.25±4.17 18.96±4.52 22.64±3.08*#LVEF(%) 60.09±10.24 63.04±9.95* 63.79±10.33*#二尖瓣 EOA(cm2) 1.07±0.32 2.53±0.60* 2.26±0.47*#主动脉瓣EOA(cm2) 0.71±0.22 2.28±0.41* 1.49±0.43*#
2.2 不同PPM程度患者超声心动图各指标变化
患者二尖瓣、主动脉瓣PPM程度为无或轻度组56例,中度组25例,重度组22例。无或轻度组、重度组术后6个月Vjet低于中度组,差异有统计学意义(P<0.05),各组患者同时点其他指标比较,差异无统计学意义(P>0.05),见表2。
表2 不同PPM程度患者手术前后超声心动图各指标变化比较(±s)
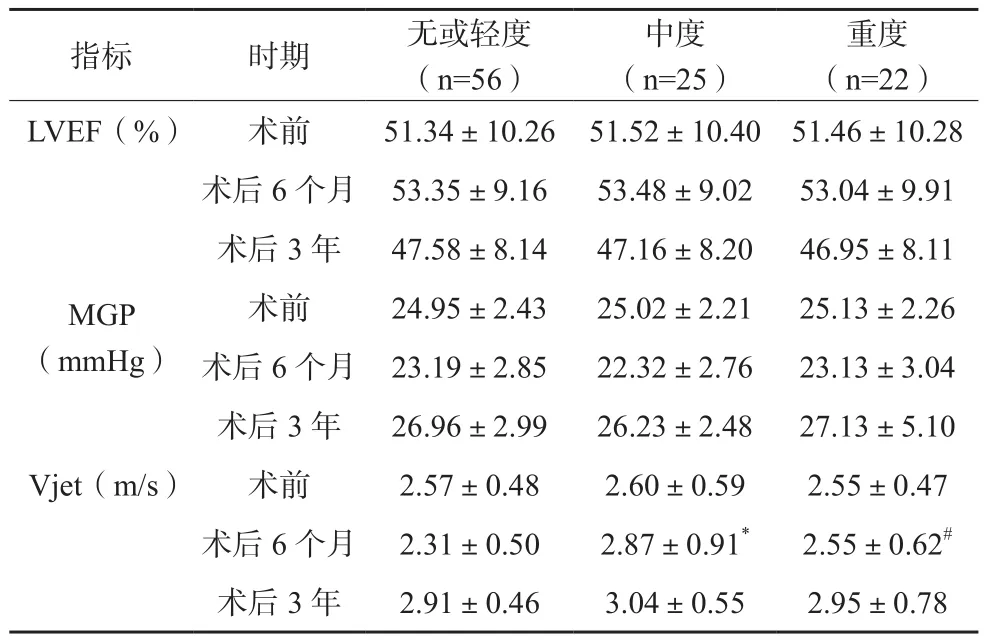
表2 不同PPM程度患者手术前后超声心动图各指标变化比较(±s)
注:与无或轻度组比较,*P<0.05;与中度组比较,#P<0.05
重度(n=22)LVEF(%) 术前 51.34±10.26 51.52±10.40 51.46±10.28术后6个月 53.35±9.16 53.48±9.02 53.04±9.91术后3年 47.58±8.14 47.16±8.20 46.95±8.11 MGP(mmHg)指标 时期 无或轻度(n=56)中度(n=25)术前 24.95±2.43 25.02±2.21 25.13±2.26术后6个月 23.19±2.85 22.32±2.76 23.13±3.04术后3年 26.96±2.99 26.23±2.48 27.13±5.10 Vjet(m/s) 术前 2.57±0.48 2.60±0.59 2.55±0.47术后6个月 2.31±0.50 2.87±0.91* 2.55±0.62#术后3年 2.91±0.46 3.04±0.55 2.95±0.78
3 讨论
心脏瓣膜病累及二尖瓣和主动脉瓣时,患者二尖瓣叶可见明显增厚、钙化、交界融合,并伴有瓣下结构改变,同时,主动脉瓣也存在纤维化增厚改变,上述病理改变可导致心室舒张期血液由主动脉瓣反流至左心室,此时左心室不仅接受正常来自左心房的血液,还接受来自主动脉反流的血液,是造成左室负荷上升、舒张末期张力增加的主要原因[8-9]。随着瓣膜病变的加剧,患者左心室可逐渐发生代偿性肥厚、扩大,进而发生心肌间质纤维化、心肌相对性缺血,甚至左室功能减退、失代偿,并以较高的跨瓣血流速度、较大的跨瓣压差、非理想的有效瓣口面积为主要表现[10-12]。
瓣膜置换术是解决二尖瓣、主动脉瓣病变的首选方式,人工瓣膜支架的存在和缝合环对血流的阻挡、局部湍流的发生,均使得左心房、左心室血流动力学无法完全达到正常标准[13-14]。在本次研究中,患者术后3年LA、LV均较术前降低,RV、LVEF、二尖瓣EOA及主动脉瓣EOA均升高,显现出二尖瓣及主动脉瓣置换术在降低跨瓣流速、跨瓣压差,增加有效瓣口面积、缩小心腔方面的积极作用[15],然而,需要注意的是,患者术后3年超声心动图各项指标均未达到正常标准,说明手术效果仍存在一定提升空间。在术后6个月超声心动图的观察中,可以发现,患者术后6个月LA、LV、LVEF、二尖瓣EOA及主动脉瓣EOA均较术前升高,表明患者左室重构主要发生在术后6个月内,与过往研究一致[16],因此,重视术后6个月内药物治疗及康复干预,有望进一步促进左室重构、缓解临床症状。
由于瓣膜的增厚、钙化、纤维化等因素导致的二尖瓣及主动脉瓣环境减小,均可导致瓣膜的尺寸受到限制,加之缝合环的存在,植入瓣膜的有效面积必然无法超过正常瓣口面积,因此,患者术后PPM现象广泛存在[17]。本研究103例患者中,二尖瓣中、重度PPM发生率为33.00%,主动脉瓣中、重度PPM发生率为45.63%,说明主动脉瓣较二尖瓣更易发生PPM。有学者指出,主动脉瓣部位PPM可妨碍患者术后左室肥厚的逆转,在增加远期心血管并发症发生率的同时,往往进一步影响其心功能改善程度,从而使患者近远期生存率显著降低[18]。此外,本研究结果还显示,中度PPM者,其术后6个月Vjet较高,而较高的血流速度可导致主动脉壁正常结构损害,甚至形成主动脉瘤,因此,在强调术后长期血压、心率控制的同时,还应重视主动脉部位PPM的预防,如扩大主动脉瓣瓣环、选择血流动力学参数更佳的人工瓣膜等,从而尽可能保证手术效果与患者近远期预后质量。
[1] PERLMAN G Y, CHEUNG A, DUMONT E, et al. Transcatheter aortic valve replacement with the Portico valve: one-year results of the early Canadian experience[J]. EuroIntervention, 2017,12(13): 1653-1659.
[2] THOURANI V H, KODALI S, MAKKAR R R, et al.Transcatheter aortic valve replacement versus surgical valve replacement in intermediate-risk patients: a propensity score analysis[J]. Lancet, 2016, 387(10034): 2218-2225.
[3] SCOTT W C, MILLER D C, HAVERICH A, et al. Operative risk of mitral valve replacement: discriminant analysis of 1329 procedures.[J]. Circulation, 1985, 72(2):108-19.
[4] WILLIAMS P D, DE BELDER M A, MAREDIA N, et al.Embolization of Left Atrial Appendage Thrombus During Transcatheter Aortic Valve Replacement: A Potential Mechanism of Periprocedural Stroke[J]. JACC Cardiovasc Interv, 2015, 8(13): 1770-1771.
[5] KODALI S, THOURANI V H, WHITE J, et al. Early clinical and echocardiographic outcomes after SAPIEN 3 transcatheter aortic valve replacement in inoperable, high-risk and intermediate-risk patients with aortic stenosis[J]. Eur Heart J,2016, 37(28): 2252-2262.
[6] PALMER S, CHILD N, DE BELDER M A, et al. Left atrial appendage thrombus in transcatheter aortic valve replacement:incidence, clinical impact, and the role of cardiac computed tomography[J]. JACC Cardiovasc Interv, 2017, 10(2): 176-184.
[7] 李慧, 段福建, 王剑鹏, 等. 心外膜超声心动图在心脏外科手术中的应用研究[J]. 中国超声医学杂志, 2016, 32(6): 554-556.
[8] REARDON M J, ADAMS D H, KLEIMAN N S, et al. 2-year outcomes in patients undergoing surgical or self-expanding transcatheter aortic valve replacement[J]. J Am Coll Cardiol,2015, 66(2): 113-121.
[9] 邓云丹, 李永波, 钱永军, 等. 二尖瓣置换术患者同期行三尖瓣成形术后两年超声心动图评价的随机对照试验[J]. 中国胸心血管外科临床杂志, 2016, 23(7): 658-665.
[10] DOUGLAS P S, HAHN R T, PIBAROT P, et al. Hemodynamic outcomes of transcatheter aortic valve replacement and medical management in severe, inoperable aortic stenosis: a longitudinal echocardiographic study of cohort B of the PARTNER trial[J]. J Am Soc Echocardiogr, 2015, 28(2): 210-217.
[11] TRUNFIO G, KONSTADT S, RIBAKOVE G, et al. The Sudden Appearance of a Mobile Mass in the Ascending Aorta on Transesophageal Echocardiography After Transcatheter Aortic Valve Replacement[J]. Anesth Analg, 2015, 121(6): 1460-1463.
[12] DEL TRIGO M, MUÑOZ-GARCIA A J, WIJEYSUNDERA H C, et al. Incidence, timing, and predictors of valve hemodynamic deterioration after transcatheter aortic valve replacement:multicenter registry[J]. J Am Coll Cardiol, 2016, 67(6): 644-655.
[13] 马金本. 碳纳米管与瓣膜基质体外共建人工瓣膜支架及对内皮细胞形态和功能的影响[D]. 上海:上海交通大学, 2009.
[14] FENG W, COADY M. Epicardial Tachosil Patch Repair of Ventricular Rupture in a 90-Year-Old After Mitral Valve Replacement[J]. Ann Thorac Surg, 2016, 101(6): 2361-2363.
[15] THYREGOD H G H, STEINBRÜCHEL D A, IHLEMANN N,et al. Transcatheter versus surgical aortic valve replacement in patients with severe aortic valve stenosis: 1-year results from the all-comers NOTION randomized clinical trial[J]. J Am Coll Cardiol, 2015, 65(20): 2184-2194.
[16] LEON M B, SMITH C R, MACK M J, et al. Transcatheter or surgical aortic-valve replacement in intermediate-risk patients[J]. N Engl J Med, 2016, 2016(374): 1609-1620.
[17] CREMER P C, RODRIGUEZ L L, GRIFFIN B P, et al.Early Bioprosthetic Valve Failure: Mechanistic Insights via Correlation between Echocardiographic and Operative Findings[J]. J Am Soc Echocardiogr, 2015, 28(10): 1131-1148.
[18] DE MARCHENA E, MESA J, POMENTI S, et al. Thrombus formation following transcatheter aortic valve replacement[J].JACC Cardiovasc Interv, 2015, 8(5): 728-739.

