复方盐酸吡格列酮格列美脲片与格列美脲片治疗2型糖尿病的疗效与安全性对照研究*
蒲丹岚,尹经霞,谢 洁,杨刚毅,廖 涌△
(1.重庆市巴南区人民医院内分泌科 401320;2.武警重庆总队医院内分泌科,重庆 400061; 3.重庆医科大学附属第二医院内分泌科 400010)
糖尿病作为一种慢性非感染性疾病,患病人数以惊人的速度急剧上升,对人类健康造成了极大的危害,被公认为是仅次于心脑血管病和恶性肿瘤的第三大死因,越来越受到人们重视。在糖尿病患者中,2型糖尿病(T2DM)发病率占95%以上,它是以胰岛素分泌受损和胰岛素抵抗为特征的异质性疾病[1]。若糖尿病的治疗管理不及时,其引发心脑血管疾病,甚至失明、截肢等并发症,严重影响患者的生活质量和预期寿命[2]。口服降糖药是控制血糖的有效方法,也是基础治疗,在T2DM的治疗过程中占有非常重要的地位[3]。近年来随着新技术、新方法的不断涌现,口服降糖药的品种、剂型日益增多。复方盐酸吡格列酮格列美脲片是盐酸吡格列酮(ACTOS)和格列美脲的复方制剂,该药将这两种临床广泛使用且能够相互补充的药物结合在了一起,具有相辅相成的效果。ACTOS的治疗靶点是胰岛素抵抗,而格列美脲主要是促进胰岛素的分泌。同时ACTOS和格列美脲都是广泛用于治疗糖尿病的药物,二者安全性均较好。药物实验研究显示,这两种药物结合在一起与单组分用药在药代学、药效学参数方面具有生物等效性[4],可用于T2DM患者的血糖控制治疗。对于血糖控制欠佳的糖尿病患者临床处方经常是多种药物联合使用,这不仅增加了患者的经济负担,也影响患者的服药依从性,所以将两种药物制成复方制剂可以使患者更为方便的服用,达到联合用药的效果。本研究对复方盐酸吡格列酮格列美脲片与单用格列美脲片治疗T2DM的疗效进行对比,以评价复方盐酸吡格列酮格列美脲片治疗T2DM的有效性及安全性。
1 资料与方法
1.1一般资料 搜集2013年9月至2014年5月就诊于重庆市巴南区人民医院及武警重庆总队医院门诊或住院的T2DM患者33例纳入本研究。本研究遵循赫尔辛基宣言及药物临床试验质量管理规范(GCP)指导原则,得到重庆市巴南区人民医院及武警重庆总队医院临床药物试验伦理委员会批准。所有研究对象纳入前均经充分知情,自愿参加本临床研究,并签署了书面知情同意书。入选标准:(1)符合1999年世界卫生组织(WHO)糖尿病诊断标准[空腹血糖(FPG)≥7.0 mmol/L,负荷后2 h血糖(2 hPPG)≥11.1 mmol/L]确诊为T2DM;能够理解试验全过程并自愿参加本研究,签署知情同意书;年龄30~75岁,性别不限;(2)20 kg/m2≤BMI≤45 kg/m2;(3)血糖控制欠佳(6.5%≤HbA1c≤8.5%);(4)单用或联合服用稳定剂量格列美脲片4 mg已超过30 d的患者(治疗剂量稳定 3 个月以上);联合用药者包括使用二甲双胍、α-葡萄糖苷酶抑制剂,但除外噻唑烷二酮(TZD)类、二肽基肽酶Ⅳ(DPP-Ⅳ)抑制剂、胰岛素和胰高血糖素样肽Ⅰ(GLP-Ⅰ)受体激动剂或类似物;(5)能够且愿意使用便携式血糖仪检测空腹血糖、餐后血糖者。排除标准:(1)1型糖尿病患者;(2)对格列美脲或吡格列酮过敏者;过去12个月内接受过TZD治疗的患者;使用胰岛素或其他胰岛素增敏剂的患者;(3)近3个月有严重低血糖病史者;(4)近6个月有糖尿病急性并发症者(糖尿病酮症酸中毒、高血糖高渗状态等);(5)血肌酐异常(大于18 mg/L),肾小球率过滤<40 mL·min-1·1.73 m-2的患者;(6)肝脏功能损害(ALT 或 AST大于或等于正常值上限的 3 倍以上)的患者;(7)妊娠或哺乳期女性;(8)有药物滥用或酗酒者;(9)恶性肿瘤患者,重要脏器严重疾病者;(10)已参加其他临床试验(临床注册号11001331),依从性差,不能按要求完成试验者。
1.2研究方法 本研究为前瞻性随机、双盲、双模拟阳性药平行对照临床试验,总治疗周期14周(2周导入期,12周稳定治疗期)。符合入选标准的患者给予个体化的饮食及运动管理2周,在2周的饮食指导期内所有入选者给予4 mg格列美脲联合安慰剂洗脱治疗,并停用其他联合应用的口服降糖药物。治疗中连续出现2次FPG 13.5 mmol/L的患者,判定为严重高血糖,予以退组处理。洗脱治疗结束时进行基线值测定,对仍符合入选标准(6.5%≤HbA1c≤8.5%)的受试者按照2∶1的比例进行分组(试验组22例,对照组11例)。试验组服用30 mg/4 mg复方盐酸吡格列酮格列美脲片(海南国瑞堂制药有限公司研制)和2 mg×2格列美脲模拟片(海南国瑞堂制药有限公司提供),对照组服用2 mg×2格列美脲片(赛诺菲生产)和30 mg/4 mg复方盐酸吡格列酮格列美脲模拟片(海南国瑞堂制药有限公司提供),进入12周的稳定治疗期。
为了消除减肥的影响,试验期间受试者需坚持个性化的体质量维持饮食。如果受试者服用稳定剂量的降脂药物超过60 d,试验期间可以继续服药,且剂量不能改变。
所有受试者在试验期间禁用其他降糖药物(胰岛素、胰岛素类似物和其他口服降糖药)、影响糖代谢的药物,如糖皮质激素、化疗药物、甲状腺素、雌激素等及CYP2C9诱导剂、CYP2C9抑制剂、利福平、氟康唑等及其他研究者认为影响疗效评判的药物。
1.3资料收集与评价
1.3.1数据收集 由专人负责测量身高、体质量、腰围、臀围、血压等人体学指标,方法固定、统一。其中,体质量指数(BMI)=体质量(kg)/身高(m2),腰臀比(WHR)= 腰围/臀围,胰岛素抵抗指数(HOMA-IR)=空腹血糖(FPG)×空腹胰岛素(FINS)/22.5。血浆葡萄糖测定采用生化类葡萄糖氧化酶法(日立全自动生化分析仪7020);血浆胰岛素(FINS)测定采用电化学发光法(罗氏Cobas601);HbA1C测定采用高压液相法(BIO-RADD-10);血脂测定采用酶法(日立RL7600)。
1.3.2疗效评价指标 主要疗效指标:治疗前后HbA1c变化值,治疗后HbA1c自基线值下降的绝对值。次要疗效指标包括:治疗前后FPG、FINS以及胰岛素抵抗指标的变化情况;治疗后两组HbA1c≤7.0%和HbA1c≤6.5%的百分比;BMI、收缩压(SBP)、舒张压(DBP)、体脂百分比(FAT)、总胆固醇(TC)、低密度脂蛋白C(LDL-C)治疗前后变化。
1.3.3安全性评价指标 两组患者治疗前后BMI、腰臀比、体脂率、血压、血脂等变化情况;低血糖不良事件的发生率。

2 结 果
2.1研究整体完成情况 本研究共纳入组随机化患者33例,年龄47~75岁,中位年龄63岁,男17例,女16例;脱落2例(依从性差),最终31例完成研究(试验组完成21例,对照组完成10例)。
2.2治疗效果评价
2.2.1两组患者基线资料比较 两组患者治疗前的性别、年龄、BMI、FAT、WHR、SBP、DBP、HbA1c、FPG、FINS、HOMA-IR、胰岛β细胞分泌指数(HOMA-β)等指标差异无统计学意义(P>0.05),两组患者具有可比性,见表1。
2.2.2两组治疗前后主要疗效评价指标比较 (1)各项指标比较:经12周的治疗,试验组治疗前后HbA1c上升幅度为(0.99±1.87)%,差异有统计学意义(P<0.05);对照组HbA1c下降幅度为(-0.02±0.90)%,差异有统计学意义(P<0.05)。试验组FPG下降幅度为(0.94±1.87)mmol/L,差异有统计学意义(P<0.05);对照组FPG下降幅度为(0.37±2.62)mmol/L,差异无统计学意义(P>0.05)。试验组治疗前后FINS、HOMA-IR下降差异有统计学意义,对照组FINS、 HOMA-IR变化差异无统计学意义(P>0.05)(表2)。(2)治疗后HbA1c<7.0%达标率比较:试验组HbA1c<7.0%达标16例(76.2%),对照组HbA1c<7.0%达标3例(30.0%);通过Fisher精确概率法检验比较,两组HbA1c<7.0%达标率差异有统计学意义(P=0.017)。(3)治疗后HbA1c≤6.5%达标率比较:试验组HbA1c≤6.5% 6例(28.57%),对照组HbA1c≤6.5% 1例(10%);通过Fisher精确概率法检验比较,两组HbA1c≤6.5%达标率差异无统计学意义(P=0.206)。
2.2.3两组治疗前后次要评价指标比较 试验组经复方吡格列酮格列美脲治疗12周后WHR、三酰甘油(TG)较治疗前降低,而高密度脂蛋白C(HDL-C)较治疗前升高,差异有统计学意义(P<0.05);试验组BMI、SBP、DBP、FAT、TC、LDL-C治疗后差异无统计学意义(P>0.05)。对照组治疗12周后LDL-C、HDL-C、TC较治疗前升高,WHR较治疗前下降,差异有统计学意义,BMI、SBP、DBP、FAT、TG治疗后差异均无统计学意义(表3)。
2.3安全性评价
2.3.1两组治疗后各安全性指标变化情况 两组患者治疗后的BMI、FAT、WHR、SBP、DBP差异均无统计学意义(P>0.05),见表4。
2.3.2两组治疗前后不良事件发生情况 试验组共有6例不良反应:1例(4.8%)上呼吸道感染(可能与研究药物无关,自行缓解),5例(23.8%)轻度低血糖(进食后缓解)。对照组有3例不良反应:3例(30.0%)轻度低血糖(进食后缓解)。通过Fisher精确概率法检验比较发现两组低血糖发生率,差异无统计学意义(P=0.310)。试验组及对照组均无夜间低血糖和严重低血糖事件(<2.8 mmol/L),两组均无严重不良事件发生。
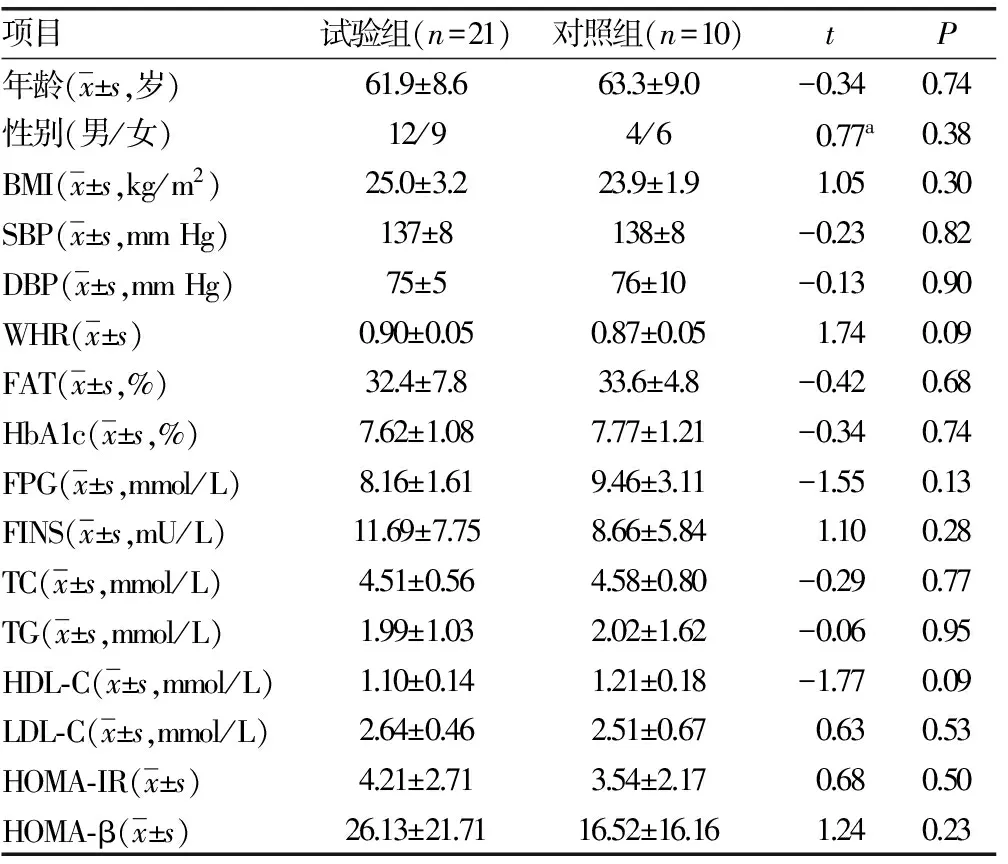
表1 试验组和对照组治疗前各项指标比较
a:Fisher精确检验F值
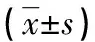
表2 两组治疗前后FPG、HbA1c及胰岛素抵抗指标变化情况
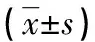
表3 两组治疗前后次要评价指标比较
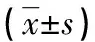
表4 两组治疗后人体学指标比较
3 讨 论
吡格列酮具有提高肌肉和脂肪组织对胰岛素的敏感性,抑制肝脏葡萄糖异生作用,在减少胰岛素分泌的同时改善对血糖的控制[5-6]。格列美脲为新一代磺酰脲类降糖药物,起效迅速、作用半衰期长,每天只需服药1次,能提高患者用药的依从性[7];临床前试验和国外上市后的临床研究显示,格列美脲有明显的胰内和胰外双重降血糖作用,主要是通过与65×103受体蛋白结合,作用于三磷酸腺苷(ATP)敏感型钾通道,引起钾通道闭合、钙通道开放,刺激胰岛β细胞分泌胰岛素,同时通过胰外作用,增加周围组织对胰岛素的敏感性以达到降糖的目的[8-9]。这两个药物作用机制相结合有助于控制T2DM患者的空腹和餐后血糖,又避免了降糖药物导致低血糖反应的发生,对患者BMI、血压、心率等无不良影响,不增加心血管事件的发生,对肝肾功能无损害。应用TZD降糖药联合磺脲类降糖药物治疗T2DM增强疗效,改善胰岛素抵抗,加强机体细胞对葡萄糖的摄取利用,有效控制血糖。动物实验还发现,经吡格列酮治疗能有效降低血脂,同时通过调节纤溶酶原激活物抑制剂-1(PAI-1)、C反应蛋白(CRP)等炎症因子进一步改善胰岛素抵抗,稳定血管内皮功能,延缓β细胞功能衰退等[10]。
本研究在血糖控制不佳的T2DM应用复方吡格列酮格列美脲进行治疗,结果显示降糖疗效显著。单用4 mg格列美脲血糖下降不明显时,应用复方吡格列酮格列美脲(30 mg/4 mg)的患者FPG、HbA1c较基线水平仍有所下降。本研究同时也显示,在治疗12周后 FINS下降,HOMA-IR得到改善。此外,本研究还发现经复方吡格列酮格列美脲片治疗后,WHR、TG较治疗前降低,而HDL-C较治疗前升高,提示复方吡格列酮格列美脲片在改善血脂及代谢综合征方面可能具有重要作用。但本研究样本量偏小,其在改善血脂及代谢综合征方面的作用还有待于进一步论证。
低血糖是格列美脲和吡格列酮治疗过程中常见的不良反应之一,严重低血糖有出现意识障碍,甚至死亡的风险,是糖尿病选择用药的重要注意事项。参与本研究的患者均无夜间低血糖和严重低血糖事件发生。两组患者在低血糖发生率上无显著差异,提示复方吡格列酮格列美脲片治疗T2DM与单用格列美脲片治疗相比不增加低血糖的发生风险。
研究时间短、纳入研究的样本量偏小为本研究的不足之处,还需纳入更大样本量和更长时间的研究评估复方吡格列酮格列美脲片治疗T2DM的疗效和安全性。
总之,复方吡格列酮格列美脲片作为一个结合两种药物优势的复合制剂在临床治疗实践中疗效显著,不仅服用方便、有利于提高患者依从性,还能改善患者血糖控制情况,提高患者生活质量;耐受性、安全性好,低血糖发生率低,是糖尿病患者控制血糖的又一新选择,值得临床上进一步的推广验证。
[1]DABELEA D,MAYER-DAVIS E J,SAYDAH S,et al.Prevalence of type 1 and type 2 diabetes among children and adolescents from 2001 to 2009[J].JAMA,2014,311(17):1778-1786.
[2]CHENG J,CHEN H,LIN Y,et al.A competing risk analysis of sequential complication development in Asian type 2 diabetes mellitus patients[J].Sci Rep,2015(5):15687.
[3]BAIN C.Treatment of type 2 diabetes mellitus with orally administered agents:advances in combination therapy[J].Endocr Pract,2010,15(7):750-762.
[4]谢琨,南峰,陈枳潓,等.复方盐酸吡格列酮格列美脲片的生物等效性研究[C]//第十三次全国临床药理学学术大会论文集,成都,2012:311-314.
[5]TOZZO E,BHAT G,CHEON K,et al.Pioglitazone increases whole body insulin sensitivity in obese,insulin-resistant rhesus monkeys[J].PLoS One,2015,10(5):e0126642.
[6]PABLOS-VELASCO P P.Pioglitazone:beyond glucose control[J].Expert Rev Cardiovasc Ther,2010,8(8):1057-1067.
[7]赵咏桔.格列美脲的作用特点及临床应用[J].辽宁实用糖尿病杂志,2004,12(1):53-55.
[8]MU K D,KABADI U M.Effects of glimepiride on insulin secretion and sensitivity in patients with recently diagnosed type 2 diabetes mellitus[J].Clin Ther,2004,26(1):63-69.
[9]尚军洁.格列美脲双重作用机制的临床观察[J].中国医药指南,2014,10(10):139-139,140.
[10]周斌,蒋晓真,顾哲.吡格列酮对合并代谢综合征的2型糖尿病患者血清炎症因子及胰岛素抵抗的影响[J].实用医学杂志,2010,26(2):305-307.

